石油沥青基MoS2/多孔碳复合材料的制备及其锂存储性能
李 云,杨 旺,李永峰
(中国石油大学(北京)重质油国家重点实验室,北京 102249)
当今世界,化石燃料在能源结构中仍然发挥着 至关重要的作用[1]。然而,它的过度消费造成了严重的资源短缺和环境污染,严重地影响了人们的日常生活和身体健康[2-3]。此外,诸如沥青和石油焦等低价值的石油副产品也越来越多。为了实现碳中和的愿景,太阳能、潮汐能、风能、生物质能和地热能等可再生能源在过去几十年中得到了广泛地开发[4]。然而,所产生的能量只有在能量存储器的帮助下才能得到有效的利用。迄今为止,许多科研人员一直都在探索高性能且实用的储能系统,尤其是锂离子电池(LIBs)和钠离子电池(SIBs)[5-9]。
石油沥青具有丰富的多环芳烃、丰富的杂原子以及成本低等优点,在合成碳基储能材料方面具有巨大的潜力[10-13]。Gao 等[14]以石油沥青为碳源,制备了一种N/P共掺杂的碳纳米片,该材料表现出优异的电化学性能。Peng等[11]也以石油沥青为原料,合成了一种具有优异可逆容量和倍率性能的氮掺杂碳负极材料。因此,沥青可用于制备高性能的LIBs和SIBs 负极材料。但是,经过几代人的研究,纯碳材料的电化学性能已经非常接近其极限值,但仍远远不能满足市场需求[15]。硫化钼(MoS2)具有高的理论比容量(669 mA·h/g),并且已经被广泛研究[16]。遗憾的是,MoS2的导电性差,大大地限制了其应用。普遍认可的方式是将MoS2和高导电性的碳材料复合,实现材料的优势互补。
本工作开发了一种模板法,首先以NaHCO3为模板制备了一种掺硫多孔碳材料(SPC),随后,在其表面原位生长了一层垂直阵列的MoS2纳米片,最终,制备了一种MoS2/多孔碳复合材料(MoS2/SPC)。在反应过程中,NaHCO3高温裂解产生大量CO2气体,气体的产生衍生出大量的孔结构。随后,以MoCl5为钼源,升华硫为硫源,在多孔碳表面原位生长了一层垂直阵列的MoS2纳米片。该MoS2/SPC 复合材料实现了MoS2和碳基底材料的良好接触,其相互交错的结构可以大大提高电子的传递速率,缩短锂离子和电子的传输路径。经过LIBs 负极测试,MoS2/SPC复合材料展现出优异的倍率性能和长的循环寿命。在0.1 A/g 和1 A/g 电流密度下,MoS2/SPC 电极的可逆比容量分别达到了1034 mA·h/g和730 mA·h/g。在0.1 A/g电流密度下循环100 次后,其比容量仍保持在1400 mA·h/g。在0.5 A/g 电流密度下经过400 次循环后,MoS2/SPC电极的可逆比容量达到了1069 mA·h/g。
1 实验材料和方法
1.1 SPC、MoS2和MoS2/SPC的制备
石油沥青(各成分质量含量为C:82.1%、S:5.0%、N:0.8%、O:5.5%、H:6.6%)由中国石油天然气股份有限公司提供。将1.5 g NaHCO3和1 g 沥青粉均匀研磨。随后,将混合粉末转移至管式炉,以10 ℃/min 的升温速率加热到800 ℃,在Ar 气氛下保持2 h。待自然冷却至室温之后,经过水洗烘干得到SPC材料(图1)。

图1 SPC的合成过程示意图Fig.1 Schematic illustration of the formation process of SPC
将1 mmol的MoCl5和4 mmol的升华硫混合并置于石英舟中,盖上盖子置于石英管中间。在Ar气氛下,以10 ℃/min 的升温速率加热到800 ℃保持1 h,待自然冷却至室温之后得到MoS2纳米片产品。
将所得到的1 g SPC与2 g的升华硫混合研磨,置于石英舟一端,将1 g MoCl5放置在另一端,盖上盖子置于石英管中间。在Ar 气氛下,以10 ℃/min的升温速率加热到800 ℃保持1 h,自然冷却至室温之后得到MoS2/SPC产品(图2)。

图2 (a)SPC和(b)MoS2/SPC的合成过程示意图Fig.2 Schematic illustration of the formation process of(a)SPC and(b)MoS2/SPC
1.2 材料表征
采用扫描电子显微镜(SEM,Hitachi SU3500)观察材料的形态结构,采用拉曼光谱仪(Horiba,激发光波长为532 nm)和X射线衍射(XRD,Bruker D8 Advance)分析材料的组成,采用CHI660D电化学工作站对电极材料进行循环伏安法(CV)和电化学阻抗谱(EIS)测量。采用Brunauer-Emmet-Teller(BET)氮气吸附/脱附法测定了样品的比表面积和孔隙分布。通过热重分析测定了材料的MoS2含量和碳含量。
1.3 电化学测试
电极浆料的制备:首先将活性材料(80%,质量分数,余同)、PVDF(10%)和导电炭黑(10%)分散到一定量氮甲基吡咯烷酮中,搅拌8 h 得到均一的浆体。将所得浆体均匀涂布在铜箔上,在100 ℃下干燥12 h,冲压成13 mm 直径的小圆片,活性物质负载量在1.5 mg左右。
半电池的组装:在充满氩气的手套箱里组装扣式电池,以锂片作对电极,电解液为1 mol/L 的LiPF6溶解在碳酸乙烯酯和碳酸二甲酯的混合物中。
2 实验结果与讨论
2.1 多孔碳的形成机理及形貌表征
为了验证多孔碳的成孔机理,将SPC/NaHCO3样品分散到蒸馏水中,超声0~3600 s不等,随后快速将水抽干,利用SEM 观察不同超声时间样品的形貌变化。如图3(a)所示,SPC/Na2CO3原料表面没有任何孔,经过XRD 测试显示该原料中主要以Na2CO3相为主。随着超声时间的增加,样品表面逐渐显露出密密麻麻的孔隙结构[图3(a)~(f)]。当超声时间达到3600 s 时,样品展现出丰富的孔结构。XRD 测试显示,Na2CO3相的衍射峰已经完全消失。综上所述,NaHCO3裂解产生的CO2和Na2CO3是形成多孔结构的主要原因。

图3 超声不同时间的SPC/NaHCO3样品的SEM图像:(a)0 s;(b)30 s;(c)60 s;(d)300 s;(e)600 s和(f)3600 s[(a)和(f)中的插图为超声0 s和3600 s后的SPC/NaHCO3和SPC样品的XRD谱图]Fig.3 SEM images of SPC/NaHCO3 at different ultrasound time:(a)0,(b)30,(c)60,(d)300,(e)600,and(f)3600 s[Inset of(a)and(f)is the XRD spectra of SPC/NaHCO3 and SPC after 0 and 3600 s]
2.2 SPC、MoS2和MoS2/SPC样品的表征
图4 为SPC、MoS2和MoS2/SPC 三种样品的形貌结构图。如图4(a)~(c)所示,SPC 样品呈现出丰富的三维孔结构,并且该三维孔结构由相互交联的骨架结构构成,骨架表面非常粗糙。另外,纯MoS2纳米片样品呈现出垂直阵列排布,纳米片的尺寸在5~10 μm 之间[图4(d)~(f)]。MoS2/SPC 样品汇聚了SPC 和MoS2样品的结构优势,SEM 图显示SPC碳骨架结构被MoS2纳米片均匀覆盖,其纳米片尺寸大概只有500 nm[图4(g)~(i)]。其尺寸明显小于纯MoS2样品的纳米片尺寸,这主要归因于SPC粗糙的表面结构在原位生长MoS2纳米片的过程中,钼源均匀地分布在SPC 的表面,大大减弱了钼源和硫源的团聚生长作用。所得的小尺寸且超薄的阵列MoS2纳米片结构为锂离子提供了丰富的活性嵌入和脱出位点,并且其超薄的纳米片在锂化和去锂化过程中能够保持良好的结构完整性。

图4 (a)~(c)SPC、(d)~(f)MoS2和(g)~(i)MoS2/SPC的SEM图Fig.4 SEM images of(a)~(c)SPC,(d)~(f)MoS2 and(g)~(i)MoS2/SPC
为了检测MoS2/SPC 材料的化学成分,对其进行了XRD 和Raman 测试。图5(a)显示MoS2/SPC 材料的XRD 图谱中有明显的MoS2相的峰。通过拉曼光谱进一步探测了MoS2/SPC 材料的组成,观察到有明显的MoS2相的峰。此外,在1345 cm-1和1591 cm-1附近还出现了两个明显的峰,它们分别对应着无序碳的D 带和结晶石墨化碳的G 带[图5(b)][17]。通过测试材料的比表面积和孔隙分布,发现MoS2/SPC 杂化物的比表面积达到了179 m2/g,远优于SPC 的比表面积(55 m2/g),并且其主要以微孔和介孔为主。此外,MoS2/SPC 杂化物中碳含量为84%。
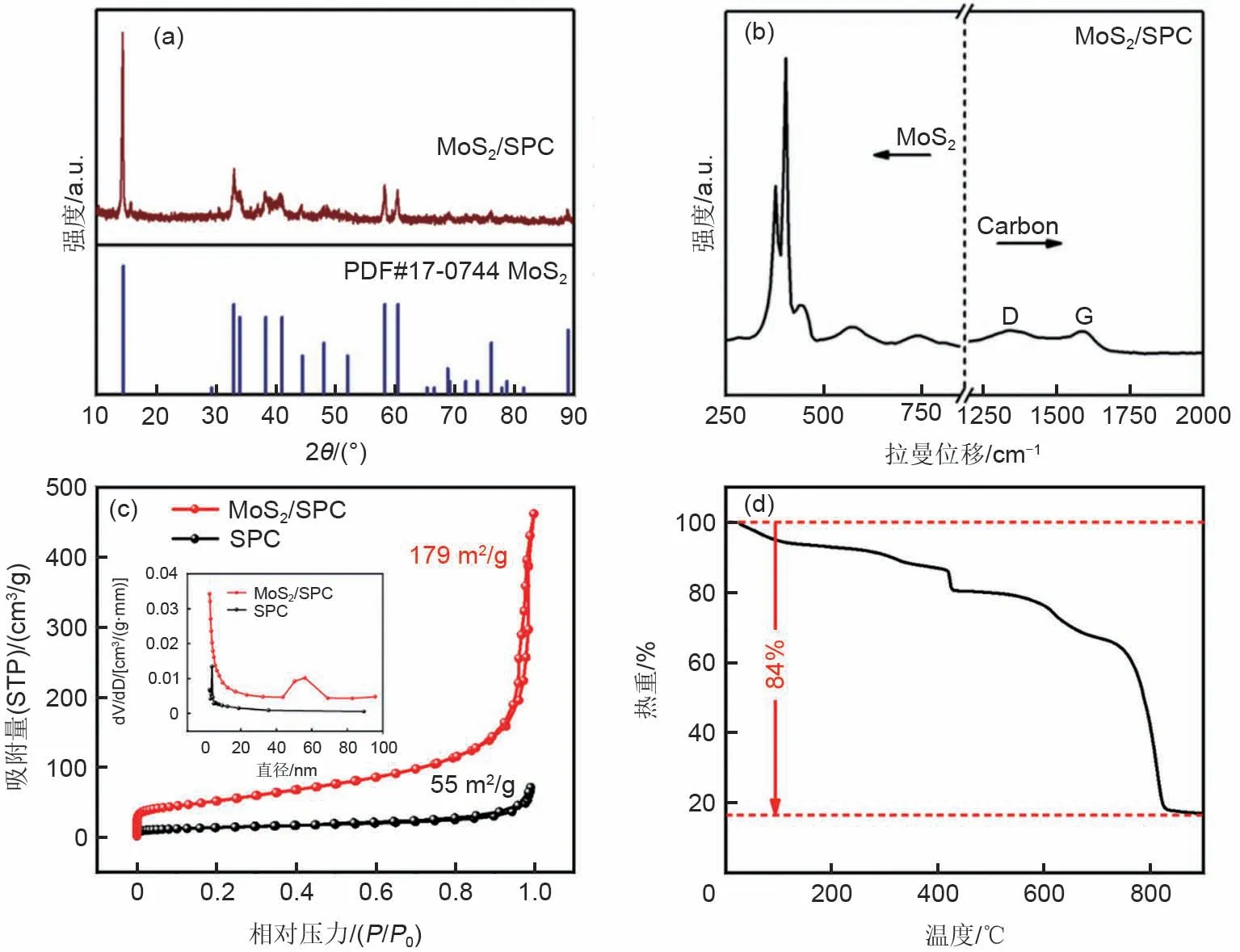
图5 MoS2/SPC的(a)XRD;(b)Raman;(c)比表面积和孔隙分布和(d)碳含量Fig.5 (a)XRD,(b)Raman,(c)specific surface area and pore properties,and(d)carbon content of MoS2/SPC
2.2 SPC、MoS2和MoS2/SPC样品的电化学性能
MoS2/SPC 复合物的薄层阵列MoS2纳米片以及相互交错的三维结构,使该化合物有望成为一种优异的锂电池负极材料。经过性能测试,MoS2/SPC 电极展现出优异的倍率性能[图6(a)]。MoS2/SPC 电极的初始充放电容量分别达到2413 mA·h/g 和1072 mA·h/g。这种首次充放电期间的不可逆容量是由于固体电解质相界面膜(SEI)的产生造成的。循环几圈之后,第二圈和第三圈的充放电曲线几乎重合[图6(b)],该结果表明SEI 膜形成后不可逆容量被消除。在0.1、0.2、0.5、1、2 和4 A/g 电流密度下,MoS2/SPC电极的比容量分别达到了1045、940、830、725、592 和433 mA·h/g[图6(c)]。当电流密度回到0.1 A/g 并循环60 圈后,MoS2/SPC 电极的可逆容量达到了1391 mA·h/g。并且其倍率性能远优于SPC 和MoS2电极的性能。此外,还评估了几种电极的循环性能。图6(d)显示SPC 和MoS2电极表现出较差的循环性能。然而,MoS2/SPC电极展现出很好的循环稳定性,循环400 圈后获得了1069 mA·h/g 的高可逆容量,远优于SPC 和MoS2电极的循环性能[图6(d)]。观察电极容量的变化趋势,MoS2/SPC 电极出现了明显的容量波动。产生容量波动主要存在以下原因。在锂化和去锂化过程中,MoS2/SPC 电极发生着复杂的副反应,随着反应的进行锂离子不断被消耗,电极容量呈下降趋势。然而,随着副产物的分解再生,出现了容量再生现象,也就产生了容量波动现像[18-19]。MoS2/SPC 电极的电化学过程可以总结在以下方程式(1)和(2)[20-21]中。

图6 (a)SPC、MoS2和MoS2/SPC电极在0.1、0.2、0.5、1、2和4 A/g电流密度下的倍率性能;(b)MoS2/SPC电极前三圈的初始充放电曲线;(c)MoS2/SPC电极在0.1、0.2、0.5、1、2和4 A/g电流密度下的充放电曲线;(d)SPC、MoS2和MoS2/SPC在0.5 A/g下的循环性能Fig.6 (a)rate performance of SPC,MoS2 and MoS2/SPC at 0.1,0.2,0.5,1,2,and 4 A/g,(b)initial chargedischarge profiles of MoS2/SPC electrode,(c)charge-discharge profiles of MoS2/SPC electrode at 0.1,0.2,0.5,1,2,and 4 A/g,(d)cycling performance of SPC,MoS2 and MoS2/SPC at 0.5 A/g
另外,还测试了SPC、MoS2和MoS2/SPC 电极的CV 和EIS 性能。MoS2/SPC 电极的电阻仅有80 Ω,远小于SPC和MoS2电极的电阻[图7(a)],说明MoS2/SPC电极具有更好的导电性。测试了MoS2/SPC 电极在不同扫描速率下的CV 曲线[图7(b)]。峰值电流(i,mA)和扫描速率(v,mV/s)服从公式logi=blogv+ loga[22],其中通过拟合logi-logv图的斜率计算出b值。如图7(c)~(d)所示,拟合得到的MoS2/SPC 电极的氧化还原峰的b值均在1 左右,表明该电极由电容性行为主导。MoS2/SPC电极优异储锂性能可归因于以下原因(图8):①垂直阵列的MoS2纳米片的充分暴露大大缩短了锂离子和电子的扩散通道[23-24];②导电碳基板可以增强电子的转移能力[25];③反应过程中纳米网络结构可以保持材料结构的完整性,并实现了电解质的高效渗透[15,26]。鉴于其优异的电化学性能,MoS2/SPC 的锂存储性能优于之前已经报道的MoS2基碳复合材料(表1)。

表1 不同MoS2基材料作为LIBs阳极的电化学性能比较Table 1 Comparisons of electrochemical performance of different MoS2-based materials as LIBs anodes
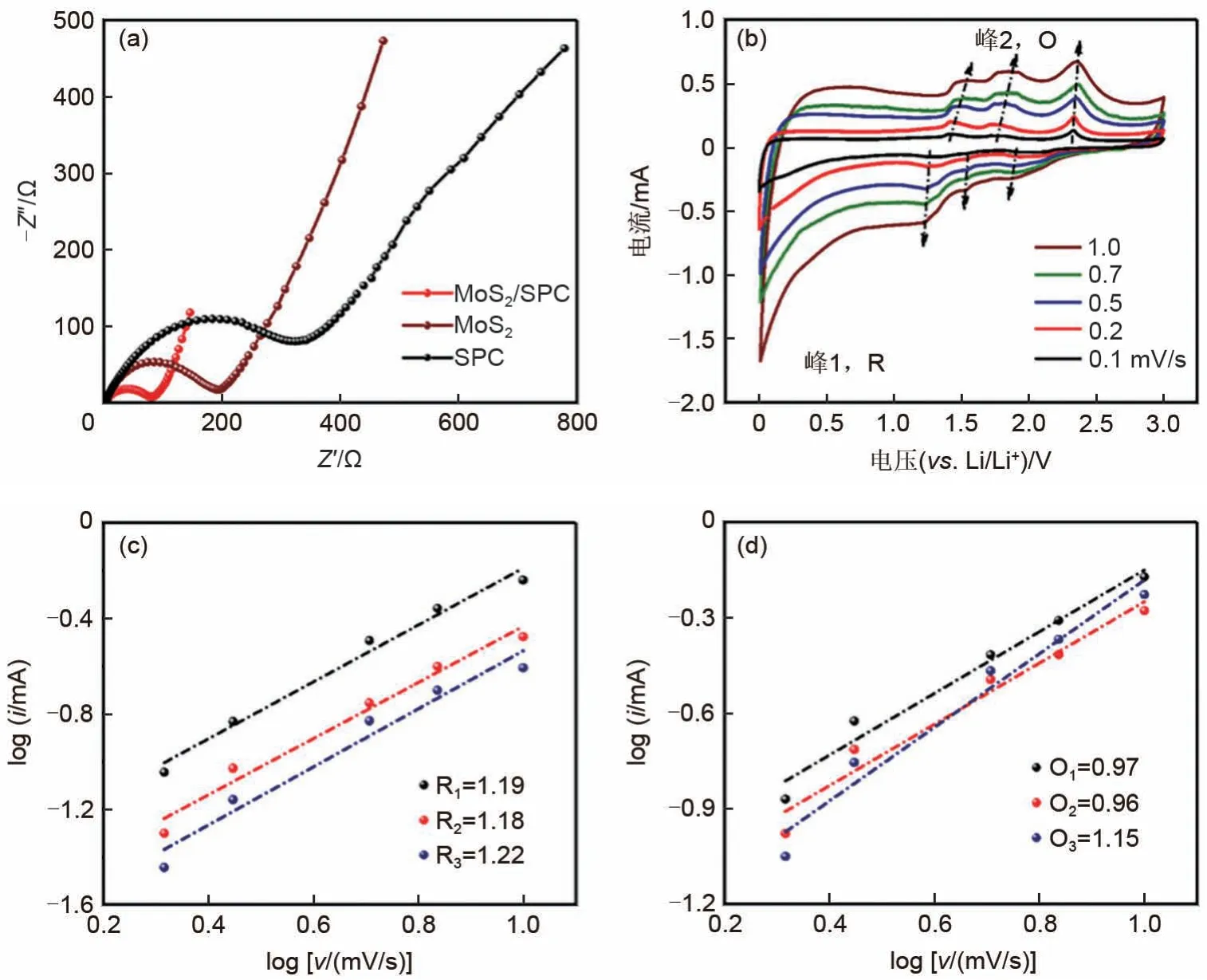
图7 (a)SPC、MoS2和MoS2/SPC电极的Nyquist曲线;(b)MoS2/SPC电极在不同扫描速率下的CV曲线,(c),(d)几个氧化还原峰的log i-log v曲线Fig.7 (a)Nyquist plots of SPC,MoS2 and MoS2/SPC electrodes,(b)CV curves of MoS2/SPC at different scan rates,(c),(d)log i-log v plots at several redox peaks

图8 MoS2/SPC杂化物中Li+和e-的传输路径示意图Fig.8 Schematic diagrams of transport paths for Li+and e-in the MoS2/SPC hybrid
3 结 论
以低沸点的MoCl5为钼源,升华硫为硫源,沥青为碳源,开发了一种模板法并成功合成了一种MoS2/SPC 三维复合结构。MoS2纳米片在SPC 的表面呈现出垂直阵列排布,从而实现了MoS2和碳基底材料的良好接触,其相互交错的结构大大提高电子的传输速率,缩短了锂离子和电子的传输路径。另外,该多孔结构为锂离子提供大量丰富的反应活性位点。当作为锂离子电池负极进行测试时,该材料在0.5 A/g 的电流密度下循环400 圈后,还保持着1069 mA·h/g的高可逆容量。本工作可为低成本石油沥青的高附加值利用提供了一个崭新的思路。

