IVF治疗中垂体降调节形成大卵泡后直接穿刺取卵的临床病例分析
王含必,邓成艳,周远征,郁琦,孙正怡,甄璟然,王雪,肖亚玲,刘美芝
(中国医学科学院 北京协和医学院 北京协和医院妇产科学系,疑难重症及罕见病国家重点实验室, 国家妇产疾病临床研究中心,北京 100730)
体外受精-胚胎移植(IVF-ET)治疗中,多卵泡同步发育时高水平雌二醇(E2)促进正反馈诱发黄体生成素(LH)峰过早出现的概率为20%~25%[1],而卵泡期LH血清浓度过早升高会影响卵母细胞质量及IVF结局。促性腺激素释放激素激动剂(GnRH-a)的降调节作用有效抑制了早发性LH峰,使周期取消率由15%~20%降为2%[2]。GnRH-a使用初期有“点火”效应(FSH和LH一过性升高),而后垂体进入降调状态。“点火”效应可能刺激卵泡长大导致卵巢囊肿形成[3],发生比例为10%~29%[4]。个别情况下这种增大的卵泡可能发育成熟,曾有文献报道对GnRH-a降调后形成的大卵泡进行穿刺取卵后受精移植[1-2]。此方法均为个案报道,至今共报道11例,其中仅4例妊娠。本文对我院尝试此方法的6例患者的诊治经过进行总结分析,以期为临床决策提供依据。
资料及方法
一、研究对象
回顾性分析2013年1月至2021年9月在北京协和医院辅助生殖中心接受早卵泡期GnRH-a减量降调节方案治疗的患者资料。其中6例降调节后形成异常增大卵泡(≥2枚且直径≥18 mm卵泡)且伴有血清E2升高(E2>734.00 pmol/L)的患者,在评估卵泡数量、大小及E2水平,并获得患者充分知情后,未经控制性卵巢刺激(COS)而直接扳机后穿刺取卵行IVF-ET。分析这6例患者的临床及治疗特点。
二、IVF-ET早卵泡期GnRH-a减量降调节方案
月经周期第2天,FSH升高(>10 U/L)和/或窦卵泡大小不均匀的患者选择GnRH-a减量降调节方案。长效醋酸曲普瑞林(3.75 mg/支,易普生,法国)1/5~1/2的剂量,肌肉注射,剂量的选择根据患者的年龄、生殖激素水平及窦卵泡大小及数量综合评定。分别于注射后14 d和20 d返诊,抽血查生殖激素水平,同时经阴道超声检查了解卵泡情况。
使用GnRH-a后卵巢反应有以下3种情况:(1)稳定状态:无E2水平的异常升高且无异常增大的卵泡,当生殖激素水平及卵泡大小符合降调节标准后开始COS;(2)出现增大的卵泡:卵巢中见直径>10 mm的卵泡,则穿刺抽吸囊内液,降调节第20天或次日再次抽血查生殖激素及经阴道超声评估降调节情况,符合降调节标准后开始COS;(3)出现异常增大的卵泡:卵巢中见≥2枚且直径≥18 mm的卵泡,同时伴有血清E2>734.00 pmol/L(200.00 pg/ml),患者充分知情同意后当晚注射重组人绒毛膜促性腺激素(r-HCG)250 μg(艾泽,Profasi,250 μg/支,雪兰诺,瑞士),扳机后36 h~38 h穿刺取卵,获得成熟卵母细胞后继续进行IVF-ET。若符合新鲜胚胎移植条件则行鲜胚移植,否则行冻融胚胎移植(FET)。移植后进行常规黄体支持治疗。
三、观察指标
研究期限内早卵泡期GnRH-a减量降调节患者一般情况;出现异常增大卵泡的患者的相关处理及妊娠结局。
四、统计方法
本研究采用描述性统计。
结 果
一、早卵泡期GnRH-a减量降调节后患者一般情况
2013年1月至2021年9月在北京协和医院辅助生殖中心接受IVF-ET治疗的患者中,采用早卵泡期GnRH-a减量降调节方案者共5 887例。其中,841例因降调节期间形成增大的卵泡[平均直径(12.16±5.37) mm]行穿刺抽吸囊内液;6例患者降调节后出现异常增大卵泡(≥2枚且直径≥18 mm)且伴有血清E2值升高(E2>734.00 pmol/L),经患者充分知情同意后未经COS直接扳机后穿刺取卵。
二、早卵泡期GnRH-a减量降调节后出现异常增大卵泡患者的处理及妊娠结局
6例降调节过程中出现异常增大卵泡(2~7枚≥18 mm卵泡)且伴有血清E2升高(2 572.67~17 616.00 pmol/L)的患者,经征得患者同意,不经过COS而直接艾泽扳机后穿刺取卵,对取得的成熟卵母细胞进行IVF-ET,其中4例妊娠。
1.患者基本情况:年龄31~39岁;体质量指数(BMI)偏低,16.40~19.25 kg/m2,均值(17.94±0.87) kg/m2;不孕年限1.5~16年;IVF指征详见表1。

表1 6例降调节后异常增大卵泡直接穿刺取卵患者的基本情况
2.早卵泡期基础资料及GnRH-a使用量:6例患者基础窦卵泡计数(AFC)、基础激素水平各异,无特别的规律表现;GnRH-a的用量相近(表2)。
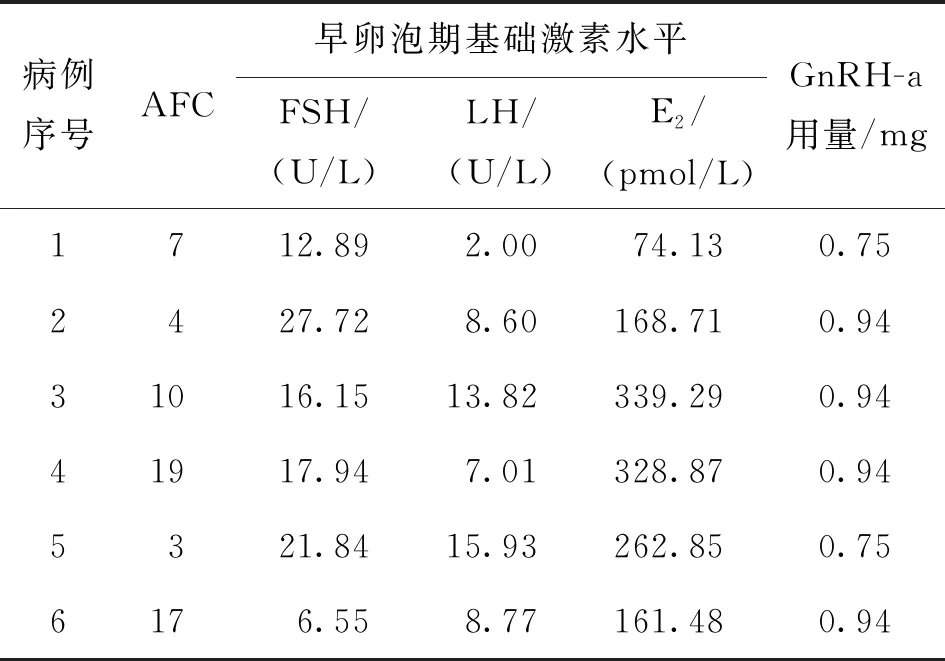
表2 6例降调节后异常增大卵泡直接穿刺取卵患者的早卵泡期基础资料及GnRH-a使用量
3.患者具体治疗过程及结局:第1例,首次注射GnRH-a后,20 d时出现3枚直径10 mm卵泡,血清FSH 9.17 U/L、LH 4.61 U/L、E2458.93 pmol/L、孕酮(P)1.94 nmol/L;再次注射GnRH-a 1.875 mg,14 d后经阴道超声发现双侧卵巢共7枚直径≥20 mm大卵泡,E2值13 675.08 pmol/L。艾泽扳机36 h后取卵,取卵当日双侧卵巢见7枚28~30 mm卵泡,取出成熟卵母细胞3枚,IVF受精2枚。胚胎移植后11 d血清E215 145.91 pmol/L、P>127.20 nmol/L、HCG 130.93 U/L。妊娠至41周顺产一健康男婴,身长50 cm,体重3 325 g。
第2例,GnRH-a降调14 d时出现2枚直径≥20 mm大卵泡,E2值4 055.79 pmol/L。艾泽扳机36 h后取卵,获得成熟卵母细胞1枚,IVF受精形成1枚受精卵,胚胎移植后11 d血清E21 956.48 pmol/L、P>127.20 nmol/L、HCG 145.66 U/L。妊娠至足月40周,顺产一健康女婴,身长50 cm,体重3 850 g。
第3例,GnRH-a降调14 d时出现5枚直径≥20 mm大卵泡,E2值12 101.90 pmol/L。艾泽扳机36 h后取卵,获得成熟卵母细胞2枚,IVF受精2枚,因内膜薄取消移植,冻存卵裂期胚胎2枚。两个月后复苏移植,人工周期内膜准备后移植卵裂期胚胎2枚(8Ⅱ,8Ⅲ),移植后7 d查血清E23 235.14 pmol/L、P>127.20 nmol/L、HCG 70.70 U/L。早孕期超声提示宫内双胎,妊娠23周时因胎膜早破流产。
第4例,GnRH-a降调14 d时出现5枚直径≥20 mm大卵泡,E2值17 616.0 pmol/L。艾泽扳机36 h后取卵,获得成熟卵母细胞4枚,IVF受精形成4枚受精卵,新鲜胚胎移植2枚未孕,冻存D5囊胚1枚。人工周期内膜准备,移植冻融胚胎后受孕,血HCG阳性,但超声未见孕囊样回声,HCG最终转阴。
第5例,GnRH-a降调14 d时出现3枚直径≥20 mm大卵泡,E2值2 947.63 pmol/L。艾泽扳机36 h后取卵,获得成熟卵母细胞1枚,卵胞浆内单精子注射(ICSI)受精,形成受精卵1枚(4Ⅲ),胚胎移植后11 d检查未孕。此后又重新开始两新周期IVF治疗,皆因胚胎质量差,未获得可移植胚胎而放弃治疗。
第6例,GnRH-a降调14 d时出现3枚直径≥20 mm大卵泡,E2值2 572.67 pmol/L。艾泽扳机36 h后取卵,获得成熟卵母细胞2枚,IVF受精形成1枚受精卵(6Ⅳ),胚胎移植未孕。再次行常规COS后获卵7枚,成熟卵4枚,IVF受精形成受精卵1枚(4IV),丢弃胚胎未移植。
6例患者扳机日激素水平及胚胎移植情况见表3。其中4例妊娠患者扳机日单卵泡E2平均值为2 133.96 pmol/L(1 953.58~3 523.20 pmol/L),2例未妊娠者单卵泡E2平均值为920.03 pmol/L(982.54 pmol/L,857.56 pmol/L)。4例妊娠患者单个卵泡对应的E2平均值最低为1 953.58 pmol/L(532.31 pg/ml),因此粗略界定扳机日单卵泡对应的最低E2值>1 835.00 pmol/L(500.00 pg/ml)。

表3 6例降调节后异常增大卵泡直接穿刺取卵患者扳机日激素水平及妊娠结局
讨 论
Brown[5]在1978年首次提出了FSH阈值的概念,即启动卵泡生长的最低FSH值,若低于这一阈值,即使延长用药时间也无法使卵泡生长。早卵泡期GnRH-a降调节方案使用长效GnRH-a抑制内源性LH峰。GnRH-a使用后虽有“点火”效应,但多数患者不受影响,无异常增大的卵泡,可能因GnRH-a刺激垂体释放的FSH未达到卵泡生长的阈值。
GnRH-a使用后少数患者会形成增大的卵泡,其中绝大多数形成1枚增大的卵泡,且卵泡直径多数在10~15 mm,同时伴有较低的血清E2值。可能是GnRH-a使垂体贮存的促性腺激素(Gn)迅速释放刺激卵泡生长,而后GnRH-a长期占据受体抑制FSH、LH分泌,进而抑制卵巢分泌E2。目前认为GnRH-a使用后形成增大的卵泡提示卵巢低反应,是卵巢功能不良、妊娠率低的可靠预测指标[2]。对这类患者多采取超声引导下经阴道穿刺抽吸囊内液以消除不良影响,或直接取消周期。
1992年Parinaud等[6]首次报道GnRH-a降调节后诱发的大卵泡经HCG扳机后可获得成熟卵母细胞。至今全球报道的采用该治疗方法的11例中仅4例妊娠。我中心采用该治疗方法的6例中4例妊娠,回顾分析这些患者的临床特点以期寻找选择该治疗方法的依据。6例患者BMI值偏低,均值(17.94±0.87)kg/m2,这一特点是否与经GnRH-a降调节治疗后可获得成熟卵母细胞有关有待更多的数据支持。
GnRH-a降调后出现大卵泡时首先评估大卵泡的数量。GnRH-a使用后多数情况诱发单个大卵泡形成。我们选择的6例患者形成的大卵泡数最少为2枚,最多者7枚。获卵数多是增加妊娠机会的必要因素,但非唯一因素。因此对于降调后形成大卵泡数越多的患者选择此方案的可行性越大。既往报道的病例中,1例PCOS患者注射布舍瑞林后14 d发生卵巢过度刺激,每侧卵巢各有20枚以上的大卵泡[7]。Azem等[1]报道1例使用GnRH-a后获得19枚成熟卵母细胞,E2值为13 498.26 pmol/L,ICSI形成19枚受精卵。这2例报道中获卵数多可能因这些卵泡的FSH阈值接近,多卵泡同步化生长。
其次,评估GnRH-a降调形成大卵泡后的血清E2水平。随着卵泡的生长成熟,血清E2值逐渐升高,因此临床中将血清E2值视为卵泡发育成熟的参考指标[8-9]。在自然周期中,单卵泡发育成熟后血清E2值平均约1 101.00 pmol/L。本文中4例妊娠者GnRH-a降调后出现的大卵泡,单个卵泡对应的扳机日E2均值为2 133.96 pmol/L,甚至高于自然周期中的单个成熟卵泡E2平均值;2例未妊娠者单个大卵泡对应的扳机日E2均值为920.03 pmol/L,低于自然周期的卵泡E2平均值,且这2例患者因卵巢功能差在随后的IVF常规COS治疗后都未能获得可移植胚胎,最终放弃治疗。这也从侧面说明这2例患者采用GnRH-a降调后直接扳机取卵失败不能排除与其自身卵巢功能差有关。GnRH-a使用后形成大卵泡同时伴有E2水平明显升高者并不多见,E2水平明显升高提示存在卵泡成熟的可能性。分析GnRH-a的“点火”效应促进卵泡成熟的可能原因有:(1)卵泡本身对Gn短期刺激的高敏性;(2)循环中的Gn未被完全抑制[10];(3)GnRH-a增加卵泡对循环中Gn的敏感性[11],尽管循环中FSH浓度低,但生物活性增强继续刺激卵泡生长;(4)有研究发现卵巢中有GnRH-a受体的表达[12],因此推测GnRH-a可能直接作用于卵巢,对刺激卵泡生长及E2生成有调节作用[11]。内源性GnRH或外源性GnRH-a可能通过自分泌、旁分泌作用与卵巢组织的受体结合刺激卵泡生长[13]。胰岛素样生长因子Ⅱ和表皮生长因子影响卵巢细胞增殖,也参与这一调节[14-16]。本文中未经COS直接穿刺取卵方案的患者E2水平升高后反馈抑制FSH,其中1例FSH<0.10 U/L,另外5例平均FSH 0.65 U/L。而此时垂体受到GnRH-a降调作用的影响无LH峰出现,LH均值为6.82 U/L。
因早卵泡期GnRH-a降调节后对形成的大卵泡采用直接穿刺取卵的治疗方法为另辟蹊径的非常规治疗方案,需谨慎抉择。首先,由于仅在GnRH-a降调后出现≥2枚直径≥18 mm卵泡,同时伴有血清E2水平明显升高的患者才可能考虑尝试直接扳机取卵的方法,而临床中较少出现这种情况;其次,这种方法未经COS治疗,可能面临更大的取卵后无成熟卵母细胞甚至无卵母细胞的风险,治疗前患者需充分知情,在患者理解支持的前提下方可尝试使用该方案。受限于上述两因素,至今尝试该治疗的样本例数过少,无法进行统计分析,结果缺乏可靠性,希望以后能够继续尝试进行更大样本量的对照研究以期获得可靠数据支持。
总之,早卵泡期GnRH-a减量降调节后若形成≥2个直径≥18 mm的卵泡,同时伴随E2水平明显升高,尤其单个大卵泡对应的E2平均值>1 835.00 pmol/L(500.00 pg/ml)时,不经COS而直接扳机后穿刺取卵IVF-ET的方法不失为一种选择。尽管此为非常规治疗方法,但也并非全无理论依据,若能够选择合适的病例有望增加成功妊娠的机会,一旦成功妊娠,则在极大简化了治疗流程的同时也节省了高额经济支出,使患者获益良多。

