莫匹罗星软膏微生物限度检查方法适用性研究及水分活度测定*
李 翠,闵 红,谢毓华,杨晓莉
(陕西省食品药品检验研究院·国家药品监督管理局药品微生物检测技术重点实验室,陕西 西安 710065)
莫匹罗星软膏(2%)是类白色亲水性软膏,主要成分为莫匹罗星,为皮肤科外用抗菌药物,对革兰阳性菌的抑制作用较强,常被用于因其引起的脓包、毛囊炎等皮肤感染[1]。目前,国内有6个莫匹罗星软膏生产企业,关于其微生物限度检查方法适用性研究较少,且尚无对于多个企业产品微生物限度检查方法的对比研究[2-3]。水分活度影响微生物生长,作为评价微生物风险和产品稳定性的重要依据,已用于食品和化妆品的风险控制[4-6]。2006年,《美国药典29-国家处方集42》中收载了《水分活度测定在非无菌制剂中的应用》,以指导水分活度在非无菌制剂中对微生物的控制[7-10]。参考文献[11-12],本研究中对6 个生产企业127 批次莫匹罗星软膏进行了微生物限度检查方法适用性的验证,并测定了样品的水分活度,为企业的产品研发、生产环节控制、产品的放行,以及药品的监管检验提供参考。现报道如下。
1 材料与方法
1.1 仪器、试药、菌株与培养基
仪器:SX - 500 型蒸汽灭菌器(日本Tomy 公司);BS2202S型电子天平(德国赛多利斯公司,精度为0.01 g);IPP260 型生化培养箱(德国Memmer 公司);VITEK2 型全自动微生物鉴定系统(法国梅里埃有限公司);CH 型三目显微镜(日本奥林巴斯公司);Aqualab4TE 型水分活度仪(美国Decagon公司)。
试药:莫匹罗星软膏[中美天津史克制药有限公司(T1),香港澳美制药有限公司(T2),湖北人福成田药业有限公司(T3),杭州朱养心药业有限公司(T4),广东恒建制药有限公司(T5),河北九正药业有限公司(T6),含量均为2%]。
菌株:铜绿假单胞菌Pseudomonas aeruginosa[CMCC(B)10104],枯 草 芽 孢 杆 菌Bacillus subtilis[CMCC(B)63501],金黄色葡萄球菌Staphylococcus aureus[CMCC(B)26003],白色念珠菌Candida albicans[CMCC(F)98001],黑曲霉Aspergillusniger[CMCC(F)98 003],均购于中国医学细菌保藏管理中心。
培养基:沙氏葡萄糖液体培养基(SDB,批号为200804),沙氏葡萄糖琼脂培养基(SDA,批号为200927),胰酪大豆胨液体培养基(TSB,批号为200605),胰酪大豆胨琼脂培养基(TSA,批号为200909),均购于北京陆桥技术有限责任公司,培养基的适用性检查均符合2020年版《中国药典(四部)》要求。
1.2 菌液制备
取1.1项下5种试验菌,按2020年版《中国药典(四部)》通则[11]要求,用0.9%无菌氯化钠溶液稀释成适宜浓度的菌悬液,供微生物限度检查方法适用性检查用。
1.3 微生物限度计数方法适用性试验
方法A:1∶10常规法。无菌称量样品10 g,加入90 mL TSB 作为稀释液,制成1∶10(m∶V)供试品溶液。取供试品溶液,分装于无菌试管中,每管9.9 mL,平行5 管,分别加入1.2 项下5 种试验菌液,使最终含菌量不大于100 cfu/ mL,作为试验组。取供试品溶液,分装于无菌试管中,每管9.9 mL,分别加入TSB 0.1 mL,作为供试品对照组。无菌吸取9.9 mL TSB 稀释液,分装于5 管无菌试管中,分别加入1.2 项下5 种试验菌液,使最终含菌量不大于100 cfu/mL,作为菌液对照组。分别无菌吸取上述3组菌液1 mL,注皿,随即注入TSA或SDA,按药典规定条件培养、计数。进行3次重复试验,计算样品中5 种试验菌的回收率。计算公式为回收率(%)=(试验组菌落数-供试品对照组菌落数)÷菌液组菌落数×100%。
方法B:1∶20 稀释法。取方法A 项下供试品溶液50 mL,加入50 mL TSB 作为稀释液,制成方法B 的供试品溶液。其余操作同方法A。
方法C:1∶50 稀释法。取方法A 项下供试品溶液20 mL,加入80 mL TSB 作为稀释液,制成方法C 的供试品溶液。其余操作同方法A。
方法D:中和法。将方法A 项下稀释液替换为含5%聚山梨酯80(V/V)的TSB,制成方法D 的供试品溶液。用含5%聚山梨酯80(V/V)的TSB 代替TSB,作为中和剂对照组。其余操作同方法A。按方法A项下方法计算5种试验菌的回收率比值和中和剂的回收率。计算公式为中和剂回收率=中和剂对照组/菌液对照组。回收率比值均应在0.5~2.0范围内。
方法E:1∶20稀释中和法。取方法D项下供试品溶液50 mL,制成方法E的供试品溶液。其余操作同方法D。
方法F:1∶50稀释中和法。取方法D项下供试品溶液20 mL,制成方法F的供试品溶液。其余操作同方法D。
方法G:薄膜过滤法(冲洗量为每膜300 mL)。按方法D项下方法制备供试品溶液。先用冲洗液0.1%蛋白胨水溶液润洗滤膜,同时取100 mL置过滤器中,加入1 mL供试品溶液,过滤,用冲洗液冲洗滤膜,冲洗量为每膜300 mL,分3 次冲洗,在最后1 次冲洗时加入阳性试验菌液,加菌量不大于100 cfu/ mL,作为试验组。其余操作同方法D。
方法H:薄膜过滤法(冲洗量为每膜500 mL)。将试验组冲洗量增加至每膜500 mL,其余操作同方法G。
方法I:中和-薄膜过滤法(冲洗量为每膜300 mL)。试验组的冲洗液选用含0.1%聚山梨酯80(V/V)的0.1%蛋白胨水溶液,其余操作同方法G。
方法J:中和-薄膜过滤法(冲洗量为每膜500 mL)。冲洗量为每膜500 mL,其余操作同方法I。
1.4 控制菌检查方法适用性试验
1.4.1 金黄色葡萄球菌
方法A:直接接种法。按1.3项下方法D制备供试品溶液。取10 mL,接种于TSB 增菌液至100 mL,并接入阳性对照菌液金黄色葡萄球菌,接种量不大于100 cfu/mL,混匀,按规定条件培养。取上述培养物划线接种,于甘露醇氯化钠琼脂选择性分离平板上培养,有疑似或典型菌落生长时,进行生化试验或用仪器进行鉴定确认,根据鉴定结果确定方法适用性试验是否通过。整个试验过程需进行阳性和阴性对照试验。
方法B:培养基稀释法。TSB 增菌培养基的体积增加至200 mL,其余操作同1.4.1项下方法A。
方法C:培养基稀释法。TSB 增菌培养基的体积增加至400 mL,其余操作同1.4.1项下方法A。
方法D:培养基稀释法。TSB 增菌培养基的体积增加至800 mL,其余操作同1.4.1项下方法A。
方法E:薄膜过滤法。取1.3 项下方法A 1∶10 供试品溶液10 mL,按1.3项下方法G进行薄膜过滤(冲洗量为每膜300 mL),过滤后取膜接种于TSB 增菌培养基至100 mL。其余操作同1.4.1项下方法A。
方法F:薄膜过滤法。冲洗量增加至每膜500 mL,其余操作同1.4.1项下方法A。
方法G:中和-薄膜过滤法。冲洗液调整为含0.1%聚山梨酯80(V/V)的0.1%蛋白胨水溶液,其余操作同1.4.1项下方法E。
1.4.2 铜绿假单胞菌
方法A:直接接种法。按1.3 项下方法D 制备供试品溶液。取10 mL,接种TSB 至100 mL,同时接入阳性对照菌液铜绿假单胞菌,接种量不大于100 cfu/ mL,混匀,按规定条件培养。取上述培养物接种至溴化十六烷基三甲铵琼脂选择性培养基上分离培养,有疑似或典型菌落生长时,进行生化试验或用仪器进行鉴定确认。整个试验过程需进行阳性和阴性对照试验。
1.5 水分活度测定
取127 批次样品适量,平铺至测量皿,置已校准的水分活度仪中,平行测定3次,取平均值。
2 结果
2.1 微生物计数方法适用性试验结果
分别采用10 种方法对6 个生产企业的莫匹罗星软膏开展了需氧菌计数方法适用性研究。采用方法A-H时,5 种试验菌中金黄色葡萄球菌和枯草芽孢杆菌的回收率均为0,铜绿假单胞菌、白色念珠菌、黑曲霉的回收率均为50%~200%,样品对革兰阳性菌金黄色葡萄球菌和枯草芽孢杆菌表现出较强的抑制作用,对白色念珠菌、黑曲霉和铜绿假单胞菌无抑制作用或抑制作用可忽略不计,采用此方法不能有效去除样品的抑菌性,需优化试验方法;采用方法I 中和- 薄膜过滤法(冲洗量为每膜300 mL)时,T1 和T5 两个生产企业的枯草芽孢杆菌试验菌回收率为50%~200%,但其他4 个企业均不能满足要求;采用方法J 中和薄膜过滤法(冲洗量为每膜500 mL)时,6 个生产企业的试验菌回收率均为50%~200%,表明采用此方法对6个生产企业的莫匹罗星软膏进行方法适用性验证,可有效去除抑菌性,方法适用性试验通过。
采用方法A 对6 个生产企业的样品进行霉菌和酵母菌计数方法适用性研究,发现6 个生产企业的2 种试验菌的回收率均为50%~200%,表明莫匹罗星软膏对白色念珠菌和黑曲霉无抑制作用或抑制作用可忽略不计,故方法适用性试验通过。
2.2 控制菌检查方法适用性试验结果
采用方法A 直接接种法对6 个生产企业的莫匹罗星软膏的铜绿假单胞菌进行方法适用性研究,结果铜绿假单胞菌在分离平板上的形态典型,经分离鉴定确认为目标试验菌,表明此样品对铜绿假单胞菌无抑制作用,方法适用性试验通过。采用方法A-F 6种方法对6 个生产企业的莫匹罗星软膏的金黄色葡萄球菌进行方法适用性研究,均未检出金黄色葡萄球菌,表明样品对金黄色葡萄球菌有较强的抑制作用,采用培养基稀释法、直接薄膜过滤法都不能有效去除样品的抑菌性,需优化改进试验方案,建立科学、合理的试验方法。采用方法G中和-薄膜过滤法时,培养物在甘露醇琼脂平板上的形态典型,将典型菌落分离纯化,采用VITEK2 型全自动微生物鉴定仪鉴定,结果确认为金黄色葡萄球菌,方法适用性试验通过,表明在冲洗液中加入适量中和剂可有效去除样品的抑菌性。
2.3 水分活度测定结果
6 个生产企业样品的水分活度最高值为0.145。结果表1。
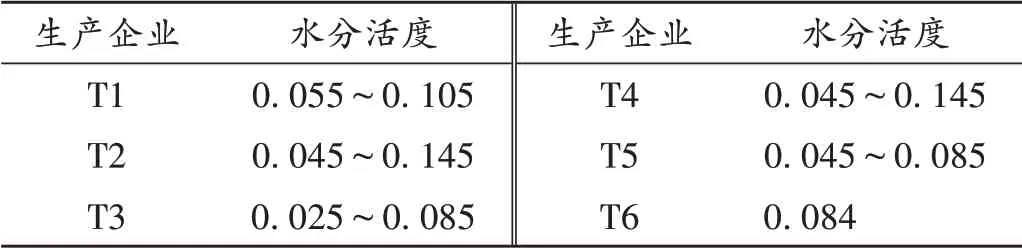
表1 6个生产企业样品水分活度测定结果Tab.1 Determination results of water activity of samples from six manufacturers
3 讨论
本研究中分别采用10 种方法对6 个生产企业的莫匹罗星软膏进行了微生物限度检查方法适用性验证,结果显示,莫匹罗星对革兰阳性菌有较强的抑菌作用。故首先需消除样品的抑菌性,才能进行样品的微生物限度检查,确保结果的准确、可靠。本研究中采用稀释法、中和- 稀释法、薄膜过滤法、中和- 薄膜过滤法等进行了方法优化,发现在供试品溶液和冲洗液中均加入一定浓度的聚山梨酯80后,可消除样品的抑菌性,各试验菌的回收率均满足2020年版《中国药典(四部)》要求。聚山梨酯80作为一种非离子型表面活性剂,可降低季铵类化合物、酚、醛、对羟基苯甲酸类的活性,用于常见干扰物的中和剂[11,13-17];在供试品溶液制备和冲洗液中添加有效的中和剂,除可有效去除样品的抑菌性外,还较稀释法和薄膜过滤法操作简单,不易引起污染。故进行抑菌性较强样品的微生物限度检查方法适用性研究时,选择合适的中和剂不仅可快速去除样品的抑菌性,还可降低检验成本,提高检验效率。
莫匹罗星的水分活度值较低,不易出现微生物增值现象。本研究中127批次莫匹罗星软膏的水分活度值均低于0.60,未因生产企业的不同而出现较大幅度的差异。当水分活度低于0.60时,所有微生物都不会出现增殖现象[18-20],建议检测样品的微生物时,可考虑适当减少检测次数,根据监测实验室历史微生物检查数据和对水分活度的检测结果,制订该产品的微生物检验周期[7-8]。

