孕妇孕晚期血流动力学指标与胎盘功能的关系
廖文珺,林巧玲,郑秀珠
广东省惠州市惠东县人民医院妇产科,广东惠州 516300
健康孕妇的血管血容量与心输出量(CO)随着孕周的增加而增加,子宫动脉的阻力会逐渐降低,形成子宫胎盘低阻力循环,母体表现为血压与外周血管阻力(PVR)降低[1],以保证胎盘与胎儿的血供。孕妇在孕晚期,胎儿对营养物质的需求逐渐增大,胎盘所需的血流灌注增加,母体的身体负荷逐渐加重。相关研究认为,血流动力学异常改变会导致胎盘功能障碍[2]。有学者通过重复测定平均动脉压(MAP)和血清胎盘生长因子(PLGF)以预测先兆子痫[3-4],而子痫是妊娠期高血压的并发症之一,其发生也与胎盘功能异常有关;母体的子宫动脉搏动指数(UtA-PI)上升及PLGF降低、可溶性FMS样酪氨酸激酶1(sFlt-1)水平上升与胎盘功能障碍有关[5],上述研究表明血流动力学的改变会影响胎盘功能,但暂不清楚母体的哪些血流动力学指标变化会影响胎盘功能。为探讨孕妇孕晚期的血流动力学指标与胎盘功能的关系,本研究纳入了接受规律产检的188例孕晚期孕妇作为研究对象,以探讨母体血流动力学改变对胎盘功能的影响。
1 资料与方法
1.1一般资料 本研究通过本院伦理委员会批准后,选取2017年1月至2021年1月于本院规律产检的188例孕晚期孕妇作为研究对象,其中95例孕晚期胎盘功能正常(PLGF≥100 pg/mL)的孕妇作为正常组,93例孕晚期胎盘功能不全(PLGF<100 pg/mL)的孕妇作为异常组。纳入标准:(1)均为单胎妊娠;(2)孕周35~37周;(3)无妊娠期合并症(如糖尿病、高血压、甲状腺功能亢进或减退);(4)无红斑狼疮;(5)无肾脏疾病;(6)检查依从性良好;(7)签署知情同意书。排除标准:(1)慢性高血压;(2)先兆子痫;(3)合并哮喘;(4)合并心脑血管疾病;(5)胎儿生长受限;(6)合并慢性感染;(7)胎儿染色体异常。孕妇的一般资料见表1。
1.2方法
1.2.1临床资料收集 调查并记录孕妇的年龄、孕周、是否吸烟、体质量、受孕方法(包括自然受孕或应用促排卵药物)、是否为经产妇、胎次。
1.2.2血流动力学 由有经验的超声心动图专家应用荷兰Canon Aplio I900扫描仪测定两组孕妇的血流动力学指标,在胸部后方放置4个双表面电极,让孕妇休息15 min后保持直立坐姿,以消除主动脉下腔静脉压迫对母体CO的影响,获得标准胸骨旁与心尖视图,每分钟记录5次,用5个周期的平均值评估心脏各参数,记录CO,CO=每搏量(SV)×心率(HR),并测量UtA-PI、HR、MAP、PVR,PVR=80×MAP/CO。
1.2.3胎盘功能 (1)标本采集与处理:采集孕妇的空腹静脉血液2 mL,用离心机以3 000 r/min的速度常温离心20 min,分离血清,保存于-80 ℃。(2)PLGF测定:取血清标本使用酶联免疫吸附试验(ELISA)进行检测,应用Alere Triage的仪器和配套试剂检测血清中的PLGF,检测操作严格按照试剂盒说明书进行。步骤如下:①校准。使用仪器配套的校准卡片校准仪器,当检测停止提示Pass即为校准合格;校准手动单道移液器,同时设定里程为250 μL;②加样。使用移液器取250 μL待检测血清加入PLGF测试卡;③测定。输入待检测序号,将PLGF测试板置于仪器中,即开始进行PLGF水平检测,15~20 min可获知定量结果。(3)sFlt-1测定:血清标本采用ELISA进行检测,使用上海瑞番生物科技有限公司提供的试剂盒及Thermo热电FC酶标仪进行检测,操作严格按照试剂盒说明书进行。操作步骤包括加样、加酶及温育、洗涤、显色、终止。用酶标仪测定在450 nm波长各孔的吸光度(A)值,绘制标准曲线,计算待测标本的水平。所有标本检测均由同1人进行。
1.3观察指标 (1)临床资料:包括一般资料、胎盘功能(PLGF、sFlt-1)、母体血流动力学参数(HR、MAP、CO、PVR、UtA-PI);(2)分析孕妇胎盘功能障碍的危险因素。
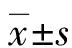
2 结 果
2.1两组患者的临床资料比较 正常组PLGF、HR、CO水平高于异常组,sFlt-1、MAP、PVR、UtA-PI水平低于异常组(P<0.05),见表1。
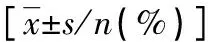
表1 两组患者的临床资料对比
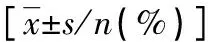
续表1 两组患者的临床资料对比
2.2影响胎盘功能的Logistic回归分析 Logistic回归分析显示,sFlt-1(OR=13.901,95%CI:4.199~46.024)、CO(OR=0.449,95%CI:0.266~0.759)、PVR(OR=1.008,95%CI:1.005~1.011)、UtA-PI(OR=4.629,95%CI:1.060~20.204)是胎盘功能障碍的影响因素(P<0.05),见表2。
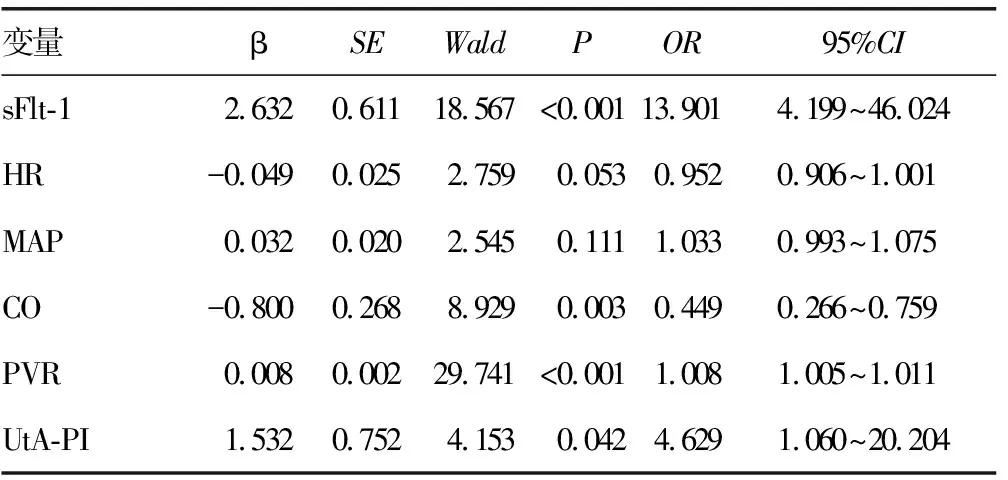
表2 影响胎盘功能的Logistic回归分析
3 讨 论
已有研究证实,孕妇血流动力学改变会引起胎盘功能受损,并导致相关并发症,如妊娠期高血压,因母体的血压升高,子宫动脉对胎盘的血液供应减少,胎盘的血管发育不良,阻断了胎盘血管的重铸过程,进而引起子痫、死胎等情况[6-7]。ANDRIETTI等[8]、HERRAIZ等[9]通过检测孕妇的MAP、PLGF和sFlt-1/PLGF 以预测先兆子痫,而子痫是胎盘功能受损相关并发症;VALIO等[10]在胎盘素受损、胎儿低氧血症导致死产的妊娠案例中观察到UtA-PI、sFlt-1水平升高、血清PIGF水平降低,均提示孕妇血流动力学与胎盘功能密切相关,但对于其中具体的相关性尚不明确。
本研究结果显示,血清sFlt-1、CO、PVR及UtA-PI与胎盘功能有关。考虑原因为胎儿在子宫中的发育需依靠胎盘从母体获取营养,且胎盘还会产生多种激素以维持妊娠,孕晚期孕妇在胎盘激素的作用下,胎盘滋养细胞侵入子宫肌层内螺旋动脉逐渐增多,使得子宫血管管径扩张且无弹性,子宫动脉的阻力会逐渐降低,形成子宫胎盘低阻力循环,维持足够的胎盘血流灌注,母体表现为CO增加、MAP与PVR降低[11-12]。孕晚期孕妇的身体负荷加重,心血管功能发生了潜在的异常改变,容易发生血管痉挛,血流量减少。而母体的CO下降,则需通过母体PVR的增加来缓冲,以维持母体动脉血压,使得MAP、UtA-PI升高,导致子宫动脉对胎盘血流灌注减少,胎儿脐动脉阻力升高,子宫动脉向胎盘输送氧气的减少与胎盘血管阻力的增加相匹配,胎盘血流供应和氧合减少,阻断了血管的重铸过程[13-15],引起胎盘功能异常,滋养层细胞生成减少,血清PLGF水平降低,sFlt-1水平升高。UMAPATHY等[16]认为MAP升高、胎盘缺氧引起的血管内皮损伤为sFlt-1大量升高的主要诱因之一,且整个妊娠期血压升高的人群有着较高水平的sFlt-1及sFlt-1/PLGF。
此外,也有研究表示,PLGF、sFlt-1也可影响孕妇的血流动力学。sFlt-1由滋养细胞分泌,主要表达于胎盘合体滋养细胞和绒毛毛细血管内皮细胞的细胞膜或胞质中,其可拮抗血管生成;PLGF的功能是调节滋养层细胞与内皮功能,促进新生血管生成,其血清水平可用于判断胎盘合体滋养层细胞存在的供氧压力[17-18]。胎盘的血供和氧合减少时,滋养层细胞生成减少,血清PLGF水平降低,sFlt-1水平升高。PLGF也是一种强效的动脉血管舒张剂,可参与妊娠期血管张力的调节,血管紧张素(Ang)Ⅱ可使得微动脉、静脉收缩,血压增高,而PLGF通过减弱血管对Ang Ⅱ的反应以降低血压[19-20]。sFlt-1与血管内皮生长因子(VEGF)结合,拮抗VEGF促进血管增殖、成形的功能,诱导内皮功能障碍,减少血管生成,并使得VEGF不能磷酸化一氧化氮合酶(NOS)中的Ser1177,从而抑制NOS激活,阻碍NOS依赖的血管舒张,间接影响血管舒张[21]。sFlt-1可减弱PLGF的作用,导致血管张力失调,引起孕妇血压升高,CO下降[22],提示胎盘功能与孕妇的血流动力学可互相影响。
综上所述,血清sFlt-1及血流动力学指标CO、PVR、UtA-PI与胎盘功能有关,在孕妇孕晚期胎盘功能检测中可增加CO、PVR、UtA-PI的检测。本研究不足之处在于:因胎盘成熟度是直接评价胎盘功能的指标,而本研究未观察孕妇的血流动力学变化是否会影响胎盘的成熟度,另外,未观察血流动力学与胎儿体重和妊娠结局的关系。在更深入的研究中,可探讨血流动力学与胎儿体重和妊娠结局的关系。

