不同直径球囊扩张联合CAS治疗症状性重度颈动脉狭窄的效果比较
贺亚龙,范百亚,康 静
1.陕西省延安市人民医院神经内科,陕西延安 716000;2.陕西省延安市中医医院神经内科,陕西延安 716000
颈动脉是脑部的主要供血血管之一,颈动脉狭窄是颈部大血管管腔变窄所导致的一种疾病,当出现与狭窄相关的临床症状时,称为症状性颈动脉狭窄。据文献报道,重度颈动脉狭窄的患者,即便采用有效的药物控制,2年内脑缺血事件发生率也高达26%以上,而60%以上的脑卒中是由颈动脉狭窄造成,严重脑卒中可导致患者残疾甚至死亡[1-2]。颈动脉内膜剥离术(CEA)与颈动脉支架植入术(CAS)是2014年美国心脏协会/美国卒中协会缺血性脑卒中二级预防指南及2015年我国颈动脉狭窄相关指南推荐的治疗手段,具有复发率低,术后恢复快等优点[3],但对于颈动脉解剖结构异常者更推荐采用CAS[4]。CAS术前需先使用球囊进行扩张,再将自膨式支架植入。5 mm球囊在临床上应用较多,但有些学者认为4 mm球囊对颈动脉的刺激性较小,不容易发生高灌注损伤等并发症[5]。目前,关于这2种直径球囊在CEA中的应用价值还存在一定的争议,且相关研究也较少。基于此,笔者将通过比较4 mm与5 mm球囊扩张在症状性重度颈动脉狭窄CAS治疗中的疗效及安全性,以期为临床提供参考依据。
1 资料与方法
1.1一般资料 选择2018-2020年陕西省延安市人民医院神经内科收治的80例症状性重度颈动脉狭窄患者为研究对象,按照所用球囊直径分为4 mm球囊组与5 mm球囊组,每组40例。2组患者基线资料比较,差异均无统计学意义(P>0.05),具有可比性,见表1。本研究经本院医学伦理委员会批准,患者及家属均签署知情同意书。纳入标准:(1)诊断符合中华医学会外科学分会血管外科学组制订的《颈动脉狭窄诊治指南》[6],经数字减影血管造影(DSA)证实狭窄程度超过70%;(2)存在与颈动脉狭窄相关的临床症状,例如头晕、记忆力减退、意识障碍等;(3)患者年龄≥18岁。排除标准:(1)伴有动脉瘤、动脉夹层等疾病;(2)伴有严重心肺疾病、肝肾功能不全、全身性感染、恶性肿瘤等;(3)凝血功能异常、免疫功能低下、血压不能有效控制者;(4)对手术中相关药物过敏者;(5)孕妇及哺乳期女性。
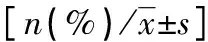
表1 两组患者基线资料比较
1.2方法 术前给予100 mg阿司匹林片与75 mg氯吡格雷片,每天1次,持续3~5 d。于右侧股动脉进行穿刺,将8F动脉鞘置入;沿着动脉鞘将泥鳅导丝与8F导引导管进行置入,到达颈总动脉末端,DSA再次观察病变情况;将微导丝置入,通过狭窄段;沿着微导丝将保护伞置入,到达于C1段远端,然后将保护伞释放;按照分组情况,沿着保护伞导丝将4 mm×30 mm的球囊(4 mm球囊组)或5 mm×30 mm的球囊(5 mm球囊组)置入至狭窄段,进行扩张。保持收缩压在100~140 mm Hg,维持正常心率,将球囊系统撤出,然后沿着保护伞导丝将8 mm×40 mm的自膨式支架置入至狭窄处,在DSA下对支架位置进行调整及确定,满意后释放支架。术后继续服用阿司匹林片与氯吡格雷片,持续6个月。
1.3观察指标 (1)于术前及术后1 d,采用DSA检测颈动脉狭窄程度。(2)于术前及术后1 d,采用彩色多普勒超声对狭窄段和C1段远端收缩期峰值流速(PSV)及舒张末期流速(EDV)进行检测。(3)于术前及术后1 d,采用γ-谷氨酸氨基转移酶(γ-GT)检测试剂盒检测血清γ-GT水平,采用酶联免疫吸附试验检测血清白细胞介素-6(IL-6)水平。(4)随访6个月,观察并发症情况,主要包括高灌注综合征、颈动脉窦反应、脑卒中、支架内再狭窄等。
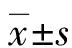
2 结 果
2.1两组颈动脉狭窄程度比较 术前,两组颈动脉狭窄程度比较,差异无统计学意义(P>0.05);术后1 d,两组颈动脉狭窄程度均明显降低(P<0.05),5 mm球囊组明显低于4 mm球囊组(P<0.05)。见表2。
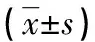
表2 手术前后两组颈动脉狭窄程度的比较
2.2两组PSV及EDV的比较 术前,两组之间狭窄段和C1段远端PSV及EDV的比较,差异无统计学意义(P>0.05);术后1 d,两组的狭窄段PSV及EDV均明显降低(P<0.05),5 mm球囊组明显低于4 mm球囊组(P<0.05),两组的C1段远端PSV及EDV均明显增高(P<0.05),5 mm球囊组明显高于4 mm球囊组(P<0.05)。见表3。
2.3两组血清γ-GT及IL-6水比较 术前,两组血清γ-GT及IL-6水平比较,差异无统计学意义(P>0.05);术后1 d,两组血清γ-GT及IL-6水平均明显降低(P<0.05),两组之间的差异无统计学意义(P>0.05)。见表4。
2.4两组并发症的比较 两组均未发生死亡等严重不良事件。4 mm球囊组发生2例高灌注综合征、10例颈动脉窦反应、1例脑卒中、3例支架内再狭窄,并发症发生率为40.00%;5 mm球囊组发生3例高灌注综合征、8例颈动脉窦反应、1例脑卒中、2例支架内再狭窄,并发症发生率为35.00%;两组的并发症发生率比较,差异无统计学意义(χ2=0.936,P=0.410)。
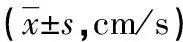
表3 手术前后两组狭窄段和C1段远端PSV及EDV的比较

表4 手术前后2组血清γ-GT及IL-6水平的比较
3 讨 论
CAS是目前临床上治疗重度颈动脉狭窄的主要方法,其能够迅速解除颈动脉的狭窄,改善颈动脉的血流状态,从而改善脑卒中等临床疾病的预后[7]。在进行CAS前需要先使用球囊扩张,其目的是对血管病变严重程度、病变长度、有无钙化、血管直径等有更好的了解,并估计支架置入的难易及可能性等,提供靶病变的更多信息,利于支架置入,避免或减少支架在置入过程中出现的支架不能到位[8]。但不同直径球囊对CAS的治疗效果及安全性是否会产生不同的影响,在临床上还没有定论。
本研究比较4 mm与5 mm球囊扩张联合CAS治疗症状性重度颈动脉狭窄的效果,结果显示,所有患者的CAS均获得成功,术后5 mm球囊组的颈动脉狭窄程度明显低于4 mm球囊组,与陈瑞卿等[9]的研究结果一致;本研究还采用彩色多普勒超声对两组患者的狭窄段及C1段远端PSV及EDV进行了评估,结果显示,术后1 d时两组的狭窄段PSV及EDV均较术前明显降低,C1段远端PSV及EDV均较术前明显增高,5 mm球囊组的变化幅度更大,提示两种直径球囊扩张联合CAS均能有效改善症状性重度颈动脉狭窄患者的血流动力学,与袁晨等[10]的研究结果基本相符,而5 mm球囊组的改善效果更显著,可能与大直径球囊对狭窄血管腔扩张更充分,颈动脉狭窄程度降低幅度更大有关。γ-GT是一种转移酶,主要催化γ-谷氨酰基转换反应,以往研究证实,血清γ-GT水平与颈动脉内膜斑块厚度存在密切关系,与颈动脉硬化的发生发展也存在密切关系,是颈动脉硬化的独立危险因素[11]。IL-6是一种功能广泛的多效性细胞因子,具有促进炎性反应的作用,有研究表明,IL-6参与了动脉粥样硬化的发生发展过程[12]。本研究中,术后1 d时两组血清γ-GT及IL-6水平明显降低,但两组间的差异无统计学意义(P>0.05),提示两种直径球囊扩张对颈动脉硬化的影响效果一致。
两组均未发生严重并发症。CAS手术过程中会对颈动脉窦压力感受器产生刺激,出现颈动脉窦反应,既往文献报道,其发生率在40%~80%[13],本研究中4 mm球囊组发生10例(25.00%),5 mm球囊组发生8例(20.00%),均低于既往的文献报道,可能与样本量及判定标准不同有关;高灌注综合征是由于颈动脉高度狭窄被解除后,同侧脑血流量成倍增加超出脑组织的代谢需要所致,既往研究报道其发生率在0.5%~7%[14],本研究中4 mm球囊组发生2例(5.00%),5 mm球囊组发生3例(7.50%),发生例数较少,还需要进一步扩大样本量进行研究;内皮损伤和内皮功能失调及新生内膜增殖是支架内再狭窄发生的共同特征和基本机制,有文献报道其发生率在6%左右[15],本研究中4 mm球囊组发生3例(7.50%),5 mm球囊组发生2例(5.00%),与既往文献一致。本研究中两组的并发症发生率比较,差异无统计学意义(P>0.05),还需要进行长期随访进一步完善结论。
综上所述,两种球囊均安全有效;与4 mm球囊相比,5 mm球囊在改善颈动脉狭窄程度及血流动力学方面更具优势。本研究还存在一定的局限性,例如样本量不够大,随访时间不足等,今后将继续深入研究。

