清肺颗粒固态发酵培养基成分研究
张 艳,薛沾枚,刘雪松,苏 景,郝敬友,唐 伟,刘彦凯,孙洪杰,史同瑞
(1.黑龙江省农业科学院畜牧兽医分院,齐齐哈尔 161005;2.黑龙江省动物疫病控制中心,哈尔滨 150069;3.哈尔滨绿达生动物药业有限公司,哈尔滨 150039)
中草药的传统提取方法有浸提法、水煎法、醇提取和水蒸馏法等,这些方法虽然操作简单,但存在提取率低、易破坏中药有效成分、降低药物疗效等弊端[1-3]。为了更加科学、高效地提取中药活性成分,人们一直在探索创新并优化中药的提取技术[4-5]。生物发酵中药是利用微生态学、仿生学等方法将中药或其提取液以1株或几株益生菌作为菌种,在体外模拟动物肠道环境对中药有效成分的生物学转化的一种方法[6-8]。清肺颗粒是由板蓝根、葶苈子、浙贝母、桔梗、甘草等多味中药组成的方剂,具有清肺平喘、止咳化痰的功效,主治肺热咳喘、咽喉肿痛[9]。解淀粉芽孢杆菌是一种需氧益生芽孢杆菌,可产生多种生物酶,如纤维素酶、淀粉酶、蛋白酶和β-葡聚糖酶等[10-11],各种生物酶有助于植物细胞壁的裂解,使药物的有效成分更彻底地释放出来。清肺颗粒组方中板蓝根和葶苈子占比较多,故选择二者共有的活性成分(R,S)-告依春为评价指标。采用可产生多种生物酶的解淀粉芽孢杆菌固态发酵法可显著提高清肺颗粒组方(R,S)-告依春的提取率。为进一步优化清肺颗粒组方的固态发酵工艺,本试验在单因素法筛选培养基组成的基础上,以响应面法确定了培养基各组分配比,并比对发酵清肺颗粒与传统工艺清肺颗粒药物有效成分(R,S)-告依春含量的差异,以期为清肺颗粒生产工艺改良奠定基础。
1 材料与方法
1.1 材料
板蓝根、葶苈子、桔梗、甘草、贝母、麸皮、玉米面和黄豆粉均由哈尔滨绿达生动物药业有限公司提供;蔗糖、甘露醇、麦芽糖、可溶性淀粉、酵母浸膏、(NH4)2SO4、NH4Cl、尿素、蛋白胨、葡萄糖、CaCO3、KH2PO4、MgSO4、MnSO4、NaCl均为分析纯,均购自齐齐哈尔市现代精细化工有限公司;解淀粉芽孢杆菌由黑龙江省农业科学院畜牧兽医分院微生物研究室分离鉴定并保存。
分析天平(型号:WT1003H)购自常州万泰天平仪器有限公司;电热恒温培养箱(型号:DH4000II)、超净工作台(型号:CJ-2S)购自天津市泰斯特仪器有限公司;恒温培养摇床(型号:SPH-2102C)购自上海世平实验设备有限公司;立式压力灭菌器(型号:LDZX-75KBS)购自上海申安医疗器械厂;高速多功能中药粉碎机(型号:DFY-500)购自温岭市林大机械有限公司。
1.2 高效液相色谱(HPLC)法测定(R,S)-告依春含量
1.2.1 色谱条件 色谱柱为InertSustain C18,流动相为甲醇∶0.02%磷酸=7∶93,流速为1.0 mL/min,柱温为25 ℃,检测波长为245 nm,进样量为10 μL。
1.2.2 对照品溶液制备 精密称取(R,S)-告依春对照品4 mg,加入100 mL容量瓶中,加甲醇定容至刻度,摇匀,制成40 μg/mL的对照品溶液。
1.2.3 线性关系考察 精密移取一定量对照品溶液于容量瓶中,用甲醇定容制成浓度分别为2.5、5、10、20和40 μg/mL的溶液,上样量10 μL,测定峰面积,以浓度为横坐标,以峰面积为纵坐标,绘制标准曲线。
1.2.4 精密度、稳定性、重复性和加样回收率试验 分别精密量取浓度为0.5、5和10 mg/mL的对照品溶液,上样量10 μL,测定峰面积。精密度试验连续上样6次,计算相对标准偏差(RSD);稳定性试验,间隔2 h分别进样,在12个时间点测定峰面积,计算RSD值;重复性试验,同一供试品溶液,连续制备6份,分别测定各中药有效成分平均含量,计算RSD;加标回收率检验,将已知浓度的样品加入一定量标准样品再进行检测,计算它们的平均回收率和RSD值。
1.3 发酵菌的活化
将冻存的解淀粉芽孢杆菌解冻后划线接种于营养琼脂平板,37 ℃培养24 h,平板上挑取单个菌落接种营养肉汤,37 ℃摇床130 r/min培养18~22 h。
1.4 发酵培养基单因素筛选
基础培养基配方:蛋白胨20 g,葡萄糖10 g,氯化钠5 g,水1 L,pH 7.0~7.2。按受试营养成分与基础培养基中碳源、氮源和无机盐基本一致的原则替换。
4.以学术英语为导向,设计具有逻辑风格的英语课程。教师作为课堂设计的主导者,需要具备为课程设计的能力,以此启发学生进行思考。学术英语课堂不再是教师单纯对知识点讲解,更需要通过引导者的身份来指引学生进行学习。教学实践中,我们应从话语主题或背景出发,注重内容意义、写作目的、运用意境等多角度,让学生自发产生疑问,教师通过富有逻辑地讲解和分析让学生对所质疑的事物有一种顿悟的感觉,最终实现围绕其论证的理解、分析与评估等批判性思维方法和策略训练学生提出和解决问题的能力,促进学生批判性思维能力的培养。
1.4.1 碳源筛选 分别以10 g/L蔗糖、10 g/L甘露醇、10 g/L麦芽糖、50 g/L玉米面、50 g/L可溶性淀粉和100 g/L清肺组方中药粉替代基础培养基中的葡萄糖,其他成分不变,同时以基础培养基作为对照。将发酵菌液以2%接菌剂量接种,置于37 ℃以130 r/min振荡培养18 h,混匀取样,HPLC法测定(R,S)-告依春含量,试验重复2次。
1.4.2 氮源筛选 分别以50 g/L黄豆粉、50 g/L麸皮、10 g/L酵母浸膏、10 g/L (NH4)2SO4,10 g/L NH4Cl、10 g/L尿素替代基础培养基中的蛋白陈,其他成分不变,按1.4.1方法培养。
1.4.3 无机盐筛选 分别以3 g/L CaCO3、2 g/L KH2PO4、2 g/L MgSO4、0.2 g/L MnSO4替代基础培养基中的NaCl,其他成分不变,按1.4.1方法培养。
1.5 发酵培养基成分优化
1.5.1 响应面法优化培养基成分 在单因素试验基础上,以中药粉比例、氮源比例、无机盐比例、和水比例4个因素为自变量,以(R,S)-告依春含量(Y)为评价指标,按表1的因素水平表设计响应面试验方案,筛选最优培养基参数。

表1 发酵培养基成分因素水平
1.5.2 验证试验 按前文方法接种优化的固态发酵培养基,37 ℃培养24 h,测定每克固态发酵物中的(R,S)-告依春含量,验证预测结果的准确性,试验重复3次。
1.6 (R,S)-告依春含量比对
HPLC法测定工艺优化前、后发酵培养基中(R,S)-告依春含量,应用外标法计算,重复3次。
1.7 数据处理与分析
2 结 果
2.1 HPLC法测定(R,S)-告依春含量
2.1.1 线性关系考察 (R,S)-告依春对照品标准曲线为y=22 219x-36 975,相关系数(R2)为0.9994,(R,S)-告依春含量在2.5~40 μg/mL范围内线性关系良好(图1)。(R,S)-告依春标准品色谱图见图2,出峰时间16.848 min。
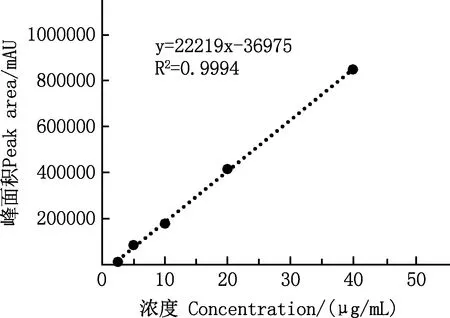
图1 (R,S)-告依春标准曲线Fig.1 Standard curve of epigoitrin

图2 (R,S)-告依春标准品色谱图Fig.2 Liquid chromatogram of epigoitrin standard
2.1.2 精密度、稳定性、重复性和加样回收率试验结果 精密度试验RSD分别为2.68%、1.82%和0.74%,说明建立方法的精密度良好。稳定性试验RSD分别为1.42%、1.72%和2.08%,表明供试品溶液在24 h内稳定性良好。重复性试验RSD分别为1.28%、2.26%和0.98%,表明方法的重复性良好。 加样回收率试验平均回收率分别为100.07%、99.27%和99.85%,RSD分别为1.04%、0.94%和1.78%,说明方法的准确性良好。
2.2 发酵培养基成分的筛选
2.2.1 碳源筛选 由图3A可知,以葡萄糖为碳源的发酵底物中每克中药中(R,S)-告依春含量最高,为0.0178 mg/g,其次为清肺组方中药、可溶性淀粉和甘露醇,分别为0.0177、0.0174和0.0174 mg/g,均显著高于其他碳源(P<0.05),且这几种碳源间差异不显著(P>0.05),综合考虑选择清肺组方中药为碳源。
2.2.2 氮源筛选 由图3B可知,以黄豆粉为氮源的发酵底物中每克中药中(R,S)-告依春含量最高,为0.0176 mg/g,其次是尿素和蛋白胨分别为0.0174和0.0173 mg/g,均显著高于其他氮源(P<0.05),故选黄豆粉为氮源。
2.2.3 无机盐筛选 由图3C可知,以碳酸钙为无机盐的发酵底物中每克中药中(R,S)-告依春含量最高,为0.0175 mg/g,其次是对照氯化钠和硫酸镁,均为0.0174 mg/g,均显著高于其他无机盐(P<0.05),故无机盐选用碳酸钙。
2.3 发酵培养基成分优化
2.3.1 响应面统计模型 按照表1的设计进行试验,根据表2的结果建立回归方程如下:Y=0.018+3.333A×10-4+3.083B×10-4-1.667C×10-4+1.75D×10-4-1.75AB×10-4-1.25AC×10-4+AD×10-4-7.5BC×10-5+7.5BD×10-5-CD×10-4-4.833A2×10-4-7.458B2×10-4-5.833C2×10-4-3.708D2×10-4。
2.3.2 方差分析 二次多项式方差分析表见表3。由表3可知,该模型具有统计学意义,决定系数R2=0.98,调整后的Adj.R2=0.96均较高,失拟项P>0.05,说明模型失拟性不显著,回归模型拟合程度高。其中A、B、C、D、AB、AC、A2、B2、C2和D2对方程影响显著。由各因素一次项F值的大小可知,影响(R,S)-告依春含量的因素主次顺序为A>B>D>C,即碳源影响最大,氮源次之,水和无机盐影响作用较小。
2.3.3 双因素交互分析及最优值预测 二维等高线图与三维效应图见图4。随着中药比例和氮源比例及无机盐和中药比例逐渐增加,(R,S)-告依春含量逐渐升高,并在原点位置达到最高值。经Design Expert软件分析得到的最佳理论培养基成分为药粉30.2%、黄豆粉10.27%、碳酸钙0.198%和水59.91%,此条件下的每克发酵中药中(R,S)-告依春含量为0.0184 mg/g。
2.3.4 验证性试验 结合具体试验条件,最终选取的最佳培养基成分为:中药粉30%、黄豆粉10%、碳酸钙0.2%和水59.8%。 经3次重复固态发酵后,每克固态发酵物中(R,S)-告依春含量分别为0.0184、0.0182和0.0184 mg/g,平均值为0.0183 mg/g,与预测值标准差为0.001。真实值与预测值相吻度好,重现性良好,证明所得最佳培养基成分可靠。

肩标不同字母表示差异显著(P<0.05);肩标相同字母表示差异不显著(P>0.05)Values with different letter superscripts mean significant difference (P<0.05);While with the same letter superscripts mean no significant difference (P>0.05)图3 碳源(A)、氮源(B)和无机盐(C)对发酵中药中(R,S)-告依春含量的影响Fig.3 Effects of carbon source (A),nitrogen source (B) and inorganic salt (C) on the content of epigoitrin in fermented traditional Chinese medicine

表2 试验设计及优化结果

续表
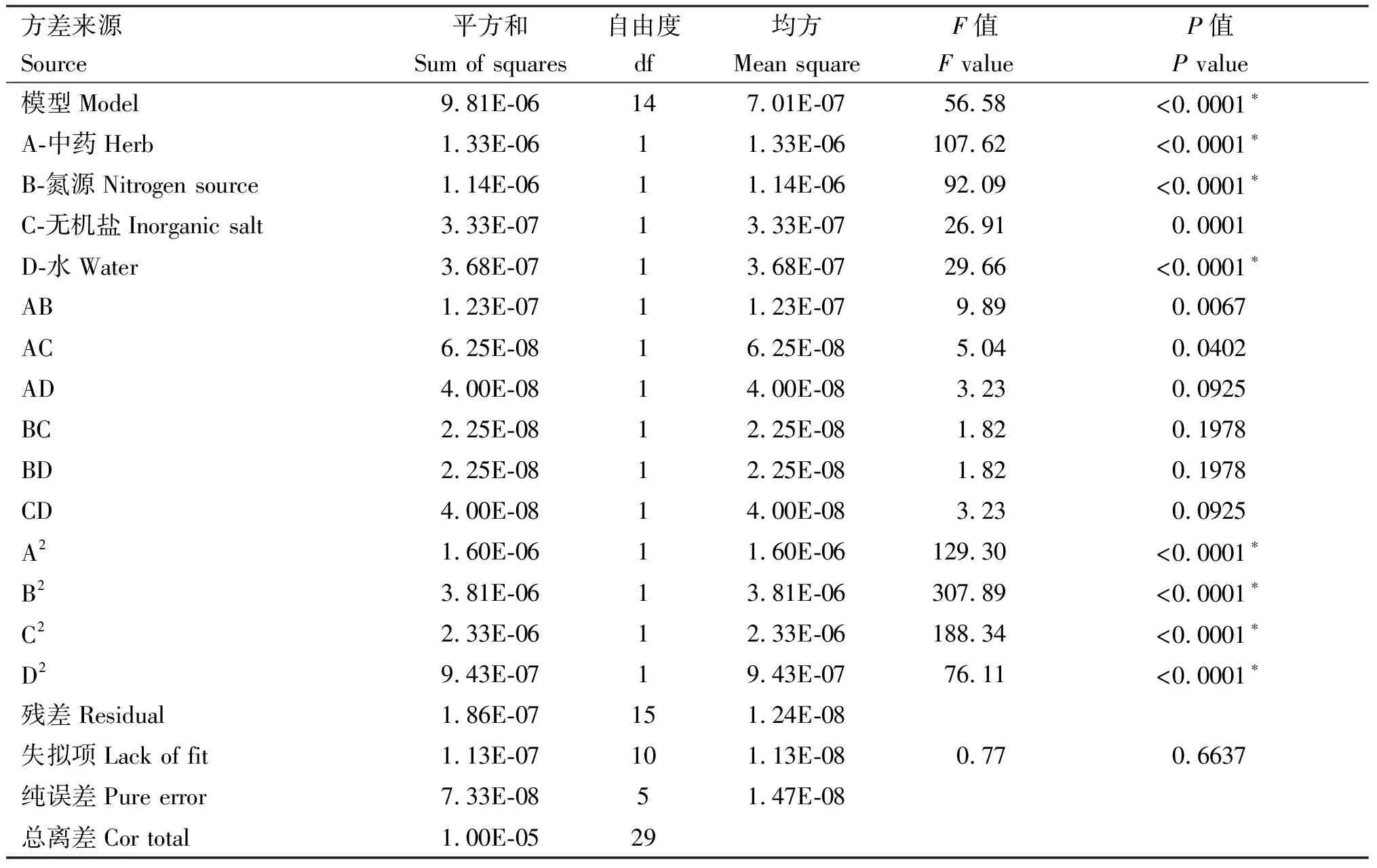
表3 二次多项式模型方差分析表
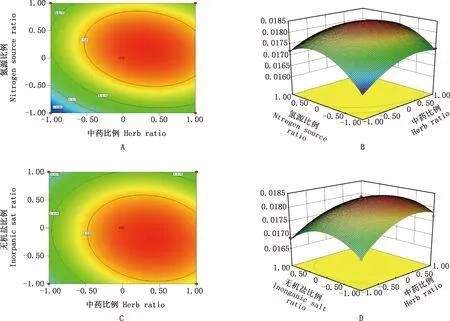
A、B,氮源比例与中药比例间的等高线图与3D效果图;C、D,无机盐比例与中药比例间的等高线图与3D效果图A and B,Contour plots and 3D renderings between nitrogen source and herb ratio;C and D,Contour plots and 3D renderings between inorganic salt and herb ratio图4 各因素与指标之间的等高线图与3D效果图Fig.4 Contour plots and 3D renderings between various factors and indicators
2.4 (R,S)-告依春含量比对
由图5可知,水煎工艺、发酵工艺的出峰时间分别为16.713和16.704 min与标准品出峰时间16.848 min基本相符。发酵后的(R,S)-告依春含量为0.0184 mg/g,发酵前为0.0150 mg/g。在同等条件下,发酵后较发酵前的(R,S)-告依春含量提高了22.36%(P<0.01)。

图5 水煎工艺(A)和发酵工艺(B)中(R,S)-告依春液相色谱图Fig.5 Liquid chromatogram of epigoitrin in decoction process (A) and fermentation process (B)
3 讨 论
芽孢杆菌菌体自身能合成蛋白酶、淀粉酶和脂肪酶,以及可降解饲料中复杂碳水化合物的酶,如果胶酶、葡聚糖酶、纤维素酶等,其中很多是动物本身不具有的酶[12-14]。陶荣霞[15]研究了17株益生芽孢杆菌产酶能力,结果显示,多数菌有产蛋白酶、纤维素酶、半纤维素酶和淀粉酶的能力,只有少数菌株具有微弱的产脂肪酶能力。本试验采用的发酵菌株可产蛋白酶、纤维素酶、木聚糖酶、β-葡聚糖酶、β-甘露聚糖酶和淀粉酶,但不产植酸酶和脂肪酶。
目前,有关益生菌生物发酵的研究报道很多,但多集中在液体发酵,固态发酵较少。王卉等[16]研究解淀粉芽孢杆菌L-S60的固态发酵工艺显示,花生饼粉、麦麸和棉粕的质量比为53∶35∶12,蛋白胨3.0 g/kg,葡萄糖2.0 g/kg,无水硫酸镁0.2 g/kg时每克固态发酵培养物中的解淀粉芽孢杆菌数十分理想。史同瑞等[17]研究解淀粉芽孢杆菌发酵黄芪工艺显示,培养基中含黄豆粉10%、黄芪粉30%、CaCO30.2%、水58.8%时,每克固态发酵培养物中的解淀粉芽孢杆菌数较为理想。秦宇轩等[18]研究解淀粉芽孢杆菌L-H15的固态发酵参数结果显示,豆粕和麦麸质量比为1∶2.8,稻壳20%,蛋白胨0.38%,乳糖0.2%时,每克固态发酵培养物中的解淀粉芽孢杆菌数可达1.68×1010CFU/g。上述研究结果均表明,在提供适当比例的碳源、氮源和无机盐情况下,解淀粉芽孢杆菌可在固体发酵培养物中良好生长。
本研究是对清肺中药组方进行固态发酵,由于中药中含有较多的糖类成分可替代基础培养基中的碳源,故没有另外添加葡萄糖;经解淀粉芽孢杆菌固态发酵提取的清肺颗粒中(R,S)-告依春含量较传统的水煎工艺显著提高。同样有一些益生芽孢杆菌对中药进行固态发酵,获得了药物有效成分含量显著提高的结果。侯美如等[19]利用解淀粉芽孢杆菌发酵黄芪,固态发酵物中多糖含量提高了39.59%,黄酮含量提高41.59%和皂苷含量提高22.63%。白海等[20]采用枯草芽孢杆菌等混合益生菌对中药渣进行固态发酵,固态发酵物中蛋白质含量提高了47.3%,多糖含量提高了1.4%。 丁嘉伟等[21]利用11种混合益生菌对青蒿药渣进行固态发酵,发酵物中获得了更高含量的双氢青蒿酸、青蒿乙素和粗蛋白质。朱庆贺等[22]应用固态发酵技术发酵当归,固态发酵物中的多糖含量达24.91 mg/g,适合产业化推广。但也有研究表明,益生菌的生物发酵会降低中药中某种有效成分的含量。郑言等[23]采用地衣芽孢杆菌对银杏叶进行了固态发酵,结果显示发酵物中粗蛋白质、粗灰分、粗脂肪和粗氨基酸含量均有提高,总黄酮和粗纤维含量却大幅降低。综上所述,合理利用益生菌并采用适宜条件进行固体发酵在饲料添加剂领域和兽药开发领域具有一定的应用潜力。
4 结 论
本试验筛选的固态发酵培养基为清肺组方中药粉30%、黄豆粉10%、CaCO30.2%和水59.8%。37 ℃固态发酵24 h,每克固态发酵培养物中(R,S)-告依春含量达0.0184 mg/g,较传统水煎提取法提高了22.36%,优化的固态发酵基料可促进(R,S)-告依春含等活性成分释放。

