蟾皮标准关键控制指标的研究
程民 代磊 张婷


摘要:目的:建立蟾皮标准的关键控制指标。方法:采用TCL法鉴别蟾皮中华蟾酥毒基,依法测定重金属及有害元素、33种禁用农药、黄曲霉毒素等,UV法测定游离总生物碱的含量。结果:薄层鉴别特征显著,药材重金属及有害元素不合格率为0.07%,33种禁用农药和黄曲霉毒素均合格,游离总生物碱含量在0.05%~0.26%之间。结论:该方法简单可行,专属性强,重复性好,可用于蟾皮的质量控制。
关键词:蟾皮;华蟾酥毒基;游离总生物碱
【中图分类号】 Q969.35+8.6 【文献标识码】 A 【文章编号】2107-2306(2022)03--02
蟾皮为蟾蜍科动物中华大蟾蜍Bufo bufo gargarizans Cantor的干燥皮[1],始载于《本草纲目拾遗》[2],别名有蛤蚆皮、癞蟆皮、干蟾皮等,于夏秋季节捕捉,杀死或烫死,剥取外皮,贴于板上或撑开、干燥,具有清热解毒,利水消胀的功效[3],用于小儿疳积、咽喉肿痛、肿瘤。目前蟾皮的质量标准无国家标准,仅有几个省的地方标准收载且质控指标少、简单,标准不能全面反映和控制蟾皮质量的现状,本研究采用UV法对5-羟色胺成分进行定量分析,TLC法对华蟾酥毒基进行鉴别,重点解决吲哚类生物碱成分质量控制方法的建立,同时按《中国药典》2020年版四部方法对33种禁用农药、重金属及有害元素、黄曲霉毒素等进行考察,最终形成蟾皮多成分控制系统的科学、实用、先进、可控的蟾皮药材质量标准。
1 材料
1.1 主要仪器
Evolution220紫外可见分光光度计(赛默飞世尔科技(中国)有限公司),Agilent 8890-7000D气相色谱-三重四极杆串联质谱仪(安捷伦科技公司),Agilent 1290-6470液相色谱-三重四极杆串联质谱仪(安捷伦科技公司),Agilent 7800电感耦合等离子体质谱仪(安捷伦科技公司),Evolution220紫外可见分光光度计(赛默飞世尔科技(中国)有限公司),Linomat 5卡玛半自动点样仪(CAMAG),TLC Visualizer卡玛薄层色谱数码成像系统(CAMAG),MARS6微波消解仪(培安有限公司),XPE56分析天平(梅特勒-托利多国际贸易(上海)有限公司)。
1.2 主要药品与试剂
蟾皮对照药材(批号:120963-201405,来源中国食品药品检定研究院),华蟾酥毒基对照品(批号:110803-201807,来源:中国食品药品检定研究院),33种禁用农药混合对照品(批号:S057535,来源:天津阿尔塔科技有限公司),30种禁用农药混合对照品(批号:S062923,来源:天津阿尔塔科技有限公司),磷酸三苯酯对照品(批号:120132-202009,来源:上海奈启生物科技有限公司),黄曲霉毒素混合溶液(批号:61001-202006,来源:中国食品药品检定研究院),5-羟色胺盐酸盐对照品(批号:111656-202002,纯度:97.8%,来源:中国食品药品检定研究院);硅胶GF254板(TLC Silica gel 60 F254)(规格:10cm×20cm,厂家:Merck);盐酸、冰醋酸、对二甲氨基苯甲醛等试剂均为分析纯。
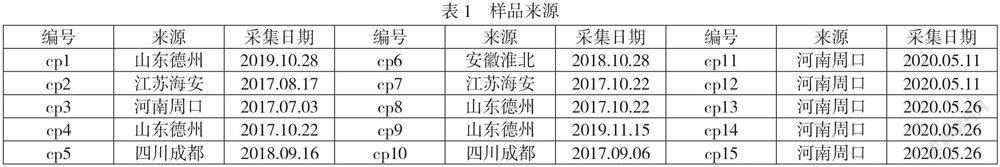
15批蟾皮均经安徽省中药材标准编制工作专家委员会鉴定,见表1。
2 方法与结果
2.1薄层鉴别
取本品粗粉1.0g,加甲醇20ml,超声处理30分钟,滤过,滤液蒸干,残渣加甲醇2ml使溶解,作为供试品溶液。另取干蟾皮对照药材1.0g,同法制成对照药材溶液。另取华蟾酥毒基对照品,加甲醇制成1ml含0.2mg的溶液,作为对照品溶液。照薄层色谱法(《中国药典》2020年版四部 通则0502)试验,吸取上述三种溶液各5~10μl,分别点于同一硅胶G薄层板上,以环己烷-三氯甲烷-丙酮(4:3:3)为展开剂,展开,取出,晾干。喷以10%硫酸乙醇溶液,加热至斑点显色清晰,置紫外灯(365nm)下检视。供试品色谱中,在与对照药材和对照品色谱相应的位置上,显相同颜色的荧光斑点。详见图1。
2.2重金属及有害元素
按《中国药典》2020年版四部2321铅、镉、砷、汞、铜测定法中的电感耦合等离子体质谱法对15个批次的样品进行检查,15批样品中有一批超出《中国药典》2020年版重金属及有害元素标准要求,超标元素为汞元素,不合格率为0.07%,结果见表2。
2.3 33种禁用农药
按《中国药典》2020年版四部通则2341农药残留量测定法第五法(气相色谱-串联质谱法、高效液相色谱-串联质谱法)对15个批次的样品进行检查,15个批次的蟾皮按照《中国药典》2020年版的标准禁用农药残留项均合格,没有超标的存在,但蟾皮中禁用农药检出率为86.7%,该现象可能是蟾蜍在未代谢掉的环境中进食产生了富集现象,结果见表2。
2.4 黄曲霉毒素
按《中国药典》2020年版四部通则2351真菌毒素测定法中的第二法(液相色谱-串联质谱法)对15个批次的样品进行检查,15批蟾皮药材黄曲霉毒素均为未检出,结果见表2。
2.5 游離总生物碱含量测定
2.5.1检测波长的选择
根据蟾皮药材所含成分的理化特性,以及《中国药典》2020年版四部、各地方标准中记载、相关文献报道对蟾皮的研究,使用紫外-可见分光光度计为测定仪器,选定555nm为检测波长。
2.5.2 显色剂用量的选择
制备样品做反应液用量的考察,分别取1.0 ml, 1. 5 ml, 2.0 ml样品液,再分别加1%冰醋酸溶液(1.0 ml, 0. 5 ml, 0 ml)补至2 ml,加入15%对二甲氨基苯甲醛盐酸溶液2 ml,反应30min 后测定,结果3种测定结果近似,无显著性差异,为了减少操作步骤和误差,最终确定选用2.0 ml样品液加入反应液2.0 ml进行反应。
2.5.3 样品的提取方法
取本品粗粉(过10目筛)约300 mg,精密称定,置具塞锥形瓶中,加1%冰醋酸溶液25ml,称定重量,超声处理(功率250W,频率40kHz) 30分钟,取出,放冷,再称定重量,用1%冰醋酸溶液补足减失的重量,摇匀,滤过,取续滤液,即得。
2.5.4 样品浓度与峰面积之间的线性关系考察
精密称取5-羟色胺盐酸盐对照品,用水配制成浓度为0.072mg/ml的浓溶液,摇匀。精密量取0.25 ml、0.5 ml、1.0 ml、2.0 ml、4.0 ml置5ml量瓶中,加入水至刻度,摇匀。取2 ml上述对照品溶液,加15%对二甲氨基苯甲醛盐酸(2→3)溶液2 ml,摇匀,室温放置30分钟,照紫外-可见分光光度法 (通则0401),以相应试剂空白,在555nm的波长处测定吸收度,以吸收度为纵坐标,浓度为横坐标,绘制标准曲线,其回归方程为:y=0.07392+0.01840x,R=0.9967。
2.5.5 精密度试验
精密吸取同一浓度对照品溶液,重复测定6次,进行精密度试验,结果5-羟色胺RSD为0.05%,表明精密度良好。
2.5.6 样品稳定性试验
按供试品溶液的制备方法制备供试品溶液,室温下自然放置,分别于0、15、30、45、60、90、120分钟测定含量,结果样品放置2小时后,RSD为3.08%;0-45分钟的RSD为1.72%,故样品在45分钟内稳定性良好。
2.5.7 样品重复性试验
分别精密称取6份,按照上述样品的提取处理方法,对样品进行提取处理。结果5-羟色胺RSD为0.61%,表明该方法有良好的重复性。
2.5.8 回收率试验
采用加样回收法,精密称取5份已知含量同一批号的样品150 mg,分别精密加入对照品溶液(0.072 mg/ml)5 ml,各加入20 ml1%冰醋酸溶液,称重。超声30 min,补足失重。滤纸过滤后,水性过滤头过滤,各取2 ml上述续滤液,加15%对二甲氨基苯甲醛盐酸(2→3)溶液2 ml,摇匀,室温放置30分钟,照紫外-可见分光光度法 ( 通则0401 ),以相应试剂空白,在555nm的波长处测定吸收度,结果平均回收率为98.57%,相对标准偏差为2.03%,,表明方法准确性良好,结果见表3。
2.5.9 样品含量测定
按上述方法测定各批号蟾皮中游离总生物碱含量,计算含量结果,即得。结果见表7。
3讨论
3.1 TCL条件的筛选 本实验根据文献报道[4][5][6],选用脂蟾毒配基、华蟾酥毒基、沙蟾毒精对照品,比较了三氯甲烷-甲醇(9:1)和环己烷-三氯甲烷-丙酮(4:3:3)展开剂系统,对供试品溶液制备方法、不同点样量、不同点样方式、3种不同厂家薄层版、不同温度不同湿度、预平衡进行了考察,结果个别供试品色谱中,在与脂蟾毒配基、沙蟾毒精对照品色谱相应的位置上,荧光斑点不清晰,分析原因为脂蟾毒配基、沙蟾毒精在蟾皮中含量低,受蟾皮加工方式的影响,会导致脂蟾毒配基、沙蟾毒精在蟾皮中批间差异大,故将此薄层色谱鉴别方法中仅选用华蟾酥毒基对照品,结果该方法专属性、耐用性强,薄层鉴别特征显著。
3.2 超声提取时间的选择
分别精密称取相同重量样品3份,分别加入25ml 1%冰醋酸溶液,称重,以上各样按不同超声时间处理,分别为30 min, 60 min和90 min,超声,补足失重,滤纸滤过,0.45 μm过滤头滤过,各取2 ml续滤液,分别加入15%对二甲氨基苯甲醛盐酸溶液2 ml,反应30min 后测定,于紫外-分光光度计555nm处测定相应吸光度。结果超声30分钟和60分钟含量近似,因此选取超声提取30 min。
参考文献:
[1]国家药典委员会.中华人民共和国药典(四部)[S].北京:中国医药科技出版社,2020:558.
[2]周谧,傅兴圣.不同采收情况与干蟾皮中酯类成分含量对比研究[J].海峡医药,2018,30(10):41-44.
[3]李宝晶,,吳炎,王磊,等.蟾皮中的蟾蜍甾烯类成分及其细胞毒活性研究[J].中草药,2021,52(10):2876-2883.
[4]周谧,傅兴圣,朱琳,等.干蟾皮药材质量标准研究[J].药学与临床研究,2017,25(3):209-212.
[5]喻昌燕,孟令杰,姜念,等.蟾皮化学成分和药理活性的研究进展[J].中草药,2021,52(4):1206-1220.
[6]焦安妮,于敏,李蕾,等.高效液相色谱-串联质谱法测定干蟾皮中华蟾酥毒基和酯蟾毒配基[J].中草药,2019,50(15):3687-3690.

