雷替曲塞联合伊立替康治疗晚期结肠癌患者的疗效及安全性
赵 林
晚期结肠癌患者会出现腹痛、消化道出血、肠穿孔以及肿瘤转移的现象,由于肿瘤的存在可能会导致肠梗阻,引发剧烈腹痛,甚至会因肠管破裂穿孔引起腹膜炎。目前,临床上针对晚期结肠癌的治疗,主要采用奥沙利铂、5-氟尿嘧啶联合治疗方案对患者进行化疗[1]。但对于一线化疗失败的晚期结肠癌患者而言,想要获得更加满意的疗效有较大的难度[2]。雷替曲塞作为一种喹唑啉叶酸类似物,其能够有效抑制肿瘤细胞增殖,在临床上主要用于晚期结直肠癌的治疗。本研究就雷替曲塞联合伊立替康治疗晚期结肠癌患者的疗效及安全性进行分析。现报道如下。
1 资料与方法
1.1 一般资料
选取2018年1月至2019年12月沈阳市肛肠医院收治的50例晚期结肠癌患者作为研究对象,按治疗方案不同分为对照组与观察组,各25例。对照组年龄50~77岁,平均(65.53±4.24)岁,男14例,女11例,ECOG评分0~2分,平均(1.24±0.06)分;观察组年龄47~79岁,平均(65.26±4.31)岁,男15例,女10例,ECOG评分0~2分,平均(1.27±0.08)分。两组患者一般资料比较,差异无统计学意义(P>0.05)。具有可比性。
纳入标准:经病理学检测确诊为晚期结肠癌;经一线化疗方案治疗失败或缓解后再次出现进展;预计生存期≥6个月。排除标准:有化疗禁忌证;预计生存期<3个月。
1.2 方法
对照组患者接受伊立替康、5-氟尿嘧啶、亚叶酸钙治疗。伊立替康(齐鲁制药(海南)有限公司,国药准字H20084571,规格2 ml∶40 mg)350 mg/m2用5%葡萄糖注射液或0.9%氯化钠注射液稀释后,静脉滴注90 min,每3周一次接受治疗;亚叶酸钙(江苏恒瑞医药股份有限公司,国药准字H20000418,规格15 mg×30片),200 mg/m2静脉滴注2 h,第1~5天;5-氟尿嘧啶(南通精华制药股份有限公司,国药准字H32022246,规格10 ml∶0.25 g×5支/盒)400 mg/m2,静脉滴注46 h,连用5 d。
观察组患者接受伊立替康联合雷替曲塞治疗,伊立替康的用药方式、剂量与对照组相同。雷替曲塞(南京正大天晴制药有限公司,国药准字H20090325,规格2 mg),3 mg/m2,用0.9%氯化钠注射液或5%葡萄糖注射液50~250 ml溶解稀释,静脉输注给药,给药时间15 min。21 d为1个周期,两组治疗2个周期。
1.3 临床评价
1)疗效判定标准:完全缓解,病灶完全消失,并持续4周;部分缓解,病灶总面积减少50%以上,持续4周;稳定,可测量病灶总面积减少25%~50%,并持续4周;进展,可测量病灶总面积增加25%以上,或出现新的病灶[3]。治疗有效率(%)=完全缓解例数+部分缓解例数/总例数×100%。2)不良反应:比较两组恶心呕吐、贫血、神经毒性、粒细胞减少、腹泻发生情况。3)生存时间:比较两组生存时间。4)肿瘤标志物:包括糖类抗原199(CA199)、癌胚抗原(CEA)。
1.4 统计学分析
采用SPSS 20.0统计软件进行数据分析,计数资料以百分率表示,组间比较采用χ2检验,计量资料以±s表示,组间比较采用t检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组临床疗效比较
观察组治疗有效率高于对照组,差异有统计学意义(P<0.05)。见表1。

表1 两组患者临床疗效比较
2.2 两组不良反应发生率比较
观察组不良反应发生率低于对照组,差异有统计学意义(P<0.05)。见表2。
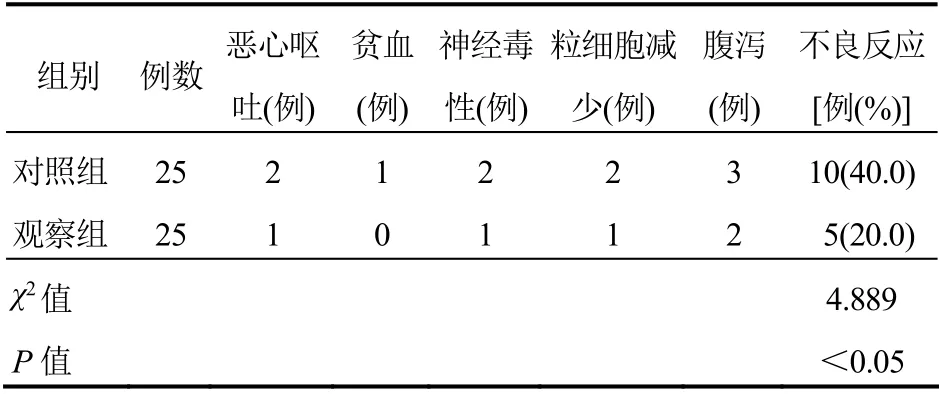
表2 两组患者不良反应发生率比较
2.3 两组生存时间比较
观察组生存时间为(12.03±1.33)d,对照组为(9.06±1.02)d,差异有统计学意义(t=4.519,P<0.05)。
2.4 两组CA199、CEA水平比较
两组治疗前CA199、CEA水平比较,差异无统计学意义(P>0.05);治疗后观察组CA199、CEA水平低于对照组,差异有统计学意义(P<0.05)。见表3。
表3 两组患者CA199、CEA水平比较(±s)
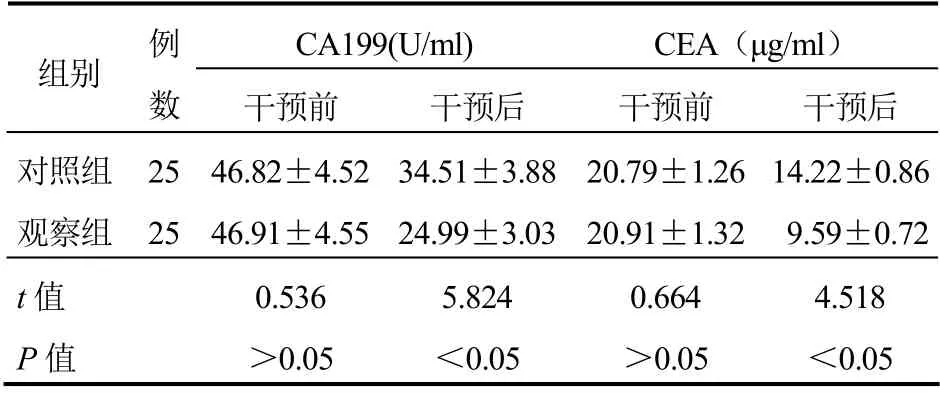
表3 两组患者CA199、CEA水平比较(±s)
CA199(U/ml) CEA(μg/ml)组别 例数 干预前 干预后 干预前 干预后对照组 25 46.82±4.52 34.51±3.88 20.79±1.2614.22±0.86观察组 25 46.91±4.55 24.99±3.03 20.91±1.32 9.59±0.72 t值 0.536 5.824 0.664 4.518 P值 >0.05 <0.05 >0.05 <0.05
3 讨论
结肠癌的病因尚未完全明确,目前认为主要是环境因素与遗传因素综合作用的结果。临床研究显示,结肠癌多发生黏液癌等非典型病理学症状,在RNF43基因变异的结肠癌中,多具有黏液癌和低分化型的病理学症状倾向,而APC基因变异的结肠癌多具有典型大肠癌的高分化型病理学症状[4]。
对于晚期结肠癌患者接受化疗是有效的治疗手段,靶向药物贝伐珠单抗能够在一定程度上延长患者的生存时间,但由于其带给患者沉重的经济负担,因此接受度不高。面对这种情况,针对晚期结肠癌患者的治疗,如何能够在提高疗效的同时保证其安全性是目前临床研究的重点。对于部分晚期结肠癌患者接受一线化疗方案无法获得满意的疗效,需改变治疗方案。目前,对于晚期结肠癌,临床常采用伊立替康治疗,这是因为伊立替康能够影响DNA的合成,导致DNA双链结构断裂,杀灭肿瘤细胞[5]。
在伊立替康的基础上联合雷替曲塞,其作为临床上一种新型喹唑啉叶酸盐类似物,其主要作用机制在于阻断肿瘤细胞DNA合成。DNA合成需胸腺嘧啶脱氧核苷三磷酸盐(TTP),而雷替曲塞其能够抑制胸苷酸合酶活性,而胸苷酸合酶是合成TTP的关键成分之一。与5-氟尿嘧啶相比,雷替曲赛可有效增强对胸腺嘧啶合成酶的抑制能力,有更强的抗肿瘤作用。有研究指出,雷替曲塞作为特异性的胸苷酸合成酶抑制剂,其可作为增敏剂使用,与5-氟尿嘧啶相比,增强效果,协同用于癌细胞治疗的效果更好[5]。雷替曲赛能够借助细胞膜外还原型叶酸盐载体系统,通过将其代谢为多谷氨酸类化合物,可实现在患者体内长时间停留并保持一定的药效浓度,从而控制病情。相关针对雷替曲赛的研究显示,将其用于直肠癌等患者的治疗,可发挥与5-氟尿嘧啶相似的治疗效果,但其不良反应发生率低于5-氟尿嘧啶[6]。本研究结果显示,观察组治疗有效率明显高于对照组。
从安全性角度比较,有研究指出用雷替曲塞的不良反应发生率低于5-氟尿嘧啶,加上使用方法简便,患者更容易接受[7]。本研究结果显示,观察组不良反应发生率低于对照组,提示与伊立替康、5-氟尿嘧啶和亚叶酸钙治疗方案比较,采用雷替曲塞联合伊立替康治疗可获得更加满意的治疗效果,且患者不良反应发生率更低。在尚红娟等[8]的研究中,观察组患者生存时间明显长于对照组;两组患者接受化疗的不良反应以血液系统毒性和消化系统症状为主,且不良反应评级处于Ⅰ~Ⅱ级,观察组患者不良反应发生率低于对照组。在本研究中其发生的不良反应以血液系统和消化系统症状为主,且处于Ⅰ~Ⅱ级。消化系统中常见的不良反应为肝脏转氨酶可逆性升高,通过对其进行保肝等对症治疗或停止化疗后,患者其指标可恢复正常,而在本研究中有1例患者出现较为严重的腹泻,通过给予盐酸哌洛丁胺胶囊以及对症治疗后得到好转,未出现因严重腹泻导致死亡者,而这可能与调整伊利替康的剂量以及加强不良反应监测,积极采取临床对症治疗有关。本研究中,治疗后观察组CA199、CEA水平低于对照组。
临床上采用氟尿嘧啶类药物治疗早期肿瘤患者,但随着临床研究的深入,发现这类药物会使患者出现严重的心脏毒性。而雷替曲赛的疗效良好和不良反应发生率较低,因此临床上逐渐应用雷替曲塞替换5-氟尿嘧啶治疗患者[9]。伊立替康是喜树碱的半合成衍生物,可促使癌细胞凋亡,延长患者生存时间[10]。在本研究中,观察组生存时间长于对照组。
综上所述,针对晚期结肠癌患者采用雷替曲塞联合伊立替康治疗,可获得更加满意的疗效,安全性良好。需要注意的是,由于本研究纳入的样本量较小,临床上仍然需要较大规模的研究来进一步验证雷替曲塞联合伊立替康治疗晚期结肠癌的疗效以及安全性。

