磁性离子印迹聚合物的制备及其对水中Pb(Ⅱ)的吸附
李 娜,祝 方,梁宇坤,叶翠平,梁文静
(太原理工大学 环境科学与工程学院,山西 晋中 030600)
铅作为一种主要的重金属污染物,广泛存在于土壤渗滤液、地下水中,给农作物带来了严重的环境风险。通常处理含重金属废水的方法大致分为化学沉淀法、离子交换法、生物处理法、吸附法和还原法,其中吸附法受到研究者的广泛关注。而离子印迹聚合物(IIP)凭借其选择性高、化学结构稳定、吸附能力强等优点成为水中重金属的优选吸附剂之一。
IIP的制备方法主要有本体聚合、悬浮聚合、沉淀聚合、表面印迹、反相乳液聚合等。例如:LI等通过反相乳液聚合合成了Cd(Ⅱ)-IIP;ZHU等采用表面印迹法合成了一种脲基官能化的Pb(Ⅱ)-IIP;JIANG等采用悬浮聚合法制备了粒径为400 μm的铅离子印迹微球。在这些方法中,反相乳液聚合易于散热,并且产物具有低黏度和高分子量;悬浮聚合得到的产品粒径相对均匀,无需研磨处理。而反相乳液悬浮聚合法可将这两种方法的优点结合起来,无需破乳,聚合物收率高。
近年来,微波辅助作为一种辅助合成手段越来越受到人们的重视。微波辅助可使反应物直接吸收微波,还可通过改变活化能来影响热反应,从而快速、均匀地加热。微波辅助方法的主要优点是简单有效地合成预期材料,因而可使印迹聚合物更加稳定和均匀。ZHU等在微波辐射下通过反相乳液聚合制备了Cd(Ⅱ)-IIP;MUSTAFAI等在微波辐射下通过沉淀聚合制备了As(Ⅲ)-IIP,而传统方法所用时间约为微波法的10倍。
本工作采用微波辅助反相乳液悬浮聚合法制备了磁性离子印迹聚合物(MIIP),对其进行了表征,并将其用于水中Pb(Ⅱ)的吸附。考察了几种单一因素及竞争离子对吸附效果的影响,分析了吸附动力学和吸附等温线,并对吸附剂的重复使用性能进行了研究,以期为实际重金属废水的处理提供参考。
1 实验部分
1.1 试剂和仪器
水杨醛、乙醇、三氯化铁、七水硫酸铁、乙二胺、Span 80、甲苯、乙二醇二甲基丙烯酸酯(EGDMA)、PbCl、甲基丙烯酸(MAA)、MgSO、十二烷基苯磺酸钠(SDBS)、偶氮二异丁腈(AIBN):均为分析纯。
火焰原子吸收光谱仪(TAS-990型,北京普析通用仪器有限责任公司),微波化学反应器(WBFY-205型,巩义市予华仪器有限责任公司),扫描电子显微镜(JSM-7100F型,日本电子株式会社),傅里叶变换红外光谱仪(Tensor 27型,德国Bruker公司),X射线衍射仪(DX2700B型,日本理学株式会社),比表面积分析仪(ASAP 2020型,美国麦克仪器公司)。
1.2 微波辅助反相乳液悬浮聚合法制备MIIP
向三口瓶中加入1.50 mL水杨醛和15 mL乙醇,于303 K搅拌1 h;随后将浴温调至343 K,向三口瓶中加入0.57 mL乙二胺,搅拌1 h,过滤、干燥,得到亮黄色片状水杨醛席夫碱晶体。
将0.298 2 g Span 80、2.0 mL甲苯和16.0 mL EGDMA置于三口烧瓶中,在303 K下剧烈搅拌;然后将3.0 mmol水杨醛席夫碱、1.2 mmol PbCl和5.0 mmol MAA溶解于蒸馏水后加入,搅拌30 min;加入0.5 g FeO(通过三氯化铁和七水硫酸铁制备),将0.308 0 g MgSO和0.871 2 g SDBS溶解于蒸馏水后加入。最后向瓶中加入0.05 g AIBN,置于80 W微波反应器中反应5 min。将产物用稀盐酸溶液连续洗脱,完全洗脱后,用无水乙醇和蒸馏水洗涤,干燥后即可获得Pb(Ⅱ)的MIIP吸附剂。
使用与上述相同的方法,在不添加任何模板离子(即不加PbCl)的情况下获得磁性非印迹聚合物(MNIP)吸附剂。
采用SEM、FTIR、XRD和BET技术对吸附剂进行表征。
1.3 吸附实验
在50 mL PbCl水溶液中加入10 mg MIIP或MNIP,用0.1 mol/L HCl和NaOH调节pH,置于锥形瓶中,在设定温度下振荡吸附一段时间。
为了验证MIIP对Cd、Zn、Cu和Pb的特异识别能力,将Pb与Cd、Zn和Cu分别组成二元混合溶液(均为氯化物溶液),将10 mg MIIP分别加入到50 mL单一离子浓度为60 mg/L的二元混合溶液中,调节pH至6,于303 K振荡吸附60 min。
采用火焰原子吸收光谱仪测定4种金属离子的浓度。
2 结果与讨论
2.1 吸附剂的表征结果
2.1.1 SEM照片和BET分析
图1显示了洗脱前后MIIP的表面形貌。如图1所示:洗脱前的MIIP表面规则均匀,相对光滑,孔隙度较低;与洗脱前相比,洗脱后的MIIP显示出粗糙、不规则和不均匀的外观。这种表面差异可能是因为Pb(Ⅱ)在洗脱剂的作用下被洗脱下来,留下了相对应的孔穴,使得比表面积增大。结合BET数据分析,洗脱后MIIP的比表面积、孔径和孔体积分别为5.283 m/g、2.6 nm和0.09 cm/g,相比于洗脱前(4.647 m/g、2.2 nm和0.06 cm/g)明显增大,增加了特异性识别位点,从而提高了MIIP的吸附性能。

图1 洗脱前后MIIP的SEM照片
2.1.2 FTIR谱图
通过FTIR谱图可以判断吸附剂上官能团或化学键的存在,并验证模板离子与单体之间的反应。如图2所示:在MIIP中观察到的580 cm处的吸收峰归属于Fe—O键的伸缩振动,表明FeO的存在;1 632 cm处的吸收峰归属于C=N键的拉伸振动,表明C=N键在离子印迹聚合物中的配位,这意味着席夫碱与铅离子发生反应;C=O键的存在反映在1 728 cm处的振动吸收峰上;2 953 cm处的伸缩振动峰归属于EGDMA中的C—H键;酚羟基在3 442 cm处的拉伸振动使吸收峰变强;1 258 cm处的吸收峰来自于聚合物的功能单体MAA中的—COOH;1 151 cm和1 457 cm处的拉伸振动分别来自于C—N和CH—N键。FTIR谱图分析结果表明,MIIP的制备是成功的。模板离子与功能单体的反应式可以用下式表示。


图2 MIIP的FTIR谱图
2.1.3 XRD谱图
如图3所示,MIIP的晶体结构通过XRD进行分析,当特征衍射峰的2值为18.32°、30.68°、35.42°、37.34°、43.4°、57.44°和62.48°时,分别对应于FeO和FeO的(111)、(220)、(311)、(222)、(400)、(511)和(440)晶面。图中的4个主峰(35.42°、43.4°、57.44°和62.48°)对应于FeO,表明合成过程对FeO的晶体结构没有影响,这与FTIR光谱结果的描述一致。

图3 MIIP的XRD谱图
2.2 吸附效果的影响因素
2.2.1 初始浓度
在溶液pH为6、吸附温度为303 K、吸附时间为120 min的条件下,Pb(Ⅱ)初始质量浓度对其吸附量的影响如图4所示。

图4 Pb(Ⅱ)初始质量浓度对Pb(Ⅱ)吸附量的影响
由图4可见,当质量浓度从0增至100 mg/L时,MIIP和MNIP对Pb(Ⅱ)的吸附量随之增大;当质量浓度超过60 mg/L时,吸附量达到最大值后保持不变;MIIP对Pb(Ⅱ)的最大吸附量可达107 mg/g,约为MNIP的两倍。上述结果表明,MIIP对Pb(Ⅱ)具有良好的选择性。这是因为在洗脱剂的作用下,模板离子从印迹结构中去除所形成的离子印迹腔可以有效提高Pb(Ⅱ)的亲和力,增加了三维特异性结合位点,同时不规则表面扩大了聚合物的比表面积,使得MIIP的吸附能力增强。
2.2.2 溶液pH
在初始质量浓度为60 mg/L、吸附温度为303 K的条件下,溶液pH对Pb(Ⅱ)吸附量的的影响如图5所示。溶液pH对MIIP上Pb(Ⅱ)的吸附量有着显著影响。随着pH的升高,吸附量逐渐增大;当pH=6时,吸附量最大。这是因为:当溶液呈酸性时,溶液中的H与Pb竞争吸附,使官能团的印迹位点出现质子化,从而大幅减少了吸附量;当pH升高时,官能团发生脱质子反应,活性中心增加,吸附量也随之增加。此外,当pH较高时,OH与Pb易发生反应,溶液呈碱性时则形成沉淀,不利于Pb(Ⅱ)的吸附。因此,选择溶液pH为6较适宜。

图5 溶液pH对Pb(Ⅱ)吸附量的影响
2.2.3 吸附温度和吸附时间
在初始质量浓度为60 mg/L、溶液pH为6的条件下,吸附温度和吸附时间对MIIP上Pb(Ⅱ)吸附量的影响如图6所示。随着温度的不断升高,MIIP对Pb(Ⅱ)的吸附量先升后降,这表明较高的温度不利于MIIP对Pb(Ⅱ)的吸附。随着时间的推移,吸附速率先快后慢,60 min后吸附量基本稳定。这可能是由于MIIP上存在较多未被占据的活性中心,当这些位置逐渐被覆盖时,吸附速率下降,吸附位趋于饱和。因此,选择吸附温度为303 K,吸附时间为60 min较适宜。

图6 吸附温度和吸附时间对Pb(Ⅱ)吸附量的影响
2.3 吸附动力学
分别采用准一级动力学方程和准二级动力学方程(见式(1)和式(2))对图5中的实验数据进行拟合,拟合结果见表1。由表1可见,与准一级动力学方程相比,准二级动力学方程的更高,且的理论值更接近实验值。这表明,准二级动力学模型能更好地描述MIIP对Pb(Ⅱ)的吸附过程。首先Pb(Ⅱ)被吸附在MIIP表面;随着金属离子浓度的降低,表面的Pb(Ⅱ)通过微孔向内部扩散;最后Pb(Ⅱ)主要被吸附在内表面上。

表1 动力学方程的拟合结果

式中:为吸附时间,min;q为时刻的吸附量,mg/g;为平衡吸附量,mg/g;为准一级吸附速率常数,min;为准二级吸附速率常数,g/(mg·min)。
2.4 吸附等温线
在溶液pH为6、吸附温度为303 K的条件下对不同浓度的溶液进行吸附实验,分别采用Langmuir和Freundlich等温吸附模型(见式(3)和式(4))对实验数据进行拟合,拟合结果见表2。Langmuir模型假设吸附表面由单层组成,吸附位点均匀分布,吸附位与被吸附的分子或离子之间不存在相互作用。Freundlich模型代表了非均相模型的体系,不局限于单层。由表2可见,Langmuir模型的值较高,且MIIP的的理论值与实验值接近,说明Langmuir模型较好地模拟了Pb(Ⅱ)在MIIP上的吸附过程,Pb(Ⅱ)离子以单分子层的形式吸附在MIIP表面。
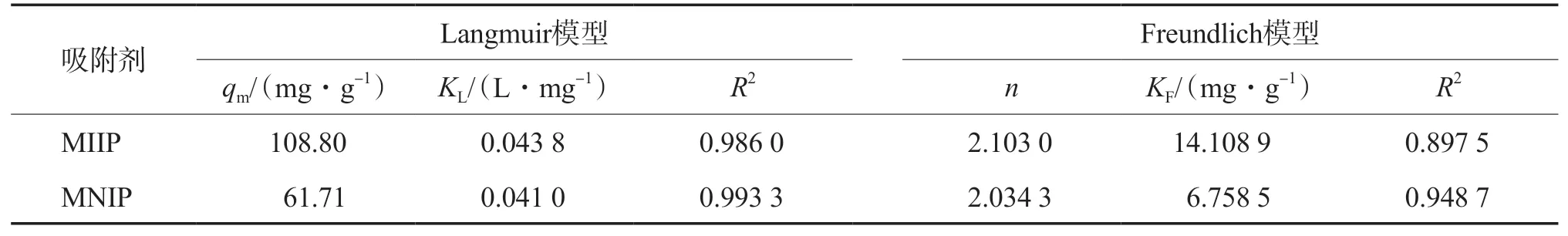
表2 等温吸附方程的拟合结果

式中:为吸附平衡时的质量浓度,mg/L;为最大吸附量,mg/g;为Langmuir吸附常数,L/mg;为Freundlich吸附能力常数,mg/g;为与吸附强度相关的Freundlich常数。
2.5 竞争性吸附
如表3所示,MIIP对Pb(Ⅱ)和3种竞争离子在二元混合溶液中具有不同的识别能力。与其他具有相似电荷和离子半径的竞争离子相比,MIIP对Pb(Ⅱ)的(分配系数)值明显高于其他3种竞争离子,说明MIIP对Pb(Ⅱ)具有特殊的吸附能力。这是因为去除模板离子后,在印迹聚合物表面形成了与Pb(Ⅱ)大小和结构相似的空穴。此外,MIIP对3种竞争离子的值(两种离子的之比)分别为3.7、2.4和2.1,MNIP的分别为0.5、0.2和0.5,这表明MIIP比MNIP具有更好的Pb(Ⅱ)识别和吸附能力。MIIP的这种高亲和力归因于在合成步骤中引入了特定的识别腔,在印迹过程中使用模板离子,使得吸附剂能够选择性地识别二元混合溶液中的Pb(Ⅱ)。

表3 MIIP和MNIP对不同金属离子的吸附特性比较
2.6 吸附剂的重复使用
MIIP用0.1 mol/L HCl洗脱后重复使用,于上述最优条件下吸附Pb(Ⅱ),重复10次结果如图7所示,吸附率为吸附量占首次吸附时的百分比。在重复使用5次后,MIIP的吸附性能没有明显降低;从第6次开始,MIIP的吸附性能略有下降。这表明,洗脱未改变MIIP的化学结构和物理性质,MIIP具有良好的重复使用性能。
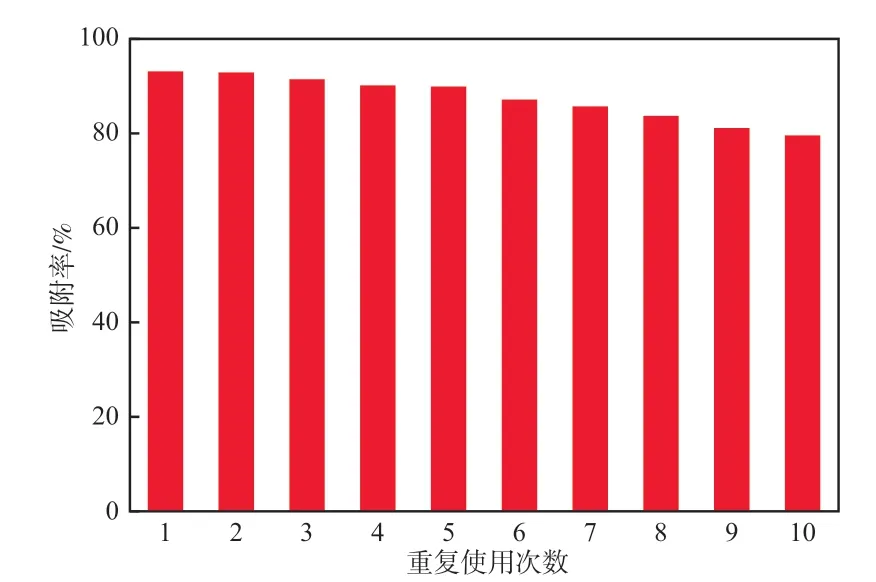
图7 MIIP的重复使用性能
3 结论
a)在初始质量浓度60 mg/L、溶液pH 6、吸附温度303 K、吸附时间60 min的优化条件下,MIIP对Pb(Ⅱ)的吸附量可达107 mg/g。
b)MIIP对Pb(Ⅱ)的吸附过程符合Langmuir等温吸附模型和准二级动力学模型。
c)MIIP能够选择性识别二元金属离子混合溶液中的Pb(Ⅱ),具有很好的Pb(Ⅱ)识别和吸附能力。
d)在重复使用5次后吸附性能没有明显变化,表明MIIP具有良好的重复使用性能。

