基于网络药理学和分子对接探讨“黄芪-黄连”药对治疗儿童肥胖症的作用机制
刘 维,张桂菊,闫文月,吴正雪
(1.山东中医药大学中医学院,山东 济南 250355;2.山东中医药大学第一临床医学院,山东 济南 250011)
肥胖症是热量摄入长期超过消耗,体内未消耗的热量以脂肪的形式储存起来,导致身体脂肪重量超标的代谢性疾病。随着社会发展和生活方式改变,肥胖和超重的人群逐年增多。《中国居民营养与慢性病状况报告(2020年)》显示,我国城乡居民超重肥胖率持续上升,6~17岁、6岁以下儿童青少年超重肥胖率分别高达19 %和10.4 %[1]。有研究表明[2],全球近10 %儿童有肥胖症的困扰。受家庭结构变化的影响[3],国内肥胖和超重儿童正逐年增加,如不进行干预,儿童肥胖大概率会持续到成年,进一步诱发高血压、糖尿病、高脂血症、胰岛素抵抗、心功能受损、非酒精性脂肪肝等疾病[4]。研究表明,肥胖症的产生与全身慢性炎症反应[5]、糖耐量异常[6]、肠道菌群[7]、脂肪细胞的增生与肥大[8]等因素相关。
中国传统医学《黄帝内经》对肥胖进行了论述,“人有肥、有膏、有肉”,“肥贵人则膏梁之疾也”。成人肥胖症的中医分型为:(1)胃腑热盛,(2)脾虚痰湿,(3)脾肾两虚[9]。通过前期研究[10-12],我们发现儿童肥胖与成人病因病机有相似性,又与成人有所不同,不可简单将其视为成人的“缩影”。小儿脾土本不足,加之当下长期高糖高脂饮食的饮食结构,肥甘厚味伤脾,脾主运化功能失常,痰浊膏脂内生,内蕴易化热。儿童肥胖以胃热湿阻、脾虚湿盛证型最为常见,脾肾两虚证所占比例相对较少。
黄芪是豆科植物蒙古黄芪和膜荚黄芪的干燥根部,性温味甘,入肺、脾两经,可益气升阳固表、利水行滞通痹;黄连是毛茛科植物黄连的干燥根茎,性寒味苦,入心、脾、胃、肝、胆、大肠经,可清热燥湿、泻火解毒[13]。黄芪与黄连配伍,二者温寒相宜,补泻兼施,既能益气健脾,又能燥湿化痰,与肥胖症虚实夹杂的病机高度契合。本文应用网络药理学和分子对接相关技术探讨“黄芪-黄连”药对治疗儿童肥胖症,以期为临床广泛使用提供依据。
1 资料与方法
1.1 “黄芪-黄连”活性成分与靶点预测
以“黄芪”“黄连”作为关键词在“中国中药系统药理学数据库与分析平台”(http://tcmspw.com/tcmsp.php,TCMSP)进行搜索,在“Ingredients”界面以口服利用度(oral bioavailability,OB值)≥30 %,类药性(drug-like,DL值)≥0.18[14],进行ADME(药代动力学和药理学)属性筛选,筛选出黄芪和黄连的主要活性成分;之后在TCMSP网站的“Related Targets”面筛选出黄芪和黄连的预测靶点。筛选结束后,通过Uniprot蛋白质数据库最新版(https://www.uniprot.org)对预测靶点进行对照规范,去除非人源基因后,将蛋白质靶点对照为标准基因名称。
1.2 预测儿童肥胖症相关基因靶点
通过人类基因数据库(Gene Cards,https://www.genecards.org)和人类孟德尔遗传基因数据库(OMIM,https://omim.org),以“childhood obesity”作为关键词进行搜索,删除重复值后,筛选出儿童肥胖症(childhood obedity)的基因靶点。
1.3 药物与疾病共同靶点筛选及蛋白互作网络构建
通过R语言编程,筛选出“黄芪-黄连”药对与儿童肥胖症的共同靶点;将共同靶点导入STRING平台[15](https://string-db.org),限定种属为人类(Homosapiens),构建出蛋白相互作用网络(PPI)。
1.4 构建药物-化合物-作用靶点-疾病作用网络图
利用Cytoscape3.7.0软件(http://www.cytoscape.org),对筛选出的“黄芪-黄连”药对中的药物、化合物、靶点以及疾病之间的相互关系构建可视化互作网络图。其中药物、化合物、靶点及疾病用“Node”表示,各节点之间的联系用“Edge”表示。
1.5 GO基因生物过程与KEGG通路富集分析
对核心靶点基因进行GO基因生物过程富集(gene ontology)[16]、KEGG信号通路富集(kyoto encyclopedia of genes and genomes)[17]分析,此过程使用Bioconductor生物信息软件包(http://www.bioconductor.org)处理。并对结果进行可视化处理。
1.6 药物有效成分和疾病核心靶点分子对接验证
从TCMSP数据库下载“黄芪-黄连”药对中主要活性物质的3D结构,以“.mol2”格式保存。PDB数据库(https://www.rcsb.org)下载核心靶点蛋白的3D结构,以PDB格式保存。利用PyMol软件去除核心靶点蛋白的水分子及小分子配体,AutoDock软件对其加氢,加电荷,对受体和配体进行分子对接,通过结合能的数值评价其结合活性。
2 结果
2.1 “黄芪-黄连”活性成分与靶点结果
在TCMSP数据库以OB≥30 %,DL≥0.18为筛选条件进行筛选,检索到“黄芪-黄连”活性成分67个(见表1)。通过TCMSP查询,得到“黄芪-黄连”药对的作用靶点共364个。将得到的主要活性成分利用Uniprot数据库进行筛选,找到各自对应的标准化的基因名,删除无效和重复靶点后,得到作用靶点109个。
2.2 儿童肥胖症的疾病靶点
通过OMIM 和Gene Cards分别获取儿童肥胖症靶点112个、 6541个,整理后共得到6600个儿童糖尿病靶点。
2.3 “黄芪-黄连”药对治疗儿童肥胖症共同靶点筛选及互作网络构建
将药对主要成分靶点和儿童肥胖症靶点进行类比分析,共得到药物与疾病共同作用靶点95个(见表2)。
利用PPI网络对共同作用靶点进行分析,得到85个节点和350条边,对其中蛋白质互作频次最高的30个节点进行统计并绘制图形(见图1)。
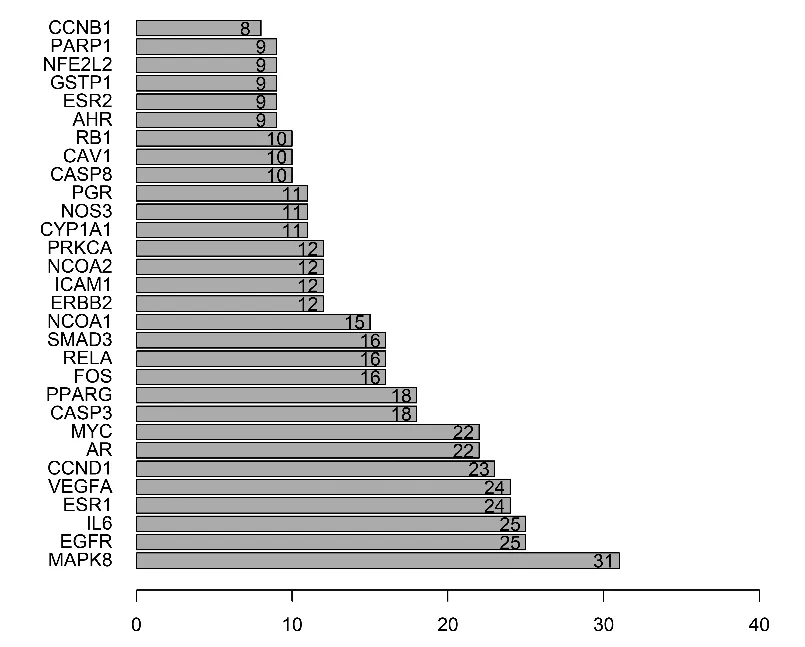
图1 蛋白频次条形图
由图1可见,“黄芪-黄连”药对的中药成分与丝裂原激活蛋白激酶8(MAPK8)、表皮生长因子受体(EGFR)、白细胞介素-6(IL6)有较高的生物结合活性,可作为其治疗儿童肥胖症的潜在靶点。
2.4 药物-化合物-作用靶点-疾病网络
通过cytoscape3.7.0软件构建药物-化合物-作用靶点-疾病调控网络,共得到135个节点(药对1个,疾病1个,核心活性成分38个,靶点95个)和415条线(见图2)。

图2 药物-化合物-作用靶点-疾病网络图
通过“NetworkAnalyzer”工具进行“度值(degree)”分析,选取度值前5的有效成分作为主要活性成分为:quercetin(槲皮素,drgree:73)、kaempferol(山柰酚,drgree:31)、isorhamnetin(异鼠李素,drgree:15)、7-O-methylisomucronulatol(黄芪异黄烷苷,drgree:15)、formononetin(刺芒柄花素,drgree:11)。
2.5 GO基因生物过程富集分析和KEGG信号通路富集分析
使用GO基因生物过程富集分析,得到106条生物过程, P值从小到大排列,取前20条生物过程可视化(见图3)。
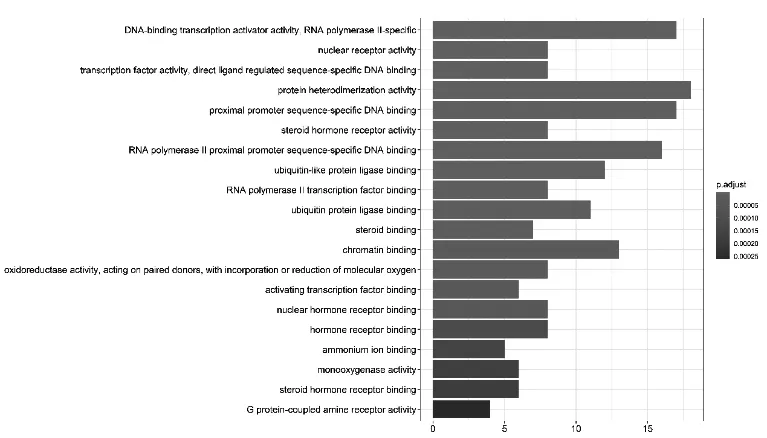
图3 GO功能富集分析图
由图3可见,protein heterodimerization activity(蛋白质异二聚活性)、DNA-binding transcription activator activity,RNA polymerase II-specific(DNA结合转录激活剂活性,RNA聚合酶II特异性)、proximal promoter sequence-specific DNA binding(近端启动子序列特异性DNA结合)、RNA polymerase II proximal promoter sequence-specific DNA binding(RNA聚合酶II近端启动子序列特异性DNA结合)、chromatin binding(染色质结合)、ubiquitin-like protein ligase binding(泛素样蛋白连接酶结合)等生物过程中靶点较为集中。
通过KEGG富集分析,一共得到信号通路119条,取P值最小的25条信号通路可视化(见图4)。
由图4可见,PI3K/Akt signaling pathway(PI3K/Akt信号通路)、Kaposi sarcoma-associated herpesvirus infection(卡波西肉瘤相关疱疹病毒感染)、human cytomegalovirus infection(人巨细胞病毒感染)、MAPK signaling pathway(MAPK信号通路)等是靶基因主要集中的信号通路。

图4 KEGG通路分析
2.6 药对主要活性成分和核心蛋白靶点的分子对接
通过AutoDock1.5.6软件对药对主要活性成分核心蛋白靶点分别进行对接,对接结合能见表3。

表3 药对主要活性成分和核心蛋白靶点对接
其中isorhamnetin(异鼠李素)、formononetin(刺芒柄花素)同丝裂原激活蛋白激酶8(MAPK8)的结合能<-5 kcal/mol。表明异鼠李素(isorhamnetin)和刺芒柄花素(formononetin)与MAPK8具有较好的结合活性[18]。其对接图见图5。
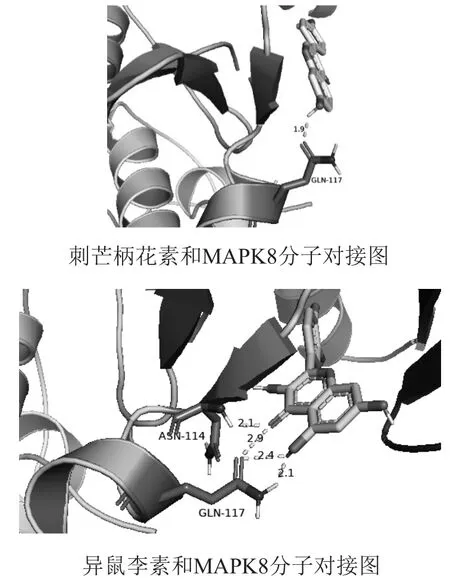
图5 有效成分分子对接图
3 讨论
本文利用网络药理学和分子对接,构建了药物-活性成分-靶点-疾病网络、有效成分分子对接图,对“黄芪-黄连”药对治疗儿童肥胖的作用机制进行了预测。在筛选出的67个活性成分中,quercetin(槲皮素)、kaempferol(山柰酚)、isorhamnetin(异鼠李素)、7-O-methylisomucronulatol(黄芪异黄烷苷)、formononetin(刺芒柄花素)、hydroxytyrosol(羟基酪醇)、Calycosin(毛蕊异黄酮)等化合物在药物调控网络中发挥重要作用。槲皮素可促进巨噬细胞的吞噬功能,影响细胞因子和炎症介质的分泌,发挥抗炎作用[19]。山柰酚通过抑制IKKβ的活化和IκBα的磷酸化来阻止NF-κB(p65)进入细胞核内,使相关炎症介质的释放受影响,抑制肥大细胞炎症反应;山柰酚还使骨骼肌PI3K/Akt-GLUT信号通路阈值增高,改善儿童肥胖症的主要并发症胰岛素抵抗,起到降低血糖的作用[20-22]。异鼠李素可通过激活PI3K/Akt信号通路影响葡萄糖代谢,进而改善肥胖[23]。刺芒柄花素可通过调节血脂代谢,减少脂肪沉积[24-25]。羟基酪醇可减少氧化应激反应和抑制NF-κB的机制调节脂肪细胞基因表达谱,进而减少巨噬细胞聚集并改善儿童肥胖症炎症[26]。毛蕊异黄酮可通过adiponectin-AMPK-eNO途径影响周围血管周围脂肪组织功能[27]。作为药物的潜在作用成分,如hederagenin(常春藤苷)、berlambine(氧化小檗碱)等,可作为未来药理学作用研究的方向。
本次共筛选出95个共同作用靶点,其中有丝裂原激活蛋白激酶-8(MAPK-8)、表皮生长因子受体(EGFR)、雌激素受体(ESR-1)、血管内皮生长因子(VEGFA)、白细胞介素-6(IL-6)等为关键靶点。研究表明MAPK-8对关键靶点为表皮生长因子受体(EGFR)、有丝裂原激活蛋白激酶-8(MAPK-8)、雌激素受体(ESR-1)细胞的增殖、分化、凋亡等过程有影响,进而抑制脂肪细胞分化[28]。EGFR则可以影响细胞的生长、增殖和分化等生理过程[29]。Khristi等[30]发现缺失ESR-1的小鼠更易肥胖。IL-6作为炎症反应的主要介质,与内分泌也有密切关系。Margareta等[31]发现人肥大细胞功能异常可产生IL-6。有研究表明[32-34]促进新的血管生成有利于健康的脂肪组织扩张,并减少脂肪组织炎症。PDGF/VEGF生长因子家族在血管生成和内皮细胞生长中发挥着重要作用,可通过ERK、PI3K/Akt通路诱导内皮细胞增殖、促进细胞迁移、抑制凋亡等[35-36]。统上,“黄芪-黄连”药对可能通过抑制炎症反应、抵抗细胞凋亡、促进细胞增殖、血管生成等主要途径发挥作用。
通过GO富集筛选出的“黄芪-黄连”药对的106生物过程主要以蛋白质异二聚活性、DNA结合转录激活剂活性,RNA聚合酶II特异性、近端启动子序列特异性DNA结合、RNA聚合酶II近端启动子序列特异性DNA结合、染色质结合、泛素样蛋白连接酶结合等为主。通过KEGG富集筛选出的119条信号通路中的靶点富集的前几条通路中,基因数目主要集中在PI3K/Akt signaling pathway、hepatitis B、Kaposi sarcoma-associated herpesvirus infection、human cytomegalovirus infection、MAPK signaling pathway等信号通路。PI3K/Akt通路与代谢关系密切[37-38],其广泛参与和调节合成糖原、脂肪、蛋白质,细胞的存活、增殖和代谢的过程[36]。“黄芪-黄连”药对的有效成分可通过直接作用于PI3K/Akt通路或通过雌激素受体等靶点激活AMPK和mTORC2,进而激活PI3K/Akt通路调节葡萄糖和脂质的代谢[39-41],改善儿童肥胖。
分子对接显示,药对的主要活性成分同细胞有丝分裂、抑制炎症有较好的结合活性,表明“黄芪-黄连”药对通过影响细胞有丝分裂和抑制炎症反应影响儿童肥胖症的发展。
本文利用网络药理学和分子对接的技术方法,对“黄芪-黄连”药对治疗儿童肥胖症的可能作用机制进行了阐述,对其潜在的作用成分、作用靶点、关键生物学过程、关键通路和可能的分子成分进行了论述,为今后中医药治疗儿童肥胖症的研究提供思路。

