石墨烯-铁氰化镍的制备及对H2O2电催化性能研究
丁小会, 陈体伟
(1.河南工程学院环境与生物工程学院 河南 郑州 451191;2.许昌学院化工与材料学院 河南 许昌 461000)
0 引言
石墨烯(Graphene,简称GE)是由一到几个碳原子层厚度的二维蜂窝状碳纳米材料,结构单元是以sp2杂化连接的碳原子构成的六元环。石墨烯具有优异的机械、热学和电学性能,由石墨烯复合材料制成的电化学传感器具有选择性好、灵敏度高、成本低等优点[1]。过氧化氢(H2O2,别名双氧水)是重要工业原料和生物酶促反应的中间产物。通常采用化学修饰电极对其进行检测。铁氰化镍 ( NiHCF) 是一种过渡金属铁氰化物,与普鲁士蓝类似,具有良好的电化学活性,常用于小分子电催化反应的电极材料[2]。铁氰化镍是H2O2电催化还原反应的一种优良的电子媒介体,但其性质不稳定[3],容易受到H2O2分解时产生的OH-的影响[4]。
因此,构建灵敏度高、检测限低、稳定安全的H2O2传感器电极成为当前的研究热点。为了改善生物传感器的电化学性能,过渡金属化合物复合碳基纳米材料就成为理想选择。李春香等采用电化学还原法制得石墨烯/铁氰化镍复合薄膜电极[5],由于二者之间产生的协同效应,使其对NO2-具有优异的电催化活性。马杨等在碳纳米管( CNTs) 修饰的玻碳电极上的基础上,采用循环伏安法合成聚中性红( PNR) /铁氰化镍复合膜,改复合材料对过氧化氢 (H2O2) 表现出优异的电催化性能和协同效应,具有灵敏度高、稳定性好和重现性好等优点,可用于H2O2传感器[6]。为此,本文以热石墨烯为载体,利用一步化学合成法制得石墨烯负载铁氰化镍纳米复合材料,并将其修饰在玻碳电极表面构建了H2O2电化学传感器。
1 实验仪器与试剂
CHI650 E电化学工作站(上海辰华仪器公司),电化学实验采用三电极体系:清洗后的玻碳电极为工作电极,饱和甘汞电极为参比电极,Pt丝电极为对电极。超声波清洗器(昆山市超声仪器有限公司,KQ218),超高速离心机(上海安亭科学仪器厂,TGL-16B),扫描电子显微镜(SEM, Hitachi, S-4800),透射电子显微镜(JEM-2100, JEOL, Japan)。
天然石墨粉(99.995%, 100目)购自Alfa Aesar Company,Ward Hill, MA。30%过氧化氢(AR,天津市科密欧化学试剂有限公司),其他试剂均为分析纯级别,实验用水均为二次去离子蒸馏水。
2 实验步骤
2.1 石墨烯-铁氰化镍的制备
2.1.1 氧化石墨的制备
采用改进的Hummer’s法制备氧化石墨烯(GO)[7]:先将石墨预氧化,称取2 g石墨粉加入含有1 g P2O5和1 g K2SO4的浓硫酸(98%)中,在80 ℃下回流6 h后冷却至室温,小心地用蒸馏水稀释、抽滤,并用水洗至中性,放置在空气中干燥24 h。将得到的预氧化石墨烯加入46 mL冰硫酸中,逐渐加入6 g的KMnO4并不断搅拌(溶液温度不能超过20 ℃),再在35 ℃下搅拌2 h后,加入92 mL蒸馏水。继续加入280 mL水和5 mL 30%H2O2,溶液变为黄褐色,反应终止。将得到的氧化石墨用500 mL的1∶10 HCl清洗以除去金属离子,水洗离心2~3遍,透析至中性,在60 ℃干燥24 h就可得到氧化石墨粉末。
2.1.2 石墨烯的制备
用热退火技术制得还原石墨烯[8],步骤如下:首先将准备好的氧化石墨粉末放在刚玉瓷舟中,然后放入管式炉石英管中,在800 ℃温度下在氩气气氛中保持1 h,得到热还原石墨烯粉末。
2.1.3 铁氰化镍的制备
一步化学沉淀法制备铁氰化镍:首先配制0.05 mol·L-1的K3Fe(CN)6溶液和0.01 mol·L-1的Ni(NO3)2溶液各100 mL,将两者混合后,发现溶液中有橘黄色沉淀生成.将混合液放在磁力搅拌器上搅拌2 h,然后放置在实验台上静置分层一段时间,当溶液中上清液澄清时,将上清液吸出,用离心机分离沉淀物,分离出来的固体即为铁氰化镍产物。最后,将铁氰化镍放于真空干燥箱中,在50~60 ℃下干燥24 h就可得到铁氰化镍固体微粒。
2.1.4 石墨烯-铁氰化镍的制备
具体步骤如下:用电子天平称取0.0394 g的铁氰化镍和0.015 g的石墨烯,将二者混合在试剂瓶中,加入10 mL的DMF,然后将试剂瓶放在超声清洗器里超声5 min,得到石墨烯-铁氰化镍复合物均匀分散悬浮液。
2.2 缓冲溶液的配制11
首先配制0.1 mol·L-1Na2HPO4溶液250 mL,0.1 mol·L-1溶液KH2PO4250 mL,移取150 mL Na2HPO4溶液和225 mL KH2PO4溶液,混合后经pH计仪器校正后得到pH为6.80的缓冲液,作为电化学测试底液。
2.3 石墨烯-铁氰化镍膜电极的制备
将玻碳电极(GC,直径为3 mm)用金相砂纸打磨,并依次用0.3 μm和0.05 μm的Al2O3悬浮液将电极表面抛光至镜面,然后依次用无水乙醇和二次蒸馏水超声清洗5 min, 取出电极用氮气吹干.用微量移液器取10 μL NiHCF@Graphene溶液滴于玻碳电极表面,置于红外灯下晾干,即可得到NiHCF@Graphene电极。
2.4 合成产物的表征
用扫描电子显微镜(SEM) ,透射电子显微镜(TEM)对石墨烯、NiHCF@Graphene的表面形貌特征进行表征。通过傅立叶变换红外光谱(FTIR)技术分析NiHCF结构中的特征红外官能团。
2.5 石墨烯-铁氰化镍的电化学行为
以NiHCF@Graphene修饰的玻碳电极为工作电极,铂电极为辅助电极,饱和甘汞电极为参比电极构成三电极体系,以pH为6.8的磷酸缓冲溶液为底液,在0~1 V电位范围内和100 mV/s扫速下,分别对NiHCF@GrapheneE修饰电极和裸GC电极进行循环伏安扫描以研究电极的电化学性能;在0~1 V范围内以不同的扫描速扫速来研究石墨烯复合物电极的电极反应动力学性能。在恒定还原电位下采用i-t技术检测不同浓度下的过氧化氢电流响应,得到不同浓度过氧化氢与其响应电流的线性拟合曲线。
3 结果与讨论
3.1 石墨烯和石墨烯复合物的形貌表征
图1是石墨烯的SEM和TEM。从图1(a)可以看出,制备的石墨烯呈薄片状,表面分布有大量的褶皱,这是由于石墨烯碳原子的π-π共轭作用引起的局部团聚现象,而典型的褶皱形貌结构是使二维石墨烯能够得以稳定存在的根本原因。从图1(b)可以看出,合成的石墨烯片层呈现出褶皱状的薄面纱形貌,这种结构特征使得石墨烯具有大的比表面积,从而为提高铁氰化镍纳米微粒的负载量提供了良好的基体支撑,这也表明成功制备了还原石墨烯。

图1 石墨烯的SEM(a)和TEM(b)
为了进一步观察石墨烯-铁氰化镍复合物中NiHCF和Graphene的分布状态,以及两者的微观结构形貌,通过SEM和TEM对石墨烯-铁氰化镍复合物的表面和结构进行了表征。图2(a)是NiHCF-GE复合物的SEM图,可以看出石墨片层的表面上均匀分散着很多细小的颗粒,也说明NiHCF颗粒很好地分散在石墨烯表面。图2(b)是NiHCF-GE复合物的TEM图,可以看出NiHCF纳米颗粒以一种无序的松散状态分散在石墨烯片层表面,NiHCF基本上以颗粒状存在,平均粒径在20 nm左右。

图2 石墨烯-铁氰化镍的SEM(a)和TEM(b)
3.2 铁氰化镍的红外表征
如图3铁氰化镍的傅里叶变红外光谱(FTIR)所示,在2097.9 cm-1出现了一个强吸收峰,该吸收峰对应于铁氰化镍中Ni-C-N-Fe键的伸缩振动模式,表明已经成功制备了铁氰化镍纳米微粒。在3434.7 cm-1处也出现了一个强吸收峰,该吸收峰对应水中O-H的伸缩振动模式,这可能是在研磨铁氰化镍和溴化钾固体时,由于溴化钾极易吸潮导致的。
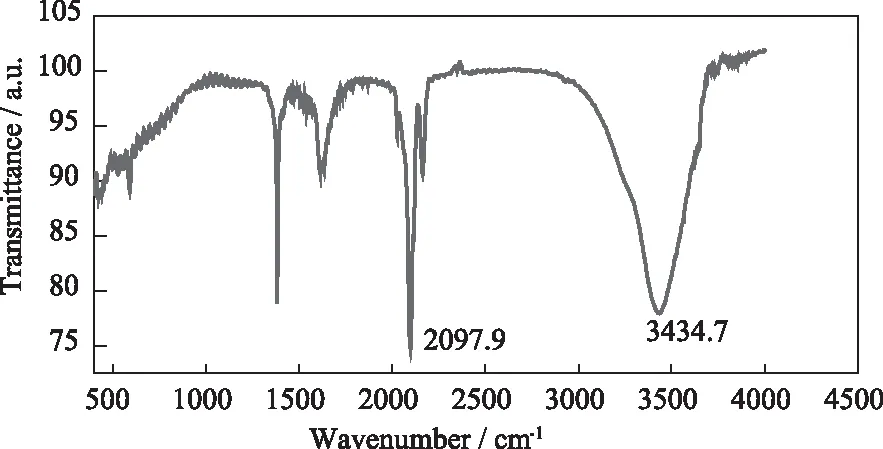
图3 铁氰化镍的红外光谱(FTIR)
3.3 石墨烯-铁氰化镍的电化学性能研究
3.3.1 铁氰化镍的电化学性能研究
图4中a曲线是铁氰化镍修饰的膜电极在10.0 mL磷酸盐缓冲液中,电位0~1 V范围内和100 mV/s扫速下扫描的循环伏安曲线;b曲线是GC裸电极在同等条件下的循环伏安曲线.可以看出,曲线(a)中GE-NiHCF修饰电极有一对很明显的氧化还原峰,曲线(b)没有明显的氧化还原峰,这说明铁氰化镍纳米微粒成功地负载在石墨烯表面。
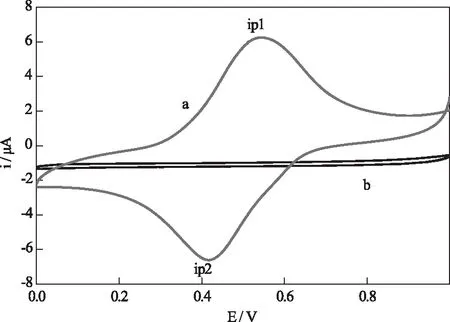
图4 铁氰化镍电极(a)与裸电极(b)在磷酸盐溶液中的循环伏安曲线
[Fe(CN)6]3-与[Fe(CN)6]4-是典型的可逆氧化—还原体系。进行伏安测定时,用铁氰化镍修饰的膜电极作为工作电极,铂片电极作为对电极,饱和甘汞电极作为参比电极,进行阴极扫描时,发生还原反应;进行阳极扫描,发生氧化反应。由于氧化峰比还原峰电位更偏正,所以ip1是氧化峰,ip2是还原峰,正向电流ip1对应着NiHCF膜的氧化和K+从膜中释放,而负向电流ip2表明NiHCF膜的还原和K+离子嵌入膜内,原理为


还原与氧化过程中电荷转移的速率很快,因此循环伏安图中阴极峰与阳极峰是对称的。
3.3.2 石墨烯-铁氰化镍修饰电极的稳定性及重现性
在最佳实验条件下,将NiHCF-GE/GC电极置于10.0 mL磷酸盐缓冲液中,在电位0~1 V 范围内,以100 mV/s的扫速进行连续循环伏安法扫描,50圈后峰电流几乎不变。电极于室温下干态放置30 d再一次进行测试,复合物修饰电极的氧化还原峰电流几乎不发生变化,表明NiHCF-GE在GC电极表面具有很好的稳定性和重现性。
3.3.3 不同扫速对石墨烯-铁氰化镍修饰膜电极的电化学行为的影响
图5是NiHCF-GE电极在10.0 mL磷酸盐缓冲液中溶液中于不同扫速(扫描速率:100、300、500、600、700、800、900 mV/s)时的循环伏安曲线。可以看出,氧化还原峰电流均随扫速的增加而增加,氧化峰电位随着扫速的增加逐渐向右移动。

图5 NiHCF-GE在不同扫速下的循环伏安图
根据电化学理论,对于扩散控制的电极过程,峰电流ip与扫描速度的平方根呈正比关系,即ip~v1/2为一直线。对于表面吸附控制的电极过程,峰电流ip与扫描速度的一次方呈正比关系,即ip~v为一直线。从图6中可以看出,还原峰的峰电流与v1/2呈线性关系,相关系数r=0.9970,说明 NiHCF-GE在CG电极表面的电化学反应过程受扩散控制的。这是由于K+作为平衡离子可以在 NiHCF-GE 薄膜的孔道中嵌入和脱出,即氧化时平衡离子从孔道中脱出;还原时平衡离子嵌入到孔道中去,电极反应速率的快慢与K+平衡离子扩散到电极表面的速率有关[9]。也就是说在高扫速下,扩散速率是电极反应的决速步骤。
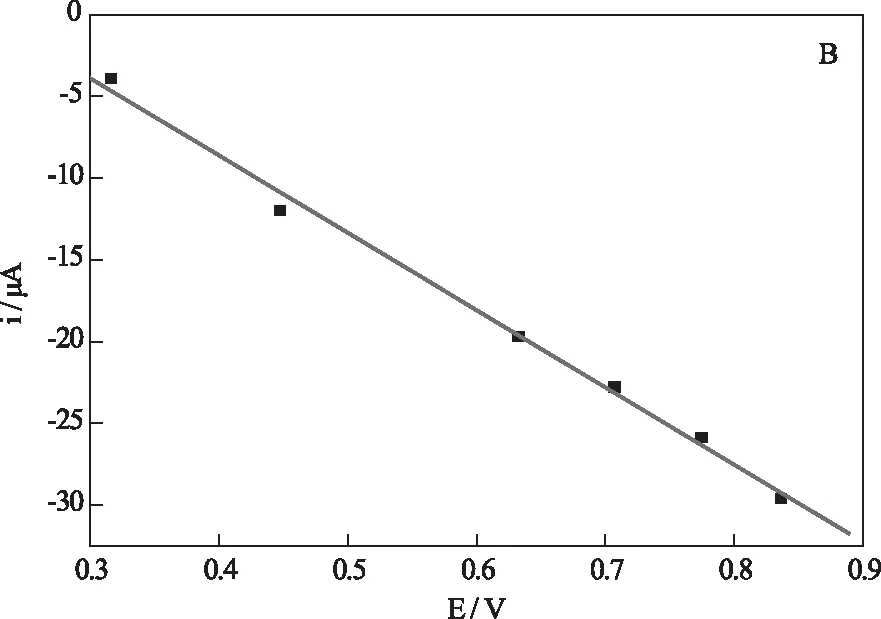
图6 还原峰电流ip与扫速v1/2线性关系图
3.3.4 石墨烯-铁氰化镍膜修饰电极对过氧化氢的响应
图7为向不断搅拌(搅拌速度为200 rpm)的10.0 mL磷酸盐缓冲液中每100 s加入0.1 mol·L-1过氧化氢10 μL时的i-t曲线图。可以看出,曲线上出现了良好的电流响应,响应时间小于10 s,随着H2O2逐渐加入,电流以台阶状逐渐升高,符合稳态电流的特征。由图8可以看出,当H2O2浓度在1×10-4~8×10-4mol·L-1范围内呈现出良好的线性关系,相关系数r=0.9938,说明石墨烯-铁氰化镍膜修饰电极能够实现对过氧化氢的快速、高灵敏度检测。
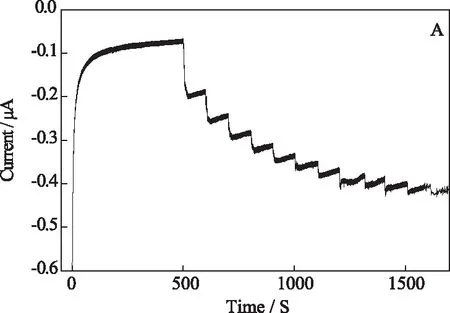
图7 NiHCF-GE电极对不同浓度H2O2的i-t图

图8 NiHCF-GE电极对H2O2 的校正曲线
4 结论
通过化学合成法一步制得石墨烯-铁氰化镍,具有条件温和、操作简单、绿色环保、能耗低等优点。该实验通过石墨烯-铁氰化镍膜修饰电极对过氧化氢的电催化性能研究,发现石墨烯-铁氰化镍复合物对过氧化氢的检测有快速、高灵敏性的特点,有望构建一个对过氧化氢高灵敏度检测的电化学传感平台。该研究有助于石墨烯-铁氰化镍材料的广泛应用。

