扶正补血食疗方含药血清干预Notch通路调控骨髓造血干细胞化疗后损伤的机制研究
汪旭,郝晓蓓,杨敏,潘娅岚,王庆,徐桂华
(南京中医药大学,江苏 南京 210023)
恶性肿瘤是全世界面临的重大健康问题,其发病率和病死率正在迅速上升[1]。目前化疗仍为恶性肿瘤临床治疗的主要措施,但约有80%的患者在此过程中会出现骨髓抑制[2],表现为贫血、出血、免疫力降低等不良反应,影响化疗的疗效甚至导致患者死亡[3]。化疗诱导造血干细胞(hematopoietic stem cells,HSCs)的衰老,造成其自我更新能力受损,这是骨髓抑制发生最为关键的机制[4]。造血微环境(即造血龛)主要包括基质细胞、细胞因子、细胞外基质等,参与支持和调控造血干细胞的自我更新、静息、凋亡等功能[5]。间充质干细胞(mesenchymal stem cells,MSCs)可分泌不同细胞因子和传递信号分子,具有免疫调节和支持造血的功能,是造血微环境中的重要成员之一[6-7]。临床发现通过MSCs 和HSCs 共移植能够促进造血微环境恢复[8]。同时,MSCs 与HSCs 体外共培养,对HSCs 体外增殖具有明显的积极作用[9]。研究发现Notch 信号通路可调控HSCs的自我更新能力,其受体和配体高表达于造血微环境和HSCs 中,同时Notch 通路在调节细胞增殖、分化过程中具有极为重要的作用[10]。
近年来基于多组分和多靶点的中医药治疗骨髓抑制已引起广泛关注,与口服升白药等现代医学治疗药物相比,毒副作用小,可明显改善患者的骨髓抑制症状,提升其生活质量。中医食疗是中医药学的重要组成部分,以食助药力、药助食威。研究表明中医食疗应用于化疗后骨髓抑制,是“药、食、养”结合,临床疗效确切,同时具有简单方便、适口性好的优势[11]。课题组在总结前期由黄芪、当归、猪蹄为主要成分的归芪猪蹄食疗方改善化疗后骨髓抑制临床疗效和对造血微环境保护作用的基础上[12-14],基于“精气血”互生理论进行了处方优化,加入黄精组成扶正补血食疗方,提出扶正补血食疗方可能对化疗后HSCs发挥保护作用,因此本研究拟通过5-FU 损伤小鼠骨髓间充质干细胞(bone marrow-mesenchymal stem cells,BMSCs)和HSCs 体外共培养模型,观察扶正补血食疗方含药血清对模拟“造血龛”中HSCs 增殖、凋亡以及Notch 信号通路基因表达的影响,初步探讨扶正补血食疗方调控骨髓造血功能的分子机制。
1 材料
1.1 实验动物
SPF 级SD 大鼠20 只,雄性,3~4 周龄,体质量(180 ± 20)g,购买于杭州医学院,合格证号:SCXK(浙)2019-0002。SPF 级C57BL/6 小鼠,4~6 周龄,雄性,体质量18~20 g;购于南京青紫兰科技有限公司,合格证号:SCXK(苏)2016-0010。于南京中医药大学实验动物中心进行饲养,自由饮食、饮水,室温(22 ±2)℃,湿度40%~60%,并已经获得南京中医药大学伦理委员会批准(批准号:201910A018)。
1.2 实验用试剂
DMEM-F12 培养基(美国,HyClone);胎牛血清(美国,Gibco);青霉素-链霉素(美国,Gibco);0.25%胰蛋白酶(上海,碧云天生物技术有限公司);CD29-FITC,CD44-FITC,CD117-APC(美国,eBioscience);5-Fluorouracil(德国,Sigma);Cell Counting Kit-8(日本,同仁);细胞周期检测试剂盒(江苏凯基生物技术股份有限公司);细胞凋亡检测试剂盒(南京福麦斯生物技术有限公司);Ficoll 分离液(天津,TBD);CD117 MicroBeads,mouse(德国,Miltenyi Biotec);mouse SCF,mouse IL-3(上海,novoprotein);TRIzol 试剂(美国,ABI);逆转录试剂盒,qPCR 试剂盒(湖南艾科瑞生物工程有限公司)。
1.3 实验用仪器
CO2培养箱(日本,Panasonic);垂直超净工作台(苏州安泰空气技术有限公司);Gallios 型流式细胞仪(美国,Beckman);MACS 免疫磁珠分选系统(德国,Miltenyi Biotec);Synergy H1MD 型多功能酶标仪(美国,Bio-Tek);DMi8型倒置荧光显微镜(德国,Leica);5810R 型高速冷冻离心机(德国,Eppendprf);Step One Plus 实时荧光定量PCR仪(美国,ABI)。
2 方法
2.1 扶正补血食疗方含药血清制备
扶正补血食疗方中当归:黄芪:黄精:猪蹄质量比例为1∶5∶2∶60。取猪蹄1 200 g洗净切块,放入砂锅并加水煮沸,去除浮沫洗净后再加入1 800 mL 清水,煮沸后改用文火熬制2.5 h。取当归20 g、黄芪100 g、黄精40 g 加水浸泡0.5 h 后加入猪蹄汤内,先大火煮沸10 min,后改文火煎50 min,过滤残渣并置4 ℃过夜。第2天去除上层油脂,放入37 ℃水浴,旋蒸浓缩至生药浓度为0.504 g/mL,分装后置于4 ℃保存备用。相关药材购于江苏省中医院,经南京中医药大学中药鉴定教研室鉴定质量合格,猪蹄购于南京市内超市,具有食品合格证书。
20 只SD 大鼠随机分为灌胃组和空白组,适应性喂养1 周后,按照1 mL/100 g 剂量灌胃,灌胃组灌服扶正补血食疗方,空白组灌服等体积生理盐水,并于每天上午9 时灌胃1 次,连续7日。于末次灌胃1 h 后腹主动脉取血,室温静置2 h,3 000 r/min 离心20 min,取上清并于56 ℃水浴30 min,过滤除菌后,分装冻存于-80 ℃保存备用。
2.2 小鼠骨髓间充质干细胞体外培养、传代及鉴定
取4~6 周龄雄性C57BL/6 小鼠,脱颈处死,放入75%乙醇中浸泡3~5 min,无菌条件下分离双侧胫骨和股骨,剪去两侧骨端,用培养基反复冲洗骨髓腔至骨髓腔变白,吹打均匀后接种于60 mm无菌培养皿中,置于37 ℃、5%CO2饱和湿度的培养箱中培养。48 h 后全量换液,随后每2~3 d 换液1 次,细胞长至70%~80%融合时,按1∶2 消化传代,传至第3 代后备用。收集第3 代的小鼠骨髓间充质干细胞,调整细胞数为1 × 106个/管,分别加入抗小鼠CD29-FITC,CD44-FITC,CD117-APC,4 ℃避光孵育30 min 后,PBS 洗2次,流式细胞仪检测。
2.3 小鼠骨髓CD117+造血干细胞免疫磁珠分选及鉴定
同“2.2”项下方法获得骨髓细胞后,过200 目滤网,450 ×g离心10 min,弃上清。用1 mL 无菌PBS 重悬,加入2 mL 小鼠Ficoll 分离液中,400 ×g离心30 min。收集第二层环状乳白色细胞层并加入PBS 重悬,400 ×g离心10 min。运用MACS 免疫磁珠分选系统分选CD117+细胞。调整细胞数为1×105每管,加入抗小鼠CD117-APC,4 ℃避光孵育30 min 后,PBS 洗2 次,流式细胞仪检测。剩余HSCs 用DMEM-F12 培养基(含10% FBS、25 ng/mL SCF、25 ng/mL IL-3、1%青霉素-链霉素)重悬,调整细胞密度为1 × 106个/mL接种于培养瓶中,置于培养箱内培养。
2.4 共培养细胞分组
选择对数生长期的小鼠BMSCs,按1.5×106个/孔种植于6孔板,待细胞贴壁之后,换无血清DMEM/F12培养基使细胞生长同步化12 h,干预24 h后将“2.3”项下方法分离提取的CD117+细胞按5 × 105个/mL 与下面3 组BMSCs进行共培养。随机分为以下3组:空白组,BMSCs+10% 空白血清;5-FU 组,BMSCs+10% 空白血清+50µg/mL 5-FU;扶正补血食疗方含药血清组,BMSCs+10%扶正补血食疗方含药血清+50µg/mL 5-FU。共培养48 h以后收集CD117+细胞做后续相关检测。
2.5 CCK-8法检测小鼠骨髓造血干细胞增殖
按“2.5”项下方法进行细胞分组,将小鼠BMSCs和HSCs种植于24孔板中,每组设3个复孔,其中BMSCs为5 × 104个/孔、HSCs 为1 × 104个/孔。收集各组悬浮的CD117+细胞,每孔样本单独离心,加入无血清DMEM/F12培养基重悬混匀后添加至96孔板中,并加入CCK-8试剂10µL/孔,于37 ℃CO2敷箱中孵育5 h,使用酶标仪在450 nm处的吸光度值,实验重复3次取平均值。
存活率(IR)=[(实验组OD 值均数-空白组OD 值均数)/(对照组OD值均数-空白组OD值均数)]×100%
2.6 流式细胞术分析小鼠骨髓造血干细胞的细胞周期
收集各组悬浮的CD117+细胞,PBS 洗涤2 次,离心去上清,加入500µL 70%冷乙醇4 ℃固定2 h。染色前用PBS,1 000 rpm 离心3 min 洗去固定液,加入500µL PI/RNase A 工作液(RNase A∶PI比例为1∶9),室温避光孵育30 min,上流式细胞仪分析CD117+细胞的细胞周期。
2.7 流式细胞术分析小鼠骨髓造血干细胞的细胞凋亡
收集各组悬浮的CD117+细胞,用预冷的PBS 洗细胞2 次,用100µL 缓冲液重悬细胞,加入5µL Annexin V/Alexa Fluor 647 和10µL 20µg/mL 的碘化丙锭溶液,混匀后于室温避光孵育15 min,在管中加400 µL PBS混匀后上机,流式细胞仪分析。
2.8 qRT-PCR 检测小鼠骨髓造血干细胞中Notch 信号通路相关的基因表达
收集各组悬浮的CD117+细胞,PBS 洗涤2 次,采用TRIzol法提取CD117+细胞的总RNA,检测RNA 浓度和纯度并逆转录成cDNA,以GAPDH 作为内参,做qRTPCR 检测骨髓造血干细胞中Notch 信号通路相关的基因表达,所用引物序列见表1,采用2-△△T法计算均值作为相对表达量。

表1 引物序列
2.9 统计学分析
采用SPSS 25.0软件进行对数据分析,结果用±s表示,满足正态性和方差齐性的计量资料采用单因素方差分析;方差不齐者采用Dunett′s T3检验,不符合正态性者采用Kruskal-Wallis H 非参数检验。以P<0.05为差异具有统计学意义。
3 结果
3.1 小鼠骨髓间充质干细胞的分离、培养及鉴定
原代培养48 h 后绝大部分细胞已经贴壁,并呈现多角形、梭形、圆形等不均一的细胞形态等(见图1A)。培养6~8 d后,细胞大部分呈扁平形或纺锤形,细胞融合达50%~60%(见图1B)。传至第3 代后细胞主要呈长梭形排列,细胞基本在24 h内贴壁,不规则杂细胞较少,间充质干细胞逐渐纯化(见图1C)。流式细胞术检测小鼠BMSCs 中97.5%呈CD29 阳性,98.8%呈CD44阳性,仅0.17%呈C-kit阳性(见图2A~C)。
3.2 小鼠CD117+细胞的形态及鉴定
倒置显微镜观察分选出的小鼠骨髓造血干细胞体积偏小,细胞形态为圆形(见图1D),行台盼蓝染色后99%细胞拒染。流式细胞术检测小鼠HSCs 中90.3%呈CD117 阳性(见图2D)。
3.3 共培养各组细胞形态
共培养空白组可见底层小鼠BMSCs 细胞呈梭形生长,排列紧密,融合度高;小鼠CD117+细胞为圆形细胞,成团或单独悬浮生长于底层细胞表面,少数散落在底层小鼠BMSCs 间隙中(见图3A)。共培养5-FU 组可见底层小鼠BMSCs 细胞形状不规则,小鼠CD117+细胞呈圆形悬浮生长于底层细胞表面,数量均显著减少(见图3B)。共培养扶正补血食疗方含药血清组底层小鼠BMSCs 和小鼠CD117+细胞形态和生长状态基本同共培养5-FU 组,但细胞数量明显增加(见图3C)。
3.4 CCK-8法检测小鼠骨髓造血干细胞增殖
与空白组相比,5-FU 组小鼠CD117+细胞活性显著降低(P<0.05);与5-FU 组相比,扶正补血食疗方含药血清干预后明显促进小鼠CD117+细胞增殖(P<0.05)。见表2。
表2 扶正补血食疗方含药血清对HSCs细胞增殖的影响(±s,n=3)

表2 扶正补血食疗方含药血清对HSCs细胞增殖的影响(±s,n=3)
注:与空白组比较,1)P <0.05;与5-FU组比较,2)P <0.05。
组别空白组5-FU组扶正补血食疗方注A450nm 3.30±0.44 1.15±0.061)1.81±0.192)存活率(%)-0.32±0.031)0.54±0.022)
3.5 流式细胞术分析小鼠骨髓造血干细胞细胞凋亡和细胞周期
与空白组相比,应用5-FU 刺激后小鼠CD117+细胞总凋亡率显著增加(P<0.05);而小鼠CD117+细胞经扶正补血食疗方含药血清处理后,含药血清组的细胞总凋亡率下降(P<0.05)。与空白组相比,5-FU 组小鼠CD117+细胞的G0/G1 期细胞占比明显增加(P<0.05);与5-FU 组比较,扶正补血食疗方含药血清组的G0/G1 期细胞占比减少(P<0.05),这表明共培养条件下5-FU 组的小鼠CD117+细胞出现G1 期阻滞,而扶正补血食疗方含药血清干预抑制了小鼠CD117+细胞的休眠状态,细胞周期更加活跃。见表3。
表3 扶正补血食疗方含药血清对HSCs细胞凋亡和细胞周期阻滞的影响(±s,n=3)

表3 扶正补血食疗方含药血清对HSCs细胞凋亡和细胞周期阻滞的影响(±s,n=3)
注:与空白组比较,1)P <0.05;与5-FU组比较,2)P <0.05。
组别空白5-FU扶正补血食疗方G0/G1期(%)49.82±0.67 55.44±0.141)52.68±0.072)凋亡率(%)5.81±0.75 27.69±2.211)13.77±1.312)
3.6 qRT-PCR 检测小鼠骨髓造血干细胞中Notch 信号通路相关的基因表达结果
与空白组相比,5-FU 组小鼠CD117+细胞Jagged1、Notch1、Notch2 基因表达降低(P<0.05),经扶正补血食疗方含药血清干预,含药血清组细胞Jagged1、Notch1、Notch2 基因表达均增加(P<0.05)。见表4。
表4 扶正补血食疗方含药血清对HSCs中Notch mRNA表达水平的影响(±s,n=3)
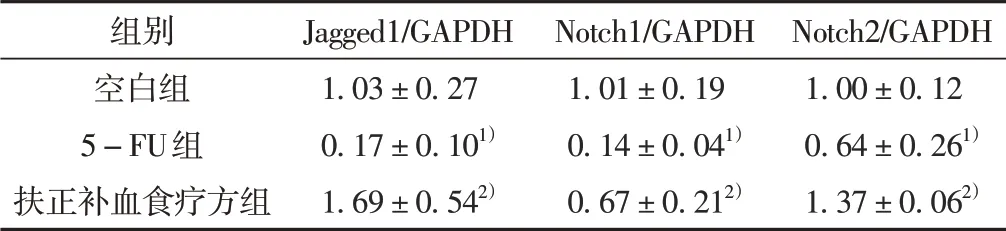
表4 扶正补血食疗方含药血清对HSCs中Notch mRNA表达水平的影响(±s,n=3)
注:与空白组比较,1)P <0.05;与5-FU组比较,2)P <0.05。
组别空白组5-FU组扶正补血食疗方组Jagged1/GAPDH 1.03±0.27 0.17±0.101)1.69±0.542)Notch1/GAPDH 1.01±0.19 0.14±0.041)0.67±0.212)Notch2/GAPDH 1.00±0.12 0.64±0.261)1.37±0.062)
4 讨论
骨髓抑制是接受化疗的恶性肿瘤患者常见的剂量限制副作用,目前促进造血功能恢复的可用方法仍然有限。造血是通过HSCs协调的自我更新、增殖和分化而发生的一个连续的血细胞产生过程。因此当高剂量化疗损害HSCs的再生和分化潜能时,就会发生以全血细胞减少为主的造血功能不足,甚至演变成危及生命的并发症。骨髓造血微环境由多种细胞和因子共同构成构成,主要为HSCs提供存活所需要的养分和传导信号,达到调控HSCs 的功能的作用。MSCs 是骨髓造血生态位的重要组成部分,在造血谱系细胞的发育、维持和增殖中发挥作用[15]。研究发现MSCs和HSCs共培养构成的造血“龛”,提供了类似骨髓的微环境,有利于促进HSCs的维持和增殖。同时MSCs能够分泌多种与造血相关的细胞因子,如IL-6、LIF、SCF 等,直接促进HSC 增殖[16]。王晓玲等[17]通过模拟辐射旁效应HSCs与BMSCs 的共培养模型,发现“芪归药对”载药血清可能通过抑制NF-κB 通路,降低HSCs 凋亡率并促进其增殖,抵抗了HSCs辐射损伤。当MSCs与HSCs直接接触时,MSCs 分泌多种黏附因子,HSCs 上也表达相应的配体[18],与其他共培养方式相比,二者直接接触支持HSCs 增殖的效果更明显[19]。因此本研究选择将BMSCs 和HSCs 共培养,建立化疗后骨髓抑制的造血“龛”模型,探究扶正补血食疗方是否可以通过保护造血“龛”功能,达到保护造血“龛”中造血干细胞的目的。
Notch 信号通路具有高保守性并广泛存在于脊椎和非脊椎动物中。Notch是一种跨膜受体,由配体-受体相互作用激活,被裂解释放其胞内结构域,直接影响靶基因的转录。此过程通过介导细胞间信号传导,在造血系统中发挥着调节造血的关键作用[20]。Rafii 课题组发现,辐照后重度骨髓抑制小鼠的Notch 信号激活,有利于抵抗HSCs 损伤和维持HSCs 自我更新[21]。在HSCs中Notch信号通路高度活化,成骨细胞中Notch配体Jagged1 表达,并激活HSCs 上Notch 受体Notch1 的表达,HSCs 数量显著增加[22]。VARNUM-FINNEY 等认为通过Jagged1-Notch2信号调控5-FU 化疗后骨髓抑制小鼠短期和长期造血重建,且抑制了髓系分化[23]。研究证明MSCs上激活的Jagged1表达增强了Notch2信号,抑制p63 并促进抗凋亡蛋白Bcl-2 的表达,减少HSCs 凋亡并改善造血恢复[24]。同时,Notch 信号通路下游主要靶分子也在HSCs 高表达[25]。提示Notch 信号途径可能在HSCs 维持和再生过程中发挥着重要调控作用。
中医古籍中并没有骨髓抑制的记载,可将其归属于“血虚”“虚劳”范畴[26]。大多数学者认为骨髓抑制的病因为“脾肾两虚”“气血不足”,因此中医主张健脾补肾、补血益气[27-28]。中医食疗方主要起到健脾养胃的功效,可有效改善临床患者化疗期间如乏力、疼痛、失眠和食欲低下等的不良反应[29]。本研究中扶正补血食疗方由当归、黄芪、黄精及猪蹄组成,方中重用黄芪,黄芪为补中益气之要药,补气而行血;当归补血活血,以使阳生阴长,气旺血生;黄精补气养阴、益肾填精,平补肺、脾、肾三经;猪蹄甘、咸、平,养肾填精。精气血互生,共奏固本培元之功,契合中医对恶性肿瘤化疗后骨髓抑制的治疗理念。课题组通过高效液相色谱实验检测扶正补血食疗方发现,本食疗方含有多种活性成分,如黄芪甲苷、当归多糖、黄精皂苷、阿魏酸等,现代药理研究证明其具有提高免疫力、抗肿瘤、抗氧化和保护脏器的功效[30-31],同时也可直接或间接促进HSCs 增殖,改善造血干细胞衰老[32-33]。猪蹄中丰富的胶原蛋白及被消化分解后产生的小分子肽,也具有补血、抗氧化及抗癌的积极作用[34]。
研究结果显示,扶正补血食疗方含药血清可以显著提高5-FU损伤的小鼠HSCs细胞活力,同时使停滞在静止期的HSCs 减少,细胞总凋亡率下降,说明扶正补血食疗方可以通过促进小鼠HSCs G0/G1 期细胞向S 期转变,促进HSCs 增殖。扶正补血食疗方可能通过增强BMSCs 和HSCs 之间的黏附作用,使更多的HSCs进入增殖期,为减少周期依赖性化疗药物5-FU 掺入到增殖的HSCs 的RNA 中,抑制其DNA 合成或干扰分化而发挥辅助作用,减少HSCs 受损。与对照组相比,5-FU 组小鼠CD117+细胞Jagged1、Notch1、Notch2 基因表达降低;与5-FU组相比,扶正补血食疗方含药血清组细胞Jagged1、Notch1、Notch2 基因表达均增加,结果说明,扶正补血食疗方能在一定程度上促进HSCs增殖,其机制可能与激活Notch 信号通路,上调Jagged1、Notch1、Notch2 的表达有关。基于组成本食疗方的中药和食物的成分多样,本研究选用含药血清进行体外实验,更符合食疗方在体内被消化、吸收、代谢和入血的过程,并得到最终的有效物质成分[35]。本研究表明拮抗HSCs化疗后损伤的物质基础,可能与其富含的多种抗炎抗氧化、补血、抗癌的活性成分有关,同时Notch信号通路参与调控,通过上调Notch 通路关键因子Jagged1、Notch1、Notch2表达水平,调节造血“龛”功能,进而促进HSCs增殖,降低凋亡率,缓解HSCs化疗损伤程度。综上所述,本研究初步阐释了扶正补血食疗方拮抗化疗毒副作用的机制,为中医食疗应用于临床防治骨髓抑制提供了实验依据。但目前仍存在一定局限性,课题组计划对食疗方中主要有效成分进行全面分析和提纯,更加明确其作用机制。同时,对于Notch 信号通路蛋白表达情况,上、下游靶点以及具体调控机制,仍需进一步深入研究。

