B2 O 3 对LTPS用基板玻璃结构和黏温性能的影响
杨国洪 孔令歆 曾召 王答成 徐莉华 兰静 郭静
(彩虹显示器件股份有限公司 咸阳 712000)
0 引言
随着电子显示行业的高速发展,液晶显示向着超薄、高清、高亮、低耗、低成本的方向迈进,基于LTPS晶体管的显示器逐步显露于市场中。面对LTPS技术的面板制造,作为元件的基板玻璃需要具备更强的热稳定性、更高的应变点。
B2O3是玻璃网络形成体,能提升玻璃的热稳定性,并降低高温黏度。它还具有助熔作用,可加速玻璃的澄清[1]。但其在玻璃中的表现也存在一些问题,如易挥发、硼反常等,会导致玻璃最终的性能与理想设计产生差异。目前,已有多数学者对B2O3对玻璃性能的影响展开研究,但都基于碱铝硅酸盐体系玻璃,对于LTPS用无碱基板玻璃体系相关信息尚少。
本文在LTPS用基板玻璃组分配比基础上,仅改变玻璃组分中B2O3含量,通过红外光谱、X射线光电子能谱分析B2O3对LTPS用基板玻璃结构的影响,同时研究B2O3对玻璃黏温特性的影响,为新型显示技术用基板玻璃料方开发提供技术支撑。
1 实验
依据无碱铝硼硅酸盐玻璃化学组成,设计5组玻璃化学料方配比,分别标号为B1、B2、B3、B4、B5。配方中所用的玻璃原料包括:石英砂、氧化铝、硼酸、氧化镁、碳酸钙、碳酸锶、硝酸钡、氧化锡。
实验设备及作用:采用ES-I000E电子天平进行玻璃配合料称量,BLMT-1800℃升降高温炉用于玻璃熔制,BLMT-1400℃马弗炉用于玻璃试样退火。利用Orton RSV 1600型高温黏度计进行黏温测试,Orton退火应变测试仪表征试样退火点与应变点,Orton软化点测试仪表征试样软化点。以德国布鲁克(Bruker)VERTEX70型傅里叶变换红外光谱仪进行玻璃红外光谱表征,AXIS SUPRA型X射线光电子能谱仪进行试样结构分析。
5组配方仅改变B2O3的含量,从B1到B5依次增加,配比见表1。
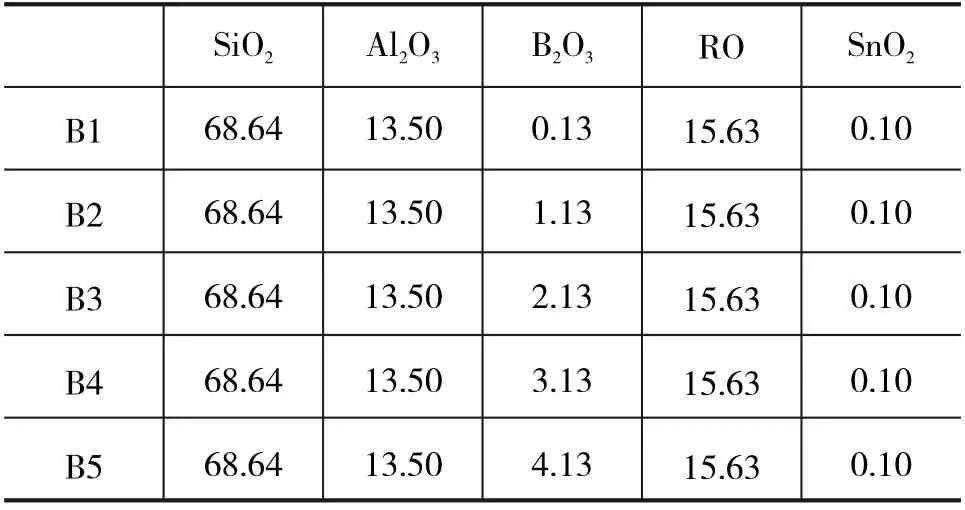
表1 不同B 2O 3组成的样品化学组成 摩尔分数/%
准确称量玻璃配合料,充分混合后装入铂金坩埚,将坩埚置于高温炉中进行玻璃熔制。熔化好的玻璃快速在模具中浇铸,待玻璃样品定型后,立即移入退火炉中退火。熔制及退火工艺如图1所示。

图1 玻璃样品熔制及退火工艺
2 结果与讨论
2.1 红外光谱分析
红外光谱作为分子结构的基础研究手段可用来定性分析物质的化学组成。为了准确分析B2O3对基板玻璃分子结构的影响,汇总硼铝硅酸盐玻璃常见的各个结构基团的红外吸收特征振动,见表2[2,3]。

表2 硼铝硅酸盐玻璃常见的红外吸收光谱特征振动
图2为不同含量B2O3玻璃试样的红外分析谱图,图中反映出8处振动吸收峰。

图2 不同含量B 2O 3玻璃试样红外分析谱图
其中,1650 cm-1和3500 cm-1附近的两个吸收峰是水的吸收特征峰,为测试过程中样品吸潮所致。对照表2可以判断,1450 cm-1处为[BO3]伸缩振动峰,B1、B2样品此处的特征峰未显现出来,而B3、B4、B5此处峰强逐渐增强,说明随着B2O3含量增加,B3+以[BO3]形式存在逐渐增多。680 cm-1处为[BO3]的弯曲振动峰,5个样品此处的峰形及峰位逐渐增强,再次验证随着B2O3含量增加,[BO3]增多。1064 cm-1为[SiO4]与[BO4]伸缩振动峰的合峰,950 cm-1处是[BO4]的伸缩振动峰,B1至B3在该处的峰形逐渐明显,峰的强度也在增强,说明伴随着B2O3在玻璃中含量增多,B3+以[BO3]形式向[BO4]转变,[BO4]含量增多。当B2O3含量大于2.13%时,1064 cm-1和950 cm-1处的合峰强度略有降低,1450 cm-1和680 cm-1处[BO3]的振动特征逐渐明显,说明B2O3含量继续升高,体系中[BO4]逐渐平衡,参与[BO4]之外的B3+仍以[BO3]形式存在。770 cm-1的振动是O-Si-O伸缩振动峰,即被游离氧断键后形成的非桥氧键。B1、B2在该处峰的振动强度较其余三个样品的弱,B3、B4、B5振动峰状态相当,但5个样品该处的峰均较1064 cm-1处弱。说明随着B2O3含量升高,玻璃中非桥氧的数量逐渐增多(仅为趋势,总归没有桥氧多);当B2O3含量继续升高,非桥氧数量维持平衡。总结来看,玻璃中B3+先以[BO3]形式存在,随着B2O3含量升高,非桥氧的数量逐渐增多,[BO3]结合非桥氧形成[BO4]参与网络架构,此时[BO4]增多,桥氧增多;随着B2O3含量继续升高,玻璃中[SiO4]含量尚未改变,网络中的[BO4]维持稳定,B3+将继续以[BO3]形式存在。
2.2 X射线光电子能谱分析
图3是不同含量B2O3样品O1s的XPS谱图。
从图3可以看出,5个样品的O1s峰形基本一致,B1到B2的峰位从531.7 eV移至532.1 eV,向高电子结合能方向移动,B2、B3、B4、B5样品的O1s峰位维持在532.0 eV。相关资料表示[4],无碱硼铝硅酸盐玻璃中的氧以桥氧(BO)和非桥氧(NBO)两种状态存在,因非桥氧的电子云密度较桥氧的高,非桥氧的电核势能比桥氧的电核势能低,所以非桥氧的O1s电子结合能比桥氧的要低。据此,可以判断5个试样随着B2O3含量的增加,B1样品到B2样品,电子结合能升高,桥氧数量增加,B2~B5这4个样品中的桥氧与非桥氧变化不大。

图3 不同含量B 2O 3样品O1s谱图
图4是试样B1s的XPS谱图,5个样品的B1s峰形基本一致,B1到B2的峰位从190.5 eV升高至192.8 eV,B2、B3、B4、B5样品的B1s峰位维持在193.2 eV。由于四配位的硼电子结合能高于三配位的硼[5],所以B1到B2电子结合能的升高说明[BO4]含量的相对升高。

图4 不同含量B 2O 3样品B1s谱图
图5是利用软件对试样O1s谱图分峰拟合结果,非桥氧从39.11%升高至76.78%(仅为趋势的反映,不代表玻璃中非桥氧的真实含量)。
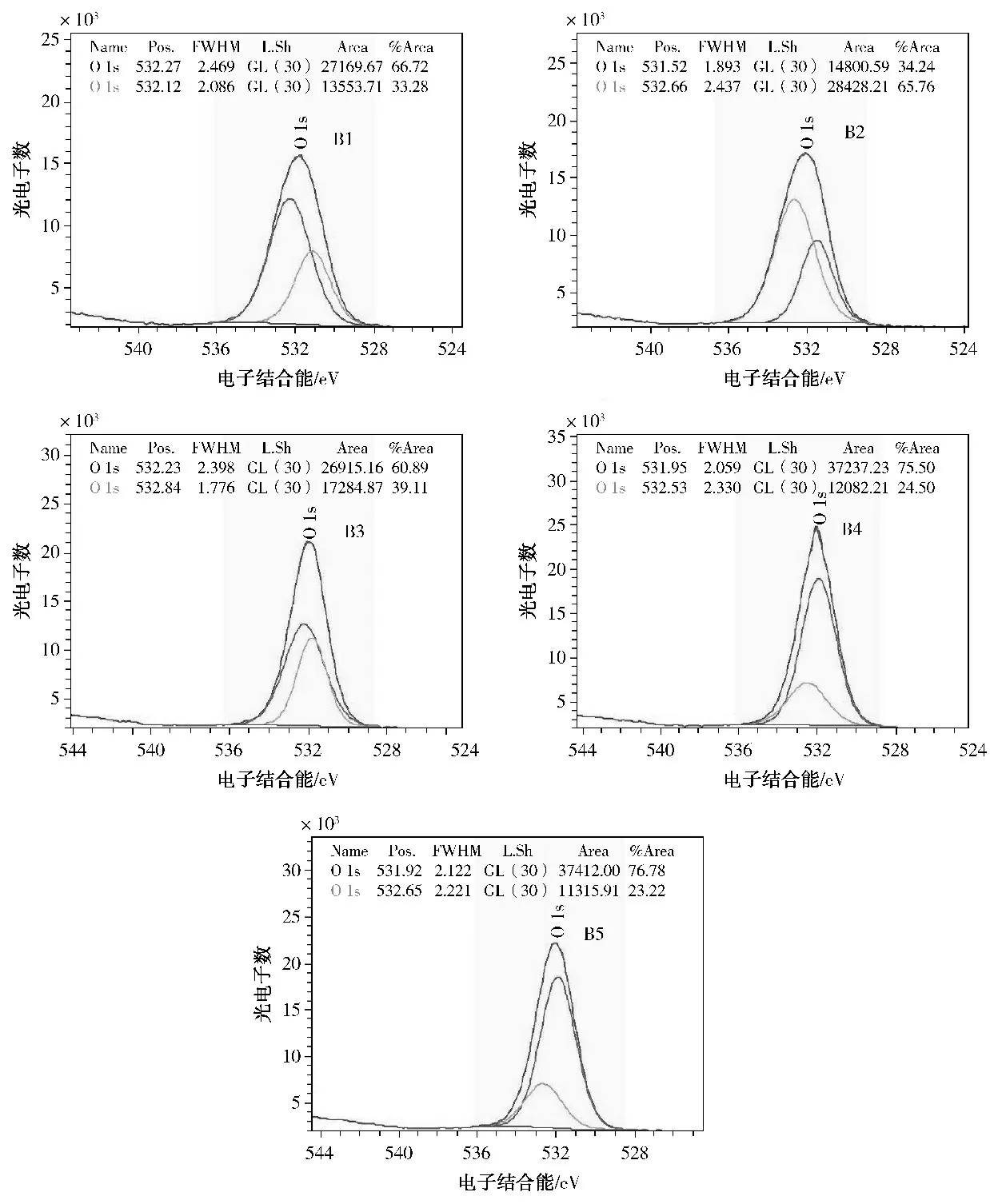
图5 不同含量B 2O 3样品O1s拟合分析谱图
图6是通过软件对试样B1s谱图分峰拟合结果,B4、B5试样的[BO3]的含量相对高于B1~B3试样。
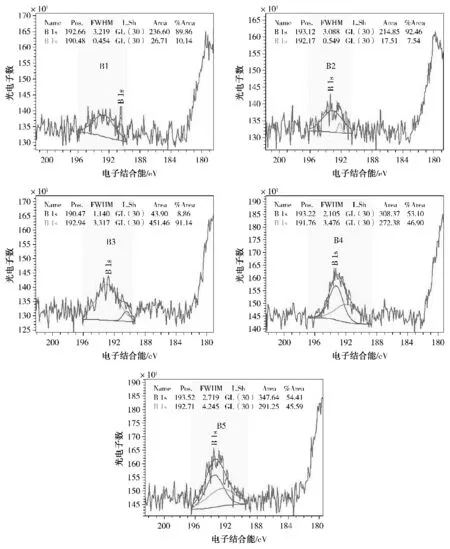
图6 不同含量B 2O 3样品B1s拟合分析谱图
结合前述,可知B3+在玻璃中的变化状态,即:先以[BO3]形式存在,并快速的向[BO4]转变,使[BO4]相对含量增多,此时体系中桥氧数多,O1s和B1s电子结合能均向高能位偏移。当B2O3含量继续增加,参与玻璃结构构建的[BO4]足够,桥氧数稳定,其余B3+则以[BO3]形式存在,所以在拟合结果中有非桥氧数相对升高以及[BO3]含量的相对增加。
2.3 黏温特性分析
不同含量B2O3玻璃试样的黏温曲线如图7所示。试样的软化点、退火点、应变点黏温特征点温度对比见表3。
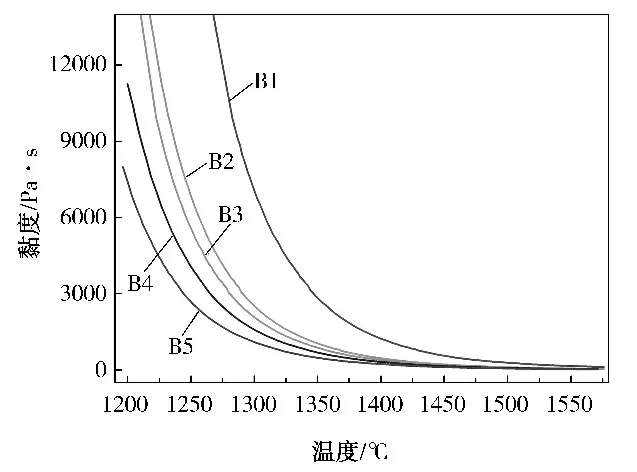
图7 不同含量B 2O 3玻璃试样黏温曲线

表3 不同含量B 2O 3玻璃试样特征温度 ℃
3 结论
在LTPS用无碱硼铝硅酸盐玻璃中,B3+以四配位的[BO4]和三配位的[BO3]形式存在,两种配位的相对含量取决于系统中的[SiO4]和游离氧的含量。本研究中,当B2O3含量较低(0.13%)时,B3+以四配位的[BO4]存在;随着B2O3含量升高,满足[BO4]的形成之外的B3+逐渐以[BO3]的形式存在。[BO3]含量的相对增多,致使玻璃黏度逐渐下降。

