牛至油博落回口服液的研制及体外抑菌活性测定
李伟浩,孙媛媛,刘聚祥
(河北农业大学动物医学院,保定 071000)
当前,大型规模化养殖已成为中国畜牧业发展的主要方向,而饲用抗生素对防治畜禽细菌性疾病、促进畜禽生长性能和饲料利用率方面均有重要作用,使得畜禽数量与产量得到很大提高,获得较为可观的经济效益。但饲用抗生素的长期添加导致了细菌耐药性、环境污染、动物源食品药物残留等一系列问题,因此中国农业农村部于2019年7月发布194号公告:“自2020年1月1日起,退出除中药外的所有促生长类药物饲料添加剂品种”,意味着中国饲料行业进入全面“禁抗”时代,因此,亟需寻求研发绿色无害的动物生长促进剂。在目前受到广泛研究和应用的替抗产品中,牛至油和博落回提取物作为植物提取物不仅具有促生长、抑菌杀菌、抗氧化和免疫调节等多种生物学功能,而且具有天然、无毒副、无耐药及无残留的优点[1-2]。
牛至油(oregano oil)是从牛至中提取的具有特殊芳香气味的挥发油,主要化学成分是百里香酚(thymol)和香芹酚(carvacrol)、萜烯类及其衍生物等[3-4]。研究表明,牛至油可显著抑制金黄色葡萄球菌、大肠杆菌、沙门氏菌类及普通变形菌类[5-6],有效调节肠道微生物区系平衡,改善肠道形态,提高食欲,进而可提高增重、饲料利用率及抗感染能力[7-8]。博落回(Macleayacordata)是罂粟科博落回属多年生草本植物,博落回中主要生物活性物质为异喹啉类生物碱,如血根碱、白屈菜红碱、原阿片碱、别隐品碱等[9-10],具有抗菌、促进肠道黏膜发育、改善料重比、提高生长性能及增强机体抗氧化能力的作用[11-12]。
最先出现的牛至油市售产品是荷兰罗帕法姆公司1995年生产的诺必达(RopadiarTM)牛至油预混剂,诺必达是纯天然牛至提取物,其牛至油含量≥5%,价格相对较高,应用成本也较高。博落回提取物(Sangrovit®)最早是由德国的Phytobiotics公司生产。国内的主要产品为湖南美可达生物资源股份有限公司研发的美佑壮博落回散,为二类中兽药制剂。这些产品均为预混剂,不适于畜禽规模化养殖的水线系统。鉴于此,本试验研制牛至油博落回提取物复合溶液剂,并测定其含量及体外抑菌活性,以期为临床提供一种适用于畜禽规模化养殖水线系统的替代抗生素促生长剂,并为其临床合理用药提供理论依据。
1 材料与方法
1.1 材料
1.1.1 药品与试剂 牛至油(批号:20200812,含量≥90%)购自江西海瑞天然植物有限公司;博落回提取物(批号:F01040 020091801,含量≥60%)购自湖南汉清生物技术有限公司;聚氧乙烯(40)氢化蓖麻油(批号:20200902)购自深圳市欧朋特科技有限公司;2,6-二叔丁基对甲酚(BHT,含量≥98%)、叔丁基对羟基茴香醚(BHA,含量≥98%)均购自上海源叶生物科技有限公司;色谱纯乙腈(含量≥99.95%)购自赛默飞世尔科技(中国)有限公司;色谱纯磷酸(含量≥85%)购自福晨(天津)化学试剂有限公司;香芹酚标准品(含量≥98%)、血根碱标准品(含量≥98%)均购自北京索莱宝科技有限公司;抗生素药敏片(青霉素、链霉素、替米考星、氟苯尼考、头孢噻呋)购自赛默飞世尔科技有限公司。
1.1.2 试验菌株及培养基 大肠杆菌标准菌株BNCC336902、金黄色葡萄球菌标准菌株BNCC186335、粪链球菌标准菌株BNCC336445均购自北纳创联生物技术有限公司;沙门氏菌标准菌株CMCC50041由河北农业大学动物医学院病理实验室提供;营养琼脂培养基、营养肉汤培养基及新生牛血清均购自北京索莱宝科技有限公司;脱纤维绵羊血购自上海源叶生物科技有限公司。
1.1.3 主要仪器 电子天平购自赛多利斯科学仪器有限公司;超纯水系统购自上海力新仪器有限公司;电热鼓风干燥箱购自上海博讯实业有限公司;超净工作台(ZHJH-1106B)购自ZHCHENG公司;恒温振荡器(THZ-98C)购自上海一恒科学仪器有限公司;生化培养箱(SPX)购自宁波江南仪器厂;立式高压灭菌器(LDZX-50L)购自上海申安医疗器械厂;高效液相色谱仪紫外检测器(SPD-20A)、控制器(CBM-20A)及泵(LC-6AD)均购自日本岛津有限公司。
1.2 牛至油博落回口服液处方筛选及优化
以牛至油和博落回提取物的溶解性状、感官性状为主要考察指标,并结合两种成分各自的理化性质,考虑到溶解能力、挥发速度、稳定性及临床应用中安全性等因素,选取适宜的溶剂、增溶剂和抗氧化剂。在水、乙醇及丙二醇等常用溶剂中确定以水为溶剂;比较不同增溶剂对牛至油与博落回提取物的增溶效果,在吐温-80、吐温-20、聚氧乙烯(40)氢化蓖麻油(RH40)中确定以RH40为增溶剂;针对植物精油易氧化问题,从符合安全标准、高效抗氧化要求的BHT、维生素E及BHA中确定以BHT为抗氧化剂。
以口服液感官评分为评价标准,设计3因素3水平的响应面分析,采用Design-Expert 10.0统计软件Box-Behnken法对试验结果进行响应面回归分析,即以牛至油、博落回提取物及RH40添加量为影响因子,各取3个水平,进行响应面分析,从而更加直观地筛选出牛至油博落回口服液最优配方。感官评分标准见表1,响应面分析因素水平见表2。

表1 牛至油博落回口服液感官评分标准

表2 响应面分析因素水平
1.3 含量测定
1.3.1 色谱条件 采用高效液相色谱法进行含量测定:色谱柱为Waters SunFire C18(4.6 mm×150 mm,5 μm);流动相为乙腈∶0.2%磷酸水溶液=7∶3;流速为1 mL/min;检测波长分别为血根碱270 nm和香芹酚275 nm;进样量为20 μL。
1.3.2 溶液配制 标准品溶液的配制:精密称取10 mg香芹酚标准品,置于25 mL容量瓶中,加入乙腈溶解,定容,制成浓度为400 μg/mL的标准品溶液;精密称取5 mg血根碱标准品,置于50 mL容量瓶中,加入乙腈溶解,定容,制成浓度为100 μg/mL的标准品溶液。阴性对照品溶液的配制:按配方称取口服液中的辅料,制成不含药品的口服液阴性对照品,精密量取100 μL阴性对照品,置于50 mL容量瓶中,加入乙腈溶解,定容。供试品溶液的配制:精密量取100 μL口服液,置于50 mL容量瓶中,加入乙腈溶解,定容。
1.3.3 专属性考察 分别取对照品溶液、供试品溶液和空白辅料制备的阴性对照品溶液,按照上述色谱条件和进样方法进样,验证香芹酚和血根碱的出峰位置是否唯一,考察香芹酚和血根碱两峰之间以及与其他杂质峰分离是否良好。
1.3.4 线性关系试验 精密量取对照品贮备溶液适量,用乙腈稀释制成香芹酚浓度分别为400、200、100、50、25和12.5 μg/mL,血根碱浓度分别为100、50、25、12.5、6.25和3.125 μg/mL的系列对照品溶液,按照1.3.1色谱条件和进样方法进样,记录各色谱峰峰面积,以浓度X为横坐标、吸收峰面积Y为纵坐标进行线性回归。
1.3.5 样品含量测定 取制备的牛至油博落回口服液10批,按供试品溶液制备方法处理,按照1.3.1色谱条件进样,记录峰面积,并计算血根碱和香芹酚的含量。
1.4 体外抑菌试验
1.4.1 试验药品的制备 按照优化后牛至油博落回口服液的组方制备牛至油博落回口服液,同时分别制备5%牛至油、1%博落回对照品溶液以及空白辅料溶液。
1.4.2 药敏片的制备 将直径5 mm的无菌滤纸片置于高压灭菌的5 mL玻璃药敏瓶中,分别加入牛至油博落回口服液、5%牛至油溶液、1%博落回溶液和空白辅料溶液,待滤纸片将药液充分吸收后将其平铺于无菌培养皿内,置于37 ℃烘箱中烘干备用。
1.4.3 菌悬液制备 用无菌接种环将活化后的大肠杆菌、沙门氏菌、金黄色葡萄球菌分别接种于营养琼脂平板上,将粪链球菌接种于血琼脂平板上,细菌菌种于37 ℃恒温培养箱中孵育24 h,然后挑取各培养基上该菌生长比较典型的菌落接种到肉汤中:大肠杆菌、金黄色葡萄球菌和沙门氏菌接种于普通肉汤中;粪链球菌接种于血清肉汤中,经过平板计数法制成细菌总数为1.5×106CFU/mL的菌悬液备用。
1.4.4 抑菌圈直径测定 采用滤纸片法(K-B法)测定抑菌圈直径。先将高压灭菌的琼脂培养基的温度降至45 ℃左右,在干燥灭菌的直径9 cm培养皿内加入15 mL培养基,待冷却凝固后,再吸取100 μL菌悬液,并用无菌涂布棒均匀涂布于相应琼脂平皿,备用。用镊子轻柔夹取自制药敏片和青霉素、链霉素、替米考星、头孢噻呋、氟苯尼考药敏片轻轻地贴于涂有菌液的培养基上。37 ℃恒温培养箱中培养24 h,观察并记录抑菌圈直径,按照美国临床和实验室标准协会(CLSI)颁布的《抗微生物药物敏感性试验执行标准》判断对药物的敏感性[13]。
1.4.5 最小抑菌浓度和最小杀菌浓度的测定 按照曾振灵[14]介绍的试管二倍稀释法进行最小抑菌浓度(MIC)和最小杀菌浓度(MBC)测定。试验组取90支经过高压灭菌的试管,分为9排,每组10支。1~3排:每管加入2 mL无菌的液体培养基,每排第1个管中加入稀释2.5倍后的牛至油博落回口服液2 mL,混匀后取2 mL加入第2管,以此类推,至第8管取2 mL废去,最后向8支试管中分别加入50 μL供试品菌液并振荡使其均匀;第9管加入液体培养基及菌悬液作无药阳性对照;第10管只加入液体培养基及试验药品作无菌阴性对照。 4~6与7~9排除试验药品分别添加5%牛至油对照溶液和1%博落回对照溶液以外,其余操作同1~3排。
阳性对照会出现细菌生长的浑浊现象,阴性对照出现无细菌生长现象,则试验成立。观察其他试管状况,不出现浑浊的浓度是口服液的MIC。将所有清晰无菌生长的试管培养液以划线法接种于相应的琼脂平板,37 ℃培养24 h,以菌落不超过5个为口服液的MBC。
1.4.6 联合药敏试验 按照吴克刚等[15]介绍的微量棋盘稀释法测定联合用药的MIC,将5%牛至油溶液与1%博落回溶液进行二倍稀释,牛至油稀释6个梯度,按高浓度到低浓度从左到右纵向加入96孔板,博落回溶液稀释6个梯度,按高浓度到低浓度从上到下横向加入96孔板,接入对数期菌液,调整菌液浓度为1×105CFU/mL,37 ℃培养24 h。以联合药敏指数(FIC)作为联合药敏试验的判断依据,计算公式为:
FIC指数=(甲药联合时MIC/甲药单独时MIC)+(乙药联合时MIC/乙药单独时MIC)
FIC指数,≤0.5为协同作用;0.5~1为相加作用;1~2为无关作用;>2为颉颃作用。
1.5 统计分析
每个试验重复3次,使用Excel 2016和SPSS 19.0进行数据处理分析,采用单因素方差分析和Tukey检验对结果进行统计分析,结果以平均值±标准差表示,以P<0.05为差异显著性判断标准。
2 结 果
2.1 牛至油博落回口服液配方的优化
2.1.1 响应面模型的建立 以牛至油、博落回提取物、RH40添加量为影响因子,以牛至油博落回口服液感官评分为响应值进行响应面优化,优化试验结果见表3。根据Design-Expert软件,以感官评分为响应值,对表3中的数据进行二次回归分析,从而得出最终的二元回归方程为:感官评分Y=93.40-5.56A-1.30B+2.44C+2.75AB+4.08AC+1.80BC-12.59A2-7.46B2-7.64C2。
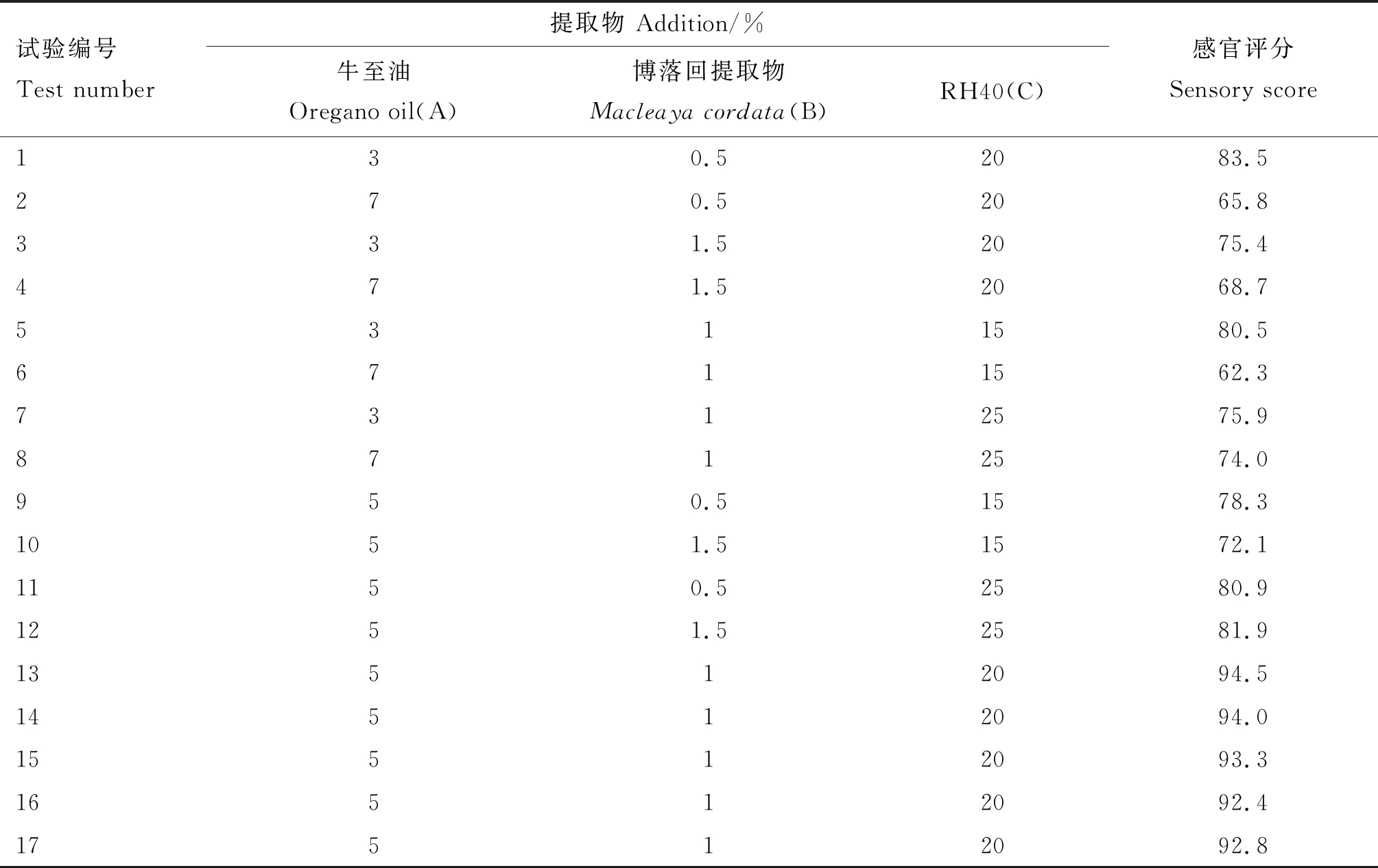
表3 响应面优化试验结果
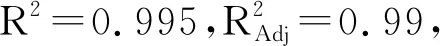
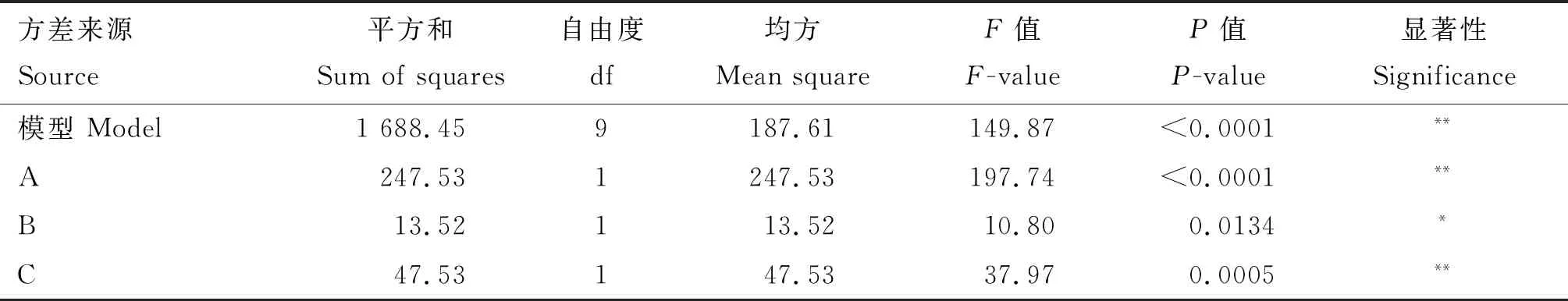
表4 响应面试验结果方差分析表
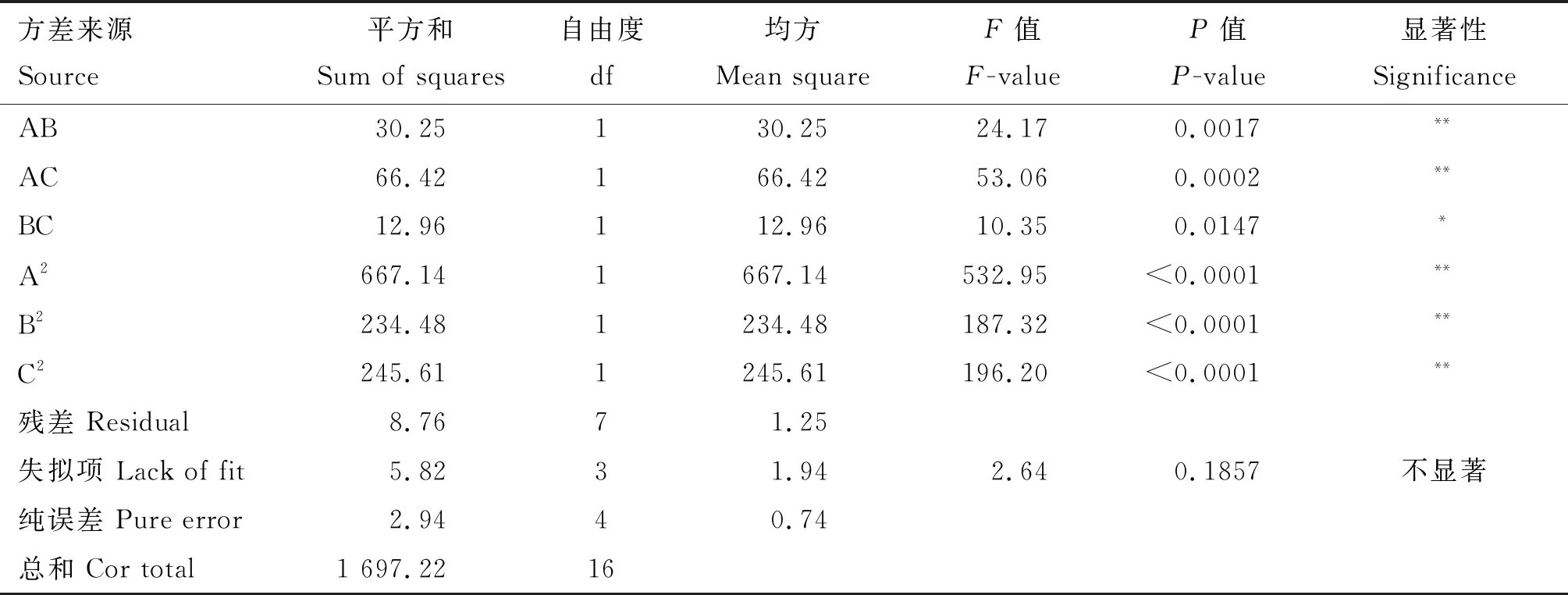
续表
2.1.2 响应面绘制及分析 采用Design-Expert软件绘制相应的响应面图和等高线图,结果见图1~3。由图1~3可知,3因素对感官评分的影响大小依次为:牛至油>博落回>RH40。等高线图形越呈圆形,表示两因素交互作用越小;等高线图形越呈椭圆形,表示两因素交互作用越大。可见,响应面分析与回归分析结果相互吻合。
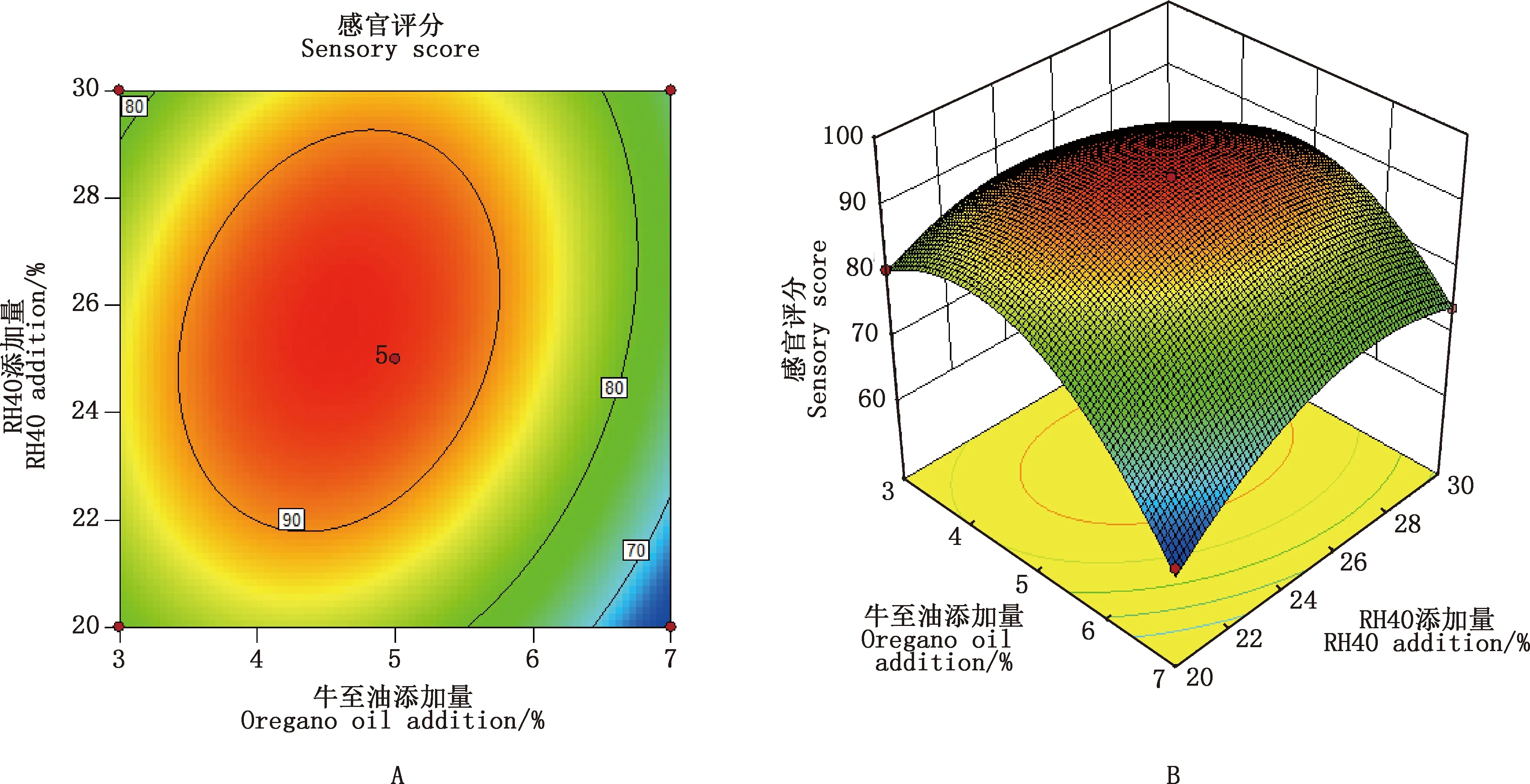
图1 牛至油与RH40添加量对口服液感官评分的二维等高线图(A)和三维响应面图(B)
2.1.3 响应面优化配方及验证试验结果 通过响应面优化得到的最佳配方为:5%牛至油、1%博落回提取物、25% RH40,0.02% BHT,余量为水。最佳感官评分为94.5。验证试验中,在该条件下进行3次平行试验,所得感官评分别为94.3、94.6和93.7,平均值94.2,说明模型模拟较好,与实测值基本吻合。
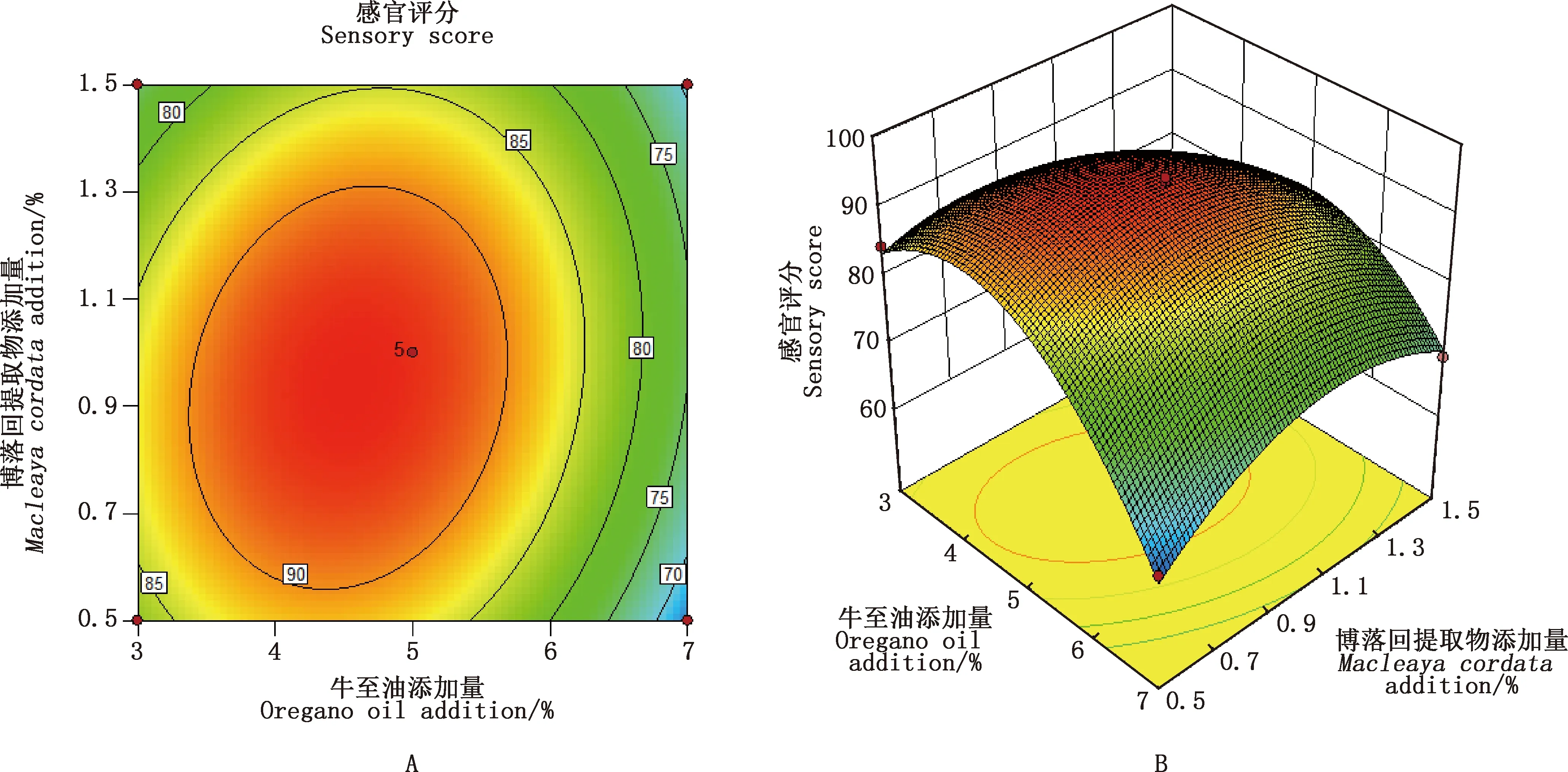
图2 牛至油与博落回提取物添加量对口服液感官评分的二维等高线图(A)和三维响应面图(B)
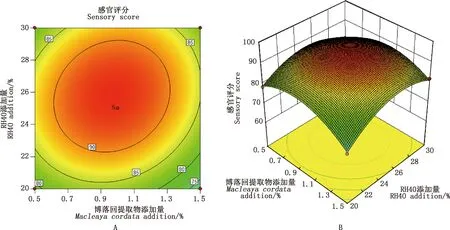
图3 博落回提取物与RH40添加量对口服液感官评分的二维等高线图(A)和三维响应面图(B)
2.2 牛至油博落回口服液含量测定试验结果
2.2.1 方法专属性验证 方法专属性结果见图4。由图4可知,阴性对照品无明显峰出现,说明可忽略口服液的辅料对含量测量的影响,香芹酚对照品、血根碱对照品出峰时间与供试品溶液中香芹酚、血根碱出峰时间相同,均在3.8和1.1 min,峰分离度良好,周围无杂峰干扰,说明该方法专属性良好,可用来测量制剂药物的含量。
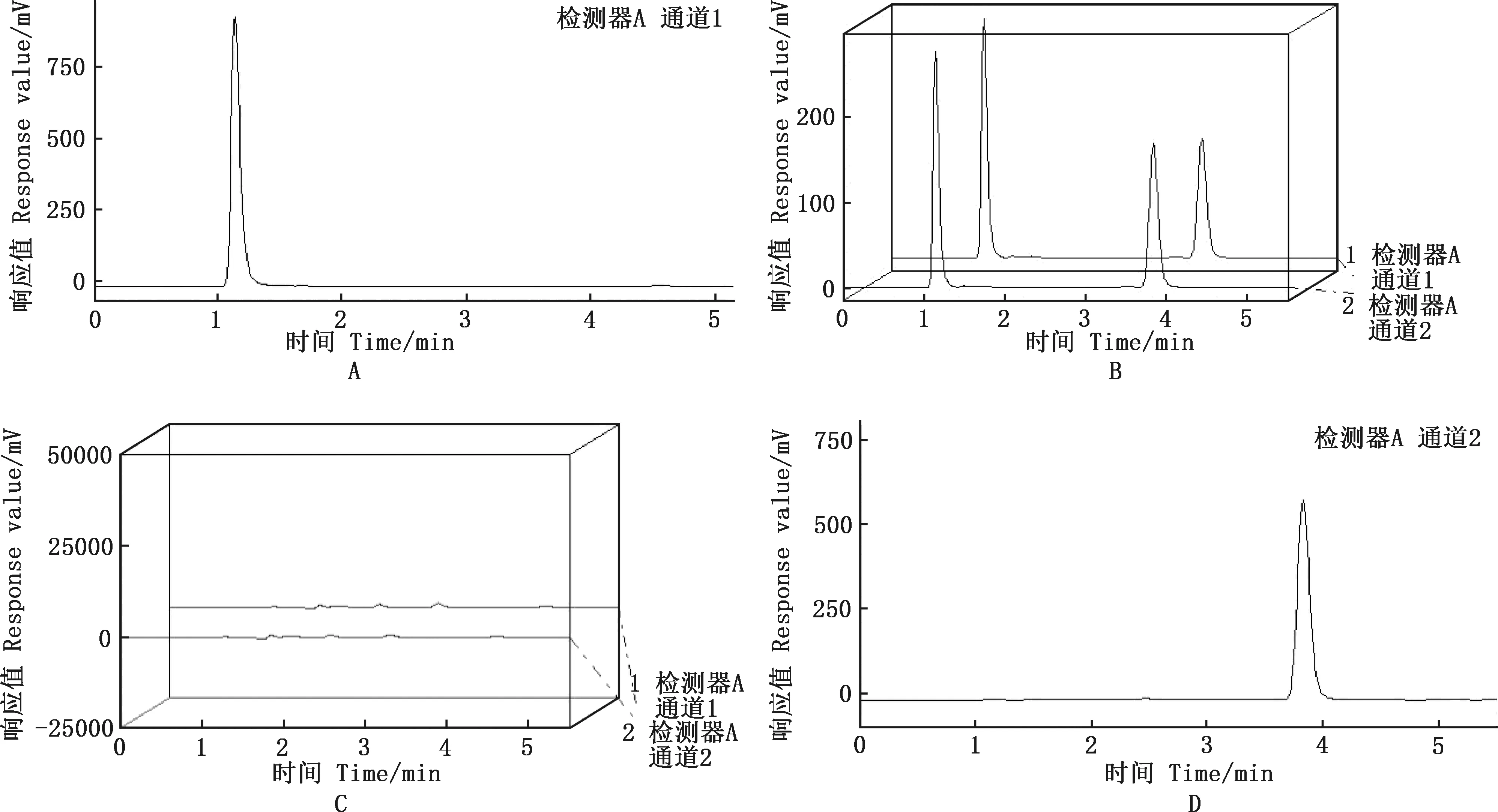
A,阴性对照品;B,香芹酚对照品;C,血根碱对照品;D,口服液样品
2.2.2 标准曲线绘制 通过测定不同浓度的香芹酚标准品溶液和血根碱标准品溶液,以浓度X为横坐标、吸收峰面积Y为纵坐标进行线性回归,结果显示,香芹酚的线性回归方程为:Y=13 578X+20 877,R2=0.9999,在香芹酚浓度12.5~400 μg/mL范围内测定方法线性良好(图5);血根碱的线性回归方程为:Y=97 560X+59 801,R2=0.9998,在血根碱浓度3.125~100 μg/mL范围内测定方法线性良好(图6)。
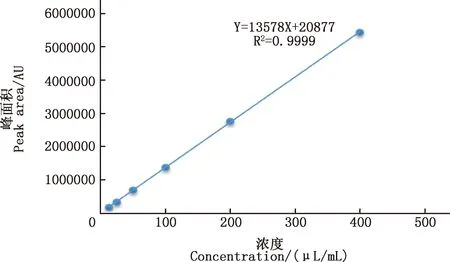
图5 牛至油博落回口服液中香芹酚含量测定标准曲线图
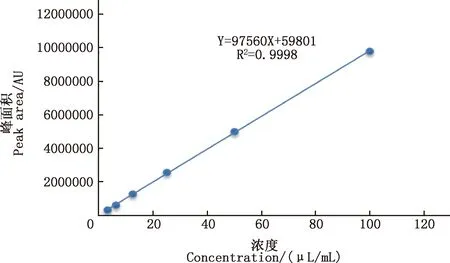
图6 牛至油博落回口服液中血根碱含量测定标准曲线图
2.2.3 样品含量测定结果 检测10批牛至油博落回口服液香芹酚的平均含量为42.59 mg/mL,血根碱的平均含量为6.51 mg/mL。
2.3 牛至油博落回口服液体外抑菌试验结果
2.3.1 抑菌圈直径 不同药物对4种细菌的体外抑菌效果见表5。由表5可知,对大肠杆菌,氟苯尼考、头孢噻呋、链霉素表现为高度敏感,替米考星及口服液为中度敏感,而青霉素、5%牛至油溶液及1%博落回溶液为低度敏感;对沙门氏菌,氟苯尼考、头孢噻呋及链霉素为高度敏感,青霉素、替米考星及口服液为中度敏感,5%牛至油和1%博落回为低度敏感;对金黄色葡萄球菌,除5%牛至油溶液表现为中度敏感外,其余均表现为高度敏感;对粪链球菌,氟苯尼考、青霉素及头孢噻呋为高度敏感,1%博落回、口服液及链霉素表现为中度敏感,5%牛至油和替米考星表现为低度敏感。表明头孢噻呋和氟苯尼考具有强大的广谱抗菌性,而研制的牛至油博落回口服液对4种菌株均表现为高度或中度敏感,抗菌谱较广,牛至油与博落回之间无颉颃作用。
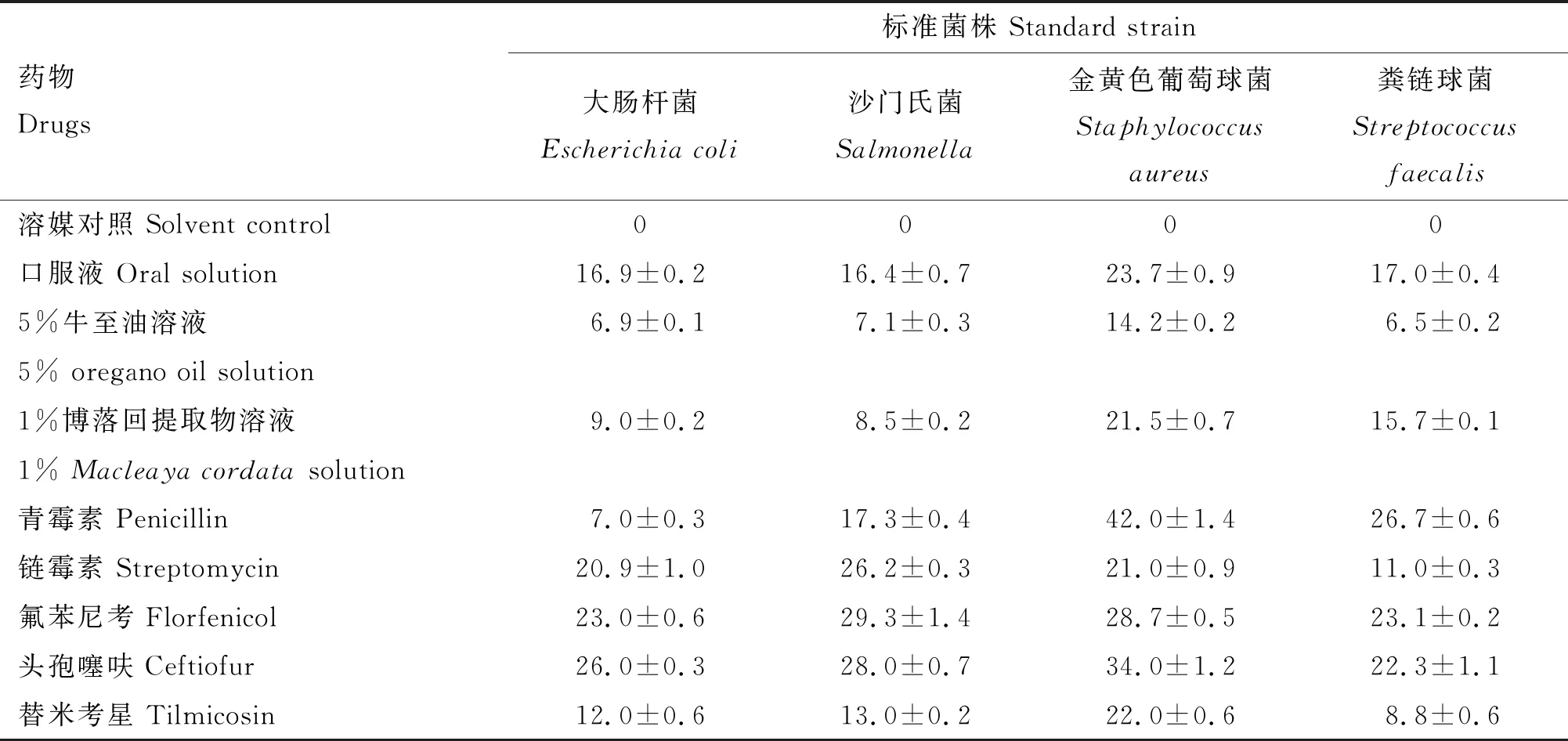
表5 滤纸片法(K-B法)测得的抑菌圈直径
2.3.2 MIC和MBC 37 ℃培养18~24 h后,空白对照孔均无细菌生长,对照孔细菌生长良好,可见培养基明显浑浊。由表6可知,牛至油博落回口服液对4种细菌菌有较好的抑制作用,对金黄色葡萄球菌和粪链球菌有良好的杀菌作用;1%博落回对沙门氏菌的抑制作用弱于其他3种菌,对金黄色葡萄球菌具有良好的杀菌作用;5%牛至油溶液对金黄色葡萄球菌的杀菌作用较大肠杆菌、沙门氏菌及粪链球稍强,其中对粪链球菌抑杀效果不明显。
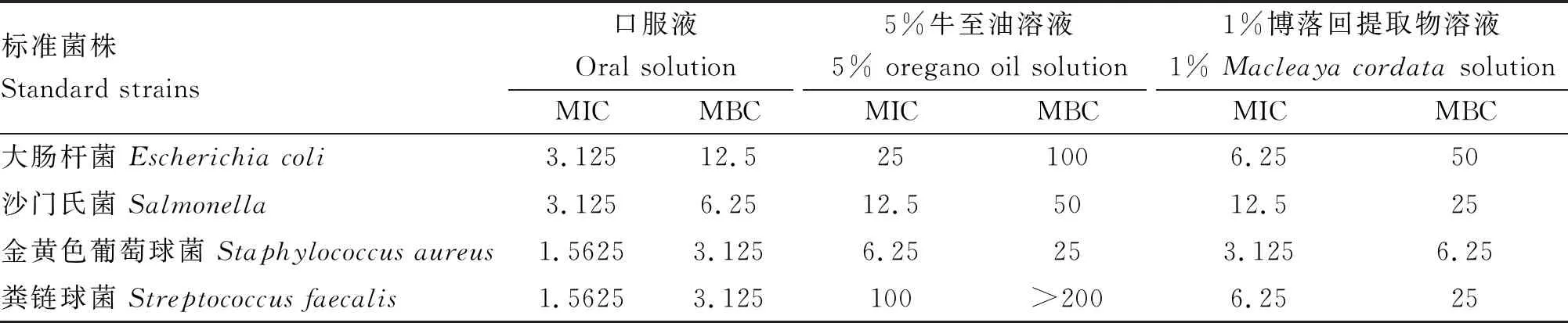
表6 3种供试药对4种细菌的最小抑菌浓度和最小杀菌浓度
2.3.3 联合药敏试验 5%牛至油溶液和1%博落回溶液对大肠杆菌、沙门氏菌、金黄色葡萄球菌、粪链球菌单独用药及联合用药时的MIC见表7~10,二者的联合药敏指数见表11,结果显示,5%牛至油溶液和1%博落回溶液的联合用药对大肠杆菌、沙门氏菌表现为相加作用,对金黄色葡萄球菌表现为无关作用,对粪链球菌表现为协同作用。
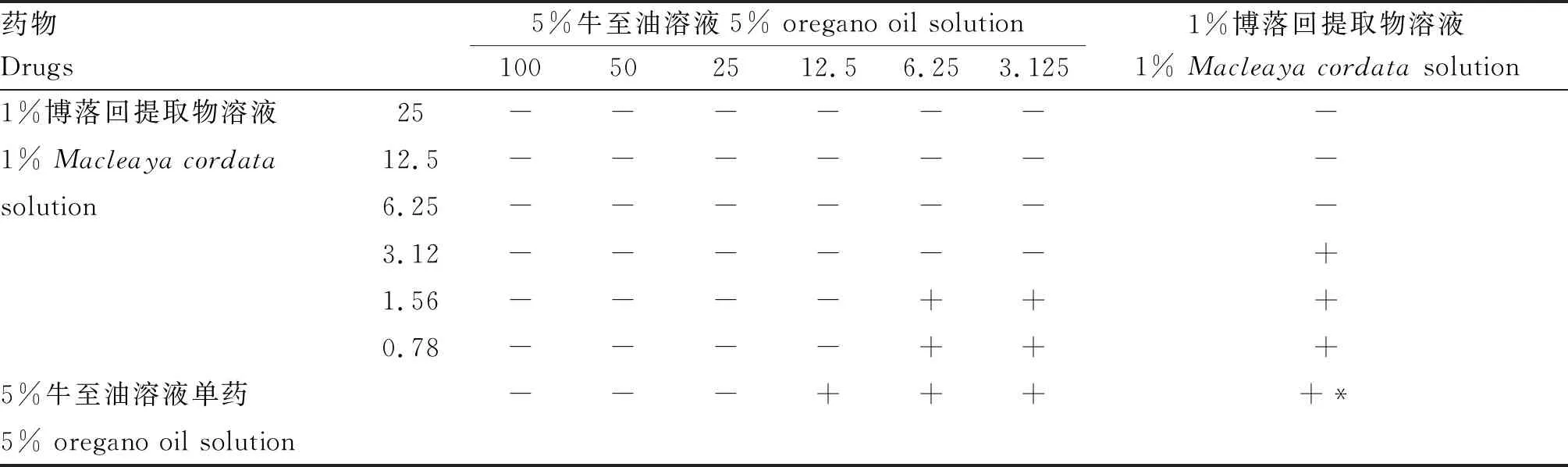
表7 牛至油和博落回提取物对大肠杆菌的联合药敏试验
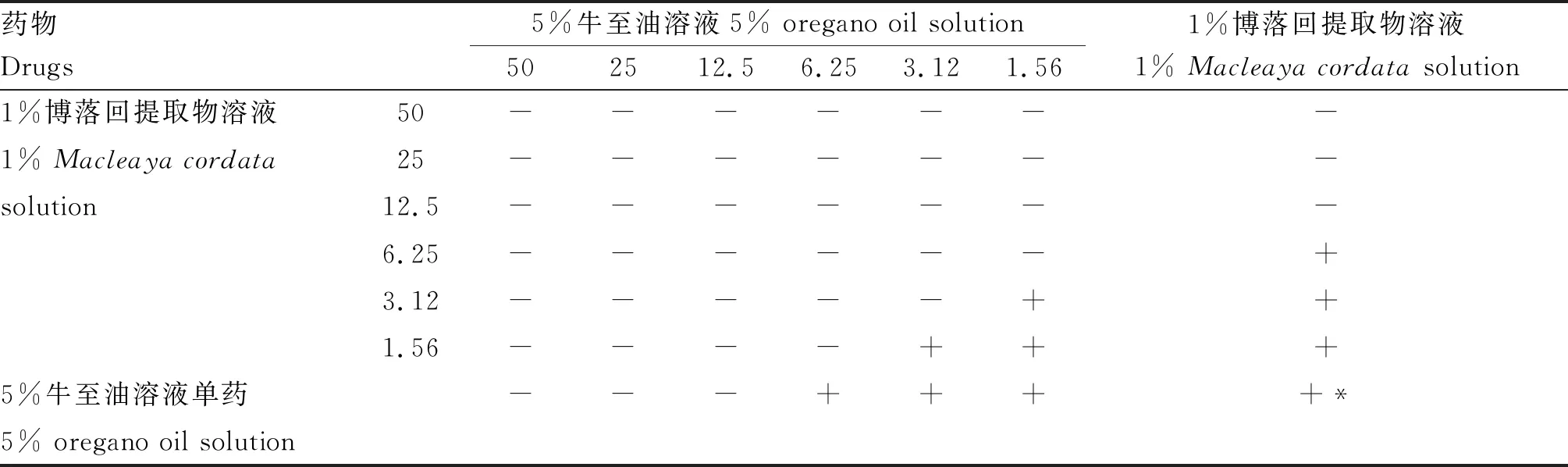
表8 牛至油和博落回提取物对沙门氏菌的联合药敏试验
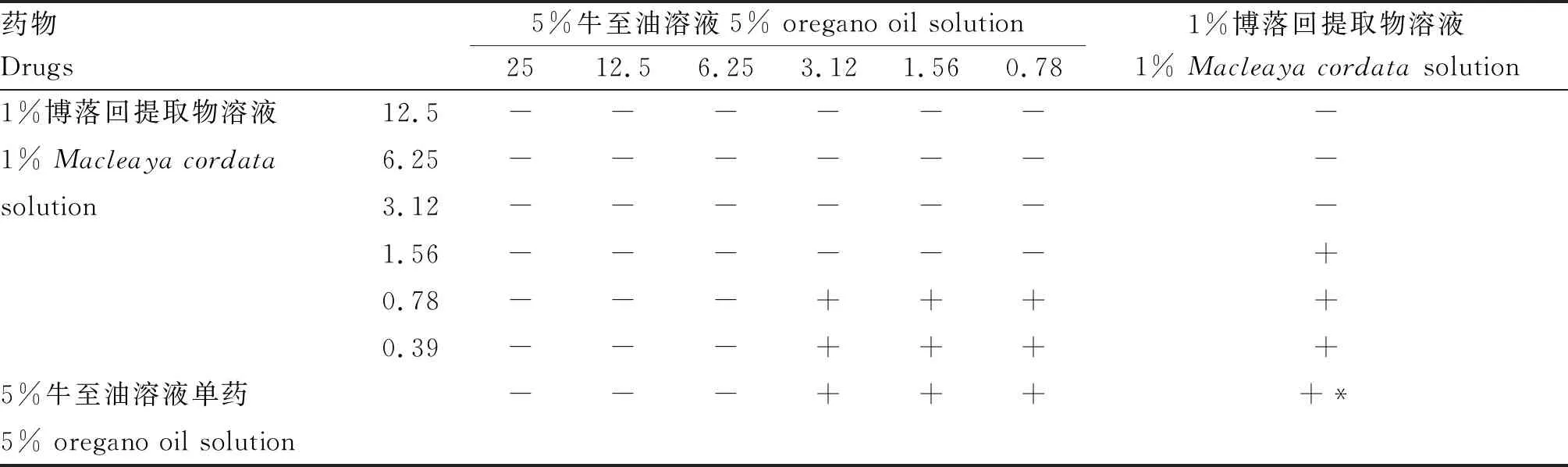
表9 牛至油和博落回提取物对金黄色葡萄球菌的联合药敏试验
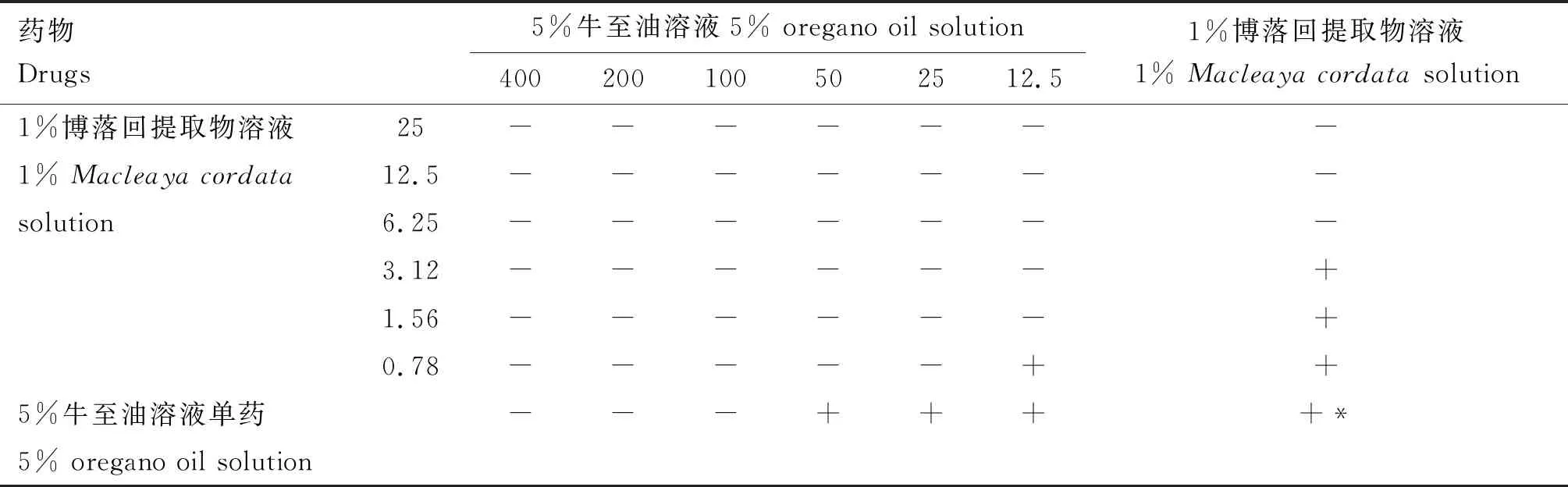
表10 牛至油和博落回提取物对粪链球菌的联合药敏试验

表11 牛至油和博落回提取物的联合药敏试验FIC指数
3 讨 论
牛至油和博落回提取物在临床上常用制剂分别为牛至油预混剂和博落回散,二者均采用混饲给药,混饲给药不仅存在拌料不均问题,而且大多数畜禽在患病后会出现食欲下降甚至食欲废绝,经常需要高剂量给药或频繁给药,往往难以保证疗效,也提高了畜禽药物中毒的可能性[16]。口服液混饮给药可以将药物均匀溶解于水中,在保证给药量的同时降低了畜禽药物中毒的可能性,也适应了规模化养殖场的水线供水系统。
3.1 牛至油博落回口服液处方优化
通过处方筛选并采用响应面法进行优化,成功制备出了牛至油博落回口服液。该制剂处方中2种成分都不溶于水,由于是口服液剂,且主要针对规模化养殖场乳头饮水给药,所以选择水作为溶剂;通过筛选不同增溶剂对牛至油和博落回提取物的增溶效果,其中RH40增溶效果最好用量最少,且无毒无刺激性,故确定RH40为增溶剂;而牛至油易氧化,应选择脂溶性抗氧化剂,其中BHT属于油脂抗氧化剂且符合安全标准,故根据BHT标准用量添加。
颜色、状态、气味等感官评价为溶液剂的主要质量要求,因此以感官评分为考察指标,应用响应面法进行优化,3个影响因素对感官评分构成三维空间的响应面图和二维平面的等高线图,能够直观地反映出3因素的相互作用和对感官评分的影响。响应面越陡峭,表示该因素对感官评分的影响越大,响应面越平缓,表示该因素对感官评分的影响越小[17]。随着牛至油、博落回提取物和RH40的增加,感官评分呈先上升后下降的趋势,说明3个因素对感官评分均有较明显的影响,且两两因素之间的交互作用均显著。结果表明,牛至油添加量对口服液感官影响最显著,RH40添加量影响次之,博落回提取物添加量对口服液感官影响最小。
3.2 牛至油博落回口服液体外抑菌试验
王新伟等[18]就牛至油对大肠杆菌和金黄色葡萄球菌的抑菌效果研究表明,牛至油对大肠杆菌和金黄色葡萄球菌均有明显抑制作用,且对金黄色葡萄球菌的抑制能力明显强于对大肠杆菌,其中低浓度牛至油对2种细菌的抑菌活性与本研究结果完全一致。许璐等[19]研究发现,牛至油与香芹酚对金黄色葡萄球菌和粪链球菌的杀菌效果相当,百里香酚对金黄色葡萄球菌的杀菌效果与牛至油和香芹酚相当,对粪链球菌的作用较弱,推测本研究中1%牛至油溶液对粪链球菌抑杀作用弱的原因可能是在水溶液的制备过程中有酚类损失。王朝元等[20]研究发现,博落回生物碱对金黄色葡萄球菌的抑菌效果较好;李美荃等[21]研究显示,随着浓度的增加,博落回生物碱对金黄色葡萄球菌、沙门氏菌及大肠杆菌的抑制效果增强,其中对金黄色葡萄球菌抑制效果最强。苏红等[22]研究博落回提取物中血根碱对沙门氏菌、金黄色葡萄球菌和大肠杆菌等的抑菌效果发现,其对金黄色葡萄球菌、粪链球菌的抑制作用最强,这与本试验结果相一致。
研究发现,牛至油和博落回提取物对革兰氏阴性和阳性菌均有较强的抑菌效果[23]。牛至油抗菌机制主要是使细胞质膜通透和去极化[24],抑制细菌生物膜的形成,影响细菌蛋白质的合成[25]等。博落回提取物抗菌机制主要是通过干扰Fts Z蛋白的装配进而抑制细菌分裂,诱导膜结合细胞壁自溶酶的释放,导致细菌溶解[26],抑制DNA合成,影响细胞膜的通透性[27]等,从抗菌机制预计2种药物联用时可以从不同途径抑制并杀死细菌,因此本研究首次将牛至油与博落回提取物联合应用,联合药敏试验结果表明,牛至油与博落回提取物之间存在着良好的正向作用,无颉颃作用,对大肠杆菌及沙门氏菌起相加作用,对金黄色葡萄球菌起无关作用,对粪链球菌为协同作用,因此可以通过联合使用提高临床抗菌效果。
4 结 论
本研究成功研制出可以与水任意比例混溶的牛至油博落回口服液,其中香芹酚含量为42.59 mg/mL,血根碱量为6.51 mg/mL,其对大肠杆菌、沙门氏菌、粪链球菌与金黄色葡萄球菌均有良好的抑制作用,对金黄色葡萄球菌和粪链球菌的抑菌效果最强。联合药敏试验结果显示,牛至油博落回联合用药对大肠杆菌和沙门氏菌起相加作用,对金黄色葡萄球菌起无关作用,对粪链球菌为协同作用,二者联合应用可以提高抗菌效果。

