兴安升麻UPLC指纹图谱及4种酚酸类质量标志物测定
康 璐, 李钰洁, 王 晓, 章弘扬, 张 敏, 胡 坪*
(1.华东理工大学化学与分子工程学院,上海市功能性材料化学重点实验室,上海 200237;2.华东理工大学药学院,上海市新药设计重点实验室,上海 200237)
升麻是毛茛科植物升麻、大三叶升麻或兴安升麻的干燥根茎[1],性味辛,归肺、脾、胃、大肠经,具有发表透疹、清热解毒、升举阳气等功效[2]。升麻为多基原药材,在我国产地分布范围较广,不同基原升麻的化学成分和含量存在一定差异, 其药理活性及临床疗效也有所不同[3]。翁倩倩等[4]对经典名方中所用升麻类药材的名称、基原、道地产地等信息进行了考证,结果表明古代药用升麻的来源主要为升麻,次为兴安升麻、大三叶升麻和其他非正品植物。近些年,随着升麻用量的不断增加,人工栽培的兴安升麻逐渐取代升麻而成为市场上主流的升麻正品药材。然而,人工栽培的升麻质量良莠不齐,市场上升麻品种鱼龙混杂,因此开发有效的方法来鉴别兴安升麻并控制其内在质量具有显著意义。
升麻中的主要化学成分为酚酸类[5-6]、三萜及其苷类[7-8]和色原酮类[9-10]等。现行标准以异阿魏酸的含量作为判断升麻药材是否合格的主要指标,然而,根据中医药理论和实践,中药是靠多种药效成分共同发挥作用[11],因此仅以单一指标成分定量分析难以反映升麻的整体质量。为此,本实验建立了兴安升麻UPLC指纹图谱,并选取阿魏酸、异阿魏酸、升麻酸B和升麻酸F作为质量标志物,开展多指标成分定量方法研究,以期为兴安升麻内在质量的整体评价提供思路,亦为含有升麻药材的经典名方开发提供参考。
1 材料
Waters Acquity Arc超高效液相色谱仪,配PDA二极管阵列检测器(美国Waters公司);KQ-500DE型数控超声波清洗器(江苏昆山超声仪器有限公司);实验室级超纯水发生器(南京易普易达科技发展有限公司);塞多利斯CPA225D分析天平(德国塞多利斯公司);800Y型高速多功能粉碎机(浙江省永康市铂欧五金制品有限公司);DF-101集热式恒温加热磁力搅拌器(河南省巩义市予华仪器有限责任公司)。
阿魏酸对照品(批号110773-201614)和异阿魏酸对照品(批号111698-201103)购自中国食品药品检定研究院;升麻酸B和升麻酸F均为实验室自制,采用红外光谱、电喷雾质谱和核磁共振波谱进行结构确认。乙腈和甲醇为色谱纯;其余试剂均为分析纯。3个不同产地的15批升麻药材及5批升麻饮片(编号S1~S20),信息见表1,由神威药业集团有限公司提供,经河北省食品药品检验院孙宝惠主任中药师鉴定为毛茛科植物兴安升麻Cimicifugadahurica(Turcz) Maxim的干燥根。
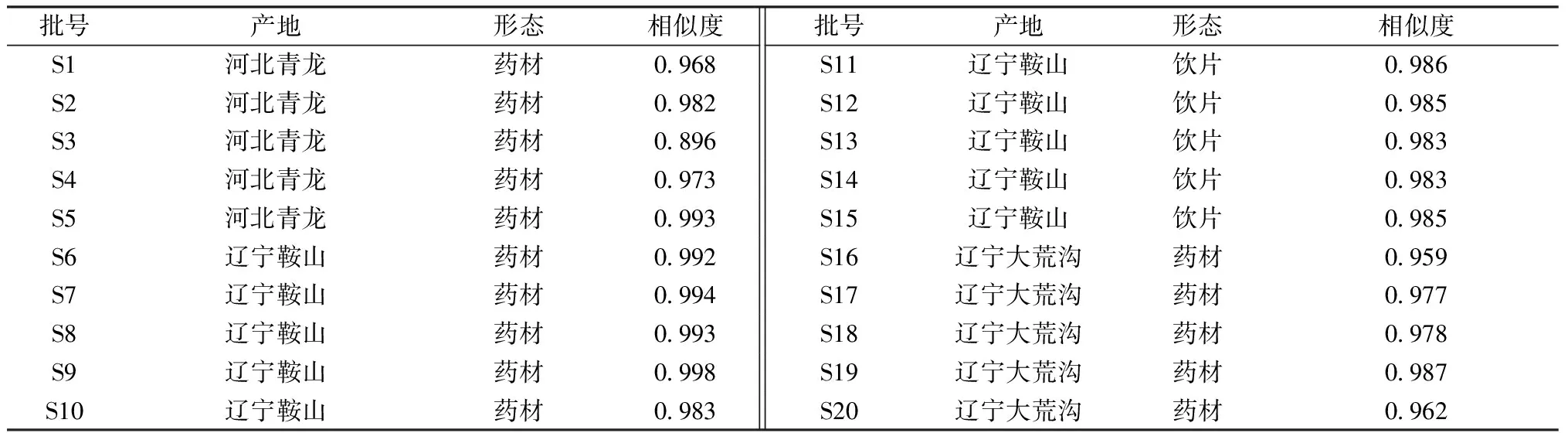
表1 20批样品相似度
2 方法与结果
2.1 兴安升麻UPLC指纹图谱建立
2.1.1 色谱条件 Agilent Eclipse Plus C18色谱柱(2.1 mm×100 mm,1.8 μm);流动相0.1%磷酸水(A)-乙腈(B),洗脱梯度(0~11 min,2%~9%B,11~15 min,9%~16%B,15~35 min,16%~28%B);体积流量0.25 mL/min;柱温35 ℃;进样量2 μL;检测波长220 nm。
2.1.2 供试品溶液制备 取本品粉末(过2号筛)约0.5 g,精密称定。置具塞锥形瓶中,精密加入30%甲醇25 mL,称定质量,超声30 min,放冷,再次称定质量,用30%甲醇补足减失质量,摇匀,经0.22 μm滤膜过滤,即得。
2.1.3 对照品溶液制备 取异阿魏酸对照品适量,精密称定,置25 mL量瓶中,加30%甲醇稀释至刻度,制成质量浓度为0.05 mg/mL的对照品溶液,即得。
2.1.4 UPLC指纹图谱方法学验证 取同一份兴安升麻供试品溶液(S2),连续进样6次,记录色谱图,对仪器的精密度进行考察。取同一批升麻,平行制备6份供试品溶液,记录色谱图,对供试品溶液制备的重复性进行考察。取同一份供试品溶液,分别于0、2、4、6、8、12 h进样,记录色谱图,对供试品溶液的稳定性进行考察。分别计算图1中11个特征峰(1~11号峰)相对于5号峰异阿魏酸(S)的相对保留时间和相对峰面积。结果表明,精密度、重复性、稳定性试验中,各特征峰相对保留时间的RSD均小于1.30%,相对峰面积的RSD均小于5.0%,方法验证结果符合指纹图谱分析的要求。
2.1.5 兴安升麻UPLC指纹图谱测定及相似度评价 采用“2.1.1”项下的色谱方法,对15批兴安升麻药材和5批饮片的供试品溶液进行分析,典型的兴安升麻UPLC指纹图谱见图1。通过对上述20批兴安升麻的指纹图谱对比分析,选取分离度良好,峰形对称的11个共有峰作为特征峰。其中将5号色谱峰(异阿魏酸)定为指纹图谱的参照峰。采用中药色谱指纹图谱相似度评价系统(2012)对20批兴安升麻的UPLC指纹图谱相似度进行了评价,结果见表2。结果显示,不同产地兴安升麻指纹图谱的相似度在0.896~0.998之间,同一产地的兴安升麻药材与饮片的指纹图谱亦具有较高的相似度。表明本实验所选取的不同产地的兴安升麻内在质量较为一致,且饮片的炮制过程对指纹图谱的相似度影响不大。
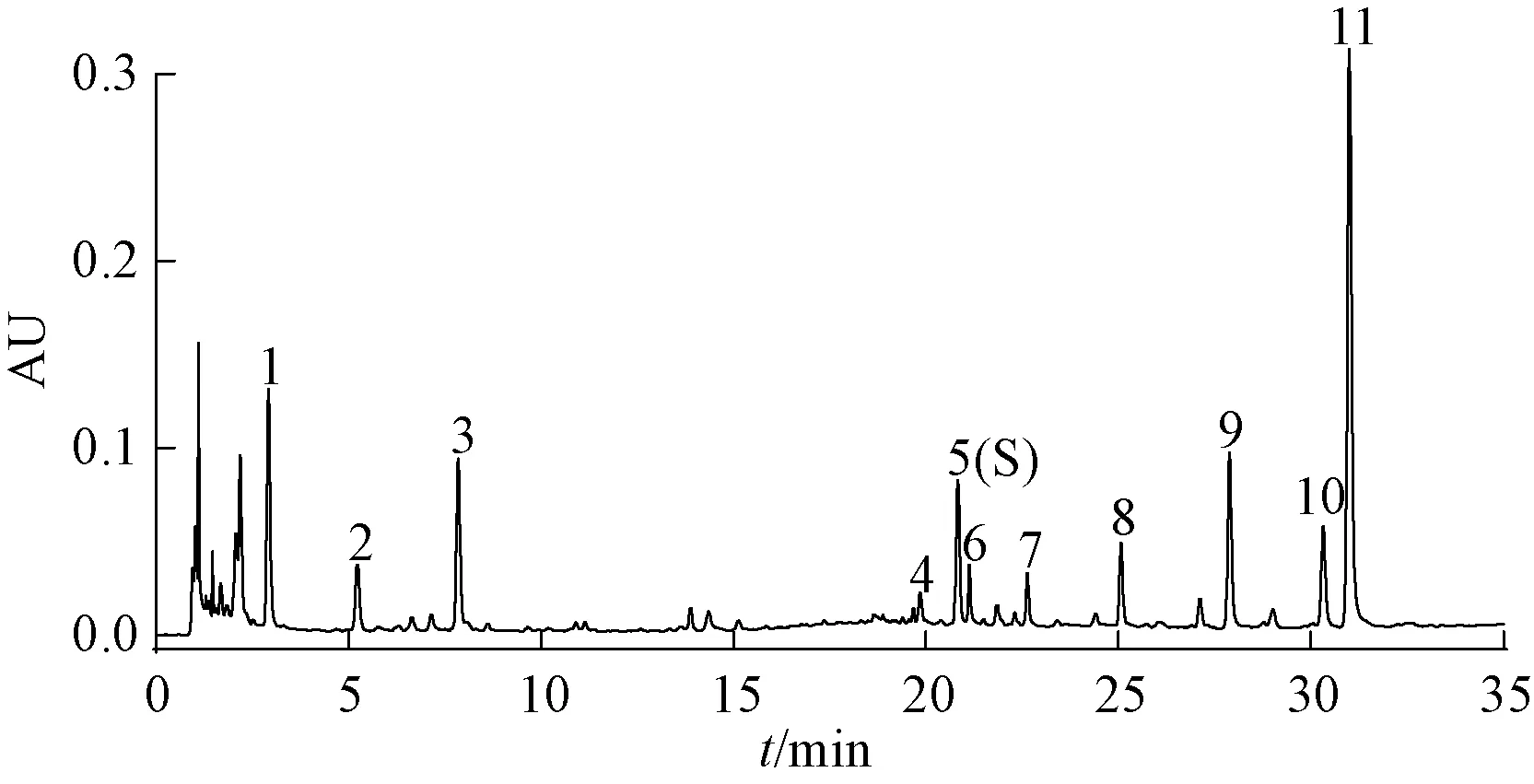
5(S)异阿魏酸5 (S) isoferulic acid图1 20批样品UPLC指纹图谱Fig.1 UPLC fingerprints of twenty batches of samples
2.2 4种酚酸类成分含量测定
2.2.1 色谱条件 检测波长为316 nm,其他条件同“2.1.1”项。
2.2.2 对照品溶液制备 分别取阿魏酸、异阿魏酸、升麻酸B和升麻酸F对照品适量,精密称定,置5 mL量瓶中,加70%甲醇溶解并稀释至刻度,分别制成质量浓度为1.054、1.016、1.072、1.026 mg/mL的对照品贮备液。吸取上述各对照品贮备液适量,制成不同质量浓度的混合对照品溶液,于4 ℃下保存。
2.2.3 供试品溶液制备 取本品粉末(过2号筛)约0.5 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇25 mL,称定质量,超声40 min,冷却,再称定质量,用70%甲醇补足减失的质量,摇匀,经0.22 μm滤膜过滤,即得。
2.2.4 方法学考察
2.2.4.1 系统适用性试验 分别吸取空白溶液、混合对照品溶液及供试品溶液,在“2.2.1”项色谱条件下进样,记录色谱图,见图2。结果显示,空白溶液对供试品测定无干扰,4种酚酸成分峰形对称,分离度良好,满足定量分析要求。
2.2.4.2 线性关系考察 取混合对照品溶液,在“2.2.1”项色谱条件下进样,记录色谱图。以对照品溶液的浓度为横坐标(X),峰面积为纵坐标(Y)绘制标准曲线,得到回归方程、线性范围及相关系数。另取阿魏酸、异阿魏酸、升麻酸B及升麻酸F对照品溶液,不断稀释,在“2.2.1”项色谱条件下测定,分别选取10倍信噪比(S/N=10)和3倍信噪比(S/N=3)对应的质量浓度为定量限和检测限,结果见表2。结果表明,4种酚酸成分在各自范围内线性关系良好。
2.2.4.3 精密度试验 取S1供试品溶液,在“2.2.1”项色谱条件下连续进样分析6次,记录色谱图。测得阿魏酸、异阿魏酸、升麻酸B和升麻酸F含量的RSD值均小于1.71%,表明仪器精密度良好。
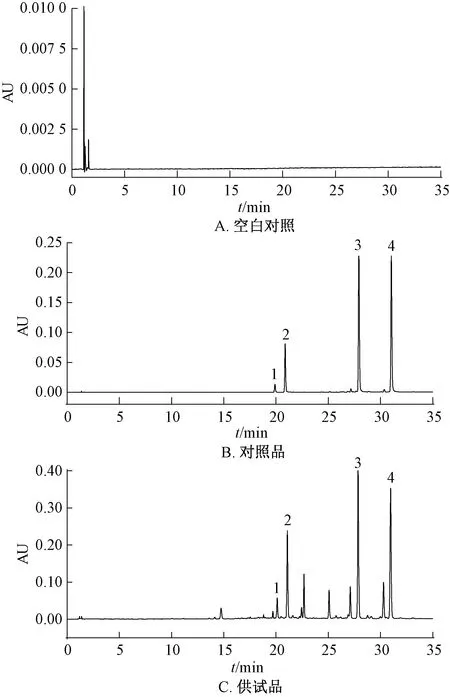
1. 阿魏酸 2. 异阿魏酸 3. 升麻酸 B 4. 升麻酸 F1.ferulic acid 2.isoferulic acid 3.cimicifugic acid B4.cimicifugic acid F图2 各成分UPLC色谱图Fig.2 UPLC chromatograms of various constituents

表2 各成分线性关系
2.2.4.4 重复性试验 按“2.2.3”项下方法平行制备S1供试品溶液共6份,在“2.2.1”项色谱条件下分别进样分析,测得阿魏酸、异阿魏酸、升麻酸B和升麻酸F含量的RSD值均小于4.67%,表明该方法重复性良好。
2.2.4.5 稳定性试验 取S1供试品溶液,在“2.2.1”项色谱条件下,分别在0、2、4、6、8、12 h进样,测得阿魏酸、异阿魏酸、升麻酸B和升麻酸F含量的RSD值均小于4.48%,表明供试品溶液在12 h内稳定性良好。
2.2.4.6 加样回收率试验 精密称取同一批次升麻样品6份,每份0.25 g,分别加入阿魏酸、异阿魏酸、升麻酸B和升麻酸F对照品8.20×10-3、0.159、1.675、1.603 mg,按“2.2.3”项下方法制备供试品溶液,在“2.2.1”项色谱条件下进样,结果见表3。
2.2.5 样品含量测定 采用已验证的定量方法对20批兴安升麻供试品溶液中阿魏酸、异阿魏酸、升麻酸B和升麻酸F的含量进行了测定,结果见表4。由表可见,20批兴安升麻药材和饮片中,阿魏酸和异阿魏酸的含量分别介于0.008%~0.018%和0.061%~0.120%,均值分别为0.011%和0.089%,含量均较低。而升麻酸B和升麻酸F的含量分别介于0.228%~1.235%和0.661%~1.373%,均值分别为0.633%和0.995%,含量均较高,为兴安升麻中主要的酚酸类成分。
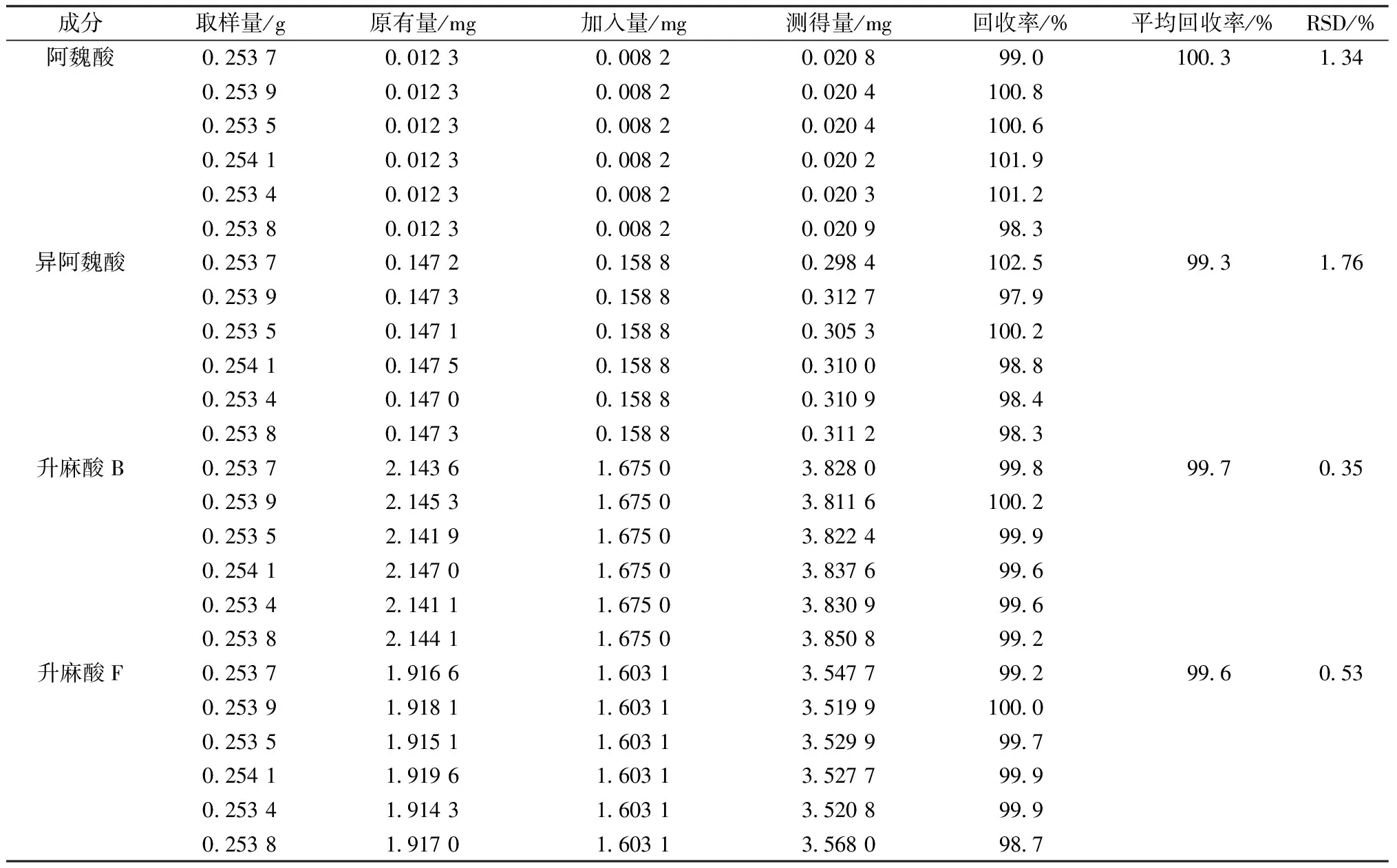
表3 各成分加样回收率试验结果(n=6)
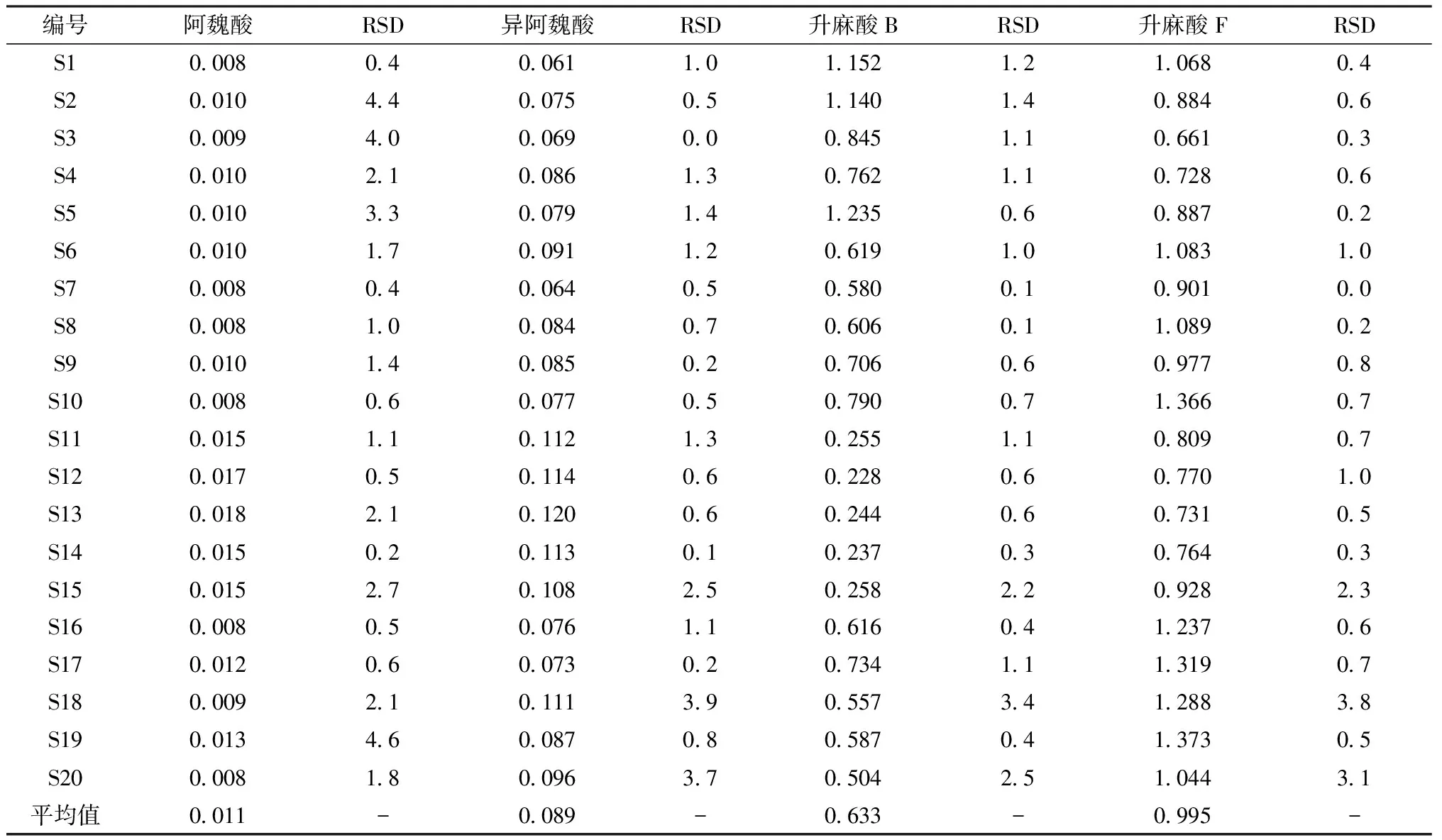
表4 各成分含量测定结果(%,n=3)
3 讨论
3.1 色谱条件优化 考察了流动相、柱温和体积流量对分离的影响。结果表明,“2.1.1”项条件下,色谱峰信息最为丰富,各特征峰的峰形对称,分离度良好,适用于指纹图谱分析。当波长为316 nm时,4个待测酚酸类成分响应均较高,且附近无杂质干扰,适用于定量研究。
3.2 提取条件选择 对提取溶剂、提取时间和提取溶剂体积进行优化。结果显示,采用25 mL、30%甲醇溶液超声提取30 min时,供试品的谱峰信息最为丰富,各特征峰峰形良好且响应值均较高。参照2020年版《中国药典》,采用回流法对兴安升麻中酚酸类成分进行提取。研究了回流时间对4种酚酸类成分的提取效率影响。结果表明,随着回流时间的增长,供试品溶液中升麻酸B和升麻酸F的含量逐渐降低,而阿魏酸和异阿魏酸的含量逐渐升高。这可能是由于在较高温度下升麻酸A和E会逐渐水解生成阿魏酸,而升麻酸B和F水解生成异阿魏酸,又由于升麻酸B和F的含量高于升麻酸A和E,所以生成异阿魏酸的含量明显高于阿魏酸[12-13]。因此,本实验采用温和的超声法替代回流法制备供试品溶液,考察了超声时间、提取溶剂和提取溶剂体积对4种酚酸成分提取效率的影响。结果显示,采用25 mL的70%甲醇,超声提取30 min时,各成分的提取效率最高。
3.3 酚酸类质量标志物含量测定的讨论 参考文献[14]报道,本实验提出以阿魏酸、异阿魏酸、升麻酸B和升麻酸F作为兴安升麻的质量标志物,对其药材和饮片进行质量评价与控制。这是由于(1)阿魏酸、异阿魏酸、升麻酸B和升麻酸F是升麻中固有的,且与其功能属性密切相关的化学成分[15-17];(2)酚酸类物质极性较强,是升麻在经典名方、配方颗粒等水煎制剂中的主要有效成分[18];(3)升麻酸B和升麻酸F在兴安升麻药材和饮片中均存在且含量相对较高,与阿魏酸和异阿魏酸同为升麻属的特征性成分,具有较强的专属性。
表2显示,4种酚酸类质量标志物在20批兴安升麻中的含量差异较大。表明同基原不同产地的兴安升麻药材中的酚酸含量具有较大差别。此外,对比辽宁鞍山产药材和饮片(S11~S15)发现,饮片中阿魏酸和异阿魏酸的含量远高于药材,而升麻酸B和升麻酸F的含量明显偏低。这可能是润透、干燥等饮片炮制过程使酚酸类成分发生了部分水解,导致升麻酸B和升麻酸F的含量下降,阿魏酸和异阿魏酸的含量升高。
4 结论
本实验提出以阿魏酸、异阿魏酸、升麻酸B和升麻酸F作为兴安升麻的质量标志物,建立了兴安升麻UPLC指纹图谱,并测定4种酚酸类质量标志物,以期从整体上把控兴安升麻的质量,也为含有升麻药材的经典名方开发提供参考。

