功能化自组装肽水凝胶在细胞培养中应用
张书筠,于 鑫,丁 晨,林 晓,朱 伟
(牡丹江医学院 免疫教研室,黑龙江 牡丹江157011)
细胞培养是生物医学领域中重要研究方法,在研究细胞功能、探讨疾病发病机制中发挥巨大作用。细胞在体内处于三维环境,接收微环境中物理、化学信号,维持细胞生物学功能,并且通过增殖或分泌因子,对受损组织进行修复[1-2]。传统细胞培养属于二维细胞培养,没有细胞外基质支持,长时间培养将影响细胞形态特征及生长、分化等生物学功能[3]。因此,越来越多的学者研究三维支架材料制备及材料与细胞间相互作用,期望能更好模拟细胞体内微环境,保证微环境结构基础及体外细胞培养的直观性、可控性[4]。虽然这些材料在一定程度上模拟细胞微环境和细胞与细胞外基质间的信号,但仍然存在一些问题,如高感染风险率、较差相容性等。理想细胞支架通常应具备适合细胞生长的孔径、良好相容性、可降解产物无毒及易于合成等特点[5]。
自组装肽水凝胶是通过对多肽分子的构成氨基酸序列进行设计,在特定条件下,可以使得多肽分子自发组装。由于大部分多肽链本身并不具备直接自组装成凝胶的性能,需要向体系中引入一些能够起到桥连作用的分子,诱导水凝胶的形成。通常的桥连剂包括蛋白质、金属离子、小分子表面活性剂等[6]。功能化自组装多肽水凝胶是在设计多肽链时增加功能基序,或者在多态水凝胶结构中嵌入生长因子、转化因子等细胞因子,从而满足不同细胞生长需要。
1 自组装肽水凝胶概述
早在20世纪90年代,就有研究人员在酵母蛋白中发现一种天然蛋白序列Zuotin,其具有β折叠结构,能自发形成三维网状结构[7]。科学家们从中受到启发,利用氨基酸的基本特性,根据需要设计出不同的多肽链形成特殊的二级结构,在合适的条件下,通过范德华力、疏水作用、π-π堆积力等相互作用,使得其能自发形成复杂的三维结构。在此基础上,自组装肽序列的设计得到不断优化,逐渐形成第一代自组装肽。第一代自组装肽序列特征是带电亲水性及疏水性氨基酸周期性交替排列。在纳米纤维亲水性表面上,带有正、负电荷氨基酸残基重复性的交替排列,有助于互补的离子相互作用形成网状结构,并进一步形成含水量超过99.5%的水凝胶支架[8-10](图1)。为提高自组装肽生物学活性,近年来研究人员在第一代自组装肽氨基酸序列基础上,加入功能性基序,合成具有生物学活性的功能性自组装肽水凝胶即第二代自组装肽[11]。
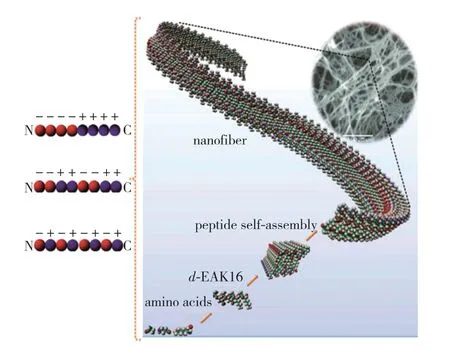
图1 自组装肽水凝胶的形成过程[10]Fig.1 Formation of self-assembled peptide hydrogels[10]
功能性自组装肽制备方法通常是将功能性基序通过甘氨酸连接到自组装肽C末端,不同功能性基序赋予自组装肽不同细胞特异性,目前研究发现的功能基序及其作用见表1[11-19]。
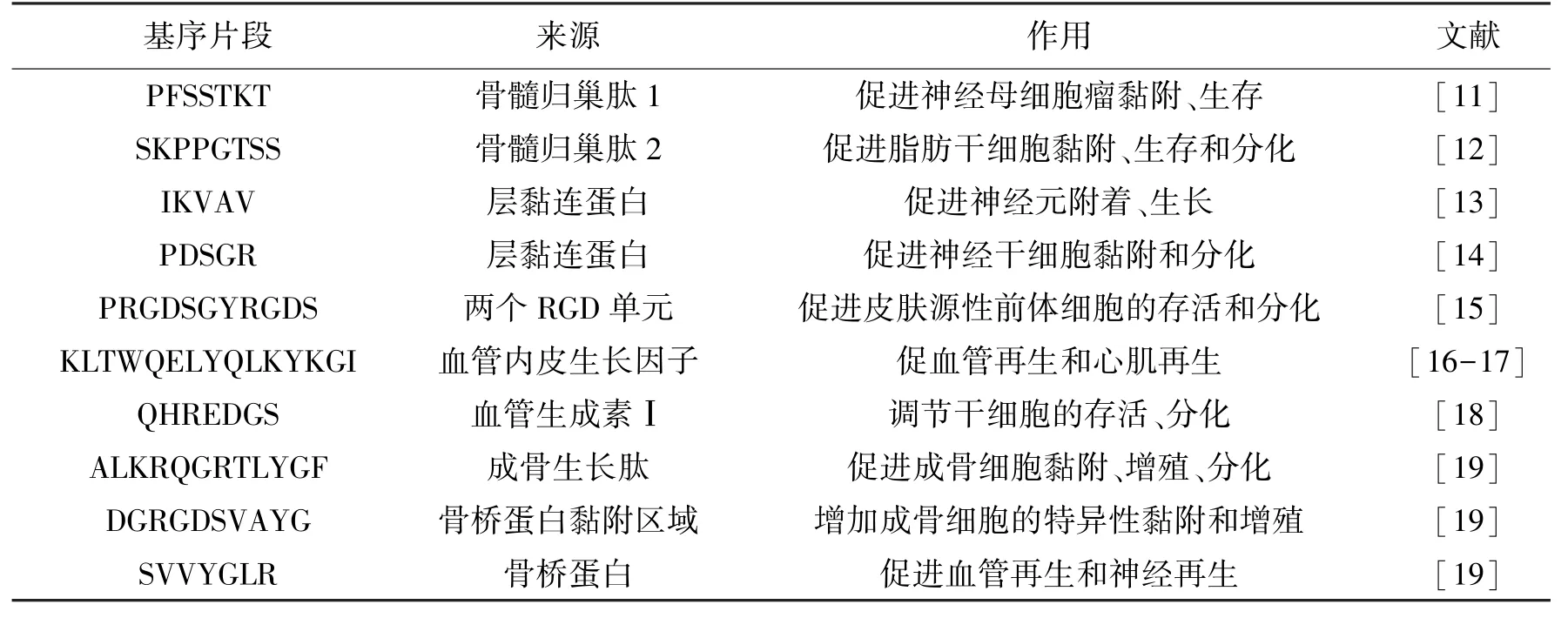
表1 自组装肽水凝胶的常见功能基序Table 1 Common functional motifs of self-assemble peptide hydrogels
除上述功能化基序外,生长因子、转化因子等可溶性蛋白也可直接或间接固定在自组装肽水凝胶上,为细胞提供信号刺激,有助于效应分子停留在靶标部位,并且以受控的方式向四周释放[20]。如携带胰岛素样生长因子Ⅰ[21]或血管内皮生长因子[22]的自组装肽纳米纤维NFs水凝胶,将其注射到实验性心肌梗死的动物模型体内,可刺激缺血部位血管内皮细胞增生,改善心肌缺血缺氧状态,并加快组织再生。
虽然功能性自组装肽具有良好生物学活性,但其刚度与实际的组织匹配度较差,因此近年来研究人员将自组装肽水凝胶与惰性生物材料混合制成复合材料,以此为细胞培养提供更接近于体内的微环境。Sheikholeslam等[23]研究发现,在碳纳米管中离子互补型肽EFK8(FEFEFKFK)分散存在,加入单价盐溶液,触发形成EFK8-SWNT水凝胶,可增强NIH- 3T3、A549细胞的附着、扩散及增殖;同时他们发现,改变水凝胶刚度不影响NIH -3T3细胞的行为,但可使A549细胞形态从球状转变为拉伸态。Anderson等[24]研究发现,不同类型细胞,其培养底物刚度阈值不同。Xu等[25]在自组装肽水凝胶中加入羟基磷灰石(hydroxyapatite,HAP)可以增加稳定性,同时促进MC3TC -E1细胞分化。这些结果表明:将惰性材料与水凝胶混合可扩大自组装肽水凝胶在组织工程中的应用范围。
2 功能化自组装肽水凝胶在细胞培养中的应用
2.1 对干细胞移植和培养的促进作用
干细胞移植治疗在临床上表现出明显的治疗效果,但是由于受损组织存在不同程度炎症反应,会影响干细胞的活性和数量,而生物材料可为干细胞提供生长环境,促进干细胞增殖和分化。Luo等[26]研究发现:用腺病毒转载修饰间充质干细胞(MSC)的人脑源性神经营养因子hBDNF的基因,并用PRG基序修饰RADA16(Ac -(RADA)4-CONH2)水凝胶来培养,可促进细胞向支架内部迁移,增加细胞活性而且诱导分化为神经元。此外,Cai等[18]将QHREDGS基序修饰RADA16形成新的自组装肽水凝胶DSAP,将DSAP包裹的MSC进行体内外研究时发现:DSAP -MSC可通过活化AKT,促进胰岛素样生长因子Ⅰ、肝细胞生长因子表达,减少心肌细胞凋亡,保护在氧和葡萄糖缺乏环境中的心肌细胞,可使心肌梗死模型鼠梗死区域胶原蛋白含量降低,心肌细胞凋亡和梗死面积减少;同时,DSAP -MSC也可促进心肌梗死模型鼠梗死区域微血管的形成,改善心脏功能。这些研究结果表明:功能性自组装肽水凝胶可以作为传递系统为干细胞治疗治疗心肌梗死提供新的方法和策略。
在自组装肽水凝胶中添加功能性基序不仅可以促进间充质干细胞黏附、生存,而且可以促进干细胞向成骨和软骨细胞分化。Tavakol等[27]将骨髓归巢肽1(BMHP1)基序通过甘氨酸与自组装肽RADA4结合形成水凝胶R -BMHP1,R-BMHP1不但能增强骨髓间充质干细胞(BMSC)的生存能力,而且R -BMHP1纳米纤维的拓扑结构与骨成型蛋白受体1A产生强静电相互作用,触发下游信号转导,导致BMSC成骨基因过度表达,发生钙沉积。这项研究表明,R -BMHP1具有成为成骨修复支架的可行性。
利用脱细胞技术,去除软骨组织细胞成分和遗传物质,保留细胞外基质成分及其力学性能,制备脱软骨细胞基质(ACM)支架,该支架不仅可模拟软骨细胞体内生存微环境,而且促进MSC附着、增殖及分化为软骨细胞[28-29]。为促进干细胞的培养,Lu等[30]将ACM支架与RAD/PFS功能化自组装肽结合,形成复合水凝胶支架ACM/RAD/PFS培养MSC,结果发现,ACM/RAD/PFS混合水凝胶促进MSC附着、增殖、软骨分化。同时,Mushahary等[31]研究发现,在复合水凝胶支架中,PFS基序有助于快速有效地招募间充质干细胞,为组织再生开辟新途径。
功能化自组装肽水凝胶还可用于神经干细胞(NSC)的三维细胞培养。Mehrban等[32]在α-螺旋卷曲肽形成的自组装水凝胶hSAF上添加RGDS基序,微管相关蛋白2表达增加,而胶质原纤维酸性蛋白表达减少;与未修饰的hSAF相比,hSAF -RGDS促进NSC向成熟神经元分化,形成更大神经球。另外,RGDS基序还可促进NSC定向迁移。
自组装肽水凝胶的功能性基序可促进干细胞黏附、分化,增强细胞活性。除此之外,自组装肽水凝胶的力学性能也可影响干细胞活性。如:Farrukh等[33]将多聚赖氨酸(PL)和IKVAV基序分别通过胺基、硫醇基与聚丙烯酰胺(PA)结合,制成双功能水凝胶,研究在PL和IKVAV基序协同作用下,其刚性对胚胎和成人神经元干细胞的影响,结果发现:在胚胎干细胞培养中,将双功能水凝胶刚度调至2 kPa,可促进胚胎皮质神经元分化,形成包含β-整联蛋白的黏着斑;在成人神经干细胞培养中,水凝胶刚度调至20 kPa,可促进NSC细胞存活、成熟、神经突起生长以及神经再生。这表明自组装肽水凝胶支架的力学性能具有引导干细胞行为的潜力。
2.2 对成骨细胞的增殖作用
功能化自组装肽水凝胶不仅可以为成骨细胞提供三维环境,还可以诱导骨细胞分泌骨特异性蛋白。Horii等[19]在自组装肽水凝胶RADA16上添加功能性基序ALK、DGR和PGR,可有效促进成骨细胞MC3T3-E1增殖,并促使细胞向三维支架迁移。Tsutsumi等[34]研究发现:两亲性肽E1Y9(Ac- EYEYKYEYKY -NH2)自组装水凝胶,具有为磷酸钙矿化储备Ca2+优点,将ALK、DGR、PGR和RGD基序与E1Y9制成混合水凝胶,所有功能化的E1Y9/E1Y9混合水凝胶对MC3T3-E1细胞均表现出良好黏附能力和相容性。特别是E1Y9-ALK/E1Y9混合水凝胶可明显促进细胞增殖,增加碱性磷酸酶、骨桥蛋白的表达,且细胞外基质有明显矿化现象。
2.3 对血管内皮细胞培养的促进作用
Liu等[16]将功能性基序PRG、KLT复合到自组装肽RADA16上,培养人脐静脉内皮细胞(HUVEC),结果发现:PRG、KLT可明显提高自组装肽RADA16的生物活性,并为内皮细胞迁移和出芽提供理想的微环境。其中,KLT/RADA16表现出更好血管生成活性,在无血管内皮生长因子时,仍可以在支架中形成新的毛细血管。为体外培养HUVEC提供类似于细胞外基质力学抗性结构,Martínez-Ramos等[35]将聚丙烯酸乙酯(PEA)支架与RAD16结合形成混合自组装肽水凝,经流式细胞仪和扫描电镜检测发现:混合自组装肽水凝胶可增加细胞存活率、增殖,促进细胞间交流。由此可见,功能性自组装肽水凝胶是体外内皮细胞培养的良好生物底物。
2.4 对肿瘤细胞的抑制作用
自装肽水凝胶RADA16可以构建三维肿瘤细胞培养模型[36],并且在肿瘤细胞恶性表型逆转方面发挥效应[37]。基于RADA16在肿瘤细胞培养中的应用,Liu等[38]设计出RADA-KLA(RADARADARADARADARADARADARADARADAGGKLAKLAKKLAKLAK-NH2)功能化自组装肽水凝胶,培养HepG2细胞后发现,RADA -KLA水凝胶能够诱导细胞死亡,降低细胞存活率和抑制细胞黏附和迁移。这说明,RADA -KLA在体外具有抗肿瘤作用,但是在体内的作用仍需要进一步研究。
3 结论与展望
综上所述,自组装肽水凝胶制备过程中可通过改变氨基酸序列、添加功能性基序等方式,设计出具有特定性能自组装肽水凝胶,为不同类型组织细胞培养提供合适的细胞外基质。自组装肽具有可降解、低免疫原性、生物相容性好等优势,但自组装肽应用仍然面临很多挑战,例如:如何调整制备条件得到具有理想结构自组装肽,怎样进一步提高功能性自组装肽生物学活性等。因此,仍需研究者更深入探讨,使自组装肽走向成熟,在细胞培养中发挥更大作用。

