白芍总苷胶囊联合羟氯喹治疗干燥综合征临床疗效的系统评价Δ
石岩硕,邱学佳,赵建群,刘 勇,吴惠珍,董占军(河北省人民医院药学部,石家庄 050051)
干燥综合征(Sjögren’s syndrome,SS)是全球范围内发病率仅次于类风湿关节炎的难治性免疫性疾病,以口、眼干燥为临床基础表现,易引发肝、肾、肺、淋巴和皮肤等多系统损害。SS的发病机制尚不明确,临床认为遗传、免疫系统障碍、感染和环境因素为发病的主要诱因[1]。该病在全球范围内的发病率为0.2%~3.0%,男女比例为1 ∶9,在中老年人群中发病率最高[2]。目前,临床尚无可根治该病的药物,通常选择中西药联合应用的治疗方案来缓解全身损伤症状,改善患者生活质量。免疫抑制剂、糖皮质激素及生物制剂为治疗方案中使用较多的西药。羟氯喹是临床比较认可的用于治疗SS 的免疫抑制剂类药物,该药治疗效果好,不良反应少,在国内外已有较多临床研究和Meta 分析等文献报道[3-4]。但也有研究发现,羟氯喹存在个体化疗效差异,可能导致临床效果不佳和实验室结果指标不理想[5-6]。白芍总苷为白芍提取物中的有效成分,对于多种细胞因子(如白细胞介素、肿瘤坏死因子和核因子κB)都具有调控作用,被广泛用于自身免疫性疾病的治疗[7]。多项临床研究结果显示,白芍总苷胶囊联合羟氯喹治疗SS 可明显提高疗效,优化实验室结果指标。但单项研究样本量小,样本质量有限,所得结论的参考价值不高。本研究通过查阅有关文献资料,选用Meta 分析的方法,将白芍总苷胶囊联合羟氯喹对比单纯使用羟氯喹治疗SS 的疗效进行系统评价,以期为临床治疗该病提供循证学数据支持及合理用药方案参考。
1 资料与方法
1.1 纳入与排除标准
(1)研究类型:已发表的白芍总苷胶囊联合羟氯喹治疗SS 的随机对照试验,不限语种。(2)研究对象:符合《原发性干燥综合征诊疗规范》[8]中相关诊断标准的患者,对年龄、区域、人种和性别属性无特殊要求。(3)干预措施:研究组患者给予羟氯喹,加服白芍总苷胶囊;对照组患者仅给予羟氯喹。两组患者的疗程均为8~12 周。(4)结局指标:①临床疗效指标,采用症状积分下降指数四级评分法评估临床治疗效果,疗效指数=(治疗前总积分-治疗后总积分)/治疗前总积分×100%,分为痊愈(疗效指数≥90%)、显效(疗效指数为60%~<90%)、有效(疗效指数为20%~<60%)和无效(疗效指数<20%),总有效率=(痊愈病例数+显效病例数+有效病例数-复发病例数)/总病例数/100%;②安全性指标,不良反应(视物模糊、胃肠道不适、头晕头痛)发生率。③实验室指标,包括红细胞沉降率(ESR)、唾液腺流率、唾液流量、Schirmer 试验结果(泪流率)和免疫球蛋白G(IgG)水平等。(5)排除标准:非随机对照试验;重复发表文献;非实验性文献、会议论文;样本量<15 例;统计方法不适合;资料不完整或不可查的文献。
1.2 文献检索策略
计算机检索PubMed、Embase、MedLine、the Cochrane Library、中国知网(CNKI)、万方数据库、中国生物医学文献数据库(CBM)、维普数据库(VIP)等数据库,检索时限为建库至2021 年12 月。英文检索词包括“Sjögren’s syndrome”“SS”“Total glucosides of paeony” “ Baishao Zonggan” “ TGP”“hydroxychloroquine”“HCQ”“random”“blind”和“meta”等;中文检索词包括“干燥综合征”“白芍总苷”“帕夫林”“羟氯喹”“随机”“对照”和“系统评价”等。
1.3 资料提取与质量评价
本研究所纳入文献由2 名经系统培训后的研究者独立筛选。资料提取的信息包括题目、作者、对象、方法、措施、结局测量与评价、是否采用分配隐藏等。由2 名研究者根据Cochrane 偏倚风险评估工具[9]进行质量评估,评估内容包括随机序列方法、分配隐藏、盲法、结局数据完整性、选择性报道和其他偏倚,2 名研究者独立评价方法学质量,有不同意见时加入第三人共同判断。
1.4 统计学方法
使用RevMan 5.3 软件进行统计分析,纳入的计数资料包括样本量、总有效病例数、发生不良反应病例数,采用相对危险度(RR)表示;纳入的计量资料包括ESR、唾液腺流率、唾液流量、Schirmer 试验结果(泪流率)和IgG 水平,指标为连续性变量,采用均数差(MD)表示。效应量由数据95%CI表示。所纳入研究之间的异质性采用Chi2检验。若文献之间的异质性无统计学差异(I2≤50%,P≥0.01),采用固定效应模型进行分析;若文献之间的异质性有统计学差异(I2>50%,P<0.01),分析是否存在方法学异质性,如果无方法学异质性,则采用随机效应模型进行分析。分别采用森林图和倒漏斗图标识各数据的分析结果和发表偏移结果。P<0.05为差异有统计学意义。
2 结果
2.1 纳入研究基本信息
经过去重和剔除不合格文献,最终纳入符合要求的随机对照试验文献共10 篇[10-19],均为中文文献,涉及患者731 例。对照组患者服用羟氯喹1 次100~200 mg,1 日2 次;研究组患者服用羟氯喹1 次100~200 mg,1 日2 次,并加服白芍总苷胶囊1 次600~900 mg,1 日3 次。文献筛选流程图见图1;纳入研究的基本信息见表1。
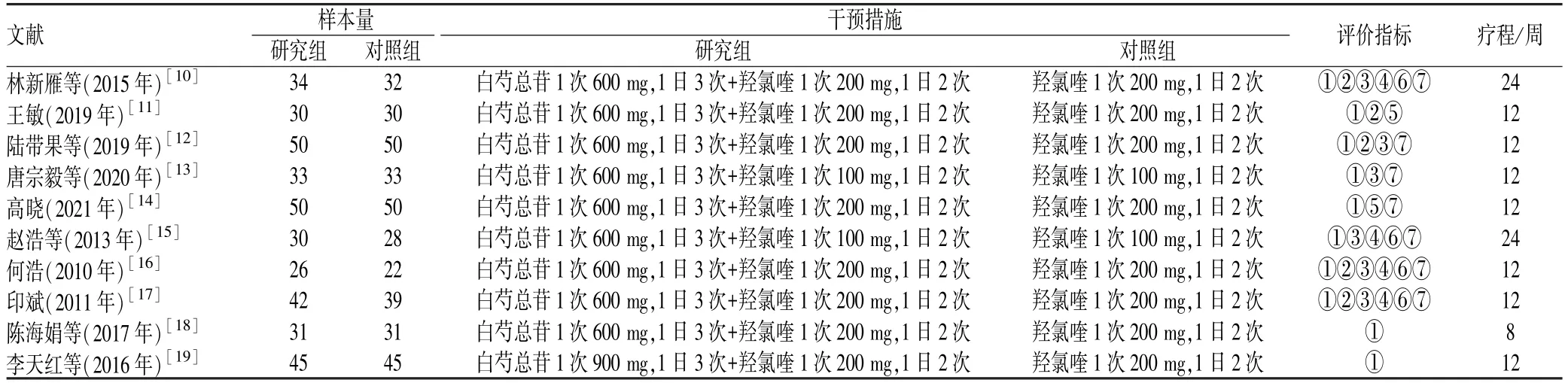
表1 纳入研究的基本信息Tab 1 General information of included studies
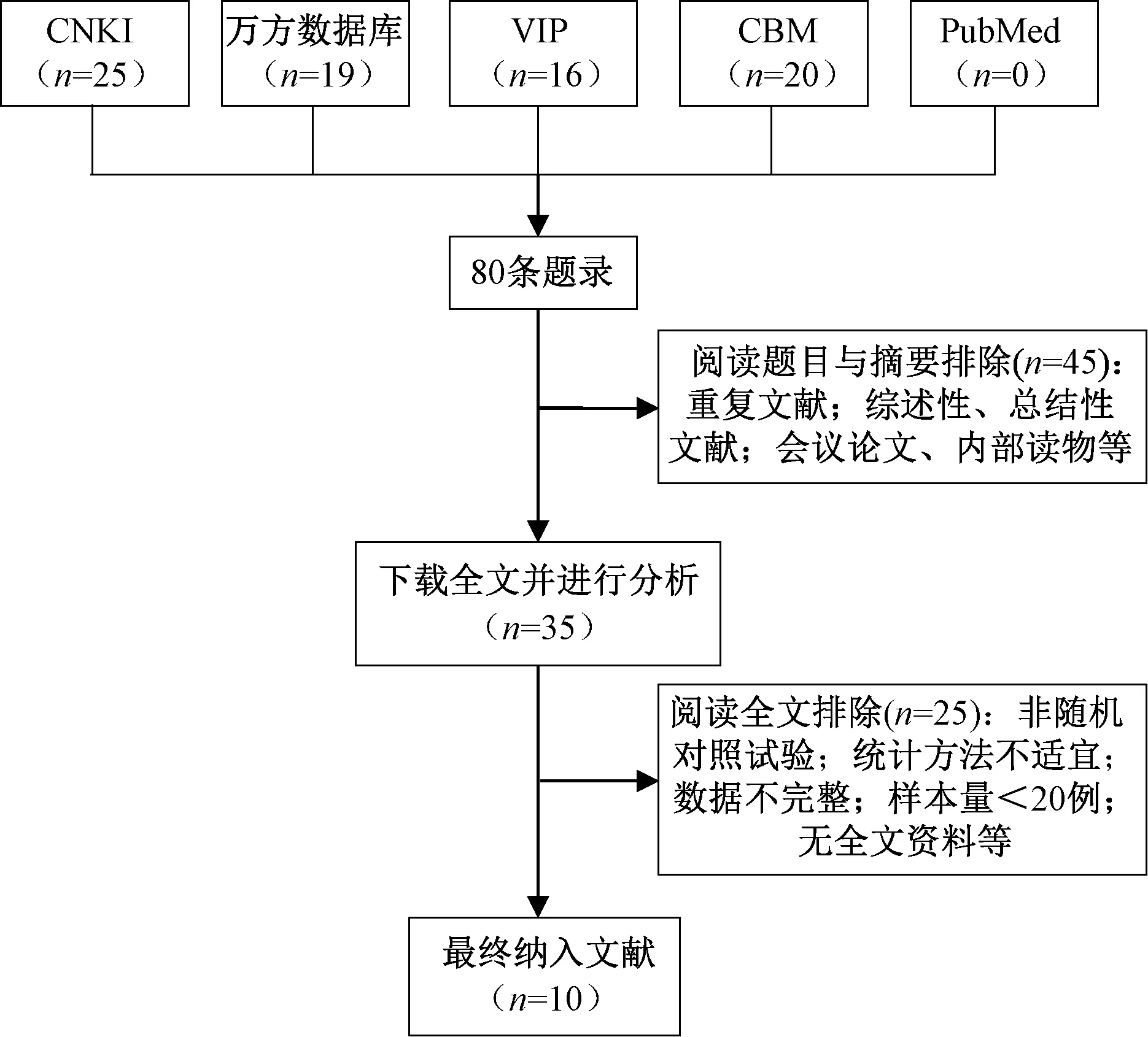
图1 文献筛选流程图Fig 1 Literature screening flow chart
2.2 偏倚风险评估
本研究所纳入的10 项随机对照试验中,2 项[12,14]使用随机数字表法,1 项[11]使用计算机随机分组法,1 项[19]根据患者意愿进行分组,其余6 项[10,13,15-18]未告知详细分组方式;10 项研究均未提及分配隐藏;所有研究数据报告完整,无失访和减员;不清楚有无其他偏倚来源。纳入研究的偏倚风险评估见图2。

图2 纳入研究的偏倚风险评估Fig 2 Risk assessment of bias for included studies
2.3 Meta 分析结果
2.3.1 总有效率:10 项研究[10-19]报告了总有效率,各研究之间无统计学异质性(P=0.09,I2=41%),采用固定效应模型合并效应量进行分析。结果显示,研究组患者的总有效率高于对照组,差异有统计学意义(RR=1.33,95%CI=1.23~1.44,P<0.000 01),见图3。
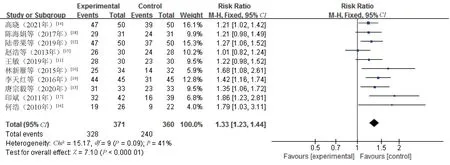
图3 两组患者总有效率比较的Meta 分析森林图Fig 3 Forest plot of Meta-analysis for the comparison of the overall effective rate between two groups
2.3.2 不良反应发生率:5 项研究[10-12,16-17]明确报告了不良反应发生情况,Meta 分析结果显示,研究组与对照组患者不良反应发生率比较,采用无统计学意义(OR=1.44,95%CI=0.73~2.84,P=0.29),见图4。
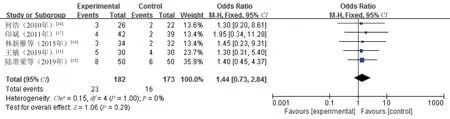
图4 两组患者不良反应发生率比较的Meta 分析森林图Fig 4 Forest plot of Meta-analysis for the comparison of the incidence of adverse reaction between two groups
2.3.3 ESR:6 项研究[10,12-13,15-17]报告了ESR,各研究之间有统计学异质性(P<0.000 01,I2=96%),采用随机效应模型合并效应量进行分析。结果显示,研究组患者的ESR 水平显著低于对照组,差异有统计学意义(MD=-8.00,95%CI=-12.07~-3.93,P=0.000 1),见图5。
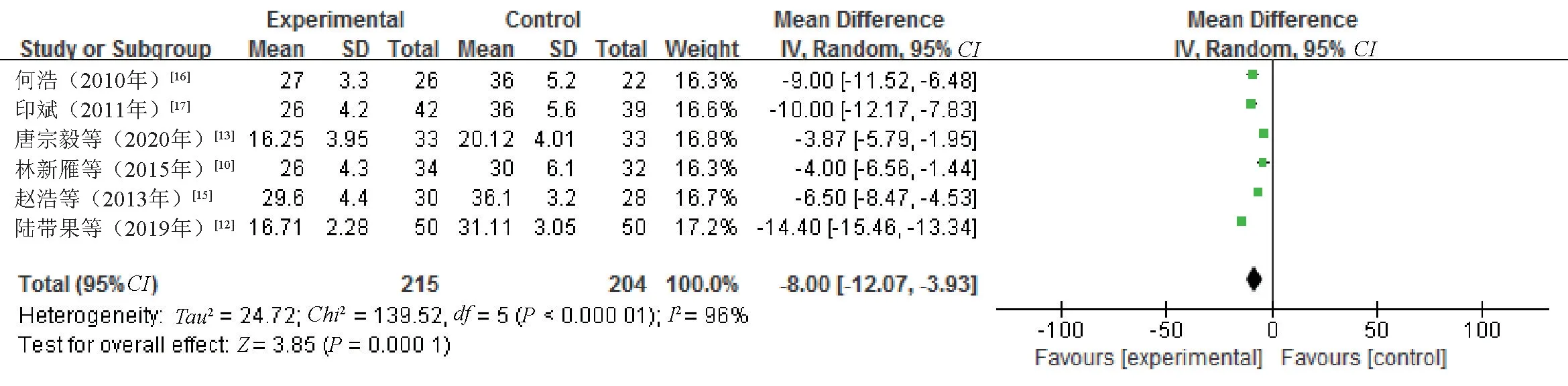
图5 两组患者ESR 比较的Meta 分析森林图Fig 5 Forest plot of Meta-analysis for the comparison of ESR between two groups
2.3.4 唾液腺流率:2 项研究[11,14]报告了唾液腺流率,使用MD分析法,各研究之间没有统计学异质性(P=1.00,I2=0%),采用固定模型合并效应量进行分析。结果显示,研究组患者的唾液腺流率高于对照组,差异有统计学意义(MD=0.03,95%CI=0.02~0.04,P<0.000 01),见图6。
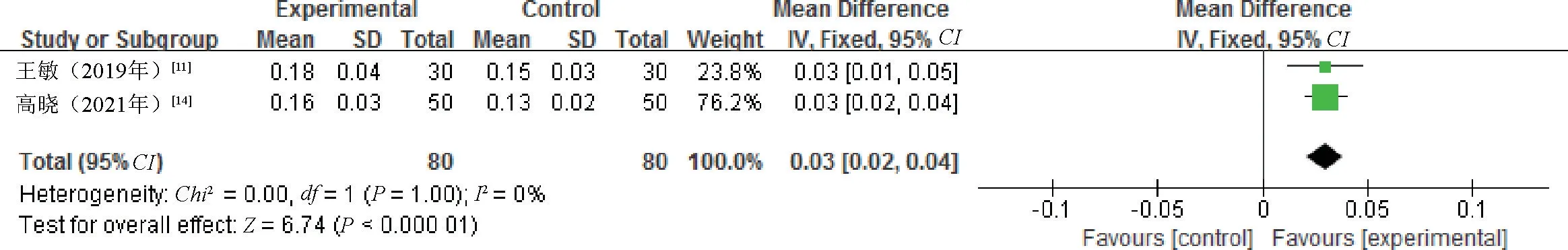
图6 两组患者唾液腺流率比较的Meta 分析森林图Fig 6 Forest plot of Meta-analysis for the comparison of flow rate of salivary gland between two groups
2.3.5 唾液流量:4 项研究[10,15-17]报告了唾液流量,因各研究间测量唾液流量的方法不一致,部分采用非刺激性唾液流量测定法,部分采用刺激性唾液流量测定法,故使用SMD分析法。各研究之间有统计学异质性(P=0.05,I2=61%),采用随机效应模型合并效应量进行分析。结果显示,对照组患者的唾液流量高于研究组,差异有统计学意义(SMD=-1.09,95%CI=-1.52~-0.65,P<0.000 01),见图7。
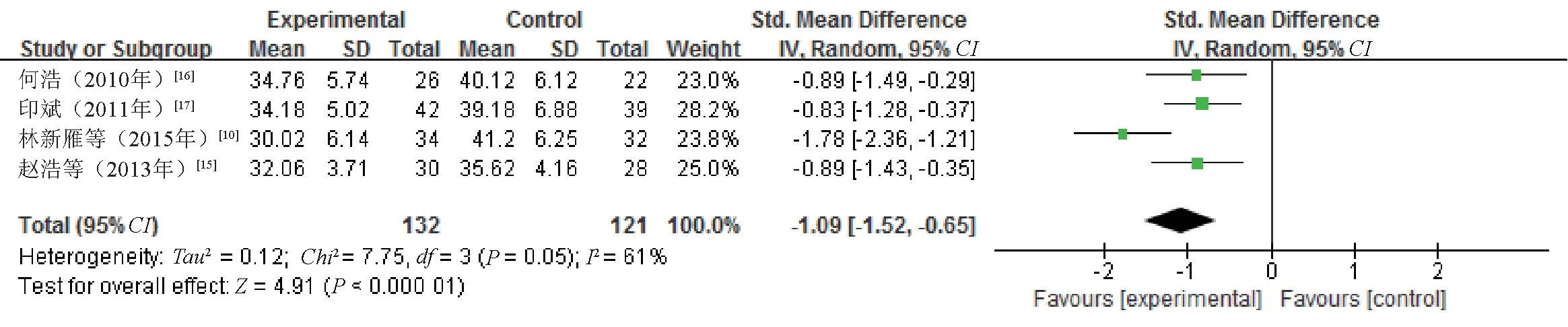
图7 两组患者唾液流量比较的Meta 分析森林图Fig 7 Forest plot of Meta-analysis for the comparison of salivary flow between two groups
2.3.6 Schirmer 试验结果:4 项研究[10,15-17]报告了Schirmer 试验结果,使用MD分析法,各研究之间有统计学异质性(P=0.004,I2=77%),采用随机模型合并效应量进行分析。结果显示,研究组患者的Schirmer 试验结果高于对照组,差异有统计学意义(MD=2.69,95%CI=1.19~4.19,P=0.000 4),见图8。
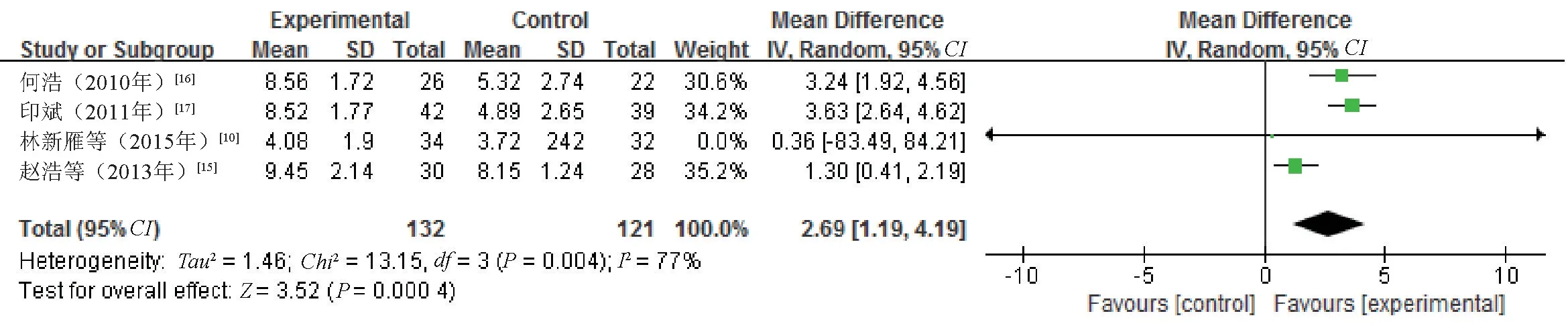
图8 两组患者Schirmer 试验结果比较的Meta 分析森林图Fig 8 Forest plot of Meta-analysis for the comparison of the results of Schirmer test between two groups
2.3.7 IgG:7 项研究[10,12-17]报告了IgG 水平,使用MD分析法,各研究之间有统计学异质性(P=0.002,I2=71%),采用随机模型合并效应量进行分析。结果显示,研究组患者的IgG 水平显著低于对照组,差异有统计学意义(MD=-3.25,95%CI=-4.06~-2.44,P<0.000 01),见图9。
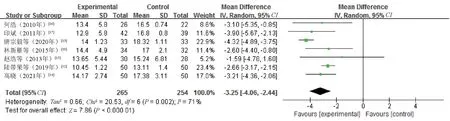
图9 两组患者IgG 水平比较的Meta 分析森林图Fig 9 Forest plot of Meta-analysis for the comparison of IgG levels between two groups
2.4 发表偏倚分析
比较白芍总苷胶囊联合羟氯喹与羟氯喹单药治疗SS 总有效率的漏斗图,纳入的10 项研究散落于漏斗图中线两侧,存在一定不对称性,提示本次Meta 分析纳入10 项研究获得的结果存在发表偏倚,见图10。
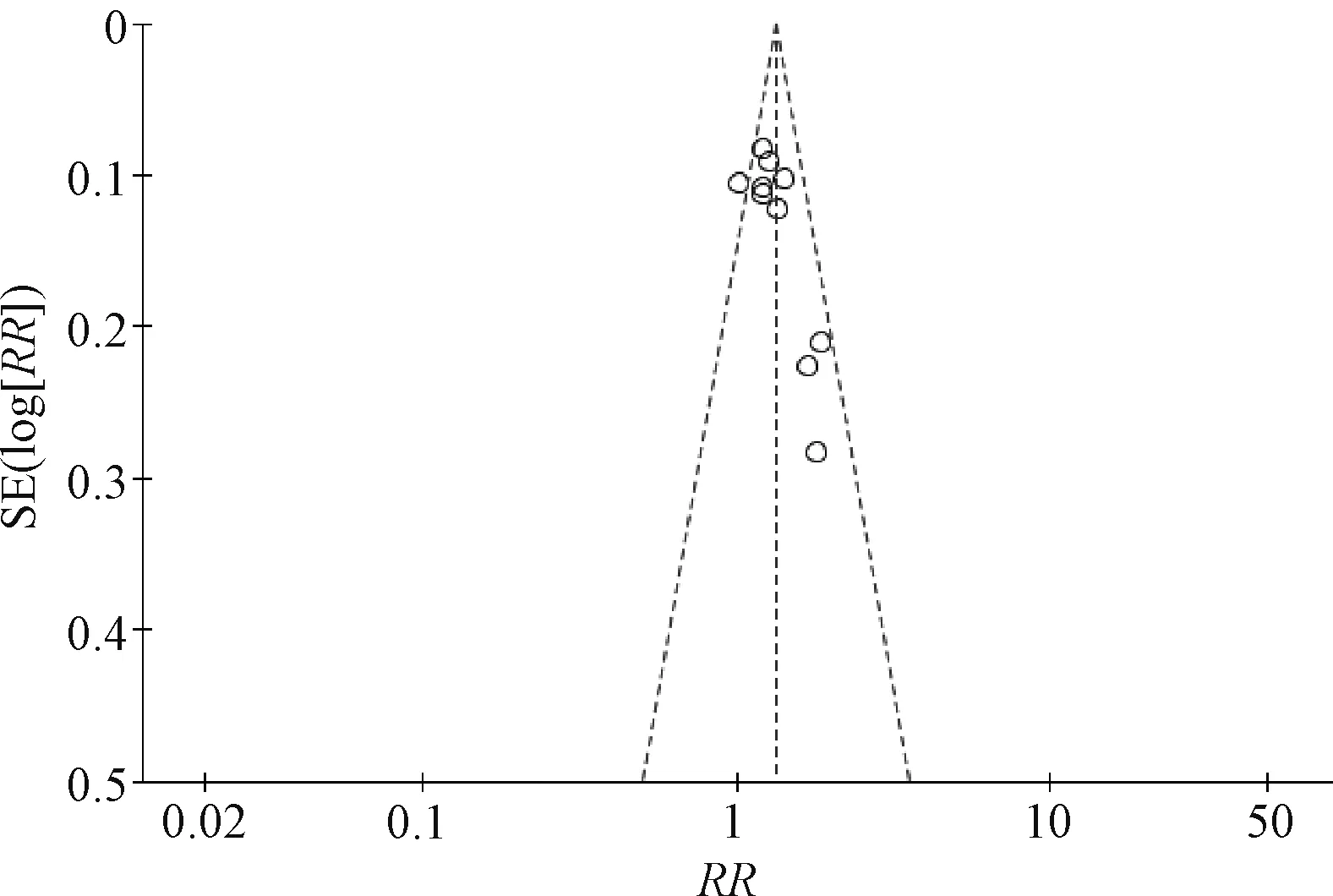
图10 总有效率的漏斗图Fig 10 Funnel chart of total effective rate
3 讨论
SS 发病机制复杂,治愈率较低,临床常用羟氯喹等免疫抑制剂来延缓病情进展。但长期使用免疫抑制剂,临床效果逐渐降低,并对患者的肝肾功能造成较大损害。因此,寻找既能提高SS 治疗效果又能缓解免疫抑制剂的肝肾负担的治疗方案成为目前临床较为关注的焦点。白芍总苷提取自中药白芍,含有多种调节免疫功能的成分,如芍药苷、羟基芍药苷和芍药花苷等。同时,白芍总苷可通过降低患者丙氨酸转氨酶和天冬氨酸转氨酶水平来保护肝脏[20]。笔者调研发现,有医疗机构使用白芍总苷胶囊联合羟氯喹治疗SS,但因为数据分散,样本量小,无法形成有效的循证支撑。
本研究系统评价了白芍总苷胶囊联合羟氯喹对比单纯使用羟氯喹治疗SS 的疗效,结果表明,采用白芍总苷胶囊联合羟氯喹治疗的研究组患者,其总有效率和实验室指标水平均优于单纯使用羟氯喹的对照组,且两组患者不良反应发生率的差异无统计学意义(P>0.05)(所纳入文献未提供肝功能指标对比)。
本次系统评价有以下方法学局限性:纳入患者年龄水平存异;干预措施时间未统一;药物日剂量存异;纳入文献质量较低且均为中文文献。
综上所述,对比单纯使用羟氯喹,白芍总苷胶囊联合羟氯喹治疗SS 的临床疗效较好,且安全性相当。受纳入研究方法学质量和样本量的限制,该结论有待更多设计严格、长期随访的大样本随机对照试验加以验证,后期需关注两药合用对比单药治疗过程中肝功能指数变化并及时更新数据。

