水液相下赖氨酸钙(II)配合物旋光异构的DFT研究
柳国洪,彭国强,张栩宾,郝成欣,刘 芳,王佐成,潘 宇*,赵丽红*
(1.白城医学高等专科学校基础医学院,吉林 白城 137000;2.白城师范学院理论计算中心,吉林 白城 137000)
0 引言
Lys是生命体必需的手性氨基酸.根据构型不同分为S-Lys和R-Lys,根据旋光性分为左旋体(L-Lys)和右旋体(R-Lys).L-Lys在人体内有生物活性,能促进人体发育、提高免疫力、增强胃液分泌和骨髓造血机能等,R-Lys无活性[1].钙是生命体重要的元素,在体内是2价态,其对骨骼形成、保证心脏规律跳动有重要作用[2-3].传统的补钙产品有醋酸钙、碳酸钙和葡萄糖酸钙,临床试验表明服用这些补钙产品或会导致肾结石,或会产生胃肠道不良反应[4].在食物中的钙被人体吸收是通过Ca2+在小肠中与氨基酸螯合后,氨基酸钙被人体整体吸收进行的[5].赖氨酸钙用于补钙更易被生命体吸收,同时还可补充Lys[6].
手性Lys的金属配合物也有手性,手性药的作用是药物分子通过与体内大分子严格地手性匹配实现的.手性不同的药物分子在活性、毒性和代谢过程方面差别很大,通常一个有效,另一个有负作用[7-8].如D-沙利度胺可止吐和镇静,而L-沙利度胺则致畸,D-沙利度胺的消旋导致了“沙利度胺事件”[9-10].因为优构体能否向劣构体转化以及转化速率均会严重影响手性药的疗效,所以手性分子旋光异构机理的研究对在临床上安全使用手性药具有重要意义.基于手性分子消旋反应的重要性,人们对Lys的旋光异构进行了广泛研究.文献[11-15]采用密度泛函理论研究了气相Lys的旋光异构以及水分子、纳米孔道(MOR分子筛及碳纳米管)和水溶剂的催化作用,结果表明:气相Lys不能消旋,纳米孔道有限域催化作用,水分子(簇)及水溶剂有较好的催化作用.
水溶剂可能改变反应的机理[16],生命体是富水环境[17],但是关于在水液相下Lys·Ca(II)旋光异构的研究鲜见文献报道.为揭示Lys·Ca(II)用于生命体同补Lys和Ca是否安全,基于文献[18-19]的研究经验,本文对水液相下赖氨酸钙(II)配合物旋光异构的机理进行了研究.
1 计算方法

2 结果与讨论
文献[28]研究表明在水液相下两性氨基酸的构象稳定.优化的两性Lys与Ca2+配合物的手性对映体如图1所示.
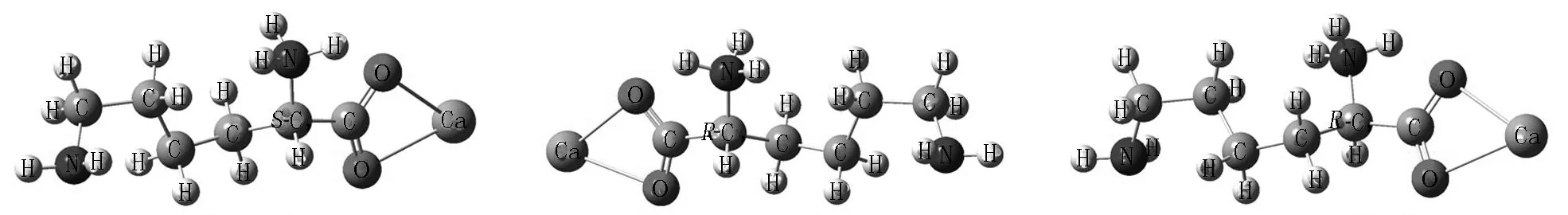
S-Lys·Ca(II) R-Lys·Ca(II) R-Lys·Ca(II)图1 在水液相下Lys_Ca(II)的手性对映体构象
在水液相下S-Lys·Ca(II)的旋光异构是在极性水溶剂和水分子(簇)的共同作用下进行的.在水溶剂中的水分子有单分子和水簇,与底物弱作用没参与反应的(H2O)n(n为构成水簇的水分子个数,n∈N,n≥1)对反应能垒影响较小[29],H2O与金属配位对非H迁移能垒影响也很小[19].为节省资源,本文对非H迁移过程不考虑(H2O)n的作用.先讨论在隐性水溶剂效应(水溶剂的极性作用)下S-Lys·Ca(II)的异构,然后讨论在显性水溶剂效应(水溶剂的极性与(H2O)n共同作用)下S-Lys·Ca(II)旋光异构决速步的反应过程,对重要的H迁移反应进行详细讨论,对其他基元反应做一般讨论.
2.1 在隐性水溶剂效应下S-Lys·Ca(II)的旋光异构
Lys·Ca(II)的旋光异构可在两性Lys向中性异构后α-H向N迁移或向O迁移的a通道和b通道上实现,异构过程如图2和图3所示,势能面如图4所示.
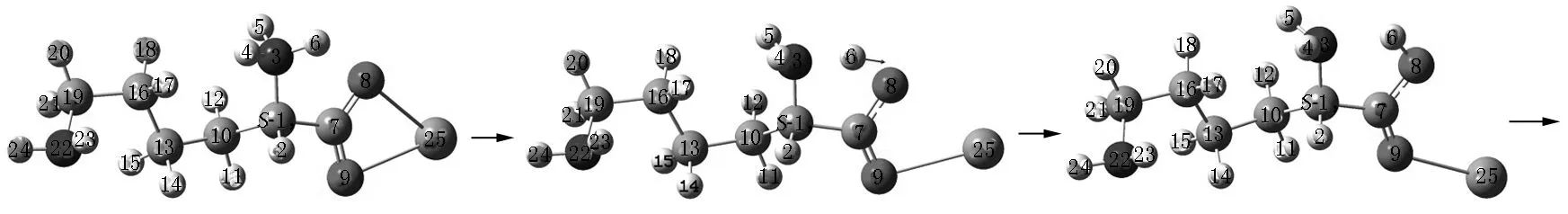
S-Lys·Ca(II) S-T1a S-I1a

S-T2a S-I2a T3a
I3a T4a后视图 R-I4a

R-T5a R-I5a R-I5a正视图
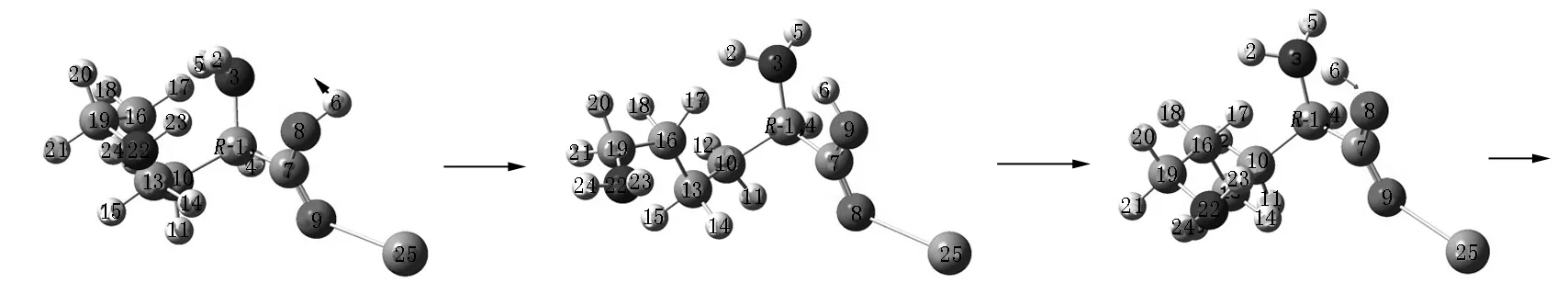
R-T6a R-I6a R-T7a
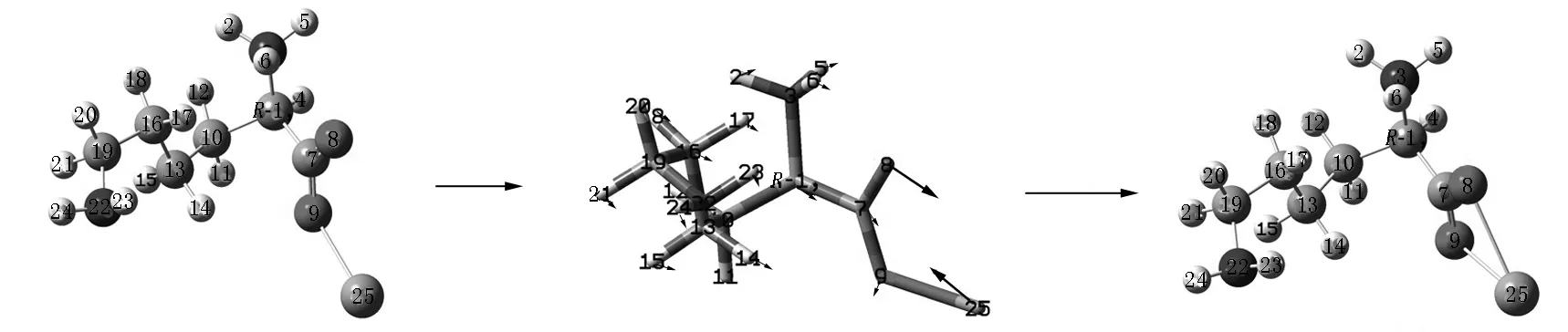
R-I7a R-T8a R-Lys·Ca(II)a图2 在隐性水溶剂效应下S-Lys·Ca(II)在a通道上的旋光异构过程

S-Lys·Ca(II) T1b I1b
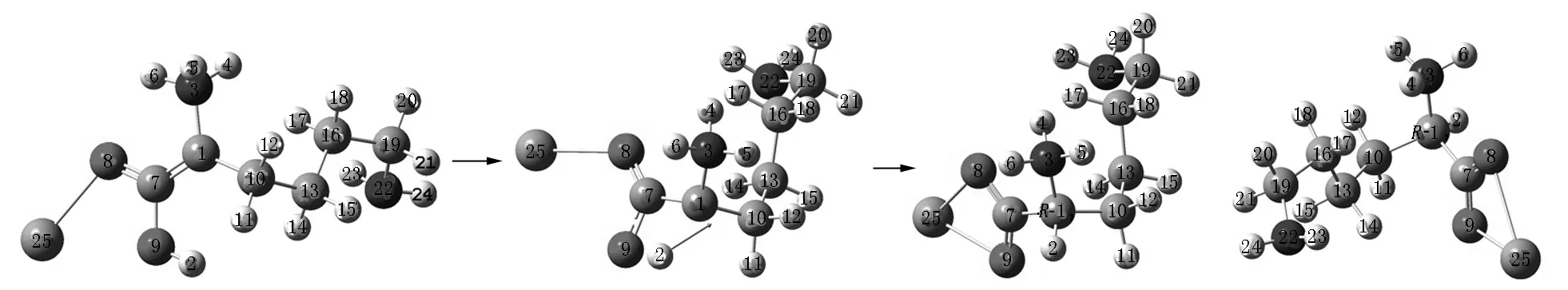
I1b后视图 T2b1 R-Lysb1(a) R-Lysb1(a)正视图
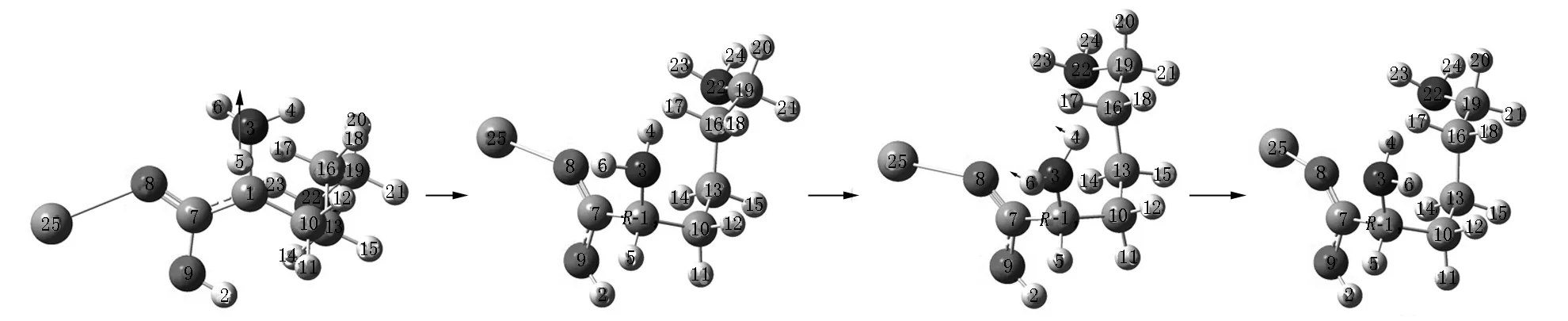
T2b2 R-I2b2 R-T3b2 R-I3b2
R-I3b2正视图 R-T4b2 R-I4b2(同R-I6a)下接R-T7a图3 在隐性水溶剂效应下S-Lys·Ca(II)在b通道上的旋光异构过程
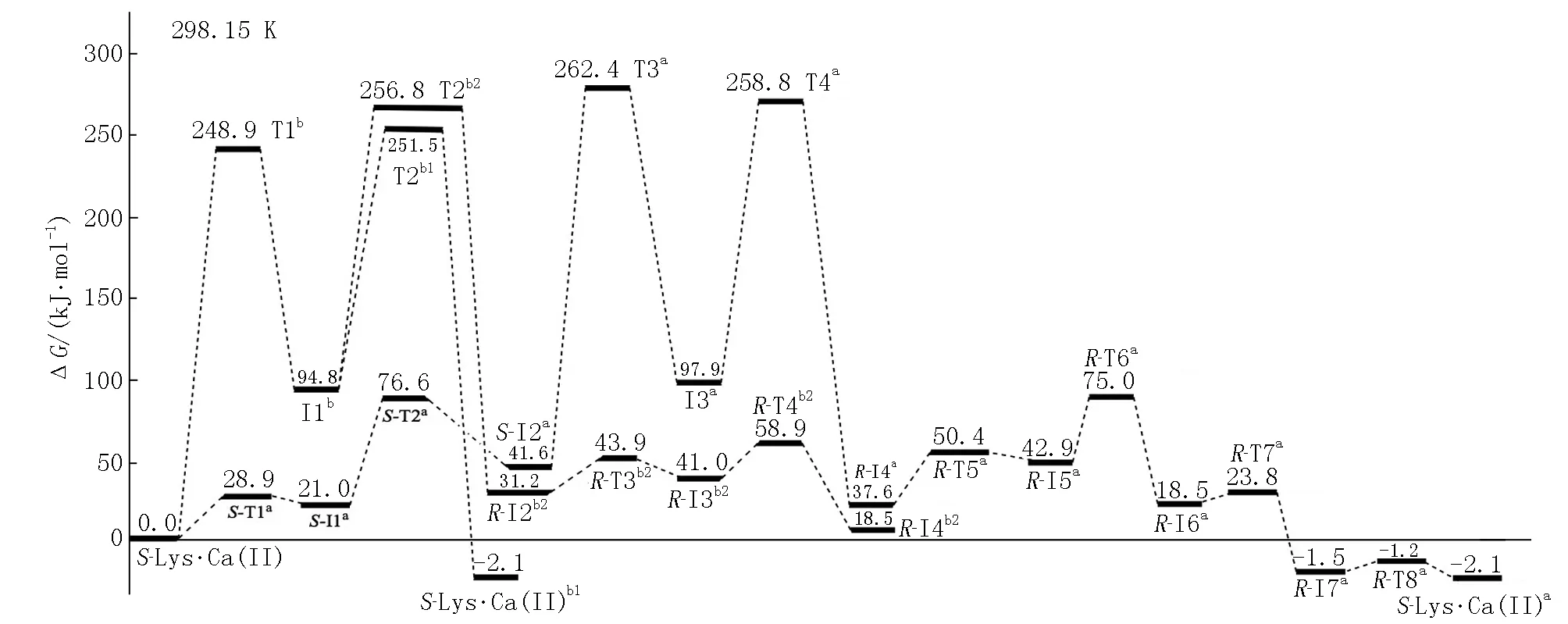
图4 S-Lys·Ca(II)旋光异构反应的自由能势能面

第2基元为S-I1a经O8—C7内旋转过渡态S-T2a.羧羟基O8—H6绕O8—C7旋转,从羧基外侧转到内侧,构象异构成S-I2a.在从S-I1a到S-T2a的过程中,O8—C7键俯视逆时针旋转90.5°,化学键内旋转所需能量不多,S-T2a产生了55.6 kJ·mol-1的内禀能垒.


第5基元为R-I4a经氨基氢H5和H2在纸面内外翻转的过渡态R-T5a.H5和H2从纸面内侧翻转到外侧(后视图),构象异构成R-I5a.在从R-I4a到R-T5a的过程中二面角H2—N3—C1—H5从116.8°增加至115.9°,非骨架形变所需能量较少,R-T5a产生的内禀能垒为12.8 kJ·mol-1.
第6基元为R-I5a经O8—C7内旋转过渡态R-T6a.羧羟基O8—H6绕O8—C7俯视逆时针旋转,从羧基内侧转到外侧,构象异构成R-I6a.在从R-I5a到R-T6a的过程中O8—C7键俯视逆时针旋转88.2°,R-T6a产生了32.1 kJ·mol-1的内禀能垒.该能垒比相同的O8—C7键逆时针旋转过渡态S-T2a产生的内禀能垒(55.6 kJ·mol-1)小很多,其原因是从R-I5a到R-T6a的过程中H6的运动方向与体系偶极矩方向相反,体系的电场力对O8—H6绕O8—C7的俯视逆时针旋转做正功.

第8基元为R-I7a经螯合环开合(O8—Ca25成键与断裂)的过渡态R-T8a.螯合环闭合,O8—Ca25成键,构象异构成R-Lys·Ca(II)a,得到了S-Lys·Ca(II)旋光异构的稳定产物.在从R-I7a到R-T8a的过程中,只是键角C7—O9—Ca25小幅改变,所需能量很少.R-T8a产生的电子能垒只有0.3 kJ·mol-1(见势能面),吉布斯自由能经校正后变为负势垒(-0.8 kJ·mol-1,没在势能面上标识),该基元反应可视为无势垒过程.其原因是过渡态有一个虚频,不计入热力学贡献,R-T8a的自由能校正量比R-I7a小1.1 kJ·mol-1,加上该基元电子能量对应的势垒只有0.3 kJ·mol-1,导致R-T8a比R-I7a的自由能低0.8 kJ·mol-1.因此,该基元的过渡态R-T8a只具有理论意义,R-I7a向R-Lys·Ca(II)a的异构是无势垒过程.



第3基元为R-I2b2(a)经氨基氢H6和H4左右翻转的过渡态R-T3b2.H6和H4从左侧翻转到右侧(后视图),构象异构成R-I3b2.从R-I2b2(a)到R-T3b1,非骨架二面角H6—N3—C1—H4从116.2°变为174.9°,所需能量较少,R-T3b2产生的内禀能垒为12.7 kJ·mol-1.
第4基元为R-I3b2经C7—C1旋转的过渡态R-T4b2.C7—C1键右视逆时针旋转73.8°,构象异构成R-I4b2,R-T4b2产生的能垒为17.9 kJ·mol-1.结构分析表明R-I4b2同于R-I6a,其接下来异构得到产物R-Lys·Ca(II)a,记作R-Lys·Ca(II)b2(a).
从图4可以看出:在隐性水溶剂效应下S-Lys·Ca(II)在a通道上异构具有优势,决速步骤是第3基元,能垒为220.8 kJ·mol-1.该能垒比极限反应能垒(167.3 kJ·mol-1)[30]还高很多,这说明在隐性水溶剂效应下Lys·Ca(II)不能消旋.a通道比b通道的决速步能垒低,其原因主要有2个:1)S-I2a比S-Lys·Ca(II)的C1—H2键活化程度更高(前者键长长且红外振动频率低(分别为3 117.1 cm-1和3 124.0 cm-1));2)a通道的反应物比b通道从反应物到过渡态C1—H2键的键长拉伸幅度更小.
正负反应能垒在40.0 kJ·mol-1以下时反应物和产物可以共存[30],因此从图4还可以看出:在a通道上的产物是R-I6a、R-I7a和R-Lys·Ca(II)a共存,只是R-Lys·Ca(II)a的分布更高.
2.2 在显性水溶剂效应下S-Lys·Ca(II)旋光异构的决速步骤
结合图3和图4可以看出:在隐性水溶剂效应下S-Lys·Ca(II)在a通道和b通道上旋光异构的决速步基元反应过程分别是S-I2a→T3a→I3a和S-Lys·Ca(II)→T1b→I1b.在显性水溶剂效应下,水分子(簇)除了与S-I2a和S-Lys·Ca(II)的钙原子配位外,同时还与S-I2a和S-Lys·Ca(II)有氢键作用.当单个水分子或水簇与钙离子配位以及2聚水和3聚水做H迁移媒介时,质子在α-C和羰基O以及α-C和氨基N间迁移的能垒相差很小[18-19],为使问题简便并节省篇幅,只考虑单个水分子与钙离子配位,做H迁移媒介的水簇只考虑2聚水情况.Ca(II)最高配位数是8,配位键键能计算结果表明:S-Lys·Ca(II)←nH2O和S-I2a←nH2O体系的H2O与Ca(II)的配位键能(严格地说还含有分子间的氢键能)在配位水分子个数n>2时基本相同,均明显大于在n=1时的配位键能,因此物种S-Lys·Ca(II)←nH2O和S-I2a←nH2O在n>2时的分布最高(前者n为2~6,后者n为2~7)(见表1).它们在2聚水作用下的质子转移反应历程如图5所示,反应势能面如图6所示.为节省篇幅,对2个配位水的情况做详细讨论,对满配的情况(S-I2a和7H2O配位、S-Lys·Ca(II)和6H2O配位)做一般讨论,对其他无配位水及存在1、3和5个配位水的情况只给出反应势能面.
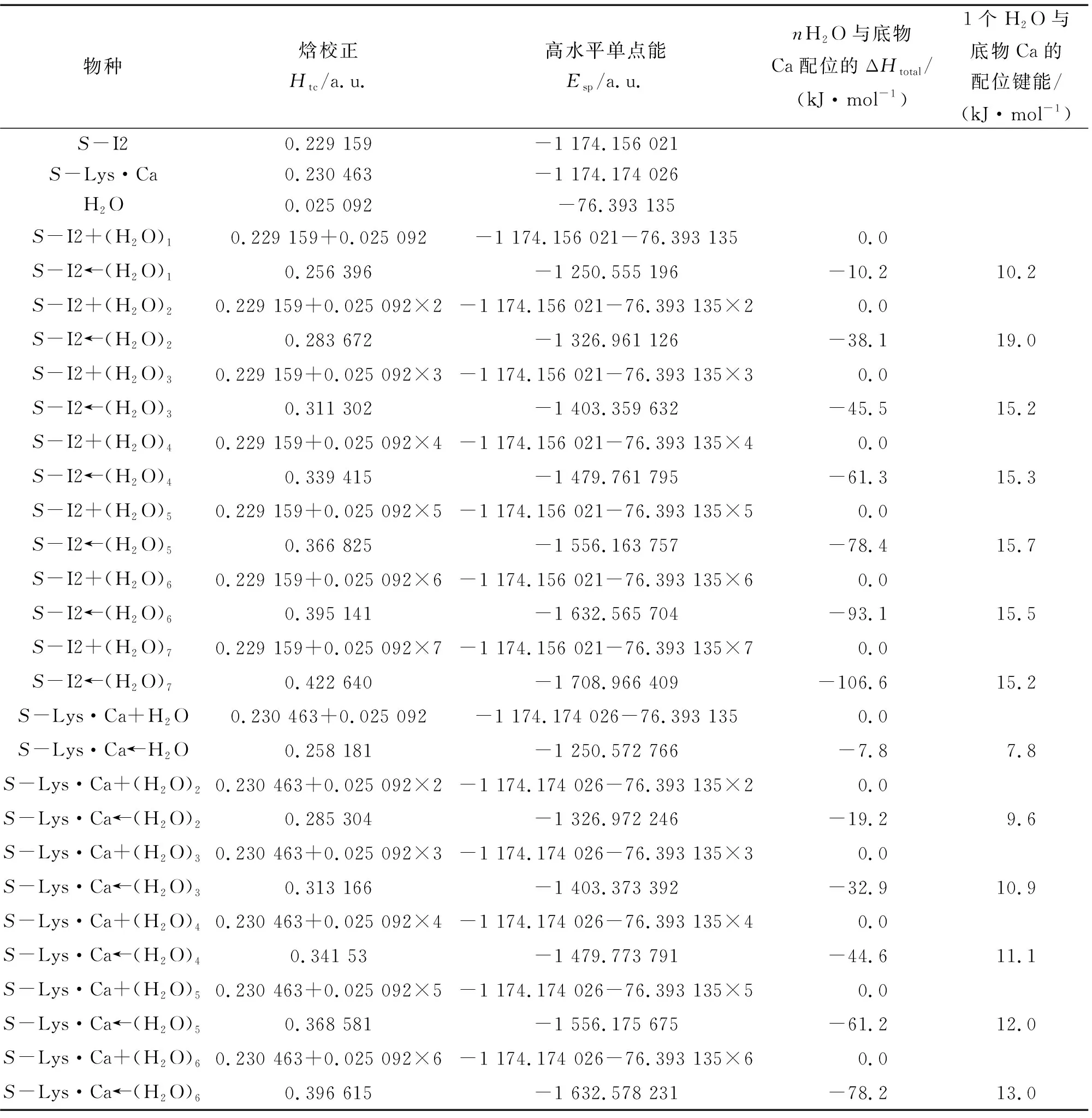
表1 S-I2和S-Lys·Ca与水分子的配位键能

图5 在显性水溶剂效应下决速步骤的反应历程
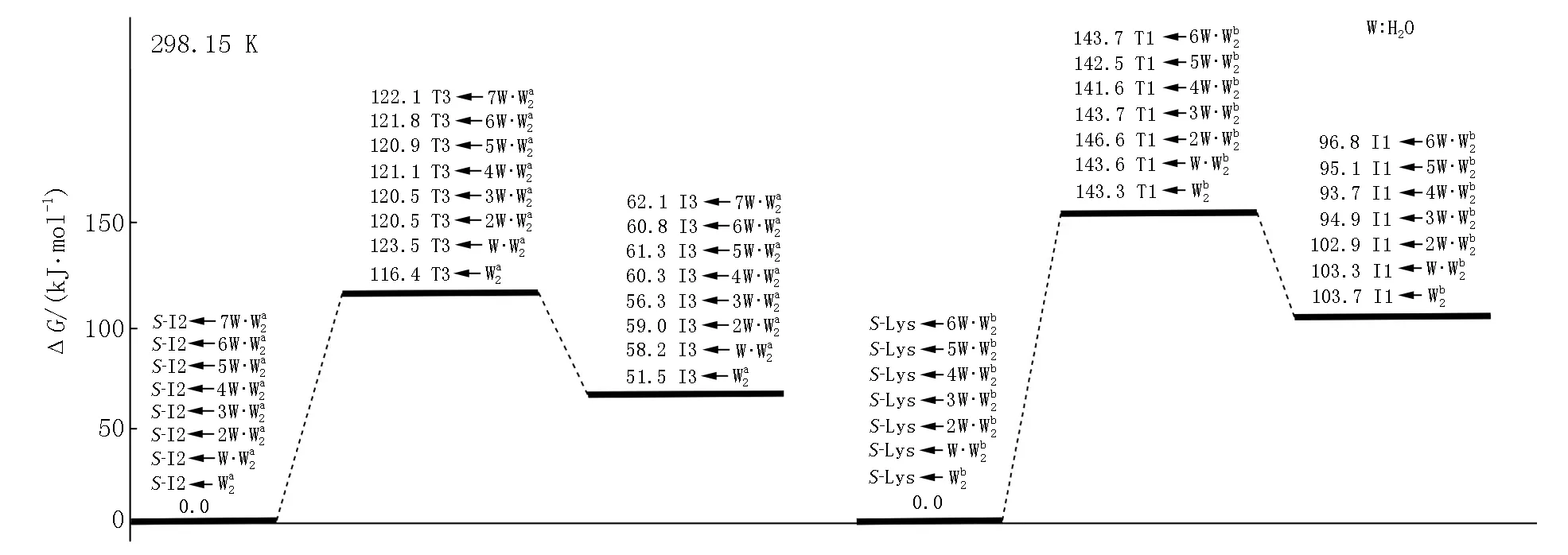
图6 在显性溶剂效应下S-Lys·Ca(II)在a和b通道上旋光异构决速步反应的自由能势能面
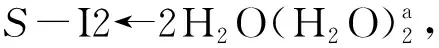
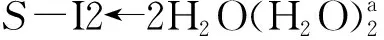
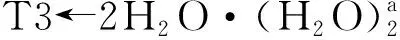
7个配位水的情况类似于2个配位水的情况,只做一般讨论.
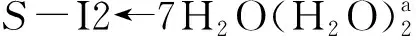
从图6可以看出:当存在0~7个配位水时,此基元的反应能垒为116.4~123.5 kJ·mol-1,在误差允许的范围内可以认为相同,这说明H2O与Ca(II)配位对反应能垒的影响可以忽略,对反应起催化作用的是做氢迁移媒介的水簇.在不同个数的H2O分子与S-I2a的Ca(II)配位时和在无H2O分子与S-I2a的Ca(II)配位时此基元的反应能垒基本相同,其主要原因是H2O分子与S-I2a的Ca(II)配位对C1—H2键的键长及红外振动频率影响甚微(当存在0~7个配位水时,C1—H2键的键长分别为0.109 2、0.109 2、0.109 3、0.109 4、0109 1、0.109 2、0.109 2和0.109 2 nm,红外振动频率分别为3 129.1、3 118.4、3 109.5、3 121.7、3 124.5、3 123.0、3 121.3和3 120.0 cm-1,C1—H2键的活化程度相差无几).
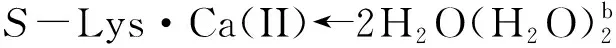

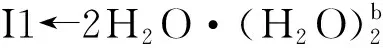
从图6可以看出:当存在0~6个配位水时,此基元的反应能垒为141.6~148.2 kJ·mol-1,在误差允许的范围内可以认为相同,这再次说明H2O与Ca(II)配位对反应能垒的影响可以忽略,对反应起催化作用的是做氢迁移媒介的水簇.在不同个数的H2O分子与S-Lys·Ca(II)的Ca(II)配位时和在无H2O分子与S-Lys·Ca(II)的Ca(II)配位时此基元的反应能垒基本相同,其原因是H2O分子与S-Lys·Ca(II)的Ca(II)配位对C1—H2键的键长及红外振动频率影响甚微(详细数据从略).
从图6可以看出:在显性水溶剂效应下S-Lys·Ca(II)的旋光异构仍然是在a通道上具有优势,决速步能垒为120.5~122.1 kJ·mol-1(存在2~7个H2O与S-I2a的Ca(II)配位的情况).该能垒远高于温和反应能垒(83.4 kJ·mol-1),但低于极限反应能垒(160.5 kJ·mol-1)[30],这说明在显性水溶剂效应下Lys·Ca(II)只能少量地消旋.从图6还可以看出:在显性水溶剂效应下S-Lys·Ca(II)在b通道上旋光异构的决速步能垒为141.6~148.2 kJ·mol-1,比a通道的决速步能垒高,其原因与在隐性溶剂效应下b通道比a通道决速步能垒高的原因相似.
3 结论
本文在MN15/SMD/6-311++G(2df,pd)//M06-2X/SMD/6-311+G(d,p)双水平上研究了在水液相下Lys·Ca(II)的旋光异构,得到如下结论:
1)Lys·Ca(II)的旋光异构有a和b2个通道,a通道是在两性Lys向中性异构后α-H质子以氨基N作桥迁移,b通道是α-H质子直接以羰基O作桥迁移;
2)在隐性溶剂效应下,a、b通道的决速步能垒分别为220.8和248.9 kJ·mol-1;
3)在显性溶剂效应下,a、b通道的决速步能垒分别降至120.5~122.1 kJ·mol-1和141.6~148.2 kJ·mol-1.
研究结果表明:Lys·Ca(II)在水液相下只能少量地消旋,可安全地用于生命体同时补充Lys和Ca元素.

