从含铀碳酸盐溶液制备过氧化铀的工艺研究
任 燕,郑 英,周志全,张海燕,叶开凯,曹令华
(核工业北京化工冶金研究院,北京 101149)
氨沉淀法和氢氧化钠沉淀法都是工业上从含铀碳酸盐溶液制备铀浓缩物产品的通用方法[1-3]。用氨沉淀法回收铀,虽然氨的价格较低;但铵根的回收和处置成本较高。氢氧化钠沉淀法制备的铀浓缩物产品为重铀酸钠,在沉淀铀的同时其他金属元素也会一起沉淀,而且产品本身含有一定量的钠离子,致使铀浓缩物产品质量无法达到核纯标准[4]。通过这两种方法制备的铀浓缩物均需采用精制工艺处理,才能得到核纯标准的铀氧化物产品。这种精制过程将产生大量的放射性“三废”,其中硝酸溶解产生的硝酸铵或硝酸钠废水在处置上存在诸多问题[5]。
另一种从含铀碳酸盐溶液制备铀浓缩物产品的方法是过氧化氢沉淀法。该法的优点是对铀的选择性高,尤其从杂质含量相对较少的中性溶液中回收铀,能制备得到核纯级的过氧化铀产品,可将纯化和沉淀过程合二为一,简化了工艺流程;且过氧化氢对环境影响较小,不产生异味,在安全环保上有明显优势。该工艺制备得到的过氧化铀为晶状易处理产品,该工艺能降低黄饼的过滤、干燥和装桶费用[6]。
针对含铀碳酸盐溶液,研究采用盐酸酸化除去溶液中的碳酸根,以过氧化氢作为沉淀剂,用NaOH调节沉淀pH,制备过氧化铀产品。
1 试验部分
1.1 试验原料及设备
某铀矿含铀碳酸盐溶液组分见表1。

表1 含铀碳酸盐溶液主要组分Table 1 Main components of uranium-bearing carbonate solution
试验用盐酸、双氧水(30%)、NaOH,均为分析纯;试验用水为蒸馏水。
试验用设备有雷氟BT100S型蠕动泵(保定雷氟),恒温水浴IKEA机械搅拌器(德国IKEA),伊尔姆MPC-1201E型真空泵(德国伊尔姆),干燥箱(上海林频)。
1.2 试验方法及原理
含铀碳酸盐溶液中含有大量碳酸氢根,对沉淀UO4有一定抑制作用,需加酸去除碳酸根及碳酸氢根,并使溶液pH达到过氧化氢沉淀铀的合适范围。采用浓HCl将溶液酸化,再加入过氧化氢沉淀UO4,用NaOH调节沉淀pH,得到的沉淀经过滤、烘干制备UO4产品,主要化学反应如下[7-9]。
溶液酸化反应:
(1)
(2)
(3)
过氧化氢沉淀反应:
(4)

(5)
干燥反应:

(6)
2 试验结果与讨论
2.1 溶液酸化试验
含铀碳酸盐溶液pH约为9,溶液中存在大量碳酸氢根及碳酸根。碳酸根与铀酰离子的强烈配合,会影响铀的沉淀[10]。试验用浓盐酸酸化含铀碳酸盐溶液到不同pH后,再加入理论计算量130%的H2O2;并用NaOH调节溶液pH=3.0,沉淀过氧化铀。试验结果见表2。
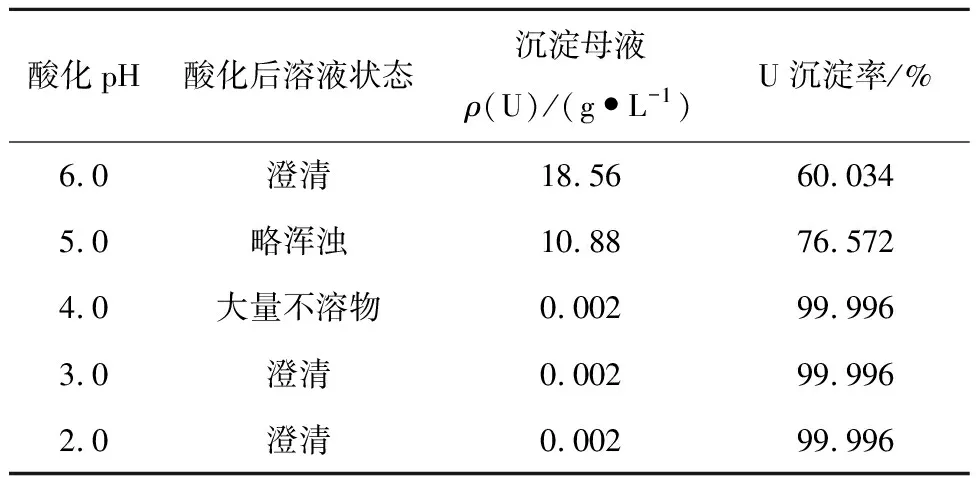
表2 溶液酸化试验结果Table 2 Test results of uranium-bearing carbonate solution acidification
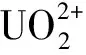
2.2 UO4产品制备试验
2.2.1 沉淀pH的影响
H2O2能否有效沉淀铀,含铀母液的pH是关键因素之一。pH过高或过低都会影响沉淀铀效果。试验采用浓盐酸将含铀碳酸盐溶液酸化至pH=3.0,加入理论计算量130%的H2O2,在沉淀反应时间1 h、反应温度20 ℃条件下,加入不同体积的5 mol/L的NaOH溶液调节沉淀pH,试验结果见表3。

表3 沉淀pH对UO4沉淀效果的影响Table 3 Influence of pH on uranium precipitation effect
由试验结果可知:当沉淀pH=1.5时,由于H+浓度过高,抑制了H2O2沉淀反应的进行,沉淀母液铀质量浓度为0.014 g/L;pH为2.0~3.5时,沉淀母液铀质量浓度可降至0.005 g/L以下,铀沉淀率达99.99%以上。但随着沉淀pH的升高,NaOH用量增加,UO4产品中的Na含量也随之增加。考虑产品纯化效果,沉淀pH在2.5左右较为适宜。
2.2.2 H2O2用量的影响
在沉淀反应过程中,为了保证铀的沉淀率,须增加H2O2用量。试验条件:含铀碳酸盐溶液酸化pH为3.0,沉淀反应时间为1 h,沉淀pH为2.5,沉淀反应温度为20 ℃。H2O2用量分别选取理论计算量的100%、110%、120%、130%、150%,开展H2O2用量对UO4沉淀的影响研究,试验结果见表4。
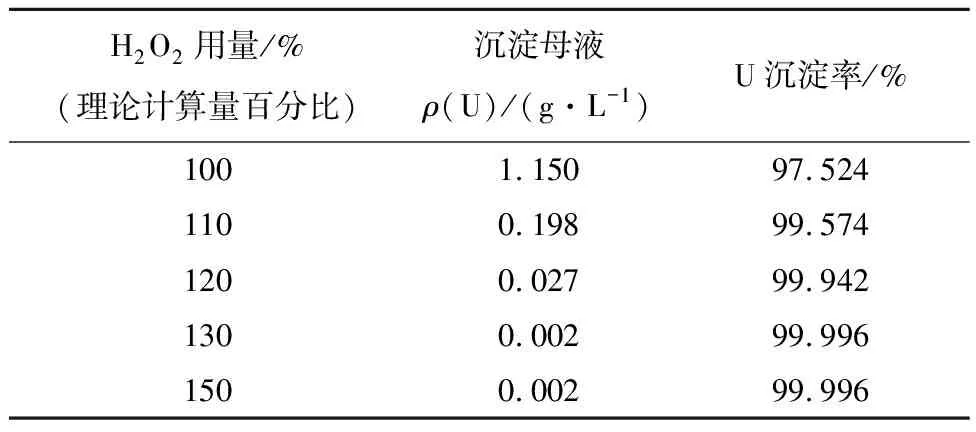
表4 H2O2用量对UO4沉淀效果的影响Table 4 Influence of H2O2 dosage on uranium precipitation effect
试验结果表明:随着H2O2用量的增加,沉淀母液的铀质量浓度随之降低;当H2O2用量为理论计算量的130%时,即可达到较为满意的沉淀效果,继续增加H2O2用量对提升沉淀效果没有显著影响。
2.2.3 沉淀反应时间的影响
试验条件:含铀碳酸盐溶液酸化pH为3.0,H2O2用量为理论计算量的130%,沉淀pH为2.5,沉淀反应温度为20 ℃。设定不同沉淀反应时间,开展沉淀反应时间对UO4沉淀的影响研究,试验结果见表5。

表5 沉淀反应时间对UO4沉淀效果的影响Table 5 Influence of reaction time on uraniumprecipitation effect
在试验过程中,加入过氧化氢后,烧杯中即刻产生淡黄色过氧化铀沉淀物;与此同时,溶液pH迅速下降。试验结果表明,在杂质含量较少的含铀碳酸盐体系中,过氧化铀的沉淀反应时间较短,反应时间控制在30 min以上,即可将铀沉淀完全。
2.2.4 沉淀温度的影响
反应温度对产品物理性能有一定影响[11]。试验条件:含铀碳酸盐溶液酸化pH为3.0,H2O2用量为理论计算量的130%,沉淀pH为2.5,沉淀反应时间为1 h。分别选取20 ℃、30 ℃、40 ℃和50 ℃,开展反应温度对UO4沉淀的影响研究,试验结果见表6。
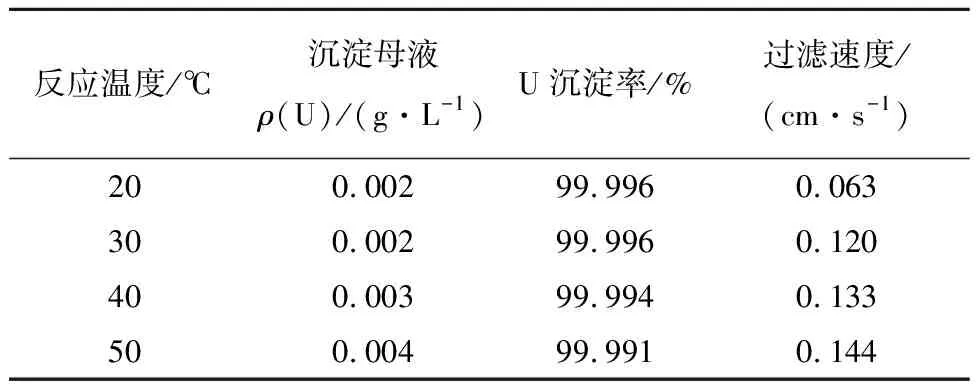
表6 反应温度对UO4沉淀效果的影响Table 6 Influence of reaction temperature on uranium precipitation effect
试验结果表明,随着温度的升高,过氧化铀滤饼的过滤速度逐渐提升。温度影响晶核的形成,在单位体积内晶核生成的数量与溶液的过饱和度成正比[12]。当温度过低时,由于溶液的过饱和度较大,导致晶核大量形成而使得沉淀颗粒变细,难以沉降和过滤。随着反应温度的升高,沉淀的沉降性能逐渐改善;但温度升高,溶解度增大,造成铀沉淀不完全。另外,当反应温度超过40 ℃后还会加快H2O2的分解,致使沉淀效果变差。因过氧化铀沉淀反应本身为放热反应,综合考虑铀的沉淀率和沉淀的过滤性能,沉淀反应温度以室温为宜。
2.3 UO4的洗涤
采用浓盐酸酸化含铀碳酸盐溶液除碳酸根过程和采用NaOH溶液调节沉淀pH过程,使得溶液中含有大量Cl-和一定量的Na+。在沉淀过程中,UO4中会夹带一定量的杂项元素,需对UO4进行洗涤。对以上最优条件下得到的UO4,采用固液质量体积比1 g/mL的去离子水进行盘洗及制浆洗,结果见表7。可以看出:盘洗的洗涤效果要优于制浆洗涤,盘洗2次,洗后产品中Cl-和Na+含量即可达到《铀矿石浓缩物》(GB/T 10268—2008)产品标准[13]。
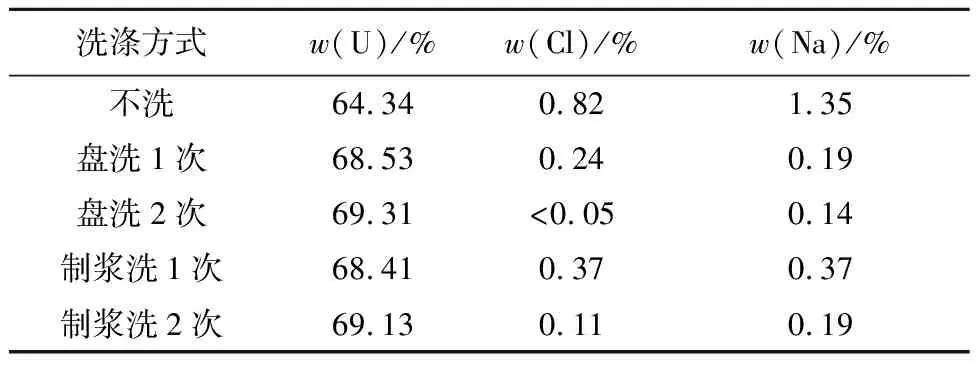
表7 UO4的清水洗涤效果Table 7 Washing test results of UO4
2.4 UO4产品分析
UO4在100 ℃下烘干3 h,得到符合《铀矿石浓缩物》(GB/T 10268—2008)产品标准的UO4,产品分析结果见表8。

表8 UO4产品的组成Table 8 Product composition of UO4
3 结论
对含铀碳酸盐溶液,采用浓盐酸酸化去除碳酸根及碳酸氢根、H2O2沉淀、NaOH调节沉淀pH,可制备得到UO4产品。在酸化pH=3.0、H2O2用量为理论计算量的130%、沉淀pH=2.5、沉淀时间0.5 h、沉淀温度为室温的条件下,铀沉淀率达99%以上,产品铀含量大于68%,所得产品质量满足《铀矿石浓缩物》(GB/T 10268—2008)要求。

