亚麻木酚素对糖尿病患者血糖及血脂的影响
贡丽雅 王 燕 石 剑
河北医科大学第二医院营养科,河北石家庄 050000
开环异落叶松酚二葡萄糖苷(secoisolariciresinol diglucoside,SDG)是亚麻木酚素的主要形式,约占亚麻木酚素的95%[1-3]。SDG 是肠内酯的重要前体物质[4],SDG 通过肠道菌群的作用代谢成为生物活性更强的肠二醇和肠内酯[5]。研究显示SDG 在抗肿瘤、抗氧化、降血脂方面有积极作用[6-8]。SDG 通过抑制血管紧张素转换酶介导血压降低[9]。动物试验表明亚麻籽提取物可以降低血糖水平、体重和进食量,改善脂质谱[10-11];然而亦有学者发现60~80 岁健康老年人及代谢综合征患者补充SDG 后血液炎症标志物和血脂并无显著改善[12-13]。目前关于SDG 对新确诊糖尿病患者血糖及血脂影响鲜有报道,因此本研究主要探讨SDG 补充对新确诊糖尿病患者血糖及血脂水平的影响。
1 资料与方法
1.1 一般资料
招募2016 年3 月至2017 年2 月河北医科大学第二医院内分泌门诊收入的糖尿病患者111 例,采用随机数字表法将其分为对照组55 例,干预组56 例。纳入标准:①口服葡萄糖耐量实验(oral glucose tolerance test,OGTT)新确诊的糖尿病;②年龄18~65 岁;③签署知情同意。排除标准:①糖尿病合并其他并发症;②妊娠、哺乳期、计划妊娠妇女;③肝肾功能异常或危重症;④无法完成试验。其中干预组男38 例,女18 例;平均年龄(49.27±10.82)岁;平均身高(168.04±7.58)cm。对照组男32 例,女23 例;平均年龄(48.64±11.05)岁;平均身高(165.82±8.98)cm。两组性别、年龄、身高等一般资料比较,差异无统计学意义(P >0.05),具有可比性。本研究经医院医学伦理委员会批准。
1.2 治疗方法
干预前测量患者清晨空腹体重。采用3 d 24 h 膳食调查表收集患者饮食基本情况,计算患者总能量摄入和碳水化合物、脂肪、蛋白质三大供能营养素比例。临床指标方面,采集干预前后患者的空腹静脉血使用全自动罗氏Cobas 8000 生化分析仪检测空腹血糖(fasting blood-glucose,FBG)、餐后2 h 血糖(2-hour postprandial plasma glucose,2hPG)、糖化血红蛋白(HbA1c)、总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)、高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)和C 反应蛋白(C-reactive protein,CRP)水平。两组患者均进行饮食运动指导,对照组给予安慰剂(淀粉300 mg/次,2 次/d);干预组给予SDG 300 mg(德斯特生物,成都)及淀粉300 mg/次,2 次/d。干预时间为12 周。
1.3 观察指标
观察身高、体重、饮食能量摄入及三大营养素供能比例变化情况;观察FBG、2hPG 和HbA1c水平变化情况;观察TG、TC、HDL-C、LDL-C 和CRP 水平变化情况。
1.4 统计学方法
所有数据使用SPSS 19.0 软件进行分析,计量资料用均数±标准差()表示,采用t 检验;计数资料用例数表示,采用χ2检验。以P <0.05 为差异有统计学意义。
2 结果
2.1 两组干预前后体重情况比较
对照组干预前后体重分别为(74.66±13.77)、(74.66±13.77)kg;干预组患者干预前后体重分别为(73.11±12.95)、(73.11±12.95)kg;两组干预前后体重比较,差异无统计学意义(P >0.05)。
2.2 两组干预前后膳食结构比较
干预前,两组三大供能营养素比例及每公斤体重能量摄入比较,差异无统计学意义(P >0.05)。干预后,两组三大供能营养素比例及每公斤体重能量摄入与干预前比较及组间比较,差异无统计学意义(P >0.05)。见表1。
表1 两组干预前后患者膳食结构比较()

表1 两组干预前后患者膳食结构比较()
注 t1、P1 值为两组干预前比较;t2、P2 值为两组干预后比较
2.3 两组干预前后血糖指标比较
干预前,两组FBG、2hPG 和HbA1c比较,差异无统计学意义(P >0.05)。干预后,干预组FBG、2hPG 和HbA1c低于干预前,且干预组FBG 和2hPG 低于对照组,差异有统计学意义(P <0.05)。见表2。
表2 两组干预前后血糖指标比较()
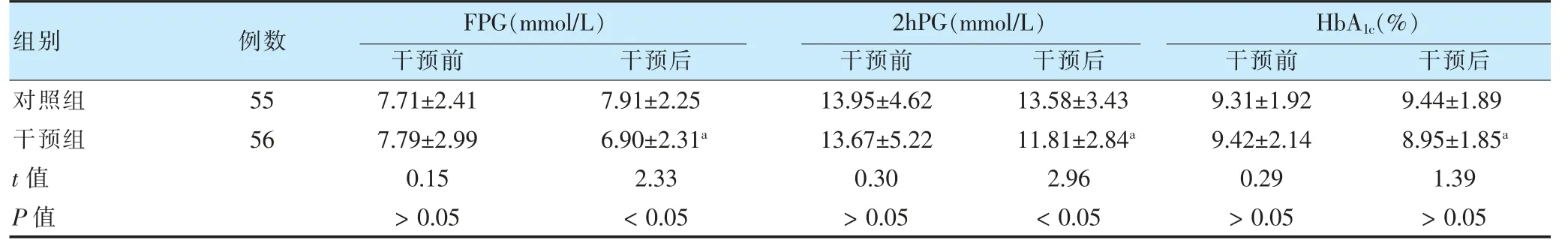
表2 两组干预前后血糖指标比较()
注 与本组干预前比较,aP <0.05。FPG:空腹血糖;2hPG:餐后2 h 血糖;HbA1c:糖化血红蛋白
2.4 两组干预前后血脂及C 反应蛋白比较
干预前,两组TG、TC、HDL-C、LDL-C 和CRP 水平比较,差异无统计学意义(P >0.05)。干预后,干预组TC、LDL-C 低于干预前,对照组TC 水平高于干预前,差异有统计学意义(P <0.05),且干预组TC 和LDLC 低于对照组,差异有统计学意义(P <0.05)。见表3。
表3 干预前后两组血脂及C 反应蛋白指标比较()
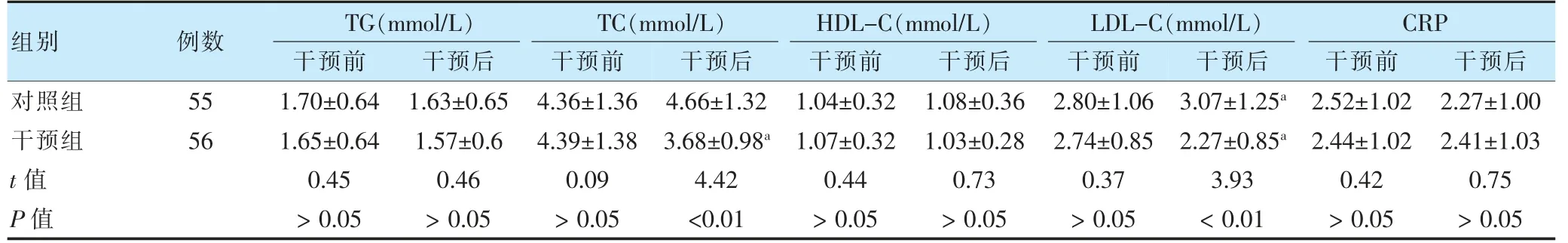
表3 干预前后两组血脂及C 反应蛋白指标比较()
注 与本组干预前比较,aP <0.05。TG:甘油三酯;TC:总胆固醇;HDL-C:高密度脂蛋白胆固醇;LDL-C:低密度脂蛋白胆固醇;CRP:C 反应蛋白
3 讨论
3.1 SDG 对血糖的影响
由于人群来源、研究方式不同,木酚素对血糖的影响研究结果并不一致。van der Schouw 等[13]研究显示西方健康男性饮食高木酚素摄入增加与胰岛素和C 肽水平降低趋势显著相关。而额外补充SDG 280 mg/d的全谷物黑麦饮食与全谷物小麦饮食并未发现对胰岛素敏感性差异影响[12]。欧洲进行的大规模调查显示并未发现木酚素摄入与2 型糖尿病相关性[14]。但Mishra等[15],其对于16 例55 岁以上绝经后妇女每日补充600 mg 的随机交叉安慰剂对照研究显示干预组血糖和HbA1c显著改善。
中国人群研究方面:中老年妇女应用400 mg SDG 8 周或600 mg 4 周干预后血糖显著降低,且存在时间剂量关系[16]。梁霞等[17]的研究显示4 周150 mg SDG 的干预对改善中老年妇女血糖有显著降低作用。另一项在中国人群进行的双盲随机交叉安慰剂对照试验结果显示,SDG 360 mg/d 与安慰剂比较HbA1c显著降低,但并未观察到FBG、胰岛素浓度、胰岛素抵抗和血脂水平变化[18]。
亚麻木酚素作为一种酚类物质,其降血糖作用可能与其淀粉酶、葡萄糖苷酶抑制作用有关,研究显示添加亚麻籽浆组的餐后血糖指数、餐后血糖显著好于对照组,食用高血糖生成指数碳水化合物食物时配合坚果油籽混合豆浆有利于控制餐后血糖,其中机制可能与其抗氧化物质的消化酶活性抑制作用有关[19-20]。有研究指出葡萄糖依赖性促胰岛素释放肽在高脂饮食诱导的胰岛素抵抗中起关键作用,动物试验显示补充亚麻籽有可以显著降低小鼠抑胃肽过度分泌情况有助于降低瘦素水平,改善瘦素抵抗[21-22]。
3.2 亚麻木酚素对血脂的影响
本研究显示,干预组和对照组在饮食能量摄入、三大供能营养素摄入无统计学差异的情况下,补充SDG 300 mg/次,2 次/d 可有效改善患者FPG、2HPG、HbA1c、TC 和LDL-C 水平。动物试验显示,给予高脂饮食诱导高脂血症大鼠每天0.6 g/kg 40%的SDG 6 周能显著降低大鼠的TC、TG 和LDL-C 水平,显著增加HDL-C 水平[10]。人群研究显示随膳食木酚素摄入增加,健康男性载脂蛋白B 和LDL-C 显著上升[14],但本研究表明,补充SDG 后干预组LDL-C 水平显著降低但HDL-C水平未见显著变化。meta 分析证实,木酚素补充剂降低TC 和LDL-C 分别为0.28 mmol/L和0.16 mmol/L,且降低胆固醇作用在绝经后女性及干预前胆固醇浓度高人群更明显[23]。本研究与该meta分析结果一致,干预后,干预组患者TC 和LDL-C 水平均显著降低。
SDG 降血脂可能的机制是:研究指出亚麻籽的抗氧化作用主要来自SDG,防止脂质的氧化损伤[24]。SDG 通过提高肝肾组织中超氧化物歧化酶和谷胱甘肽过氧化物酶的含量提高抗氧化力清除体内自由基,减缓脂质过氧化改善血脂水平[10]。SDG 通过增加脂质合成代谢相关基因表达降低血脂[25]。
本研究局限在于采用的问卷调查饮食摄入情况可能存在偏差,且并未收集受试者的体力活动情况,对于抗氧化、炎症因子方面的指标检查较少。未来应进一步深入研究SDG 改善血糖及血脂的机制。目前鲜有研究针对新诊断的无其他合并症的糖尿病患者进行SDG 的干预试验,本研究结果显示,SDG 补充对改善糖尿病患者血糖、血脂有显著作用。

