微卡免疫干预辅助治疗初治涂阴肺结核4个月治疗方案的疗效研究
刘礼亲 徐祖辉,2 黄移生 姚其能 谭云洪 周林 夏愔愔 刘二勇 黄国军 白丽琼 成诗明
病原学阴性肺结核约占我国结核病负担的一半以上,2019年全国结核病报告发病数为83.3万例,其中病原学阴性患者占55%[1]。病原学阴性肺结核在结核病的传播过程中扮演着重要角色,在美国[2]和荷兰[3]的研究证实分别有17%和13%的确诊肺结核患者是由涂阴肺结核患者传播所致。加强涂阴肺结核的治疗管理,是降低我国肺结核发病率的重要措施之一[4]。多年来,初治肺结核(涂阴和涂阳)的治疗均采用世界卫生组织(WHO)推荐的6个月化疗方案,未按照细菌学和病变程度不同进行针对性的治疗。长疗程治疗不仅可增加药物不良反应的发生,还容易造成耐药。痰涂片阴性肺结核患者意味着排菌量少,病情相对较轻,探索缩短疗程的新治疗方案势在必行。蔡青山等[5]对初治肺结核采用4个月方案治疗,发现与6个月方案相比临床疗效差异不明显,但可降低不良反应发生率。结核病的免疫治疗是重要的辅助治疗手段之一,本研究使用的微卡(注射用母牛分枝杆菌菌苗)是我国自主研发的免疫调节制剂,是WHO在《结核病研究与发展战略规划》中推荐的免疫治疗制剂[6]。本研究采用随机对照临床试验设计,对初治涂阴肺结核患者采用4个月抗结核治疗方案辅以免疫干预治疗,以评价其疗效和不良反应发生情况,为缩短涂阴肺结核患者的治疗提供依据。
资料和方法
一、资料来源
本研究资料来源于“十二五”科技部重大专项课题“涂阴肺结核患者免疫治疗干预研究”湖南省样本资料。根据地理位置、既往结核病防治策略执行情况和社会经济状况等选择邵东县和岳阳县作为研究现场。在获得患者知情同意后,由经过培训的临床医生记录患者现场调查问卷、临床检查、治疗和随访信息并录入“德派(DAP)流行病学研究系统” (http://clinical.dapchina.cn/clinical/)。
二、研究对象
2014年11月至2016年4月在湖南省邵东县和岳阳县结核病定点医疗机构新诊断的初治涂阴肺结核连续病例为研究对象。涂阴肺结核的诊断参照《WS 288—2008肺结核诊断标准》[7]。
1.纳入标准:(1)年龄≥18岁;(2)初治涂阴肺结核患者,即从未因结核病应用过抗结核药物治疗或曾有过不规则治疗但不满1个月的涂阴肺结核患者;(3)本地户籍人口或常住人口,能保证完成4~6个月的抗结核治疗以及复查,治疗完成后获得2年随访观察;(4)自愿参与研究并签署知情同意书。
2.排除标准:(1)有微卡或抗结核固定剂量复合制剂(FDC)药物的禁忌证者;(2)有药物过敏史,严重心、肝、肾、关节病变,精神或神经疾病、癫痫、免疫变态反应性疾病、严重肺部其他细菌或真菌感染;(3)并发矽肺、糖尿病、HIV/AIDS;(4)重症肺结核,如血行播散性肺结核、多发空洞(两个及以上空洞,视为多发空洞)肺结核患者、干酪性肺炎、并发结核性胸膜炎及其他肺外结核患者等;(5)孕妇、吸毒、药物成瘾者;(6)治疗前外周白细胞<4.0×109/L,肝肾功能异常、空腹血糖超过正常值;(7)近3个月内使用过其他免疫制剂;(8)患者因智障、聋哑残疾等不能配合试验者。
3.退组标准:(1)疗程中随访痰涂片或痰培养转为阳性患者;(2)疗程结束时达到本研究停药标准,但不听劝说要求继续治疗者;(3)因严重不良事件不能继续治疗者;(4)依从性差,中途自行停药而未完成疗程者;(5)其他不可预见的原因不宜继续参与者。
三、研究方法
1.随机分组:将研究对象按纳入顺序在“德派(DAP)流行病学研究系统”进行登记录入,由系统随机分配到观察组(微卡免疫辅助方案组)和对照组(标准方案组),纳入患者按各自分组接受相应的治疗方案。
2.样本量估算:按照非劣性临床随机对照试验的样本量计算公式[8],根据经验设观察组和对照组成功治疗率均为88%,检验水准α=0.05(双侧),检验效能1-β=0.80,样本量比值为1∶1,非劣效界值δ设为不低于对照组10%,观察组与对照组各需166例,共需332例。研究过程中各种原因退组或失访约15%,估算共需样本量382例。
3.治疗方案:观察组采用2H-R-Z-E-M2/2H-R-M2,M代表免疫制剂即微卡(安徽龙科马生物制药有限公司生产,22.5 μg/支,生产批号:S2001003),2表示每两周臀部肌肉注射1次,分别于开始治疗后2、4、6、8、10、12周进行注射,共6次。对照组为2H-R-Z-E/4H-R。两组在强化期服用的H-R-Z-E四联药物(生产批号:151145)均为FDC,继续期的H-R是二联FDC药物(生产批号:160301),抗结核药物FDC由浙江南洋药业有限公司提供。
四、观察指标和判断标准
1.临床疗效指标:观察患者在治疗前、强化期(2个月末)和疗程末(观察组4个月末,对照组6个月末)的以下疗效指标:(1)症状改善情况:临床症状包括咳嗽、咳痰、咯血、发热、盗汗、食欲不振、乏力和消瘦等。症状改善指有任一症状缓解或消失即为症状改善;若有任何症状无缓解或加重,出现新发症状则为症状无改善。(2)免疫功能变化,即检查外周血CD4+T淋巴细胞水平(正常参考值500~1600个/μl)。(3)X线胸片病灶吸收情况:①吸收,病灶吸收≥1/3原病灶;②无改变或病灶恶化,病灶无明显变化、病灶吸收<1/3或病灶范围扩大或播散。(4)治疗效果判断[9]:治疗成功指病原学阴性患者完成规定疗程,疗程末痰涂片或培养结果阴性或未痰检。(5)复发:观察组和对照组分别完成4个月和6个月疗程后1年、2年时进行随访,通过症状筛查、数字X线摄影(DR)胸片复查,对有症状者进行痰结核分枝杆菌复查等方法,发现为活动性肺结核者视为复发,并计算复发率。
2.不良反应观察指标:(1)抗结核药物不良反应监测:主要内容为消化系统(胃肠道反应、肝损伤)、泌尿系统(肾损伤)、运动系统(骨关节损害)、过敏反应(皮肤过敏、其他过敏反应)、神经系统(听神经损伤、视神经损伤、末梢神经炎、其他神经症状)、造血系统(粒细胞计数)等不良反应的发生情况。(2)微卡的不良反应监测:根据《注射用母牛分枝杆菌说明书》,微卡的不良反应监测主要为发热、皮疹和局部红肿。
五、统计学处理
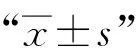
六、伦理学考虑
研究方案经过中国疾病预防控制中心医学伦理委员会审核批准(201418)。在入组前研究对象签署知情同意书,所有病历资料妥善保管并保密。
结 果
一、纳入患者治疗前的基本信息
本研究共纳入患者408例,因失访、死亡、中断治疗或涂阴转阳等原因共退组44例,其中观察组和对照组各22例,两组退组率差异无统计学意义(χ2=0.006,P=0.938)。实际完成规定疗程364例,男性292例(80.2%),女性72例(19.8%),平均年龄(54±17)岁;观察组184例,对照组180例,两组患者在性别、年龄、体质量指数(BMI)和研究现场等分布的差异均无统计学意义(P值均>0.05),具有可比性(表1)。
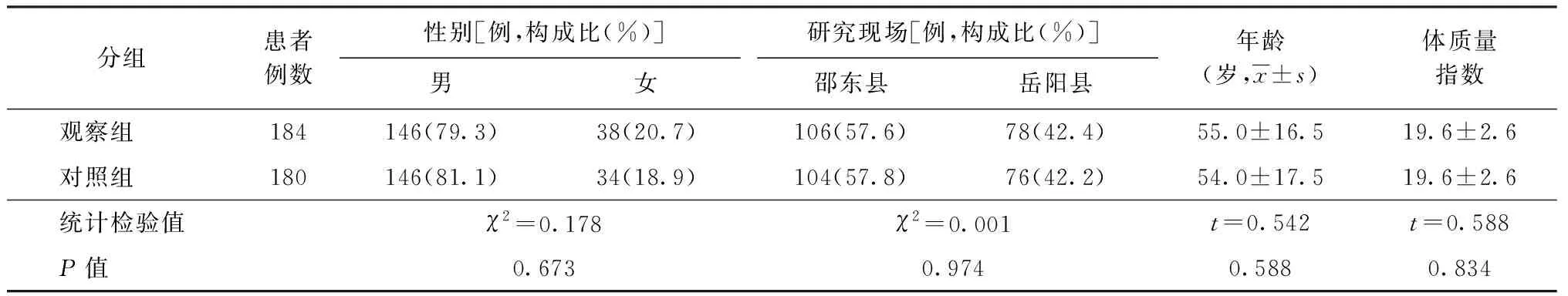
表1 两组患者一般资料比较
二、临床疗效比较
1.症状改善和病灶吸收情况:治疗前观察组有临床症状患者151例(82.1%),无症状患者33例(17.9%);对照组有症状患者148例(82.2%),无症状患者32例(17.8%)。在强化期末观察组151例有临床症状患者中,130例(86.1%)症状改善;对照组148例有症状者中128例(86.5%)症状改善。在疗程末观察组和对照组症状改善率分别为96.0%和95.3%。两组治疗前临床症状分布的差异无统计学意义(χ2=0.002,P=0.969),治疗2个月末症状改善率差异无统计学意义(χ2=0.010,P=0.921)和疗程末症状改善率差异均无统计意义(χ2=0.103,P=0.749)(表2)。
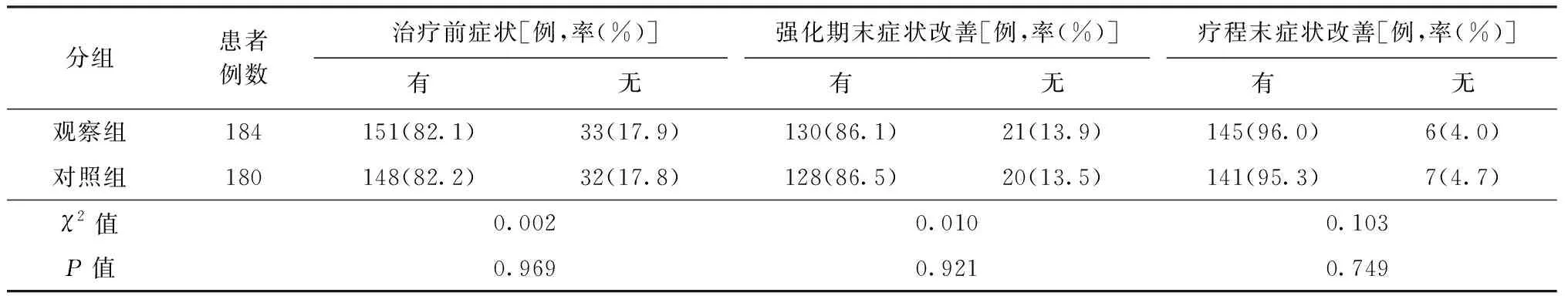
表2 两组患者在不同疗程临床症状改善情况比较
在强化期末(2个月末)观察组和对照组分别有35例(19.0%)和34例(18.9%)X线胸片表现病灶吸收,在疗程末(观察组4个月末,对照组6个月末)分别有76例(41.3%)和75例(41.7%)X线胸片表现病灶吸收。观察组和对照组X线胸片检查病灶吸收率的差异在治疗强化期末均无统计学意义(χ2=0.100,P=0.920)和疗程末(χ2=0.005,P=0.944)差异均无统计学意义(表3)。
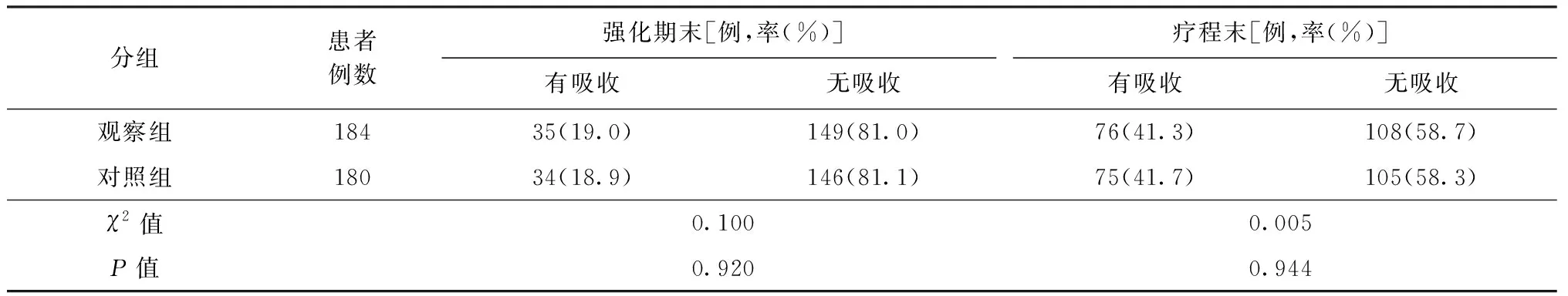
表3 两组患者在不同疗程胸部病灶吸收情况比较
2. CD4+T淋巴细胞水平:两组患者在治疗前、强化期末和疗程末的CD4+T淋巴细胞计数水平的差异均无统计学意义(P值均>0.05)(表4)。

表4 两组患者在不同疗程CD4+T淋巴细胞水平比较
3.成功治疗率和随访复发率:疗程末两组治疗成功率均为100.0%。观察组和对照组分别有174例和172例患者完成疗程结束后12个月随访,分别有1例(0.6%)和2例复发(1.2%)。分别有167例和164例患者完成24个月随访,分别有2例(1.2%)和3例(1.8%)复发。两组在疗程末治疗成功率、随访12个月和24个月的复发率的差异均无统计学意义(P值均>0.05)(表5)。

表5 两组患者完成疗程后复发率比较
三、两组药物不良反应发生情况
疗程中观察组和对照组主要药物不良反应发生从高到低依次是:肝功能损伤、骨关节损伤、药物性皮疹和胃肠道反应等,未发生严重不良反应。两组药物不良反应的总体发生率分别为19.6%和28.3%,差异有统计学意义(χ2=3.846,P<0.05),观察组不良反应发生率低于对照组(表6)。观察组出现微卡注射后局部肿胀、发热、皮疹等轻微不适者25例(13.6%),未进行医疗处理,后自行消退。
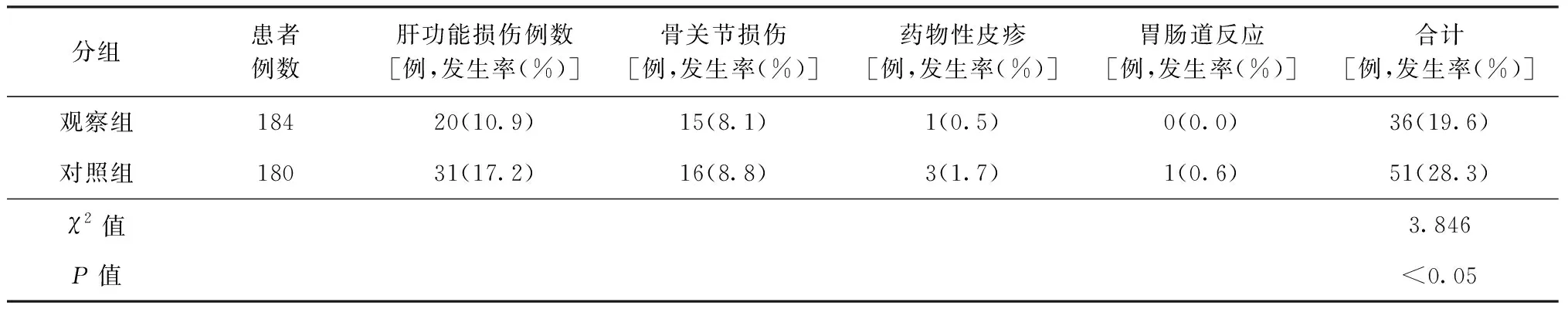
表6 两组患者药物不良反应发生情况
讨 论
细胞免疫在结核病的发生、发展和转归过程中发挥着重要作用。微卡是1964年从母牛乳腺分离出的快生长非结核分枝杆菌,富含与结核分枝杆菌相似的共同抗原[10]。具有免疫调节功能,能促进T淋巴细胞转化、增殖,释放出各种淋巴因子,抑制结核分枝杆菌等感染引起的变态反应所致的病理性损害[11]。
有研究表明,活动性肺结核患者的免疫功能紊乱可能与其体内CD4+T淋巴细胞下降、CD8+T淋巴细胞增多,CD4+/CD8+比值低下,以及辅助性T淋巴细胞Th1/Th2细胞因子比例失调有关[12]。本研究以CD4+T淋巴细胞计数水平作为机体免疫功能的评价指标,结果表明两组在强化期末和疗程末CD4+T淋巴细胞计数均值的差异均无统计学意义。虽然观察组的均值略高于对照组,这可能与结核病患者普遍处于低免疫状态,观察组接受微卡注射后提高了患者的免疫功能状态有关。
研究表明,涂阴肺结核患者发生肺部干酪性肺炎、双侧及以上肺叶受累、空洞形成的比例显著低于涂阳患者,且发生胸膜炎、肺纤维化明显高于涂阳患者[13]。本研究在强化期末和疗程末两组的胸部病灶吸收率较低,可能原因:一是涂阴肺结核患者本身胸部病灶累及肺叶相对较少,但且纤维化病灶较多,治疗后病灶吸收缓慢有关[14];二是本研究旨在通过免疫干预辅助治疗以缩短疗程,研究设计时在疗效判断中将病灶吸收<1/3者定为吸收无改变类,导致了病灶吸收低估现象。
本研究显示,两组患者在完成疗程后随访1年和2年的累计复发率均不足2%,且差异均无统计学意义,说明4个月免疫干预涂阴肺结核治疗方案与标准化疗6个月方案的复发率均较低,达到了一致疗效。与卢水华等[15]对微卡免疫治疗菌阳肺结核患者进行24个月随访得出的结果相似。
在治疗过程中,两组患者药物不良反应发生率分别为19.6%和28.3%,观察组的不良反应发生率低于对照组,这可能与观察组缩短了2个月治疗疗程,发生不良反应机会更少有关[16]。这也与全国微卡菌苗临床研究协作组[17]的报道一致。
本研究采用非劣效性临床随机对照试验来评价微卡免疫干预辅助治疗初治涂阴肺结核4个月短程方案的临床疗效,结果显示观察组和对照组患者的临床症状的改善、胸部病灶的吸收率、CD4+T淋巴细胞计数、成功治疗率和复发率方面的差异均无统计学意义。可见,微卡辅助治疗初治涂阴肺结核4个月治疗方案在临床疗效和安全性方面不劣于WHO推荐的6个月标准治疗方案,且有效缩短了涂阴肺结核患者的疗程。
志谢本研究得到了邵东县疾病预防控制中心主任尹超平、副主任阳新广和岳阳县疾病预防控制中心主任鲁升华、结核病防治科主任李继新等的鼎力相助。
利益部突声明作者均声明无利益冲突

