维持性血液透析患者不安腿综合征危险因素分析
曾颖 姜小梅 刘鹏程 高芦燕 施秋泓 姜山 沈华英 方晨 宋锴
苏州大学附属第二医院1肾内科,2内分泌科,3营养科(江苏苏州215004)
不安腿综合征(restless legs syndrome,RLS)是一种感觉运动障碍疾病,它是终末期肾脏病(end stage renal disease,ESRD)常见的并发症之一,在透析患者中日益常见,不同人群发病率差异较大[1-2]。RLS 患者常伴有睡眠障碍,两者关系密切[3-4],都会增加透析患者心血管事件及死亡风险[5-6]。但是这类透析并发症往往被忽略,因此需要得到临床医生的重视。
现阶段血液透析(HD)患者RLS 的病因尚不明确,针对RLS 更无标准化治疗方案。药物治疗多为短期有效,长期疗效不明确,存在很大弊端[7]。尽管有研究表明血液滤过(hemofiltration,HDF)及血液灌流可以不同程度地减轻RLS 的症状[8-9],但血滤吸附(hemodiafiltration with endogenous reinfusion,HFR)治疗RLS至今鲜有报道。HFR 是一种新型的血液净化治疗方式,它联合对流、吸附、弥散三种透析相关原理,将超滤液通过树脂筒再生后作为生理性置换液重新输入,同时具有联机在线血液透析滤过的优点,对滤过液进行选择性净化,可有效清除水溶性小、中、大分子毒素及蛋白集合毒素。本研究旨在通过调查HD 患者RLS 的相关危险因素,观察HFR 是否可以改善以及可能通过哪些途径减轻RLS 症状及睡眠问题,为提高ESRD 患者生活质量及生存率提供新的透析模式。
1 资料与方法
1.1 一般资料选择2020年6月1日至12月31 日期间于我院血液透析中心接受维持性血液透析(MHD)的患者247 例。入组标准:(1)年龄>18 岁;(2)接受规律性血液透析≥6 个月。排除标准:(1)接受HD 治疗前已有RLS 者;(2)患有精神类疾病者;(3)存在糖尿病神经病变;(4)合并恶性肿瘤、严重心律失常、肝功能不全等;(5)正服用中枢神经系统药物的非RLS 患者。本研究经苏州大学附属第二医院伦理委员会批准(伦理批号:JD-LK-2020-124-01)。
1.2 血液透析所有患者均使用碳酸氢盐透析液,透析液流量500 mL/min;采用4008S 型血液透析机(德国费森尤斯公司生产),透析器选用聚砜膜。每周透析3次,每次4 h,血流量200~260 mL/min。
1.3 RLS 的诊断标准采用国际不宁腿综合征研究组(International Restless Legs Syndrome Study Group,IRLSSG)制定的RLS 诊断标准[10]进行诊断,主要包括下列四方面:(1)因单腿或双腿的小腿腿部蠕动、瘙痒、蚁走、疼痛等不适感引发腿部活动,活动后不适感缓解;(2)坐、躺等静息或不活动状态时不适感出现甚至加重;(3)持续行走、伸展、搓揉等活动时,不适感部分或完全缓解;(4)夜间症状易出现且加重。并依据RLS 病情严重程度评定量表对其进行量化评分。量表共设计10 个问题,每个问题有5 个选择项,分别代表从无到有非常严重的RLS 的5 个级别,得分从0 到40 分:1~10 分为轻度,11~20 分为中度,21~30 分为严重,31~40 分为非常严重。
1.4 睡眠质量评估应用匹茨堡睡眠质量指数量表(Pittsburgh sleep quality index,PSQI)评估患者的睡眠质量。PSQI 由18 个题目构成,分为7 个部分,包括:主观睡眠质量、入睡时间、睡眠时间、睡眠效率、睡眠紊乱、助眠药物使用、日间功能障碍。每个部分按0~3 分计分,累计各部分分值得出PSQI总分,总分为0~21 分。总分越高,代表睡眠质量越差。总分≥5 分者提示睡眠质量差。
1.5 观察指标收集HD 患者一般资料及实验室指标等数据,包括性别、年龄、透析龄、体质指数、血红蛋白、白蛋白、肾功能、电解质、铁代谢指标、血全段甲状旁腺激素(PTH)、同型半胱氨酸、血β2-微球蛋白(β2-MG)水平、尿素清除指数等。
1.6 分组及治疗经不安腿诊断标准量表确诊为RLS 患者49 例,随机分为两组。观察组21 例,予HFR 治疗,即每周2 次常规血液透析,同时接受每周1 次HFR 治疗,总疗程3 个月。HFR 治疗采用意大利Bellco 公司生产的Firmula2000 型血液透析机,使用贝而克Formular Therapy 全功能血液透析滤过装置,包含Supra HFR 双腔滤器+树脂吸附罐+管路。双腔滤器为聚醚砜膜材,上段是高通量滤过器(对流型),下段是低通量滤过器(弥散型);树脂吸附柱为HFR 专用吸附柱,树脂为苯乙烯树脂;透析液为碳酸氢盐透析液。对照组28 例,给予HDF 治疗,即每周2 次常规血液透析,同时接受每周1 次HDF 治疗,总疗程3 个月。On-line HDF采用前稀释法,每次置换液量20 L。所有患者均采用全身低分子肝素抗凝,无特殊情况不改变患者原有抗凝方案。
1.7 统计学方法本研究采用SPSS 23.0 进行数据统计分析,并行正态分布检验。符合正态分布的计量资料以均数±标准差表示,不符合正态分布的数据以M(P25,P75)表示。符合正态分布资料组间比较采用t检验,不符合正态分布资料采用秩和检验。应用单因素logistic 回归进行单因素分析,将单因素分析中P<0.05 的变量作为自变量进行多因素logistic 回归分析(向前法)。以P<0.05 表示差异有统计学意义。
2 结果
2.1 临床资料247 例HD 患者中49 例符合RLS诊断,患病率19.84%。其中男31 例,女18 例,年龄(55.16 ± 13.53)岁,透析龄(71.20 ± 41.84)个月。IRIS 量表评分结果示,轻度16 例(32.65%),中度19 例(38.78%),重度9 例(18.37%),极重度5 例(10.20%)。
2.2 RLS 组与非RLS 组一般基线特征的比较与非RLS 组比较,RLS 组患者年龄小,透析龄较长,血肌酐、视黄醇结合蛋白、血磷、血全段甲状旁腺素、血β2-微球蛋白水平明显升高,尿素清除指数显著降低(均P<0.05),见表1。
表1 两组患者的临床和实验室指标的比较Tab.1 Comparison of clinical and laboratory indexes between the two groups±s
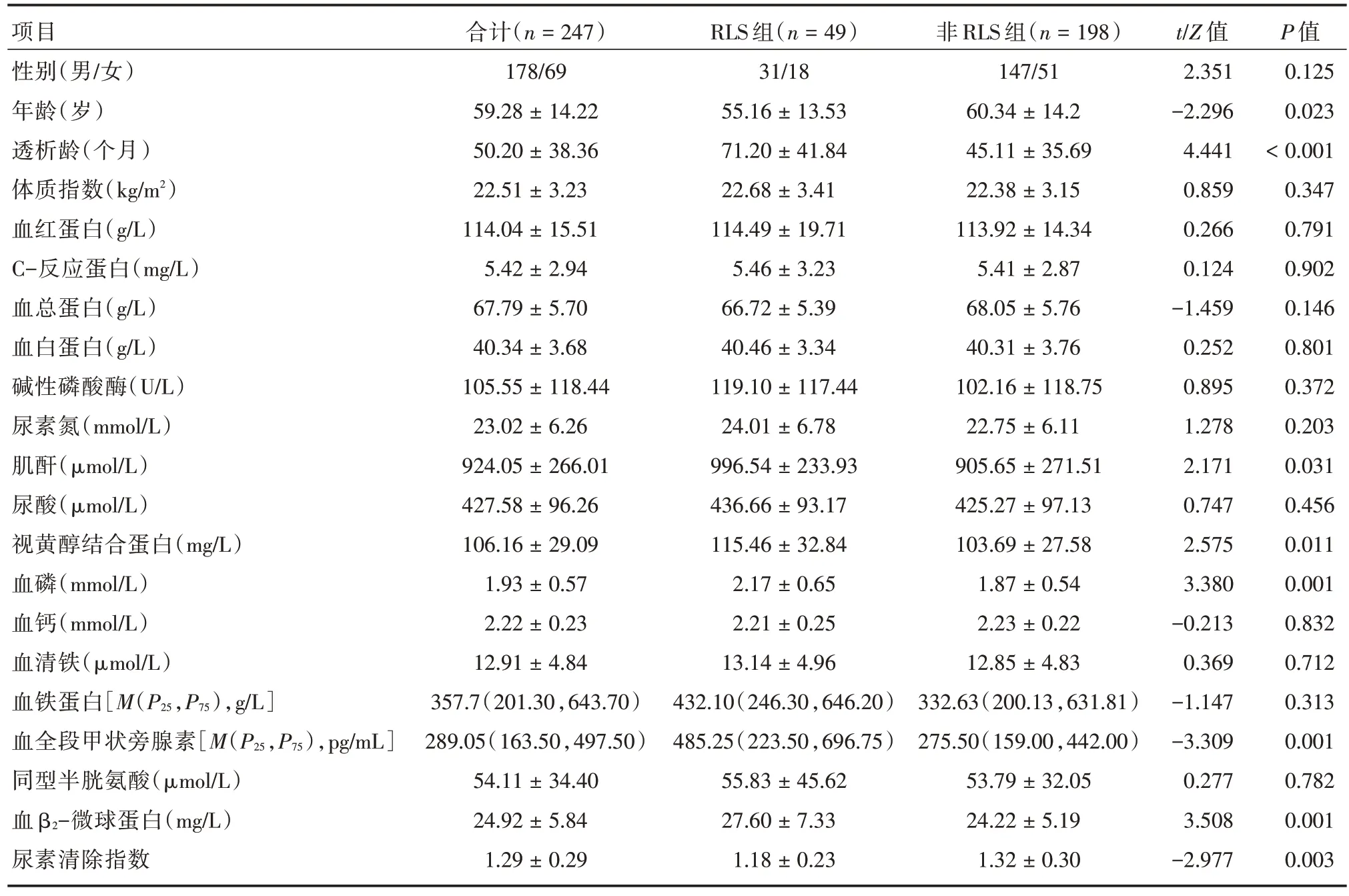
表1 两组患者的临床和实验室指标的比较Tab.1 Comparison of clinical and laboratory indexes between the two groups±s
合计(n=247)RLS 组(n=49) 非RLS 组(n=198)t/Z 值P 值178/6931/18147/512.3510.125 59.28±14.2255.16±13.5360.34±14.2-2.2960.023项目性别(男/女)年龄(岁)透析龄(个月)体质指数(kg/m2)血红蛋白(g/L)C-反应蛋白(mg/L)血总蛋白(g/L)血白蛋白(g/L)碱性磷酸酶(U/L)尿素氮(mmol/L)肌酐(μmol/L)尿酸(μmol/L)视黄醇结合蛋白(mg/L)血磷(mmol/L)血钙(mmol/L)血清铁(μmol/L)血铁蛋白[M(P25,P75),g/L]血全段甲状旁腺素[M(P25,P75),pg/mL]同型半胱氨酸(μmol/L)血β2-微球蛋白(mg/L)尿素清除指数50.20±38.36 22.51±3.23 114.04±15.51 5.42±2.94 67.79±5.70 40.34±3.68 105.55±118.44 23.02±6.26 924.05±266.01 427.58±96.26 106.16±29.09 1.93±0.57 2.22±0.23 12.91±4.84 357.7(201.30,643.70)289.05(163.50,497.50)54.11±34.40 24.92±5.84 1.29±0.29 71.20±41.84 22.68±3.41 114.49±19.71 5.46±3.23 66.72±5.39 40.46±3.34 119.10±117.44 24.01±6.78 996.54±233.93 436.66±93.17 115.46±32.84 2.17±0.65 2.21±0.25 13.14±4.96 432.10(246.30,646.20)485.25(223.50,696.75)55.83±45.62 27.60±7.33 1.18±0.23 45.11±35.69 22.38±3.15 113.92±14.34 5.41±2.87 68.05±5.76 40.31±3.76 102.16±118.75 22.75±6.11 905.65±271.51 425.27±97.13 103.69±27.58 1.87±0.54 2.23±0.22 12.85±4.83 332.63(200.13,631.81)275.50(159.00,442.00)53.79±32.05 24.22±5.19 1.32±0.30 4.441 0.859 0.266 0.124-1.459 0.252 0.895 1.278 2.171 0.747 2.575 3.380-0.213 0.369-1.147-3.309 0.277 3.508-2.977<0.001 0.347 0.791 0.902 0.146 0.801 0.372 0.203 0.031 0.456 0.011 0.001 0.832 0.712 0.313 0.001 0.782 0.001 0.003
2.3 单因素logistic 分析将两组间差异有统计学意义的指标:年龄、透析龄、血肌酐、视黄醇结合蛋白、血磷、尿素清除指数、PTH、β2-微球蛋白(P<0.05)纳入单因素logistic回归分析。其中年龄、透析龄以均值作为分界值进行二分类赋值。结果显示,年龄<60岁、透析龄≥50个月、高血肌酐、视黄醇结合蛋白、血磷、血全段甲状旁腺素及血β2-微球蛋白水平,低尿素清除指数与RLS有关(P<0.05),见表2。
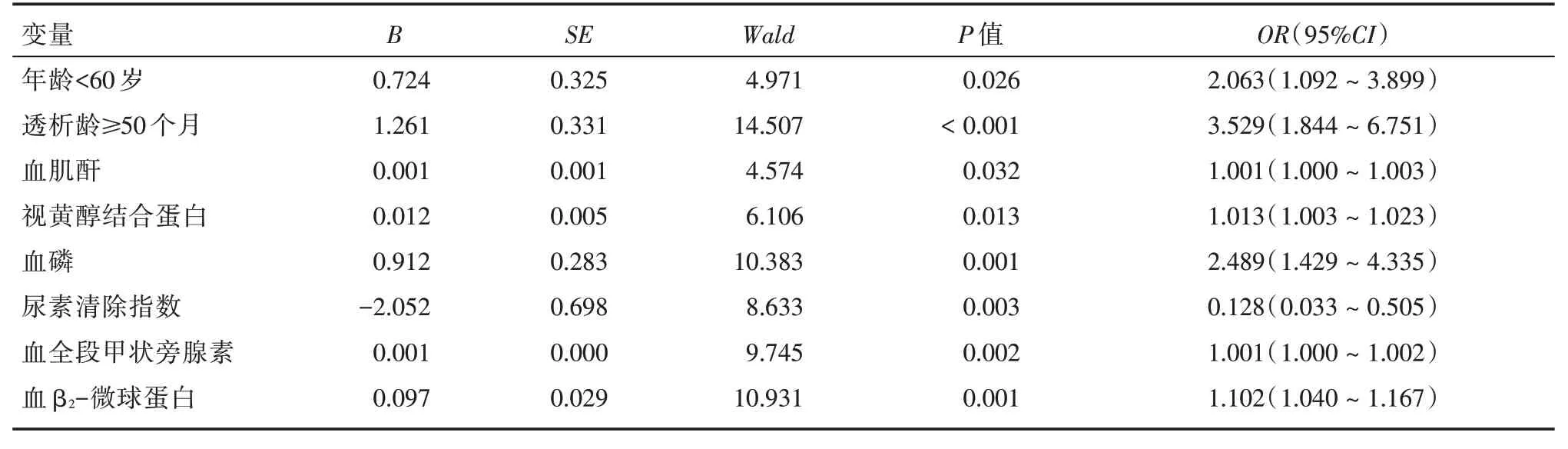
表2 HD 患者发生RLS 危险因素的单因素logistic 回归分析Tab.2 Univariate logistic regression analysis of risk factors for RLS in HD patients
2.4 多因素logistic 分析以HD 患者是否有RLS为因变量(否=0,是=1),将单因素分析P<0.05 的变量作为自变量进入多因素logistic 回归分析。结果显示,透析龄≥50 个月、高血磷水平、低尿素清除指数、高β2-微球蛋白水平是血液透析患者发生RLS 的独立危险因素(表3)。
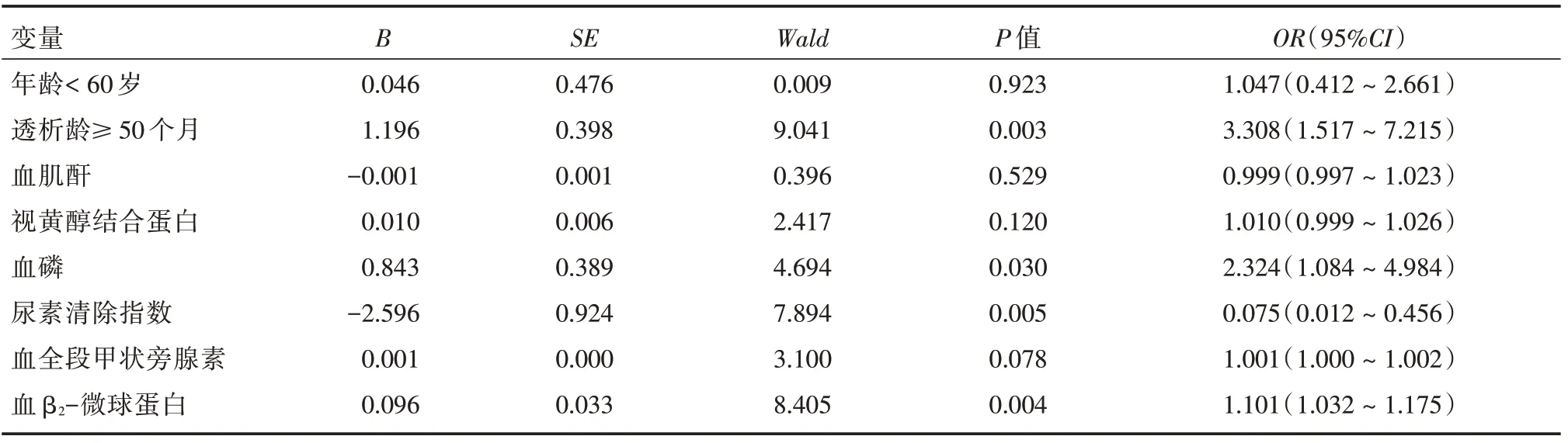
表3 HD 患者发生不安腿综合征危险因素的多因素logistic 回归分析Tab.3 Multivariate logistic regression analysis of risk factors for RLS in HD patients
2.5 两组RLS 患者治疗前后的比较49 例RLS患者被采用简单随机化法分为两组,HFR 组21例,其中女9 例(42.86%),男12 例(57.14%),年龄(50.18 ± 14.55)岁,透析龄(69.08 ± 39.13)个月,HDF 组28 例,其中女13 例(46.43%),男15 例(53.57%),年龄(55.82 ± 13.16)岁,透析龄(72.36±50.58)个月。
两组患者血磷水平、尿素清除指数水平治疗前后比较,差异无统计学意义(P>0.05)。与治疗前比较,HFR 组患者治疗后血β2-微球蛋白水平、RLS 及PSQI 评分均显著下降(P<0.05);HDF 组仅RLS 评分明显降低(t= 4.113,P= 0.002)。与HDF组相比,HFR 组患者治疗后血β2-微球蛋白及RLS评分下降程度更显著(P<0.05),见表4、5。
表4 两组RLS 患者治疗前后各参数比较Tab.4 Comparison of parameters between the two groups of RLS patients before and after treatment ±s
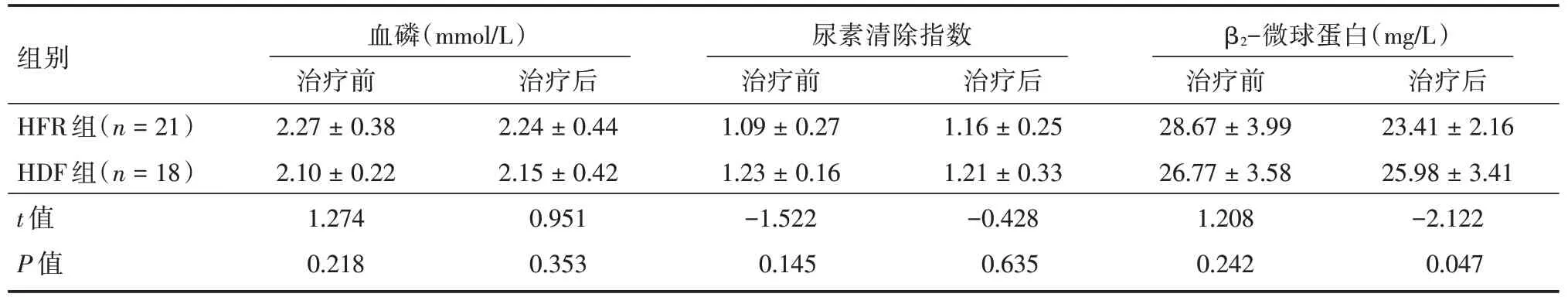
表4 两组RLS 患者治疗前后各参数比较Tab.4 Comparison of parameters between the two groups of RLS patients before and after treatment ±s
组别HFR 组(n=21)HDF 组(n=18)t 值P 值血磷(mmol/L)治疗前2.27±0.38 2.10±0.22 1.274 0.218治疗后2.24±0.44 2.15±0.42 0.951 0.353尿素清除指数治疗前1.09±0.27 1.23±0.16-1.522 0.145治疗后1.16±0.25 1.21±0.33-0.428 0.635 β2-微球蛋白(mg/L)治疗前28.67±3.99 26.77±3.58 1.208 0.242治疗后23.41±2.16 25.98±3.41-2.122 0.047
表5 两组RLS 患者治疗前后RLS 及PSQI 评分的变化Tab.5 Changes of RLS and PSQI scores of RLS patients in the two groups before and after treatment ±s
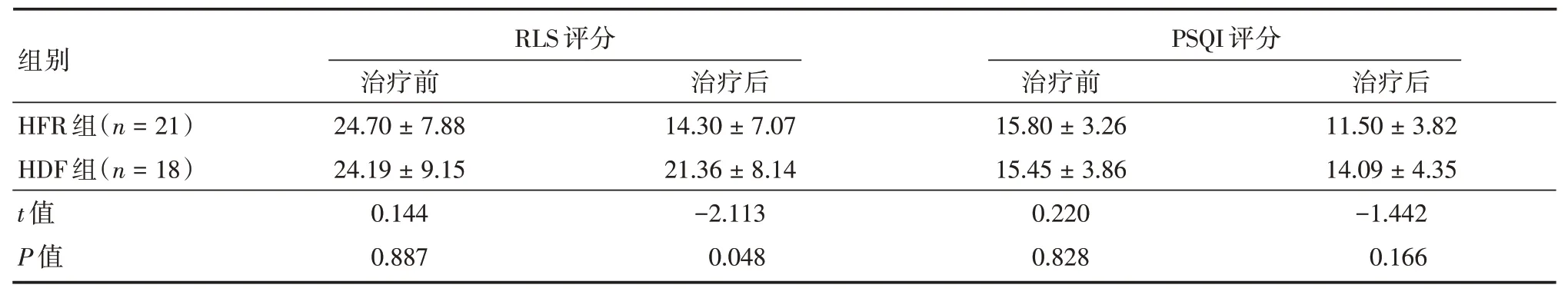
表5 两组RLS 患者治疗前后RLS 及PSQI 评分的变化Tab.5 Changes of RLS and PSQI scores of RLS patients in the two groups before and after treatment ±s
组别HFR 组(n=21)HDF 组(n=18)t 值P 值RLS 评分治疗前24.70±7.88 24.19±9.15 0.144 0.887治疗后14.30±7.07 21.36±8.14-2.113 0.048 PSQI 评分治疗前15.80±3.26 15.45±3.86 0.220 0.828治疗后11.50±3.82 14.09±4.35-1.442 0.166
3 讨论
目前围绕ESRD 患者RLS 发病因素的研究是热点。ESRD 老年患者常因尿毒症环境、衰老导致肌肉质量和躯体功能的丧失[11],IRENE 等[12]证实老年透析患者RLS 的发生率较年轻患者明显增加。但本研究未发现年龄是HD 患者RLS 的影响因素,可能与本中心HD 患者平均年龄偏低有关。本研究结果显示透析龄≥50 个月、高血磷、低尿素清除指数、高β2-微球蛋白是HD 患者发生RLS 的独立危险因素。UIABIDEEN 等[13]支持上述观点,认为血透时间越长的患者出现RLS 的几率越高。残肾功能丧失、透析不充分以及钙磷代谢紊乱等问题在长透析龄患者中普遍存在,被认为与透析患者RLS 密切相关。有研究[12]表明96%的HD 患者在肾移植后数天或数周内RLS 症状消失。但是肾移植失败的患者随着肾功能恶化再次出现RLS,且症状较之前更严重[14],这充分说明肾功能丧失与尿毒症患者继发RLS 有关。SHERIFA 等[15]研究520 例ESRD 患者,结果发现ESRD 患者发生RLS的风险较CKD3 期患者增加2.6 倍,同时证实透析不充分与RLS 独立相关。高磷血症是促进ESRD患者弥漫性血管钙化的关键因素,血管弥漫性钙化最终会导致RLS 的发生[16]。本研究也证实高磷血症在RLS 组明显升高,研究结果进一步显示高磷血症与RLS 有关。YANG 等[17]发现透析患者RLS 常伴有明显的高血磷。于晓丽等[18]认为腹透RLS 患者服用各种磷结合剂,可能会弱化其对RLS的作用。除了小分子毒素之外,不少研究证实与透析相关的中、大分子毒素,包括血β2-微球蛋白都会影响神经传导,导致神经纤维变性和脱髓鞘[19],最终进展为RLS。本研究同样发现RLS 透析患者血β2-微球蛋白水平明显高于非RLS 透析患者。STEFANIDIS 等[20]也证实较高水平血β2-微球蛋白的HD 患者继发RLS 风险明显增加。
RLS 是一种睡眠相关的运动障碍,由于夜间症状发作最为明显,因此RLS 在一定程度上影响患者的睡眠[21]。无论是RLS 还是睡眠障碍都是复杂的临床问题,有研究表明两者均与透析患者神经病变相关的中、大分子毒素有关[22]。笔者发现与HDF 治疗相比,HFR 可以显著降低血β2-微球蛋白水平。CHEN 等[23]也证实HFR 治疗可以将血β2-微球蛋白水平降低43.60%。HFR 之所以较血液滤过有优势,可能是因为HFR 与HP 作用原理类似,有效吸附中大分子尿毒症毒素、蛋白结合类毒素、炎症因子等[8],从而短时间内改善HD 患者的RLS症状及睡眠质量[24]。BOLASCO 等[25]研究表明,HFR 清除血磷的效果优于HD,因为HFR 可以清除影响血磷及骨代谢的相关炎症因子,但本研究并未发现HFR 可以改善血磷及尿素氮的水平,这可能与HFR 使用透析器表面积偏小、吸收小分子毒素的能力受限有关[23]。
本研究证实,HFR 治疗RLS 效果确切,且优于血液滤过。但本研究为单中心前瞻性研究,局限性在于样本量小、治疗时间短。在今后的研究中,需要扩大样本量,评估HFR 的长期疗效。希望通过深入探索将HFR 作为一种治疗HD 患者RLS 及睡眠问题的新手段在临床上推广。

