配标溶剂对双区大气压化学电离质谱分析环境烟气标志物3-乙烯基吡啶的影响
张 硕,李明雷,王丁众,孙世豪,潘文亮,张建勋*
1. 中国烟草总公司郑州烟草研究院,郑州高新技术产业开发区枫杨街2 号 450001
2. 河北中烟工业有限责任公司技术中心,石家庄市桥西区维明南大街1 号 050051
3-乙烯基吡啶(3-Ethenylpyridine,3-EP)是环境烟草烟气(Environmental tobacco smoke,ETS)风险评估中较常用的标志物之一,其在ETS 中的初始存在水平为 50 ng/L 左右[1-4]。GC-MS 法是分析 ETS中3-EP 的最常见方法[5-7]。为了满足仪器灵敏度的要求,在进行GC-MS 分析前,通常需要耗费较长的时间(一般是6 h)收集较大体积(通常是数百升)的ETS 用于富集3-EP。显然,通过这种方法获取的结果难以呈现环境烟气动态变化的特征。风险评估对ETS化学构成动态变化数据的需求促使分析工作者开发了一系列ETS的实时在线分析方法,其中,基于常压质谱技术的方法因简单、快速、灵敏而备受关注[8-10]。在用常压质谱技术对气体样品进行检测时,为了实现定量分析,需要配制梯度浓度的标准气体样品用于建立外标标准曲线。通常的做法是:首先向一定体积的顶空瓶中加入一定量不同浓度的标准溶液,配制系列浓度的标准气体样品,然后通过质谱直接分析标准气体样品建立标准曲线。但是,研究发现,在借助常压质谱技术进行分析时,配标溶剂能通过质子竞争和电荷转移的方式显著影响分析物在离子源内的离子化效率,从而影响分析,这也称为溶剂效应;而且这种效应在微量、痕量目标物的分析中更为明显。例如,二氯甲烷可以显著提升氯苯衍生物的离子化效率[11],甲苯可以提升多环芳香类化合物的离子化效率[12-13],而乙腈能够显著降低痕量环氧化物的离子化效率[14],此外合适的湿度能提高丙烯醛和巴豆醛的离子化效率[15]。同时不同溶剂浓度对离子化效率的影响也不同,这种溶剂效应造成分析物离子化效率改变而引起质谱信号强度的变化,势必也造成分析结果存在差异。在前期开展基于大气压化学电离(Atmospheric pressure chemical ionization,APCI)技术的研究中,也注意到溶剂效应对分析的干扰[15]。但迄今为止,在关于3-EP的常压质谱分析中,溶剂效应并没有受到应有的关注。
基于此,以本研究组开发的双区大气压化学电离(Double-region atmospheric pressure chemical ionization,DRAPCI)源为研究平台,考察溶剂效应对3-EP离子化效率的影响,比较不同溶剂背景下3-EP的分析结果,建立用于ETS 标志物快速分析的直接DRAPCI-MS 方法,旨在为环境烟气中3-EP 的分析提供方法参考。
1 材料与方法
1.1 试剂和仪器
环己烷(≥99.9%,上海星可高纯度溶剂有限公司);乙腈、甲醇(色谱纯,美国 Sigma-Aldrich公司);丙酮(色谱纯,上海安谱实验科技股份有限公司);3-乙烯基吡啶[≥96.0%,含对叔丁基邻苯二酚(p-tert-butylcatechol,TBC)稳定剂,上海阿拉丁生化科技股份有限公司]。
XevoTMTQ-MS 大气压化学电离串联质谱仪(美国Waters公司),配备MassLynx V4.1质谱仪操作软件(美国Waters 公司);GenPure 超纯水仪(德国Thermo Fisher 公司);CP224S 型电子天平[感量0.000 1 g,梅特勒-托利多仪器(上海)有限公司];石英玻璃毛细管(0.53 mm i.d.,0.68 mm o.d.,澳大利亚SGE Analytical Science公司);20 mL棕色样品瓶(上海安普公司);双区大气压化学电离源(自制),详细参数参见文献[16];烟气捕集瓶(自制),详细参数参见文献[17]。
1.2 方法
1.2.1 样品制备
标准溶液:准确称量25 mg 3-EP,分别以环己烷、乙腈、丙酮和甲醇为溶剂配制浓度为25 mg/L 的母液,随后使用对应溶剂采用逐级稀释的方式各配制一系列浓度梯度的3-EP标准溶液。
标准气体样品:探究溶剂量对3-EP离子化效率影响时,取2 μL母液于20 mL样品瓶中,并且分别添加0、2、4、6、8、10 μL对应溶剂,密封静置,待母液和所加溶剂完全挥发后,3-EP样品浓度为2.5 μg/L;在对目标物进行定量分析时,分别以4种溶剂,配制浓度为1.0、2.5、5.0、10.0、25.0、50.0、100.0、250.0和500.0 μg/L,以及1.0、2.0、10.0和50.0 mg/L的标准溶液,取10 μL 不同浓度梯度的分析物标准溶液于20 mL 棕色样品瓶中,密封静置待其挥发,其气化后的浓 度 分 别 为 0.50、1.25、2.50、5.00、12.50、25.00、50.00、125.00、250.00、500.00 ng/L,以及1.00、5.00 和25.00 μg/L。质谱及其进样条件:
电离源:DRAPCI 源;离子化模式:正离子模式;离子源温度:100 ℃;电晕放电电流:5 μA;APCI 探头温度:100 ℃;脱溶剂气:N2,流速 250 L/h;锥孔气:N2,流速10 L/h;扫描模式:全扫描模式、子离子扫描和多反应检测;扫描范围:30~200 amu;锥孔电压:30 V;碰撞电离能:30 eV;碰撞气:Ar,流速0.25 mL/min;进样深度:5 cm;进样时间:3 s。
ETS 样品:ETS 采样地点为会议室(长×宽×高:8.4 m×7.3 m×3.0 m),采样开始前,3 名志愿者在30 min 内连续抽吸9 支卷烟后离开。烟气捕集瓶放置于会议室中央高约1.2 m的操作台上,每隔10 min采样1次,连续采样3 h,每次采样时间持续10 min。质谱及其进样条件:
电离源:DRAPCI 源;离子化模式:正离子模式;离子源温度:100 ℃;电晕放电电流:5 μA;APCI 探头温度:100 ℃;脱溶剂气:N2,流速250 L/h;锥孔气:N2,流速10 L/h;扫描模式:多反应检测;离子对:106>77;锥孔电压:30 V;碰撞电离能:30 eV;碰撞气:Ar,流速0.25 mL/min;进样深度:10 cm;进样时间:3 s。
2 结果与讨论
2.1 ETS中3-EP的DRAPCI-MS特征
DRAPCI 源将放电区和电离区分离,可明显减少分析物在离子源内发生碎裂,使质谱图相对简单,且能明显提高检测的灵敏度,在小分子挥发性成分分析研究中具有明显优势[16]。结合ETS分析中对方法灵敏度的要求,尝试用DRAPCI-MS 方法分析ETS标志物3-EP。图1是抽吸卷烟后会议室中ETS的典型DRAPCI-MS 质谱图。DRAPCI 源为较“软”的电离源,一般只形成准分子离子[M+H]+,通过二级质谱分析可知,质谱图中m/z 106 的离子对应于3-EP,表明采用 DRAPCI-MS 可以实施对 ETS 中3-EP的检测。

图1 室内ETS样品全扫描质谱图及3-EP(m/z 106)子离子扫描图Fig.1 Full scan mass spectrum of indoor ETS sample and daughter scan mass spectrum of 3-EP(m/z 106)
2.2 配标溶剂对3-EP离子化效率的影响
采用直接质谱方法进行ETS 中3-EP 的定量分析,需要配制不同浓度的3-EP标准气体样品。考虑到配标溶剂可能会对3-EP的离子化造成影响,需要考察不同配标溶剂下3-EP的质谱图特征。图2是不同配标溶剂下3-EP样品的质谱图,相关质谱信号的归属见表1。可以看出,以常压质谱分析时常用的配标溶剂环己烷、甲醇、乙腈和丙酮等制备3-EP 标准气体进行质谱分析时,配标溶剂的背景信号并不干扰3-EP信号的呈现。虽然环己烷的背景谱图复杂,但是并不影响借助二级谱图对3-EP 进行定性定量分析。

表1 不同配标溶剂时3-EP的DRAPCI-MS质谱图中的离子信号和归属①Tab.1 Ion signals and attribution in DRAPCI-MS mass spectrometry of 3-EP in different standard solvents

图2 不同配标溶剂时3-EP样品的质谱图Fig.2 Full scan mass spectra of 3-EP in different standard solvents
2.2.1 配标溶剂类型对3-EP离子化效率的影响
尽管在4 种配标溶剂下,3-EP 均能呈现有效的质谱信号,但3-EP 的绝对离子强度有所不同。在3-EP浓度相同的情况下,进一步考察不同配标溶剂下3-EP 的绝对离子强度。结果显示,配标溶剂不同,3-EP的绝对离子强度不同。以环己烷为配标溶剂时,离子化效率最高,是甲醇配标情况下的3倍。
不同配标溶剂造成的3-EP离子化效率的差异,可能是离子源内溶剂分子与3-EP 竞争质子造成的。相关研究[18]已经表明,在以质子迁移为基本离子化原理的常压质谱中,溶剂与分析物之间存在严重的质子竞争现象,竞争能力的强弱在一定程度上取决于质子亲和势(Proton affinity,PA),质子亲和势越小,质子亲和能力越弱。溶剂分子的质子亲和势越小,溶剂分子与目标物分子竞争质子的能力就越弱,越有利于分析物分子离子化。文献[19]中报道,环己烷、甲醇、丙酮和乙腈的质子亲和势分别为686.9、754.3、812.0 和779.2 kJ/mol。因此,从质子亲和势角度讲,以环己烷为配标溶剂,3-EP 的离子化效率更高,其次是甲醇、乙腈和丙酮。但本研究中,实验结果显示,3-EP的离子化效率与质子亲和势之间并不成典型的正相关关系。
2.2.2 配标溶剂量对3-EP离子化效率的影响
在3-EP浓度一定的情况下,考察溶剂量变化对3-EP 的绝对离子强度的影响,结果如图3 所示。以环己烷为溶剂时,3-EP的响应强度基本不随溶剂浓度的增加发生变化;以丙酮为溶剂时,3-EP 的响应强度也相对稳定,但信号强度的重复性相对较差;以甲醇或乙腈为溶剂时,3-EP的响应强度均随溶剂浓度的增加呈下降趋势。为了了解造成信号强度下降的原因,进一步分析配标溶剂和配标溶剂背景下3-EP的DRAPCI-MS谱图。
以甲醇为配标溶剂时,3-EP的谱图中主要呈现甲醇的[S+H]+、[2S+H]+和3-EP 的[M+H]+(S 表示溶剂,M 表示3-EP)等信号峰。提高甲醇浓度后发现,甲醇二聚体的信号强度逐渐增加,而3-EP 的信号强度则呈降低趋势,如图3c所示。表明3-EP在与甲醇单体竞争质子时处于优势,更容易获得质子而离子化;而与甲醇二聚体竞争质子时处于劣势。数据显示,甲醇二聚体的质子亲和势比甲醇单体的质子亲和势高135 kJ/mol,推测甲醇二聚体的质子亲和势可能高于3-EP。在DRAPCI 源中,试剂离子优先和甲醇二聚体发生质子交换反应,从而抑制了3-EP的电离。此现象在Charles等[20]的研究中也被发现,水杨酸甲酯(PA 855 kJ/mol)的离子化只能通过与质子化甲醇单体之间发生质子转移来实现,不能与质子化的甲醇二聚体发生质子转移。DRAPCI 源的离子化区域是相对封闭的腔体结构,这种结构本身可能更有利于造成源内甲醇聚集,从而促进大量甲醇二聚体形成。初步实验数据也证明,对纯甲醇进行DRAPCI-MS 分析时,提高甲醇浓度,甲醇二聚体的信号强度逐渐增加。
以丙酮为配标溶剂时,如图2c所示,m/z 59、117离子信号归属于丙酮的[S+H]+、[2S+H]+。但不同的是,丙酮二聚体的绝对离子强度并不随丙酮浓度的升高而升高,3-EP的绝对离子强度也不会因丙酮浓度的增加发生较大变化,除了重复性相对较差外,绝对离子强度持续保持较低状态,如图3b所示。其原因有待进一步研究。


图3 不同溶剂添加量时3-EP及溶剂的提取离子流图(EIC)和溶剂添加量对3-EP离子化效率的影响(n=3)Fig.3 Extracted ion chromatography(EIC)of 3-EP and solvent at different solvent additions, and influences of solvent additions on ionization efficiency of 3-EP(n=3)
以乙腈为配标溶剂时,质谱图中主要呈现乙腈的[S+H]+、[2S+H]+、[3S+H]+和3-EP的[M+H]+等离子信号。改变乙腈的量,其二聚体和三聚体的绝对离子强度基本保持不变,但3-EP的信号仍然会随乙腈浓度的增加而降低,如图3d所示。对纯乙腈进行质谱分析,[2S+H]+、[3S+H]+的信号强度也未随乙腈浓度的增加而改变。这表明,在乙腈背景下,溶剂分子多聚体竞争质子可能并不是3-EP 信号下降的主要原因。有研究显示,乙腈能够显著降低痕量环氧化物的电离效率,并认为是由于溶剂分子与分析物之间形成的中性分子团簇,掩盖了分析物的质子化位点,抑制目标分析物的离子化[14]。推测增加乙腈浓度导致3-EP绝对离子强度下降的原因可能与之类似。
2.3 配标溶剂对DRAPCI-MS方法分析性能的影响
为了进一步确认配标溶剂对分析方法性能的影响,考察不同配标溶剂下,DRAPCI-MS 方法分析3-EP 时的性能参数。选择母离子>子离子(106>77)离子对,在质谱最佳实验条件下,以多反应监测模式(Multiple reaction monitoring, MRM)进行分析。为了实现对ETS中3-EP的定量,在顶空瓶中加入一定体积不同浓度的标准溶液,配制一系列浓度的气体标准样品,然后通过DRAPCI-MS 方法直接分析,建立标准曲线,如图4 所示。考察了4 种配标溶剂下分析方法的性能参数,结果见表2。

图4 不同溶剂下DRAPCI-MS/MS定量分析3-EP的标准曲线(n=3)Fig.4 Calibration curves of 3-EP by DRAPCI-MS/MS in different solvents(n=3)
表2 的数据显示,以乙腈或甲醇为配标溶剂时,检出限(LOD)和定量限(LOQ)数值较大,但在高浓度区间线性良好;以丙酮或环己烷为配标溶剂时,检出限和定量限相对较低,且在低浓度区间线性良好;以环己烷为配标溶剂时的检出限和定量限较甲醇更低,分别为0.38 和1.15 ng/L。这些数据正好印证了前述的实验结果,即在DRAPCI源内,乙腈和甲醇抑制3-EP的离子化,在极低的浓度下,这种抑制现象更为明显,从而影响了DRAPCI-MS 对低浓度3-EP 的检出和定量;而环己烷和丙酮并没有明显的离子化抑制现象。文献[1]中报道,ETS 中3-EP 的初始浓度约为50 ng/L,这是一个相对较低的量值。因此,从ETS 动态检测的角度看,环己烷和丙酮是比较合适的配标溶剂。

表2 不同溶剂背景下3-EP分析的性能参数(n=3)Tab.2 Performance parameters of 3-EP in different solvents(n=3)
2.4 不同配标溶剂建立的方法下ETS中3-EP测试的比较
图5显示了不同配标溶剂建立的检测方法下,室内ETS样品中3-EP浓度随时间的变化趋势。可知,室内ETS 样品中3-EP 的浓度在2 h 内从50.59 ng/L下降至1.42 ng/L,并且下降速率呈现先快后慢的趋势,这一结果和采用直接APCI-MS的分析结果基本一致[17]。造成这一变化趋势的原因,一是自然通风的环境使3-EP 浓度下降,二是3-EP 可能吸附在墙壁或者会议室内的其他物体表面,随着时间的推移,吸附在物体表面的3-EP又会解吸释放到空气中,这使得下降的趋势变得缓慢[21]。
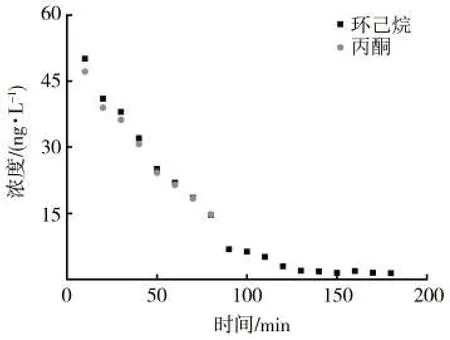
图5 不同配标溶剂建立的方法下室内ETS中3-EP浓度随时间的变化趋势Fig.5 Variation of 3-EP concentration in indoor ETS sample with time detected by methods with different solvents
显然两种配标溶剂建立的方法下,测试结果存在一定差异,但均能反映3-EP 的变化趋势。在3-EP下降到一定程度后,以丙酮为配标溶剂建立的方法不能实现有效的定量分析,缩短了检测ETS 动态变化的时间范围,这可能会限制其在ETS 风险评估中的实际应用。
3 结论
以环境烟气标志物3-EP 为目标物,研究了DRAPCI 源内的溶剂效应,结果表明:①甲醇会在DRAPCI 源内形成二聚体,并通过质子竞争的方式抑制3-EP 的电离;②乙腈会和3-EP 形成中性分子簇,掩盖3-EP 的质子化位点,从而抑制3-EP 的电离;③环己烷因为其质子亲和势低和不易形成多聚体的特点,不会影响3-EP的电离。这些研究结果表明采用常压质谱法进行定量分析,必须对配标溶剂优化。分析数据显示,在采用DRAPCI-MS 进行ETS中3-EP的分析时,最佳的配标溶剂是环己烷。

