重症胰腺炎患者发生肠内营养不耐受现状及影响因素分析
金 艳,金燕平,王毓薇,叶国良,顾君娣
宁波大学医学院附属医院,浙江宁波 315020
重症胰腺炎具有发病急骤、进展迅速、病情复杂且凶险等特点,若不及时接受正确有效的治疗患者容易因组织坏死、脏器功能障碍而死亡,病死率高达22%~36%[1-2]。重症胰腺炎病变过程中患者易出现高分解代谢,分解大量蛋白质和脂肪,增加糖异生活动,导致机体出现严重的营养不良[3-4]。早期进行肠内营养支持可维护重症胰腺炎患者肠黏膜的屏障功能,刺激肠道收缩功能,释放免疫调节因子,增强机体免疫功能,有利于降低病死率和并发症发生率[5]。部分患者在治疗期间容易出现胃潴留、肠内营养摄入量不足、肠梗阻、腹泻、腹胀等肠道不耐受现象,影响空肠营养支持效果,甚至被迫暂停或终止营养支持,对营养摄入和预后恢复造成严重影响。本研究旨在了解重症胰腺炎患者发生肠内营养不耐受现状及并分析其影响因素,为临床防治肠内营养不耐受提供参考。
1 对象与方法
1.1 研究对象
选取2018年1月至2020年3月宁波大学医学院附属医院收治的124例重症胰腺炎患者。纳入标准:符合重症胰腺炎诊断标准[6];年龄>18岁;经三腔鼻空肠管行肠内营养;认知功能正常;临床资料完整。排除标准:既往有慢性脏器功能障碍;创伤性、爆发性、免疫性、妊娠性重症胰腺炎;精神功能障碍、意识不清;免疫系统异常;无法行空肠营养支持治疗者;血液系统疾病;胰腺癌;放弃治疗或自行出院者。
1.2 研究方法
患者出院时以调查问卷的方式收集其年龄、性别、入院第1天急性生理和慢性健康状况评分(acute physiology and chronic health evaluation Ⅱ,APACHEⅡ)等临床资料,分析重症胰腺炎患者发生肠内营养不耐受的影响因素。肠内营养不耐受指喂养过程中出现返流或呕吐,或在喂养6 h后胃残余量>250 mL且喂养速度<40 mL/h[7]。APACHEⅡ评分是由急性生理参数评分(acute physiology score,APS)、年龄和慢性健康状况评分组成[8],总分为71分,分数越高则患者病情越严重。
1.3 统计学方法
应用SPSS 21.0软件分析数据。本研究数据为计数资料,以例(%)表示,采用x2检验,多因素使用Logistic回归分析,P<0.05为差异有统计学意义。
2 结果
2.1 重症胰腺炎患者发生肠内营养不耐受现状及单因素分析
124例患者中肠内营养不耐受73例(58.87%),肠内营养耐受51例(41.13%)。单因素分析结果显示APACHEⅡ评分、添加膳食纤维、腹内压、机械通气、使用镇静药、腹腔穿刺、血钾浓度、使用血管活性药、血糖、肠内营养制剂日用量、使用抗生素种类、血清白蛋白水平为重症胰腺炎患者发生肠内营养不耐受的影响因素,差异有统计学意义(P<0.05),见表1。

表1 重症胰腺炎患者发生肠内营养不耐受的单因素分析 例(%)
2.2 重症胰腺炎患者发生肠内营养不耐受多因素分析
以肠内营养不耐受为因变量,单因素分析中有统计学意义(P<0.05)的变量为自变量进行的因素Logistic回归分析。多因素Logistic回归分析赋值情况见表2。结果显示APACHEⅡ评分≥20分、未添加膳食纤维、血糖≥11 mmol/L、肠内营养制剂日用量≥700 mL、使用抗生素≥2种、血清白蛋白水平<35 g/L、腹内压≥15 mmHg是重症胰腺炎患者发生肠内营养不耐受的独立危险因素(P<0.05且OR>1)。见表3。

表2 重症胰腺炎患者发生肠内营养不耐受的相关因素自变量赋值情况
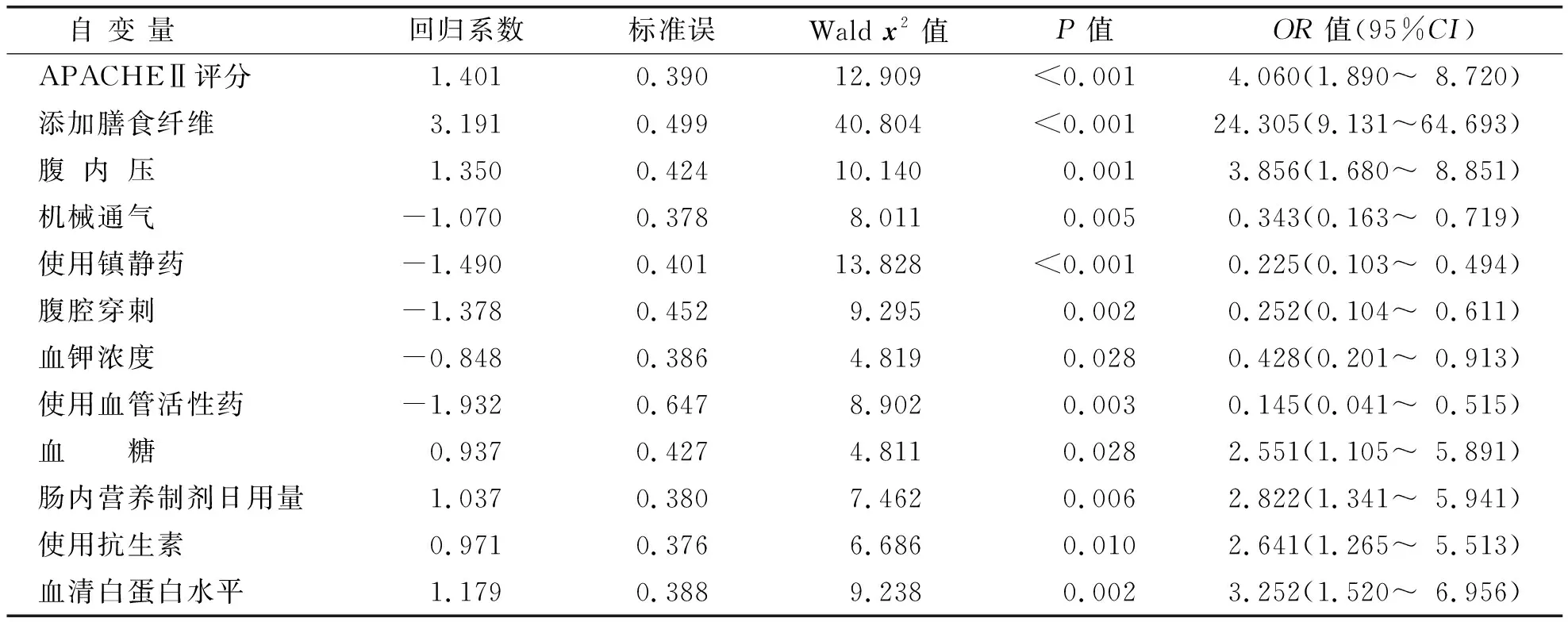
表3 重症胰腺炎患者发生肠内营养不耐受的多因素Logistic分析
3 讨论
3.1 重症胰腺炎患者发生肠内营养不耐受现状
重症胰腺炎患者机体长期处于高分解代谢状态,易并发严重的营养不良[9-10]。临床多采用空肠营养支持,但因患者合并较重的全身炎症反应,破坏肠道正常吸收功能,易出现肠内营养不耐受现象,不利于病情恢复[11-12]。本研究中,124例重症胰腺炎患者中出现肠内营养不耐受73例(58.87%),提示重症胰腺炎患者肠内营养不耐受发生率较高。
3.2 重症胰腺炎患者发生肠内营养不耐受的影响因素
3.2.1APACHEⅡ评分
本研究结果显示,APACHEⅡ评分≥20分是重症胰腺炎患者发生肠内营养不耐受的危险因素。APACHEⅡ评分是评估危重患者疾病严重程度相对权威的评价系统。APACHEⅡ评分越高表示患者病情越严重,机体处于严重应激状态,会对胃肠运动造成影响,影响胃肠道屏障功能。同时当患者处于严重应激状态时,胃肠道血流减少,释放大量白三烯等炎性介质,加重微血管收缩,诱发炎性介质释放的级联反应,引起全身炎性反应、消化液分泌等,导致肠道菌群位置改变,胃肠道的生物屏障遭到破坏。当重症胰腺炎患者接受空肠营养支持时易出现肠道营养不耐受现象。临床在对重症胰腺炎患者行空肠营养支持前需全面评估患者病情严重程度,高度重视APACHEⅡ评分≥20分患者,待病情稳定后再行营养支持,且肠内营养期间需做好体位护理,对于无禁忌要求者须抬高头部,防止返流。
3.2.2膳食纤维
本研究结果显示,未添加膳食纤维是重症胰腺炎患者发生肠内营养不耐受的独立危险因素。膳食纤维发酵能够产生短链脂肪酸,刺激结肠分泌5-羟色胺等神经递质和激素,促进肠道收缩、蠕动,利于肠动力障碍改善,还能保护肠黏膜屏障、调节肠道菌群,间接改善肠动力障碍,同时对肠道动力存在双向调节作用,能够改善腹泻、便秘等症状[13]。故添加膳食纤维能够避免患者发生肠内营养不耐受,可在肠内营养中适当添加膳食纤维,以保护胃肠黏膜、调节肠道内菌群平衡,预防肠内营养不耐受发生。
3.2.3腹内压
本研究结果显示,腹内压是重症胰腺炎患者发生肠内营养不耐受的独立危险因素。腹内压增高会压迫肠管和肠壁的血管,造成毛细血管和肠系膜静脉瘀血,肠壁缺血,导致患者发生胃肠道黏膜出血、溃烂,肠腔内细菌过度繁殖,提高炎性介质水平,破坏肠黏膜屏障,严重时可诱发腹腔间室综合征,导致胃肠功能衰竭,增加患者肠内营养不耐受发生风险[14]。将腹内压作为重症胰腺炎患者的常规监测项目,但因监测准确性容易受诸多因素影响,如膀胱内注水量、机械通气患者呼气末正压、人为误差等,需规范化培训腹内压监测,确保腹内压监测的及时性和准确性,一旦腹内压高于15 mmHg,需立即报告医生,尽早实施干预,以避免肠内营养不耐受发生。
3.2.4血糖
本研究结果显示,血糖≥11 mmol/L是重症胰腺炎患者发生肠内营养不耐受的独立危险因素。长期处于高血糖状态,多存在胃动力紊乱,尤其是胃窦部、胃体部和胃底部动力,增强幽门活动,可诱导十二直肠舒缩不协调、胃排空阻力上升、延迟胃排空,加重胃瘫,并会造成位于视丘下部腹内侧核的某些特殊细胞兴奋,降低胃肠收缩能力,削弱肠道功能,甚至引起衰竭,易发生肠内营养不耐受[15]。严格遵医嘱监测血糖,当发现血糖水平异常时及时报告医生,实施相应的治疗措施处理,确保血糖相对稳定,并按照血糖的波动情况,及时调整胰岛素使用量,防止血糖水平在短时间内快速降低,避免患者发生低血糖反应。
3.2.5肠内营养制剂日用量
本研究中肠内营养制剂日用量≥700 mL是重症胰腺炎患者发生肠内营养不耐受的独立危险因素。短时间内大量输入肠内营养液,可刺激胃肠道快速蠕动,缩短营养液在肠道内停留时间,胆盐无法再吸收,造成营养液消化吸收不彻底,增加患者肠内营养不耐受发生风险。另外,重症胰腺炎患者长期卧床不能活动且消化功能下降,大量摄入营养液会造成患者胃潴留加重,也可能会诱发肠内营养不耐受。肠内营养治疗时需遵循浓度由低到高、剂量由少到多的原则,切勿在短时间内大量输入营养制剂,并密切关注患者胃排空状态,同时可从少量的非营养物质开始,如少量的0.9%氯化钠、温水等,使肠道慢慢适应营养物质的流入,避免肠内营养不耐受现象发生。
3.2.6使用抗生素
本研究中使用抗生素≥2种是重症胰腺炎患者发生肠内营养不耐受的独立危险因素。使用抗生素会破坏肠道正常菌群,降低肠道细菌浓度,导致致病菌过度增殖或生长,减少膳食纤维转化成短链脂肪酸,而短链脂肪酸的减少会促使结肠上皮细胞凋亡,导致患者发生肠内营养吸收不良而诱发肠内营养不耐受[16]。谨慎使用抗生素,使用前需采集标本实施病原菌检测和药敏试验,提高抗生素治疗效果,并全面了解抗生素在血液中的半衰期和有效浓度、使用时机和药物配伍禁忌,当患者出现肠内营养不耐受症状时,及时配合医生处理。
3.2.7血清白蛋白水平
本研究中血清白蛋白水平<35 g/L是重症胰腺炎患者发生肠内营养不耐受的独立危险因素。重症胰腺炎患者治疗时多需实施液体复苏,输入大量液体会诱发稀释性低蛋白血症,当患者全身毛细血管通透性增加时,白蛋白会渗透至组织间隙而引起低蛋白血症,导致患者发生生化障碍和酸中毒,上述情况均会引起胃肠水肿,甚至胃瘫,易发生肠内营养不耐受[17]。当白蛋白水平急剧降低时,会增加机体分解代谢和肾上腺皮质所分泌的糖皮质激素,增加机体组织蛋白水解,抑制蛋白质的合成,加重胃肠道黏膜水肿,逐渐降低胶体渗透压,降低胃肠动力,可引起细菌移位增殖。上述情况均会延长患者胃排空时间,增加肠内营养不耐受发生风险。

