改良碳青霉烯灭活试验和碳青霉烯酶抑制剂增强试验鉴定肠杆菌目细菌产碳青霉烯酶型别的临床价值
王 芳, 邓燕燕, 林见敏, 王金金, 龚 倩, 黄声雷
(1.复旦大学附属中山医院青浦分院检验科,上海 201700;2.复旦大学附属中山医院检验科,上海 200032)
碳青霉烯类药物因其良好的细胞通透性和高度的酶稳定性,一度被认为是抗多重耐药肠杆菌目细菌的最后“一道防线”[1]。但是随着该类抗菌药物在临床的过度使用,碳青霉烯耐药肠杆菌目细菌(carbapenem resistantEnterobacteriaceae,CRE)在全球范围内广泛流行。全国细菌耐药监测网历年监测数据显示,2014—2019年,我国临床分离的肺炎克雷伯菌对亚胺培南的耐药率从4.8%上升至10.5%,对美罗培南的耐药率从4.5%上升至10.9%;上海市碳青霉烯类耐药肺炎克雷伯菌的临床分离率从18.9%快速攀升至28.7%[2]。肠杆菌目细菌对碳青霉烯类药物最主要的耐药机制是产生碳青霉烯酶。按照Ambler分子分类方法,碳青霉烯酶可分为丝氨酸酶(A类,以blaKPC为主)、金属β-内酰胺酶(B类,以blaNDM为主)和丝氨酸碳青霉烯酶(D类,以blaOXA-48为主)三大类。不同类型碳青霉烯酶的分布具有地区、人群和细菌种类的差异性,我国临床分离的肺炎克雷伯菌和大肠埃希菌产生的碳青霉烯酶分别以KPC和NDM型为主,少数菌株产OXA-48、IMP和VIM型碳青霉烯酶[4]。《肠杆菌目细菌碳青霉烯酶的实验室检测和临床报告规范专家共识》[5]推荐改良碳青霉烯灭活试验(modified carbapenem inactivation method,mCIM)/乙二胺四乙酸碳青霉烯灭活试验(ethylene diamine tetraacetic acidcarbapenem inactivation method,eCIM)和碳青霉烯酶抑制剂增强试验为临床微生物实验选择性常规开展的检测方法。本研究拟评估mCIM/eCIM和碳青霉烯酶抑制剂增强试验鉴定肠杆菌目细菌碳青霉烯酶型别的临床价值。
1 材料与方法
1.1 菌株来源
收集2019年1月—2020年1月复旦大学附属中山医院青浦分院分离自住院患者临床样本的肠杆菌目细菌130株,其中CRE100株(肺炎克雷伯菌72株、大肠埃希菌18株、阴沟肠杆菌8株、黏质沙雷菌2株);碳青霉烯类敏感肠杆菌目细菌30株,包括肺炎克雷伯菌15株、大肠埃希菌12株、黏质沙雷菌3株。
1.2 试剂和仪器
VITEK 2-Compact全自动微生物鉴定药敏仪(法国生物梅里埃公司)。M-H琼脂平板、哥伦比亚血平板(上海科玛嘉公司),亚胺培南和美罗培南纸片(美国赛默飞世尔公司),黏菌素和替加环素微量肉汤稀释板条(温州康泰公司),乙二胺四乙酸二钠和碳青霉烯酶抑制增强试剂(上海原科公司)。
1.3 方法
1.3.1 细菌鉴定和体外药物敏感性试验 采用VITEK 2-Compact全自动微生物鉴定药敏仪对临床分离株进行菌种鉴定和体外药物敏感性试验,参照美国临床实验室标准化协会M100-S28文件[6]标准判读药物敏感性试验结果,头孢哌酮-舒巴坦参照头孢哌酮的标准。黏菌素和替加环素的药物敏感性结果依据文献[7]的要求进行判断。质控菌株为大肠埃希菌(ATCC 25922)、(ATCC 35218)和铜绿假单胞菌(ATCC 27853)。
1.3.2 mCIM/eCIM 按照美国临床实验室标准化协会M100-S28文件[6]要求进行mCIM/eCIM和结果判读。质控菌株为肺炎克雷伯菌(ATCC BAA-1705)、(ATCC BAA-1706)和(ATCC BAA-2146)。
1.3.3 碳青霉烯酶抑制剂增强试验 将待测菌调制成0.5麦氏浊度菌悬液,均匀涂布于M-H琼脂平板,分别将4张10 μg/片的亚胺培南纸片(分别标记为A、B、C、D)贴于琼脂上,纸片之间距离>5 mm。B纸片上加初始浓度为0.1 mol/L的乙二胺四乙酸(ethylene diamine tetraacetic acid,EDTA)溶液10 μL,C纸片上加初始浓度为30 mg/L的3-氨基苯基硼酸(3-Aminophenylboric acid,APB)10 μL,D纸片上加EDTA和APB各10 μL。过夜孵育后量取抑菌圈直径,如B纸片比A纸片的抑菌圈≥5 mm,即可判断该受试菌产B类碳青霉烯酶;如C纸片比A纸片的抑菌圈≥5 mm,可判断该受试菌产A类碳青霉烯酶;如仅D纸片比A纸片的抑菌圈≥5 mm,可判断该受试菌同时产A类和B类碳青霉烯酶;如B、C和D纸片均比A纸片的抑菌圈<5 mm,则判断受试菌不产A类和B类碳青霉烯酶。质控菌株为肺炎克雷伯菌( ATCC BAA-1705)、(ATCC BAA-1706)和(ATCC BAA-2146)。
1.3.4 耐药基因检测 采用聚合酶链反应(polymerase chain reaction,PCR)检测KPC、NDM、OXA-48耐药基因,通过测序对阳性扩增产物进行确认。 根据参考文献[8]选取blaKPC、blaNDM和blaOXA-48的引物、PCR反应体系和条件,引物由生工生物工程(上海)技术有限公司合成并测序。
1.4 统计学方法
采用SPSS 18.0软件进行统计分析。以PCR结果为标准,比较2种方法鉴定不同碳青霉烯酶的效能。采用Kappa检验评价2种方法与PCR方法的一致性,Kappa值<0.4表示一致性较差;0.4<Kappa值≤0.8表示一致性较好;Kappa值>0.8表示一致性极好。
2 结果
2.1 体外药物敏感性试验结果
CRE对黏菌素、替加环素、头孢他啶-阿维巴坦、阿米卡星和磺胺甲噁唑-甲氧苄啶的耐药率较低,分别为0%、2.3%、13.0%、50.4%、55.7%,对其他常用抗菌药物的耐药率均>75%。
2.2 碳青霉烯类的耐药基因分布
100株CRE中,检出71株产KPC-2,23株产NDM-1,4株产NDM-5,1株产KPC-3,1株同时产KPC-2和NDM-1。72株肺炎克雷伯菌中,有70株仅产KPC-2。18株大肠埃希菌中,有13株产NDM-1,其中4株同时产KPC-2和NDM-1。见表1。
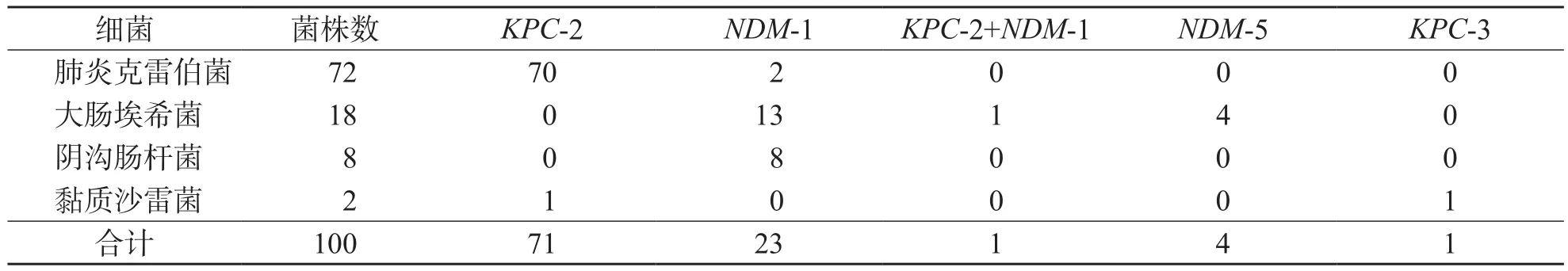
表1 100株CRE耐药基因分布 株
2.3 碳青霉烯酶抑制剂增强试验结果
以PCR结果为标准,对于72株产A类丝氨酸酶的菌株,碳青霉烯酶抑制剂增强试验可准确鉴定71株,敏感性为98.60%(71/72),特异性为100%;与PCR比较,Kappa值为0.984。对于27株产B类金属酶菌株和1株同时产A类丝氨酸酶和B类金属酶的菌株,碳青霉烯酶抑制剂增强试验可全部准确鉴定;与PCR比较,Kappa值分别为1.000和0.560。见表2、表3。
2.4 mCIM和eCIM结果
以PCR结果为标准,对于72株产A类碳青霉烯酶的菌株,mCIM/eCIM可准确鉴定70株,其敏感性为97.22%,特异性为100%;与PCR比较,Kappa值为0.969。对于27株产B类金属酶菌株,mCIM和eCIM可准确鉴定26株,敏感性为96.30%,特异性为100%;与PCR比较,Kappa值为0.976。但mCIM和eCIM无法鉴定同时产A类和B类碳青霉烯酶的菌株。见表2、表3。
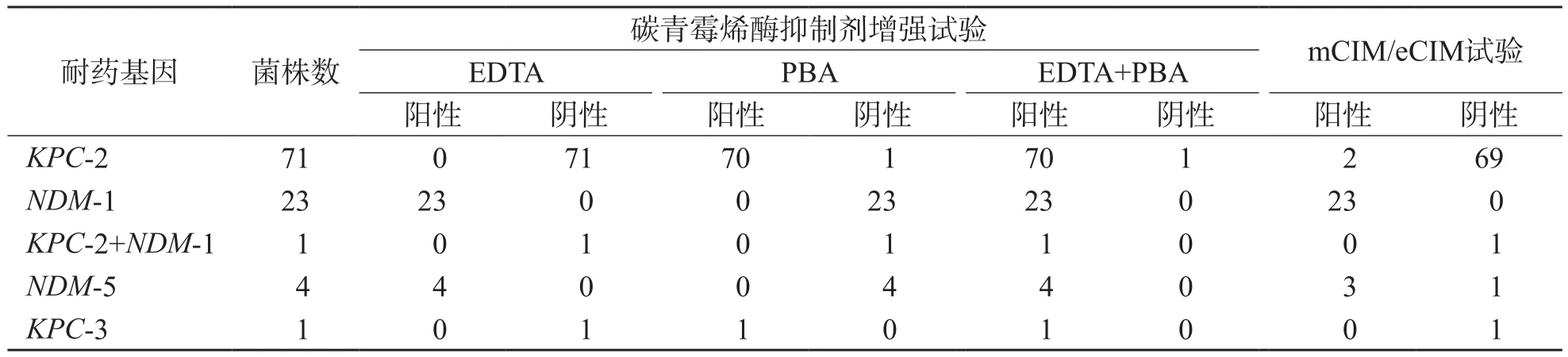
表2 碳青霉烯酶抑制剂增强试验与mCIM/eCIM结果比较 株

表3 2种方法检测效能
3 讨论
因为不同的抗菌药物在体外对产不同类型碳青霉烯酶细菌的抗菌活性有差别,如头孢他啶-阿维巴坦对产KPC和OXA-48型丝氨酸碳青霉烯酶菌株具有高度抗菌活性,但对产金属β-内酰胺酶菌株无抗菌活性[9];美罗培南-韦博巴坦和亚胺培南-雷利巴坦对产KPC型碳青霉烯酶菌株具有高度抗菌活性,但对金属β-内酰胺酶和OXA-48型丝氨酸碳青霉烯酶菌株无抗菌活性[9-11]。因此,准确而快速地鉴定CRE碳青霉烯酶的型别,对于临床合理选择抗菌药物治疗多重耐药菌的感染,降低患者死亡率,控制医院内感染和传播流行具有重要的意义[8]。
由于细菌耐药性具有遗传复杂性,目前国际上检测碳青霉烯酶的方法仍以表型方法检测为主,而分子生物学方法通常作为筛选工具或作为传统方法的补充[9]。微生物实验室用于检测碳青霉烯酶的常用表型方法有Carba NP试验、mCIM/eCIM、碳青霉烯酶抑制剂增强试验、激光解吸电离飞行时间质谱等。其中Carba NP试验结果判断主观性较强,对操作人员要求较高,且试剂需自配,有效期短[12];质谱技术需要昂贵的质谱仪,且目前缺乏统一可行的操作方法[13]。eCIM与/mCIM联合使用可以区分产金属酶和丝氨酸碳青霉烯酶的肠杆菌目细菌,成本低,操作简单,结果易于解释,适合大多数基层临床实验室开展。mCIM/eCIM联合检测丝氨酸碳青霉烯酶和金属β-内酰胺酶的敏感性>95%、特异性>92%[9]。本研究结果显示,mCIM/eCIM检测产丝氨酸碳青霉烯酶的敏感性为97.22%,特异性为100%;检测金属β-内酰胺酶的敏感性为96.30%、特异性为100%,且与PCR结果的一致性较好,但eCIM的局限性是不能区分同时含有丝氨酸碳青霉烯酶和金属β-内酰胺酶的菌株。
有学者利用APB能抑制KPC型碳青霉烯酶的原理,建立了类似美国临床实验室标准化协会定义的使用纸片扩散法筛选产超广谱β-内酰胺酶的方法,用于检测产KPC型碳青霉烯酶的肠杆菌目细菌[14]。TSAKRIS等[15]在DOI等的研究结果基础上增加金属β-内酰胺酶的抑制剂EDTA,用于检测金属β-内酰胺酶,这种双碳青霉烯酶抑制增强试验,不仅能区分金属β-内酰胺酶或KPC型碳青霉烯酶,还能检测同时产生2种碳青霉烯酶菌株,检测单产KPC或金属酶的敏感性均为100%,特异性分别为98.8%和100%。本研究结果显示,碳青霉烯酶抑制剂增强试验检测单产KPC或金属酶的敏感性分别为98.60%和100%,特异性均为100%,且和与PCR的一致性较好意,与DOI等[14]和TSAKRIS等[15]的研究结果一致。
2种方法各有局限:mCIM/eCIM检测方法操作需要经过4 h的孵育时间,操作步骤较碳青霉烯酶抑制剂增强试验繁琐,且该检测方法不能区分同时产丝氨酸碳青霉烯酶和金属β-内酰胺酶的菌株。碳青霉烯酶抑制剂增强试验需要实验室添置额外的试剂(如APB),成本较mCIM/eCIM高。
综上所述,随着CRE对抗菌药物耐药形势日趋严峻,加强临床微生物检测能力,快速检出耐药菌株,是防控CRE的关键[16]。mCIM/eCIM和碳青霉烯酶抑制剂增强试验检测丝氨酸碳青霉烯酶和金属β-内酰胺酶敏感性和特异性均超过95%,且成本较低,不同级别,尤其是基层医疗机构临床微生物实验室可以根据自身需求来选择适合本实验室的方法进行常规的CRE表型分型检测。

