可用于表征可电离化合物离子化影响的描述符研究进展
杨先海,刘会会,王连军
南京理工大学环境与生物工程学院,江苏省化工污染控制与资源化高校重点实验室,南京 210094
可电离有机化合物(ionizable organic chemicals, IOCs)是指分子结构中包含解离基团(如羟基(—OH)、羧基(—COOH)、磺酸基(—SO3H)和氨基(—NH2)等)的有机酸碱、有机两性离子和有机盐等。在人为有意生产的化学品或无意识产生的化学品中,IOCs均占有较大比例。据估计,在欧盟《化学品的注册、评估、授权和限制法规》(REACH法规)中登记注册的14多万种化学品中,约半数属于IOCs[1-3];在目前使用的药物中,约80%属于IOCs[4],而85%~95%的原料药也属于IOCs[5]。在水消毒副产物等无意识产生的化学品中,也存在大量的取代有机羧酸类、取代酚类等IOCs[6]。由于IOCs在生产、生活中的大量使用,以及在水消毒等过程中无意识的产生,导致其会通过多种途径进入各环境介质。人群、环境生物也会通过经皮、经口和呼吸等多种途径暴露于IOCs,进而引发潜在的健康和/或生态危害效应。因此,有必要从人工化学品或无意识产生的化学品中筛选识别具有潜在健康和/或生态危害效应的IOCs,并对其采取适当的管控措施,以期保护人群健康和生态安全[7]。
与不可电离化合物相比,IOCs的重要特点是在环境水体、生理或实验不同pH条件下,会解离,从而以不同比例的分子和离子形态共存。分子和离子形态存在比例取决于其本身的酸碱解离常数(pKa)和环境/生理/试验pH条件(图1)。式(1)显示了一元酸碱解离程度的计算方程[8]:
(1)
δ分子和δ离子分别是分子态和离子态的比例分数;Iab是酸和碱指示系数,酸和碱的Iab分别取1和-1。对IOCs而言,存在如下2个问题需要回答:一是其共存的分子和离子形态是否具有不同的物理化学、环境归趋和行为、生态和健康毒性效应?二是哪个形态对化合物的表观属性和效应贡献更大?
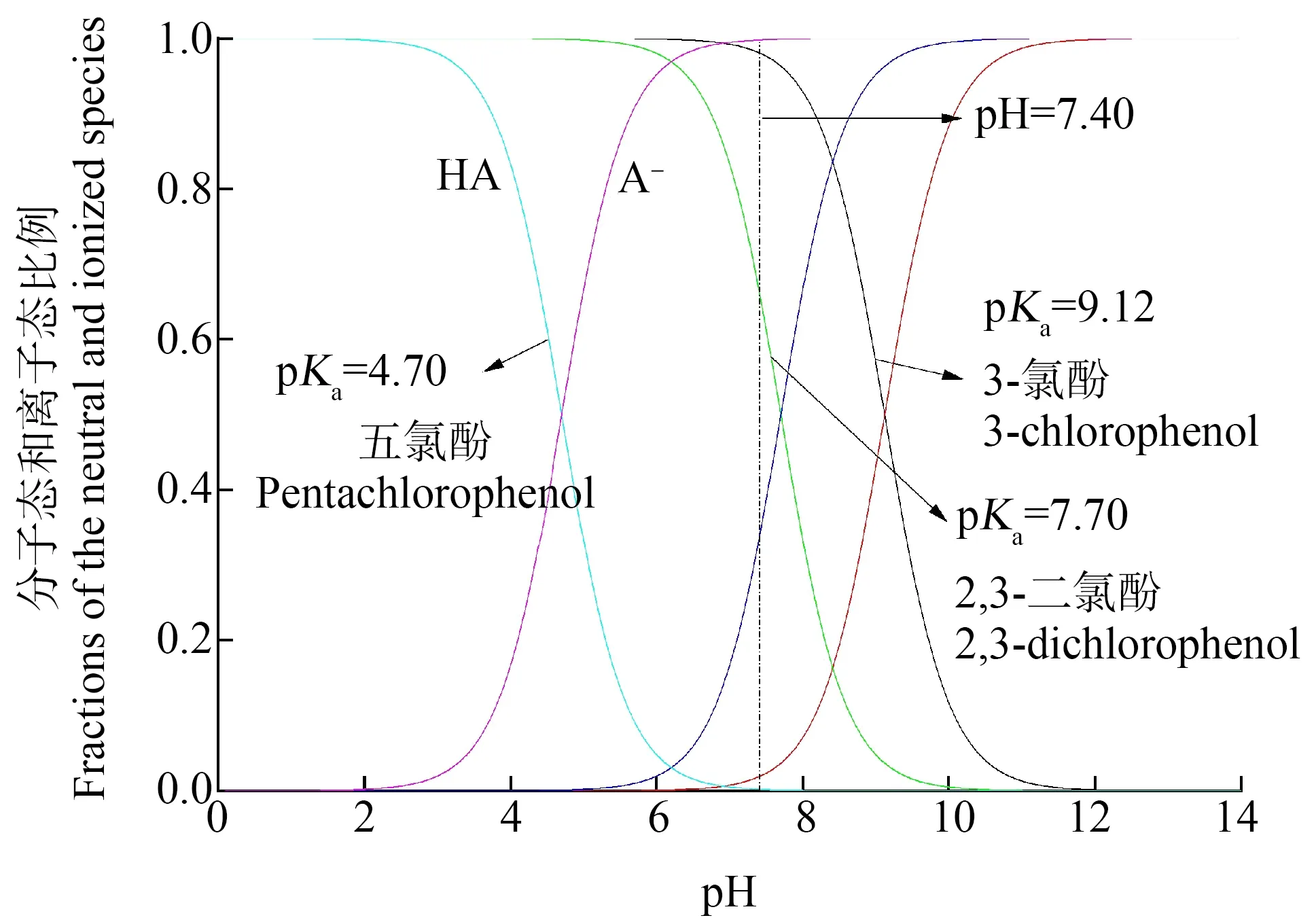
图1 五氯酚、2,3-二氯酚和3-氯酚形态分布曲线注:HA和A-分别代表分子态和离子态;化合物pKa实验数据 来源于EPI Suit 4.1TM的PhysProp数据库[9]。Fig. 1 Species distribution of pentachlorophenol, 2,3-dichlorophenol and 3-chlorophenolNote: HA and A- are the neutral and anionic forms, respectively; the pKa values of those compounds were obtained from PhysProp Database in EPI Suit 4.1TM[9].
过去数十年的研究表明,IOCs的不同形态确实表现不同的物理化学、环境归趋和行为、生态和健康毒性效应[10-14]。受到离子化影响的参数包括但不仅限于分配参数(包括有机碳-水分配系数[15-16]、牛血清白蛋白-水分配系数[17-18]、肌肉蛋白-水分配系数[19-20]、脂质体-水分配系数[3,21-23])、光解速率常数[24-25]、羟基自由基速率常数[26]、沸石的吸附能力[27]、生物富集[28]、鱼、大型溞、绿藻和梨形四膜虫等水生生物的急性毒性[29-32]、蛋白相互作用[33-34]等。相关研究已证实,部分IOCs的表观属性或毒性效应值,受其分子态对应的属性或毒性效应值控制,如生物富集、水生生物毒性效应等参数[32,35-37];而有的则取决于其离子态对应的属性或毒性效应值。我们前期的研究表明,在IOCs与人运甲状腺素蛋白(hTTR)相互作用的过程中,阴离子形态的酚类化合物、全氟/多氟类化合物与hTTR的亲和力强于对应的分子态[34,38]。Goss等[39]的研究也表明,有机酸的生物分配系数主要受阴离子控制。因此,现有的研究结果,一方面表明IOCs的表观物理化学、环境归趋和行为、生态和健康毒性效应参数确实受其离子化的影响,这意味着在开展IOCs相关的实验或理论研究时,不应忽视离子化的影响[40];二是部分IOCs的表观属性或毒性效应参数值虽然取决于分子或离子态的相应参数值,但不可否认的是仅考虑分子态或离子态贡献时,往往会导致低估其属性或毒性效应参数值[41],这说明在进行IOCs相关的研究中,应同时考虑其分子态和离子态的贡献[42]。
目前,无论是人为有意生产的化学品,亦或无意识产生的化学品,大部分仍缺乏基本的物理化学、环境归趋和行为、生态和健康毒性效应参数数据[43-45]。而由于实验方法面临成本高、耗时长等问题,很难对所有化学品一一进行实验测试。为了应对和解决该问题,欧美等国家及经济合作与发展组织(OECD)等国际组织都积极倡导使用预测技术来进行化学品优先级设定、填补数据缺失等[46-50],如(定量)结构活性/属性关系((Q)SA/PR)模型。在过去几十年里,科学家构建了许多能够预测化学品物理化学、环境归趋和行为、生态和健康毒性效应参数的定量、定性预测模型/软件/工具或专家系统。但是研究发现,绝大部分预测模型/软件/工具或专家系统并不适用于IOCs[43,51-53]。一方面的原因是这些预测工具或专家系统的模型应用域不含有IOCs[54-55];二是现有预测模型选用的描述符未考虑离子化的影响,而仅是基于IOCs分子态的描述符而构建的。而且仅采用IOCs分子态的描述符,有时很难构建可接受的模型。例如,Endo课题组在研究IOCs与牛血清蛋白之间的分配系数(KBSA/W)时,就发现常规描述符不能构建具有较好预测能力的IOCsKBSA/W模型[18]。因此,为了构建能够涵盖IOCs的预测模型,需要从两方面着手,一是在选择建模化学品时,需涵盖IOCs;二是选用能够表征离子化影响的描述符进行建模。
考虑到描述符是预测模型构建的核心要素之一[43,50],选用合适的描述符来表征离子化的影响,对于构建能预测IOCs物理化学、环境归趋和行为、生态和健康毒性效应参数的模型具有重要意义。基于此,本文总结了可用于表征可电离化合物离子化影响的描述符,即酸碱解离常数及其衍生参数、考虑离子化影响的分配系数、考虑离子参数的多参数线性自由能关系、基于形态修正的量化参数,对其主要特点进行了分析,并提出了研究展望。
1 酸碱解离常数及其衍生参数(Acid dissociation constant and derived parameters)
根据Henderson-Hasselbalch方程(式2),给定化合物的pKa值取决于其在平衡条件下分子态和离子态的浓度[56-57]。在某一特定pH条件下,具有较小pKa值的化合物,在平衡溶液中存在更大比例的离子态浓度(式3)。
(2)
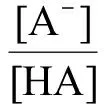
(3)
式中:[HA]、[A-]和[H+]分别是酸性物质平衡条件下对应的分子态、阴离子和氢离子浓度。

-logIGC50=-0.772+0.627logKOW
(4)
-logIGC50=-0.120+0.614logKOW-0.077pKa
(5)
-logIGC50是梨形四膜虫急性毒性效应值;logKOW是正辛醇-水分配系数;n训练集是训练集化合物数量;s是标准误差。
使用该方法表征离子化影响时,前提是能获取准确的pKa值。然而,部分化合物却很难准确测定其pKa值。例如,全氟辛酸的实验pKa值介于1.0~3.8[68],其他全氟/多氟化合物的pKa值也存在类似问题[69]。对于无法获取准确pKa值的IOCs,该如何处理呢?在这种情况下,可采用分子态(δ分子)和离子态(δ离子)的比例分数作为预测变量,而替代pKa值。根据式(1),化合物δ分子和δ离子的值取决于环境/生理/实验pH值和其pKa。在一定程度上,使用δ分子和δ离子可减少因pKa变化带来的偏差。比如,在生理pH=7.40的条件下,pKa值介于1.0~3.8的全氟辛酸δ离子值取值均为1。目前,已有很多模型采用δ分子和δ离子作为预测变量。例如,梨形四膜虫、发光菌、大型溞和鲤鱼急性毒性[32,70-72]、土壤-水分配系数[73]、溶解有机质-水分配系数[74]等参数预测模型。例如,Qin等[70]采用δ分子作用预测变量构建了能预测中性分子、IOCs对发光菌(V.fischeri) (式6)、大型溞(D.magna)(式7)和鲤鱼(式8)急性毒性的预测模型:
-logEC50(发光菌)=1.04+0.701logKOW+1.11S+1.12INO2-0.157logδ分子
(6)
-logEC50(大型溞)=1.73+0.628logKOW+0.772S+0.899INO2+0.542logδ分子
(7)
-logEC50(鲤鱼)=1.52+0.581logKOW+0.767S+1.33INO2+0.461logδ分子
(8)
-logEC50(发光菌)、-logEC50(大型溞)和-logEC50(鲤鱼)分别是发光菌、大型溞和鲤鱼急性毒性效应值;S是化合物极化性参数;INO2是分子中硝基个数。在构建全氟和多氟化合物的hTTR干扰效应预测模型时,我们选取了δ离子值作为预测变量(式9)[38]:
(9)
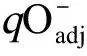
pKa实验值可从文献或数据库查询,如eChemPortal (https://www.echemportal.org/echemportal/),Drugbank (https://www.drugbank.ca/),ChemIDplus (https://chem.nlm.nih.gov/chemidplus/),Physprop (http://esc.syrres.com/fatepointer/search.asp),OECD QSAR toolbox (https://qsartoolbox.org/)等。若无实验pKa值,可采用ChemAxon (http://www.chemaxon.com),Virtual Computational Chemistry Laboratory (http://www.vcclab.org/lab),SPARC (http://www.archemcalc.com/sparc.html),SciFinder (https://scifinder.cas.org)等软件预测。
2 考虑离子态贡献的分配系数(Distribution coefficient with ionization correction)
logKOW可表征不可电离化合物或IOCs的分子态从水相分配到有机相的能力,因而从20世纪60年代开始[75],logKOW就被用来预测各种涉及分配的环境归趋和行为、生态和健康毒性效应参数[76]。例如,EPI Suit 4.1TM的ECOSARTM模块主要通过logKOW来预测化合物鱼、大型溞和绿藻急慢性毒性效应数据。但是,在涉及IOCs的场合,logKOW的预测能力可能变差。例如,图2(a)显示了在pH=6.0、7.8和9.0条件下,logKOW与IOCs对大型溞24 h急性毒性数据(-logEC50)之间的关系。由该图可知,logKOW与-logEC50之间不存在显著线性相关性(pH=7.8和9.0)或仅存在较弱的相关性(pH=6.0)。如何提高二者之间的相关性呢?一般认为,考虑离子态贡献的正辛醇-水分布系数(logDOW(pH))比logKOW更适合IOCs[77-78]。如图2(b)所示,在pH=6.0、7.8和9.0条件下,logDOW(pH)与-logEC50的Pearson线性相关系数分别从与logKOW的0.350 (P<0.01)、0.250 (P>0.05)和0.174 (P>0.05)提高到0.678 (P<0.0001)、0.798 (P<0.0001)和0.845 (P<0.0001)。这进一步说明了考虑离子化的重要性。
logDOW(pH)可以通过式(10)或(11)计算:
logDOW(pH)=logKOW-log(1+10pH-pKa)
(10)
(11)
式中:i指分子或离子态;[species]i,octanol和[species]i,water分别指第i种形态在正辛醇和水中的浓度。目前,logDOW(pH)已被广泛用于预测可电离环境污染物的相关属性或毒性效应[32,79-82]或可电离药物分子相关参数[12,78,83]。例如,Ou等[80]基于logDOW(pH)构建了预测IOCs鱼类肌肉蛋白-水分配系数(logKMP/w)的预测模型(式12):
logKMP/w=-0.715+0.743logDOW(pH=7.0)+0.0604nCar
(12)
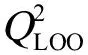
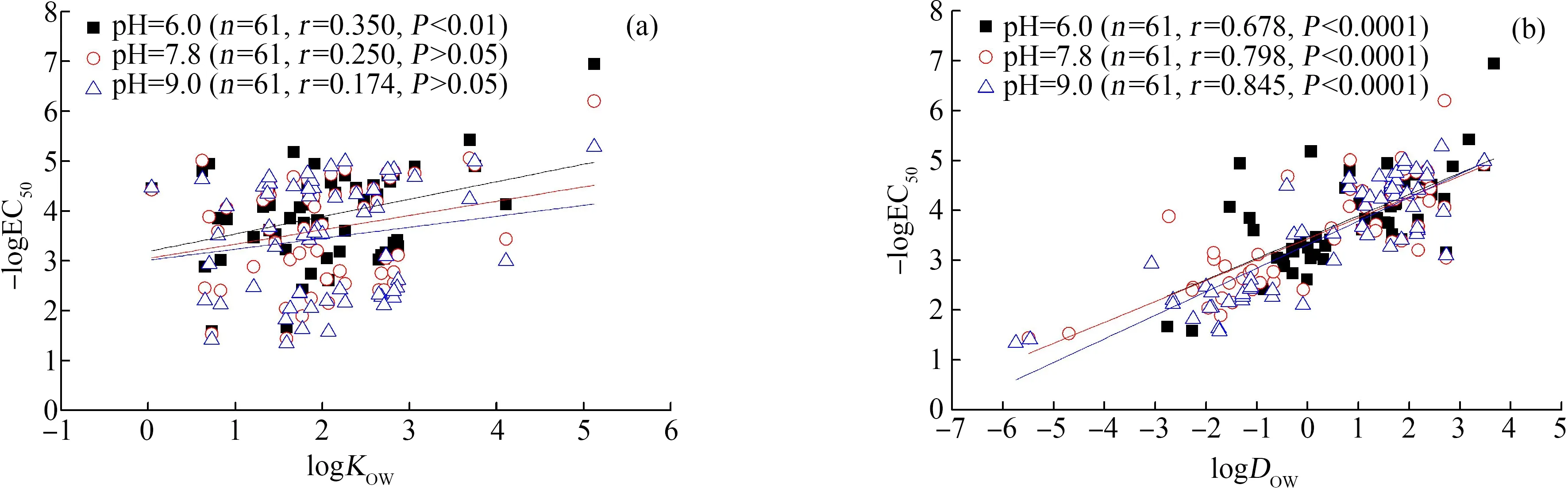
图2 logKOW, logDOW(pH)与-logEC50的关系注:logKOW表示正辛醇-水分配系数,logDOW(pH)表示正辛醇-水分布系数;可电离有机化合物(IOCs)的大型溞急性毒性数据(-logEC50, 24 h)和 相应的logKOW数据来源于Li等[84];logDOW(pH)数据采用MarvinSketch 15.6.29.0, 2015(ChemAxo, http://www.chemaxon.com)软件预测。Fig. 2 Correlation between logKOW, logDOW(pH) and -logEC50Note: logKOW is n-octanol/water partition coefficient, and logDOW is n-octanol/water distribution coefficient; the acute toxicity data (-logEC50, 24 h) of ionizable organic chemicals (IOCs) to Daphnia magna, corresponding logKOW values were obtained from Li et al[84], and logDOW(pH) values of those IOCs were predicted employing MarvinSketch 15.6.29.0, 2015 (ChemAxon, http://www.chemaxon.com).
从结构上看,测定logKOW和logDOW(pH)使用的辛醇是均相体系,而真实的生物膜含有磷脂双分子层,属于非均相体系。这意味着化合物在辛醇相的分配行为与其在真实生物膜中的分配或跨膜行为具有较大的差异。因此,相比于logKOW或logDOW(pH),使用膜-水分配系数(logKm/w)来表征化合物的膜通透性或膜累积能力具有更大的优势。然而,由于真实的生物膜很难获取及开展实际的测试,一般采用脂质体-水分配系数(logKlip/w)来近似替代logKm/w[85]。对于不可电离化合物,可以采用分子态的logKlip/w-分子作为预测变量。但是对于IOCs,需要使用在特定pH条件下进行形态修正的脂质体-水分配系数((logDlip/w(pH))来表征。其定义如下[86]:

(13)
式中:logKlip/w-分子和logKlip/w-离子-i分别是IOCs分子态和第i种离子态的脂质体-水分配系数;δ离子-i是第i种离子态的比例分数。目前,已有较多模型采用logDlip/w(pH)作为预测变量预测IOCs的相关属性或毒性。如,细菌毒性[87-88]、藻毒性[22]、斑马鱼胚胎毒性[10,89]、发光菌生物发光抑制毒性[90]、生物累积性[91-92]和吸附属性[93]等。例如,Klüver等[89]采用logDlip/w(pH)来预测IOCs的斑马鱼胚胎急性毒性参数(-logLC50)(式14):
-logLC50=-2.22+0.99logDlip/w(pH)
(14)
化合物的logKOW和logDOW值可以从文献、数据库查询得到,也可通过软件预测。如EPI Suit 4.1TM、VEGA (https://www.vegahub.eu/)、OECD QSAR toolbox (https://qsartoolbox.org/)、ChemAxon (http://www.chemaxon.com)等。logKlip/w和logDlip/w(pH)数据可通过查阅文献获取或根据文献报道的模型进行预测。例如,在前期的研究中,我们查询了290种化合物的分子态脂质体-水分配系数(logKlip/w-分子)、106种化合物的离子态脂质体-水分配系数(logKlip/w-离子)和306种化合物进行形态修正的脂质体-水分配系数((logDlip/w(pH))数据,同时构建了能预测logKlip/w-分子、logKlip/w-离子和logDlip/w(pH)数据的模型[85]。
3 考虑离子参数的多参数线性自由能关系(Ionic descriptors in polyparameter linear free energy relationship (pp-LFER) equation)
传统的多参数线性自由能关系(pp-LFER)模型可用于预测中性化合物从水相/气相到各种有机相的分配参数[94]。pp-LFER模型一般采用如下3个方程来表征[95-97]:
SP=c+eE+sS+aA+bB+vV
(15)
SP=c+eE+sS+aA+bB+lL
(16)
SP=c+sS+aA+bB+lL+vV
(17)
式中:SP一般指分配系数;E是化合物过量摩尔折射率;S是化合物极化性参数;A和B是分子整体氢键酸度和碱度;V是McGowan分子体积;L是298 K条件下,正十六烷-空气分配系数的对数值;c是常数项;e、s、a、b和v是系数。目前,该方程在预测不可电离化合物的相关分配系数方面得到了较多的应用,例如在Web of Science数据库,通过“polyparameter linear free energy relationship”作为关键词,可以检索到数十篇相关论文,在这里我们就不详细列出相关应用。为了适用于IOCs,Abraham和Zhao[98]在传统pp-LFER方程基础上通过引入了2个新的离子描述符,即J+和J-,提出了考虑离子参数的pp-LFER方程:
SP=c+eE+sS+aA+bB+vV+j+J++j-J-
(18)
通过采用考虑离子参数的pp-LFER方程,前人构建了可预测IOCs的多种参数,包括有机溶剂-水分配系数[99-101]、脂质体-水分配系数[3]、血清白蛋白-水分配系数[18]、肌肉蛋白水分配系数[20]、活性炭-水分配系数[102]和针铁矿-溶剂分配系数[103]等。例如,Henneberger等构建了能够预测IOCs鸡类肌肉蛋白-水分配系数(logKMP/w)的预测模型[20]:
logKMP/w=-0.24+0.68E-0.76S-0.20A-2.29B+ 2.51V-0.68J++2.89J-
(19)
pp-LFER建模所需参数E、S、A、B、V和L可通过查询UFZ-LSER数据库(https://www.ufz.de/ index.php?en=31698&contentonly=1&m=0&lserd_data[mvc]=Public/start)或大连理工大学陈景文教授团队开发的在线程序预测所需参数(http://www.pplfer.online/)。离子描述符J+和J-可通过查阅文献获取。
4 基于形态修正的量化参数(Chemical form adjusted quantum chemical descriptors)
化合物的量子化学描述符一般具有明确的物理化学意义,有利于进行模型机理解释[59,104]。为了预测IOCs的相关属性或毒性效应,可对量化描述符进行形态修正[34,105]:
(20)

(21)
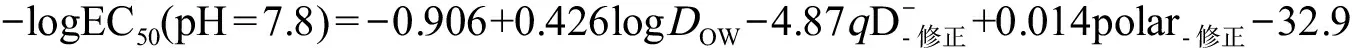
(22)
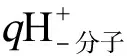
在表1中列出了18种形态修正的量化描述符。基于这些参数,我们已成功构建了IOCs与人运甲状腺素蛋白(hTTR)亲和力[34,38,107-110]、牛血清白蛋白-水分配系数[106]、脂质体-水分配系数[85]和大型溞急性毒性[8]等参数预测模型。从定义可知,基于形态修正的量化参数具有2个方面的特点:(1)可以直接根据IOCs的分子态和离子态结构计算得到;(2)可以同时考虑分子态和共存的多种离子态的贡献。

表1 基于形态修正的(Q)SA/PR模型量化参数Table 1 Proposed chemical form adjusted quantum chemical descriptors used in the (Q)SA/PR modeling
5 总结与展望(Conclusion and prospect)
IOCs的分子态和离子态对其物理化学、环境归趋和行为、生态和健康毒性效应参数均具有不同贡献。在开展IOCs相关实验和理论研究时,不应忽视IOCs离子化的影响。截止目前,研究人员针对在建模中如何考虑IOCs离子化影响的问题,提出了4种可用于表征IOCs离子化影响的描述符,即酸碱解离常数及其衍生参数、考虑离子化影响的分配系数、考虑离子参数的多参数线性自由能关系、基于形态修正的量化参数,并成功将其应用于IOCs各种分配系数、水生毒性和蛋白结合效应等参数的(Q)SA/PR模型构建。
针对现有研究进展,对今后IOCs建模研究提出了以下建议。(1) 预测指标方面:需要进一步识别还有哪些参数受离子化的影响;(2) 描述符方面:需要研究如何更准确获取所需描述符。如前所述,在建模中要考虑离子化的影响,核心是获取pKa、logDOW(pH)、logDlip/w(pH)、J+和J-、量化参数等相关描述符。但是,在现有IOCs中,仅部分具有可靠的pKa、logDOW(pH)和logDlip/w(pH)等参数的实验数据。例如,仅几百种IOCs拥有logDlip/w(pH)实验数据[85],几千种IOCs有pKa实验数据[58]。因此,需要进一步测定IOCs的pKa、logDOW(pH)和logDlip/w(pH)等参数的实验数据;同时也可以构建更多能够准确预测这些参数的模型工具。对量化参数而言,已引入了18种参数用于建模。根据Mamy等[111]的研究结果,目前文献中已报道的量化参数已达248种。需要进一步研究是否还存在其他量化参数适合用于进行形态修正并用于建模。(3) (Q)SA/PR模型构建方面:针对受离子化影响的参数,构建更多预测模型,同时考虑将其集成到现有软件工具中或开发新的软件工具。(4) 非(Q)SA/PR方法的开发与应用:需积极探索其他适合用于表征离子化影响的非(Q)SA/PR方法。IOCs的一些属性或毒性效应参数涉及小分子与生物大分子(如生物膜、蛋白等)的相互作用。而分子对接、分子动力学和耦合量子力学/分子力学(QM/MM)等分子模拟方法常用于研究小分子与生物大分子的相互作用。是否可以采用分子模拟方法来表征IOCs离子化的影响呢?在这方面,已有部分研究进行探讨,例如,Bittermann等[3,112]采用COSMOmic方法成功预测了IOCs生物膜-水分配系数。我们采用QM/MM方法研究了酚类化合物与hTTR的相互作用,发现实验测定的酚类化合物与hTTR亲和力数据(logRP)与基于酚类化合物分子态计算的结合能(E结合能-分子态)之间无显著性线性相关性。但是,当采用形态修正的结合能(E结合能-形态修正)后,其与logRP则存在显著性线性相关性[34]。因此,需要进一步探索采用分子模拟等非(Q)SA/PR方法来预测IOCs相关属性或毒性参数的可行性。

