加味消毒饮颗粒微生物限度检查方法学验证
刘 钰 吴无畏 付书婕 蒋雅娜 王国倩 潘 宇 陈 路
1.广西壮族自治区药用植物园,广西南宁 530023;2.广西壮要方医院药剂科,广西南宁 530150;3.右江民族医学院,广西百色 533000
五味消毒饮方出自清代吴谦编纂的《医宗金鉴》,处方由金银花、野菊花、蒲公英、紫花地丁、紫背天葵子五味中药组成,为中医治疗疮疔庸肿的常用方剂,广泛用于急性咽炎、扁桃体炎、严重外耳道疖肿等耳鼻喉科感染,麦粒肿、复发性单纯疱疹性角膜炎、色素膜炎等眼科感染,体表化脓性疾病、颌面部蜂窝织炎、痤疮等多种外科及外邪热毒(病原体)所侵导致的疾病[1-11]。广西壮要方医院在长期的临床医疗实践中,根据风热感冒的疾病特点,对五味消毒饮处方进行了调整,形成了加味消毒饮方药,该方药由黄芩、山银花、穿心莲、野菊花、蒲公英、栀子6 味药组成,此方药对热毒所侵引发的风热感冒如肺热咳嗽、急性扁桃体炎及多种感染性疾病都有较好的治疗效果。加味消毒饮颗粒作为新出方药,为保证用药安全性,对其进行微生物限度检查非常必要。本研究以《中华人民共和国药典》的标准为依据[12],建立了加味消毒饮颗粒微生物限度检查方法,并进行验证,为临床用药安全提供科学依据。
1 仪器与材料
1.1 仪器
YXQ-LS-100SⅡ型立式压力蒸汽灭菌器(上海博讯实业有限公司医疗设备厂);SW-CJ-2FD 型洁净工作台(苏州安泰空气技术有限公司);BSA124S 型电子分析天平(德国Sartoriu 公司,精度:0.0001 g);LHS-2C80型恒温恒湿箱(上海科辰实验设备有限公司);SPX-100B-Z 型生化培养箱(苏州江东精密仪器有限公司);JBQ-ZD8 型金温振荡器(常州普天仪器制造有限公司金坛市晶玻实验仪器厂);JBZL-08 型智能气浴恒温振荡器(常州普天仪器制造有限公司金坛市晶玻实验仪器厂)。
1.2 材料
1.2.1 试药 加味消毒饮颗粒(广西壮要方医院,批号:20200901、20200902、20200903,规格:15 g/袋)。
1.2.2 培养基 胰酪大豆胨琼脂培养基(中国食品药品检定研究院,批号:135025-201804);胰酪大豆胨液体培养基(中国食品药品检定研究院,批号:135026-201401);沙氏葡萄糖琼脂培养基(中国食品药品检定研究院,批号:135013-201001);沙氏葡萄糖液体培养基(中国食品药品检定研究院,批号:135008-201503);pH 7.0 氯化钠-蛋白胨缓冲液(北京陆桥技术股份有限公司,批号:200706);麦康凯琼脂培养基(北京陆桥技术股份有限公司,批号:190902);麦康凯液体培养基(北京陆桥技术股份有限公司,批号:190802);聚山梨酯80(北京陆桥技术股份有限公司,批号:171206)。
1.2.3 菌种 大肠埃希氏菌[CMCC(B)44102,中国食品药品检定研究院];金黄色葡萄球菌[CMCC(B)26003,中国食品药品检定研究院];白色念珠菌[CMCC(F)98001,中国食品药品检定研究院];枯草芽孢杆菌[CMCC(B)63501,中国食品药品检定研究院];绿脓假单胞菌[CMCC(B)10104,中国食品药品检定研究院];黑曲霉菌[CMCC(F)98003,中国食品药品检定研究院],本研究所用的均为第3 代菌株。
2 方法与结果
2.1 菌液制备
分别取“1.2.3”项下的大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌和绿脓假单胞菌,在胰酪大豆胨液体培养基中于34℃条件下培养24 h。取上述培养物用氯化钠-蛋白胨缓冲液(pH=7.0)制备成菌悬液,备用;取“1.2.3”项下的白色念珠菌在沙氏葡萄糖液体培养基中于25℃条件下培养3 d,取所得培养物用氯化钠-蛋白胨缓冲液(pH=7.0)制备成菌悬液,备用;取“1.2.3”项下的黑曲霉菌在沙氏葡萄糖琼脂培养基中于25℃条件下培养5 d,所得培养物加5 ml 含0.05%聚山梨酯80 的氯化钠-蛋白胨缓冲液(pH=7.0),洗下霉菌孢子,制备成菌悬液,备用。
2.2 供试液制备
取“1.2.1”项下批号为20200901 的加味消毒饮颗粒1 袋(15 g),用氯化钠-蛋白胨缓冲液(pH=7.0)制成1∶10 的供试液。取所制得供试液50 ml,加氯化钠-蛋白胨缓冲液(pH=7.0)至100 ml 稀释成1∶20 供试液,备用。
2.3 需氧菌、霉菌和酵母菌总数计数方法的验证
2.3.1 常规法 试验组:精密吸取“2.2”项下1∶10 供试液5 份,各9.9 ml,每份供试液分别加入金黄色葡萄球菌、枯草芽孢杆菌、白色念珠菌、绿脓假单胞菌及黑曲霉菌菌悬液各0.1 ml(每1 ml 所含菌数≤100 cfu),混合均匀制得染菌供试液。在平皿中分别注入上述各染菌供试液1 ml,注入胰酪大豆胨琼脂培养基进行培养,金黄色葡萄球菌、绿脓假单胞菌及枯草芽孢杆菌在34℃温度条件下培养3 d,白色念珠菌及黑曲霉菌在25℃温度条件下培养5 d。每份染菌供试液平行制备2 个平皿进行平行试验。
菌液对照组:精密吸取氯化钠-蛋白胨缓冲液(pH=7.0)5 份,各9.9 ml,每份中分别加入的菌悬液与试验组相同,其余操作步骤同试验组。
供试品对照组:精密吸取1∶10 供试液9.9 ml,加入pH=7.0 氯化钠-蛋白胨缓冲液0.1 ml,不加菌悬液,其余操作步骤同试验组。
回收率测定结果:试验组的加菌回收率比值=(试验组平均菌落数-供试品对照组平均菌落数)/菌液对照组的平均菌落数。按国家《中华人民共和国药典》[12]标准,回收率比值应为0.5~2.0。常规法中金黄色葡萄球菌、绿脓假单胞菌、枯草芽孢杆菌、白色念珠菌、黑曲霉菌的回收率比值分别为0.38、0.39、1.04、0.91、1.02。本试验中,金黄色葡萄球菌和绿脓假单胞菌的回收率比值均<0.50,由此可知采用常规法制备供试液,平皿法进行加味消毒饮颗粒的需氧菌总数测定不可行,需要更换检测方法。常规法中白色念珠菌、黑曲霉菌的回收率比值都在0.5~2.0 范围内,可见采用供试液常规法对加味消毒饮颗粒的霉菌及酵母菌总数进行测定具有可行性。见表1。
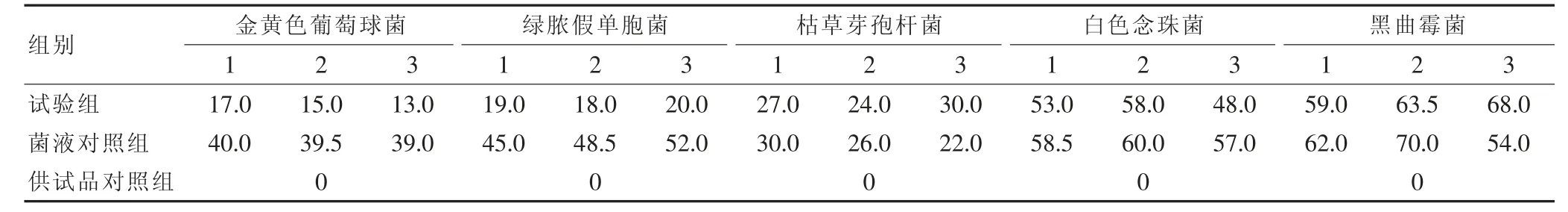
表1 常规法加味消毒饮颗粒-需氧菌、霉菌和酵母菌总数回收试验结果(cfu/ml)
2.3.2 供试液稀释法 试验组:分别精密吸取“2.2”项下1∶20 供试液9.9 ml,共5 份,每份中分别加入的菌悬液与常规法的试验组相同,其余操作步骤同常规法的试验组。
菌液对照组:精密吸取氯化钠-蛋白胨缓冲液(pH=7.0)5 份,各9.9 ml,每份中分别加入的菌悬液与试验组相同,其余操作步骤同试验组。
供试品对照组:精密吸取1∶20 供试液9.9 ml,加入pH=7.0 氯化钠-蛋白胨缓冲液0.1 ml,不加菌悬液,其余操作步骤同试验组。
回收率测定结果:稀释法中金黄色葡萄球菌、绿脓假单胞菌、枯草芽孢杆菌、白色念珠菌、黑曲霉菌的回收率比值分别为0.98、1.02、1.16、1.10、1.03。5 种试验菌的回收率比值都在0.5~2.0 范围内,由此可知采用供试液稀释法,将供试液稀释至1∶20,平皿法进行加味消毒饮颗粒的需氧菌总数测定可行。见表2。
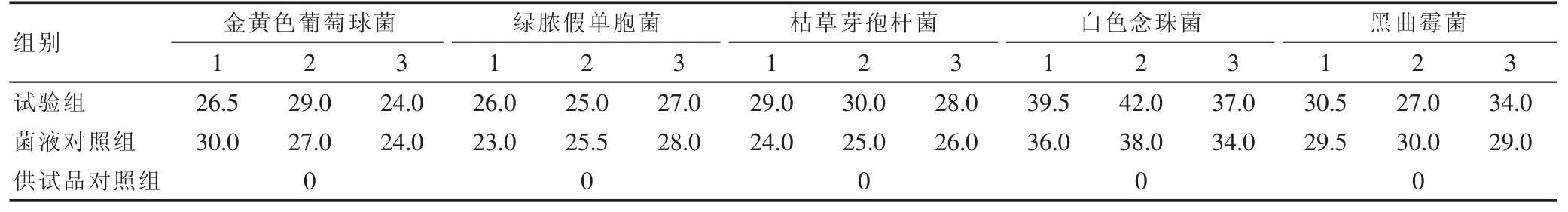
表2 稀释法加味消毒饮颗粒-需氧菌总数回收试验结果(cfu/ml)
2.4 控制菌(大肠埃希菌)检查方法的验证
试验组:取“2.2”项下1∶10 供试液及每1 ml 含菌量≤100 cfu 的大肠埃希菌菌悬液10 ml,与100 ml胰酪大豆胨液体培养基混合均匀,于35℃温度条件下培养24 h。取所得培养物1 ml 注入100 ml 麦康凯液体培养基中,在42℃条件下培养24 h 后,将所得培养物划线法接种在麦康凯琼脂培养基平板上,于35℃条件下培养24 h,观察菌落形态。
菌液对照组:不含供试液,其余操作同试验组。
供试品对照组:取10 ml“2.2”项下1∶10 供试液,接种在100 ml 胰酪大豆胨液体培养基中,其余操作同试验组。
大肠埃希菌检查试验结果:试验组、菌液对照组麦康凯液体培养基显浑浊,麦康凯琼脂培养基显粉色或红色菌落,判定检出大肠埃希菌;供试品对照组麦康凯液体培养基澄清,麦康凯琼脂培养基无菌落生长。提示常规法可用于加味消毒饮颗粒控制菌检查。
2.5 3 批样品微生物限度检查
根据所建立的微生物限度检查法,对3 批样品进行检验,分别平行试验3 次,结果见表3。

表3 3 批加味消毒饮颗粒微生物限度检查结果(cfu/ml)
综上所述,加味消毒饮颗粒的微生物限度检查方法需氧菌总数检查采用供试液稀释法(1∶20)、霉菌及酵母菌总数检查及控制菌的检查可采用供试液常规法,试验菌的回收率及控制菌检查结果均符合2020年版《中华人民共和国药典》[12]中的规定。
3 讨论
加味消毒饮颗粒由五味消毒饮通过组方调整、剂型变化而来,是首次报道的经过长期临床实践证明确有疗效的新制剂。方中山银花清热解毒、疏散风热,野菊花疏风平肝,二者合为君药;黄芩清热泻火解毒,穿心莲清热解毒、消炎止痛,栀子清热泻火凉血,蒲公英清热利尿,整方清热解毒功效见长,对各型风热感冒有良效[13-19]。加味消毒饮颗粒在微生物限度检查方法适用性试验中,采用常规法(1∶10)制备供试液检查需氧菌总数时,金黄色葡萄球菌和绿脓假单胞菌的回收率均<0.5,低于2020 年版《中华人民共和国药典》[12]规定的限度范围(0.5~2.0)。这提示采用常规法(1∶10)的稀释倍数时,样品的溶液仍然具有一定的抑菌活性,影响了金黄色葡萄球菌和绿脓假单胞菌的回收率。文献关于中药制剂微生物限度检查的报道也表明,中药制剂的本身也含有一定的抑菌作用,是微生物限度检验干扰因素之一,可以通过采取一定的方法消除中成药药品本身抑菌成分的干扰[20-25]。如本研究所示,当供试品稀释制成1∶20 的供试液,平皿法进行加味消毒饮颗粒需氧菌总数测定时,5 种试验菌的回收率均>0.5 且<2.0,提示当供试品稀释制成1∶20 的供试液时其抑菌效力有所降低。
微生物体积小,种类多,分布广泛,代谢类型及代谢产物多样,对人类生产、生活的影响巨大。药品微生物限度检查是确保药品质量和保障患者的用药安全的重要手段,也是药品监管的重要内容。此外,中药制剂的处方、制法都可能对试验结果产生影响,检验人员对方法适用性试验工作的理解认知也还存在许多不足,日常微生物检验时更需要对中药制剂具体品种进行具体分析,也预示着未来对中药制剂进行微生物限度检查将面临一定的复杂性和挑战性。

