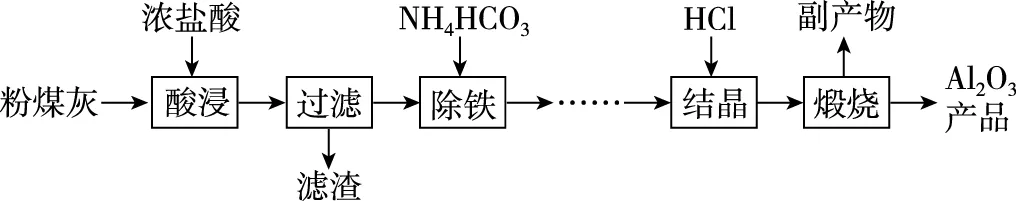
“发展性任务”教学主张下的高中化学课堂教学
——以高三微专题复习课为例
江苏 姚明站
依《中国高考评价体系》及其说明和《关于做好2021年普通高校招生工作的通知》要求,高考命题要基于立德树人的根本任务,在问题情境中认识、分析和解决问题,发挥高考命题的育人功能和导向作用,在2021年1月份的江苏省2021年新高考适应性考试(以下简称江苏省适应性考试)中,试题的开放性、灵活性明显增强,加大了归因类问题的考查力度,有效地避免了学生在学习中的“机械刷题”和死记硬背的现象,这类试题必将成为今后高考重点考查的对象。归因类问题因情境陌生、探究性强,对学生的信息的获取和处理能力要求高,导致学生缺乏解决问题的自信,产生畏难情绪和逃避心理,从而错失学科核心素养发展和学业质量水平提升的机会。
教师可以根据命题情境,设计“发展性任务”,引导学生获取和处理信息,达到提高学生证据推理意识的目的,达成使学生学会解决问题并形成解题思路的目标,发展学生的学科核心素养,提升学生的知识结构化水平。所谓“发展性任务”,是指教师能够站在发展学生学科核心素养的高度,根据《普通高中化学课程标准(2017年版2020年修订)》要求,在深度解读教材的基础上,把课堂教学目标分解为若干个梯度合理、结构鲜明、富有启发性和生成导向的学习任务。发展是事物不断前进的过程,是由旧事物到新事物的运动变化过程,其根源是内部矛盾,即事物的内因,化学就是在原子、分子的层面上研究物质发展变化的学科。所以,发展性任务必须有明确的指向性,具有矛盾性、思辨性和探究性的特征。
现以陌生非氧化还原反应方程式的书写及应用为例,说明在教学中如何设计发展性任务。非氧化还原反应多为复分解反应,也会涉及无单质参加的化合反应、无单质生成的分解反应(如铵盐、弱酸酸式盐、难溶氢氧化物、难溶碳酸盐等分解)等,以“紧凑式问题组”模式进行“微型专题”复习。
1.“酸性物质与碱性物质”反应

【例1】(2020·江苏卷·16节选)吸收工厂烟气中的SO2,能有效减少SO2对空气的污染。氨水、ZnO水悬浊液吸收烟气中SO2后经O2催化氧化,可得到硫酸盐。


图1
(1)氨水吸收SO2。向氨水中通入少量SO2,主要反应的离子方程式为____________________;当通入SO2至溶液pH=6时,溶液中浓度最大的阴离子是________(填化学式)。
(2)ZnO水悬浊液吸收SO2。向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40 min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图2)。溶液pH几乎不变阶段,主要产物是________(填化学式);SO2吸收率迅速降低阶段,主要反应的离子方程式为________________。

图2
“发展性任务”问题设计:
(1)Q1:向氨水中通入SO2的过程中,发生的反应有哪些?
Q2:该反应过程中,溶液中溶质与pH之间有什么关系?
(2)Q1:溶液pH为什么会从几乎不变到迅速降低?
Q2:向ZnO水悬浊液中匀速缓慢通入SO2过程中,发生了哪些反应?溶液pH应如何变化?
Q3:追问,为什么pH迅速降低阶段SO2吸收率也迅速降低?(从平衡移动的视角分析)
策略分析:试题以“吸收工厂烟气中的SO2”真实情境为载体,题给信息中提供了吸收SO2的方案、图像信息以及相关陌生物质的性质,信息量较大,对学生陌生信息的获取和处理能力要求高,学生解题思路不清晰是首要的答题瓶颈。研究SO2被氨水、ZnO水悬浊液吸收过程中发生的反应、对应产物以及溶液pH的变化情况,是一个动态变化的过程。教师在进行教学设计时聚集问题,结合物质的转化规律,可以设计出如上所示的发展性任务,将任务目标进行合理分解,设计出梯度合理、结构鲜明、富有启发性和导向性的问题,引导学生动态生成对问题的理解,最终使学生完成任务或解决问题,并逐步形成问题解决的流程,建构解决问题的思维模型,把握解决问题的思维路径。
2.“强酸制弱酸”原理
【例2】(2017·江苏卷·16节选)铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如图3:

注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH________(填“增大”“不变”或“减小”)。
“发展性任务”问题设计:
Q1:溶液的pH如何变化,首先要考虑什么?
Q2:“过滤Ⅰ”所得滤液主要成分是什么?“反应”生成的产物是什么?
Q3:写出反应的离子方程式,各反应的本质是什么?分析溶液pH的变化情况。

3.“水解”反应
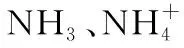
(1)沉淀:向酸性废水中加入适量Fe2(SO4)3溶液,废水中的氨氮转化为NH4Fe3(SO4)2(OH)6沉淀。
①该反应的离子方程式为________________________。
②废水中氨氮去除率随pH的变化如图4所示,当1.3 图4 “发展性任务”问题设计: Q1:沉淀氨氮反应过程中,题中给了哪些关键信息? Q2:尝试书写该反应的离子方程式,分析该沉淀氨氮的反应本质是什么? Q3:随着pH的增大,影响氨氮去除率的因素可能有哪些?氨氮去除率上升段和下降段的主要原因分别是什么? 【例4】(1)以粉煤灰(主要成分为Al2O3、SiO2,还含少量Fe2O3等)为原料制取氧化铝的部分工艺流程如图5: 图5 “除铁”生成Fe(OH)3的离子方程式:________________________。 (2)(2021·湖南省适应性考试·16节选)在加热条件下,尿素[CO(NH2)2]在水中发生水解反应,放出________和________两种气体(写化学式)。 “发展性任务”问题设计: Q1:“除铁”生成Fe(OH)3的反应物是什么? Q2:该反应的本质是什么?如何书写该反应的离子方程式? Q3:书写尿素[CO(NH2)2]在水中发生水解反应的化学方程式,总结水解的化学反应方程式书写的要点。 从例3到例4,两个例题本身就体现任务的发展性,提升理解水解反应的本质,进行发展性任务设计。从而形成更为完善的水解概念体系。 【例5】沉钴工艺流程如图6所示,请写出“沉钴”过程中的离子方程式:________________________。 图6 “发展性任务”问题设计: Q1:根据工艺流程图,寻找“沉钴”过程主要的反应物和生成物,并书写反应的离子方程式。 Q2:对照反应物和生成物,分析该反应的本质过程可能是什么? 【例6】在50℃时ZnSO4溶液中加入NH4HCO3碳化,生成ZnCO3·2Zn(OH)2·H2O、(NH4)2SO4和CO2,写出碳化过程的化学方程式:________________________。 “发展性任务”问题设计: Q1:根据原子守恒书写反应的化学方程式,该反应可如何分解?(可看成“平衡转化”和“水解”两个过程的复合) Q3:该反应溶液pH变化对产物的组成会造成什么影响? 【例7】(2021·江苏省适应性考试·16改编)取一定量蚀刻废液{主要成分为[Cu(NH3)4]Cl2}和稍过量的NaOH溶液加入到三颈瓶中,在搅拌下加热反应并通入空气,待产生大量的黑色沉淀时停止反应,趁热过滤、洗涤,得到CuO固体;所得固体经酸溶、结晶、过滤等操作,得到CuSO4·5H2O晶体。 写出用蚀刻废液制备CuO反应的化学方程式:____________________。“加热反应并通入空气”的目的是______________________________。 “发展性任务”问题设计: Q1:结合题给信息,推理书写化学方程式。 Q2:“加热反应并通入空气”的目的是什么? Q3:分析蚀刻废液制备CuO反应可能包括哪几个过程? Q4:追问,银镜反应{[Ag(NH3)2]OH溶液}必须在碱性条件下发生的原因是什么? 策略分析:非氧化还原反应的化学方程式的书写,只有能够洞悉反应的本质,才能精准地判断和书写出正确的化学方程式,方能进一步应用原理解释说明和判断。
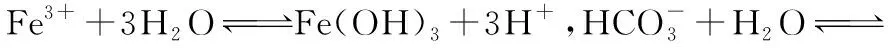


4.“平衡转化”思想



5.多重复合类


