氨氮降解菌株的筛选及降解性能研究
张国伟,靳静晨,李晨晨,高宇轩,高雅娟,张闻天,靳永胜*
1.北京农学院生物与资源环境学院,北京102206;
2.北京环氧环保科技发展有限公司,北京100101
目前,我国氨氮污染排放量已远远超出受纳水体的环境容量,氨氮指标已超过化学需氧量(chemical oxygen demand,COD)指标成为影响地表水环境质量的首要指标[1],且大量研究表明,氨氮指标超标会使江河湖泊水体逐渐富营养化[2-5]。为防止水体环境不断恶化,国家对主要污染物,如氮、磷的排放制定了严格的标准,目前生物除氮因具有低耗、高能、可持续性强等特点广泛应用于污水处理厂[6]。
科学家已发现了大量具有氨氮降解能力的菌株,如假单胞菌(Pseudomonassp.)[7-10]、粪产碱菌(Alcaligenes faecalis)[11]、芽 孢 杆 菌(Bacillussp.)[12]、酵母[13-14]等。目前越来越多的真菌被证实同样具有去氮的能力,如李伟斯[15]从河流底泥中筛选出1株链格孢属(Alternariasp.)真菌,其能够利用多种有机碳源进行生长和反硝化;杨晓华[16]从焦化废水处理单元活性污泥中筛选出1株镰刀菌属(Fusariumspp.)丝状真菌,具有较强的适应能力,初始浓度为450 mg·L-1氨氮的去除率为94.75%。刘志云[17]从鸡粪中筛选出1株拟宛氏青霉菌HL,在初始氨氮浓度为300 mg·L-1时,菌株HL的氨氮降解率为80.53%;戚文静等[18]从活性污泥中筛选出1株Galactomyces属的菌株AD-7,初始氨氮浓度291.16 mg·L-1,接种量2.21%时氨氮降解率预测值为100%,实测值仍可达到99%;曾忠强等[19]将白腐真菌丝状生物膜固定在中空的脉管载体上,构建的新型白腐真菌反应器可以控制气泡和废水流完成18批次(共进行401 d)的垃圾渗滤液连续处理,氨氮含量指标(ammonia nitrogen content index,NH3-N)和COD去除率分别达83%~97%和56%~74%。本研究从垃圾渗滤液中分离筛选出1株具有降解高氨氮能力的真菌,对其进行形态学和分子鉴定,并分析了该菌的氨氮降解特性,旨在为污水中去除氨氮提供安全、有效、经济的功能菌株。
1 材料与方法
1.1 材料
1.1.1 菌株来源 由北京南宫垃圾堆肥厂的垃圾渗滤液中筛选出1株具有氨氮降解能力的菌株。
1.1.2 培养基配比 富集培养基:葡萄糖5.0 g·L-1,(NH4)2SO42.0 g·L-1,FeSO·47H2O 0.4 g·L-1,K2HPO41.0 g·L-1,MgSO·47H2O 0.5 g·L-1,其余为去离子水,pH为7.2~7.4。
分 离 培 养 基:葡 萄 糖5.0 g·L-1,(NH4)2SO42.0g·L-1,FeSO·47H2O 0.4 g·L-1,K2HPO41.0 g·L-1,MgSO·47H2O 0.5 g·L-1,琼脂20 g·L-1,其余为去离子水。
筛 选 培 养 基:葡 萄 糖5.0 g·L-1,(NH4)2SO40.6 g·L-1,NaCl 1.0 g·L-1,FeSO·47H2O 0.05 g·L-1,K2HPO40.5g·L-1,MgSO·47H2O 0.25g·L-1,其余为去离子水。
1.1.3 主要试剂与仪器 纳氏试剂购于河南标准物质研发中心;酒石酸钾钠、过硫酸钾、葡萄糖、蔗糖、红糖、可溶性淀粉、硫酸铵、七水合硫酸亚铁、磷酸氢二钾、七水硫酸镁以及其他主要试剂均购于国药集团化学试剂有限公司。以上药品均为分析纯。DJS-2013R-2恒温摇床购于上海世平实验设备有限公司;SW-CJ-2FD超净工作台购于苏净集团苏州安泰空气技术有限公司;YP30002电子天平购于上海越平科学仪器苏州制造有限公司;UV-5500紫外可见分光光度计购于上海元析仪器有限公司;MLS-3750高压蒸汽灭菌锅购于日本SANYO公司;22331离心机购于德国Eppendorf公司;LBY纯水仪购于北京龙碧源水处理设备有限公司。
1.2 方法
1.2.1 菌种分离纯化和筛选 取渗滤液10 mL,接种于100 mL灭菌后的富集培养基中,充分摇匀,在温度为30℃、转速180 r·min-1的条件下振荡培养,富集7 d,每隔1 d补加0.5 g(NH4)2SO4。富集后经梯度稀释均匀涂布于分离培养基的平板上,在30℃培养箱倒置恒温培养,挑取平板上长出的单菌落进行重复分离纯化,直至得到单一菌株,命名为Z-5。
1.2.2 菌株的分子鉴定 利用TIAGEN真菌试剂盒提取菌株Z-5的DNA,然后以其DNA为模版、以27F(5′-AGAGTTTGATCMTGGCTCAG-3′)与1492R(5′-TACGGYTACCTTGTTACGACTT-3′)为引物,采用PCR仪扩增其内源转录间隔区(internally transcribed spacer,ITS)序列,扩增后用1%的琼脂糖凝胶电泳检测,将PCR产物送至英潍捷基(上海)贸易有限公司测序,利用测序结果在NCBI上进行Blast比对,并用MEGA 5.0做系统发育树。
1.2.3 单一因素最优条件试验 将菌株Z-5接种于100 mL筛选培养基中,置于30℃下、180 r·min-1摇床中进行培养,每24 h取样测定其氨氮浓度,其中不同的培养条件设置如下。①不同接种量:接种量分别为0.1%、0.5%、1.0%、1.5%、2.0%,氨氮初始浓度为100 mg·L-1,碳源为葡萄糖,pH为6.0,培养时间为5 d;②不同初始氨氮浓度:氨氮浓度分别为100、250、500、750、1 000 mg·L-1,接种量为1%,碳源为葡萄糖,pH为6.0,培养时间为7 d;③不同碳源:碳源分别为葡萄糖、蔗糖、红糖、可溶性淀粉,接种量为1%,氨氮浓度为100 mg·L-1,pH为6.0,培养时间为3 d;④不同pH:pH分别为5.0、6.0、7.0、8.0、9.0,接种量为1%,氨氮初始浓度为100 mg·L-1,碳源为红糖,培养时间为4 d。
1.2.4 正交试验 以100 mg·L-1氨氮为初始氮源,设计L(933)正交试验,3个因素分别为A:氨氮初始浓度;B:碳源;C:pH(表1)。
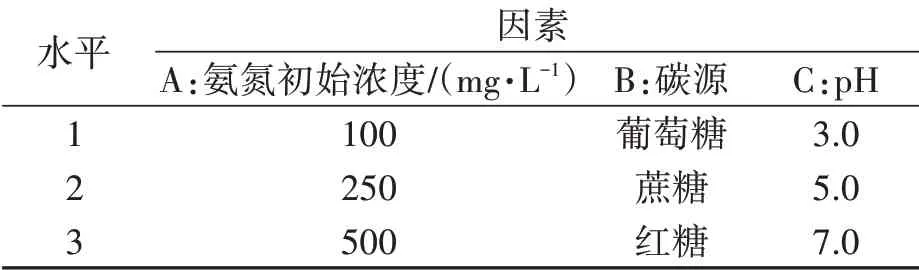
表1 因素水平表Table 1 The factors and levels scale
1.2.5 氨氮检测方法将待测样品用去离子水稀释到合适的倍数,然后用纳氏试剂分光光度法进行氨氮的测定。氨氮具体测定方法参考Fei等[12]纳氏试剂分光光度法。
2 结果与分析
2.1 菌株的形态特征
观察菌株Z-5在固体分离培养基的菌落形态,该菌株为乳白色圆形,表面不光滑,着生菌丝。增殖后菌株由乳白色转变为红褐色且有菌丝分布于培养基中。该菌属于真菌界,菌株Z-5在光学显微镜下的形态如图1所示,帚状枝双轮生,梗基每轮3~5个;瓶梗每轮4~6个;分生孢子椭圆形,经常呈长链状。

图1 菌株Z-5在光学显微镜下的形态Fig.1 Morphology of strain Z-5 under optical microscope
2.2 菌株的分子鉴定
PCR扩增菌株Z-5的ITS序列在NCBI(http://archive-dtd.ncbi.nlm.nih.gov/)网站上进行序列比对,用MEGA 5.0做分子发育树。结果表明,菌株Z-5与褐红篮状真菌(Talaromyces pinophilusKF572452.1)的同源性最高,相似性达到99%,因此初步判断Z-5属于褐红篮状菌(图2)。

图2 菌株Z-5的ITS基因序列系统发育树Fig.2 Phylogenetic tree of ITS gene sequence of Z-5 species
2.3 菌株Z-5降解氨氮能力
2.3.1 接种量对菌株Z-5氨氮降解的影响 由图3可知,当氨氮初始浓度为100 mg·L-1时,在不同的接种量条件下,氨氮降解率均随着时间的增加呈现先快速增加后逐渐平稳的趋势,同时随着接种量的增加氨氮降解率大体呈先增加后减少的趋势,第1、2 d时,随着接种量的增加氨氮降解率呈逐渐增加趋势,第3 d开始接种量1.0%时氨氮降解率升高,并在第5 d时达到峰值,为95.1%。其中接种量为0.1%、0.5%、1.5%、2.0%时均在培养第5 d氨氮降解率达到峰值,分别为79.2%、86.5%、87.8%、81.1%。以上结果表明,菌株Z-5最适的接种量为1%。
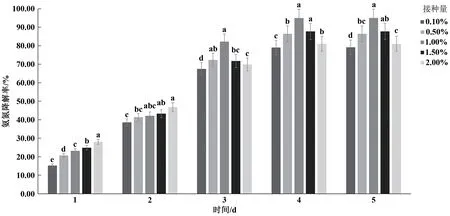
图3 接种量对菌株Z-5氨氮降解率的影响Fig.3 Effects of inoculation amount on ammonia degradation rate of Z-5
2.3.2 初始氨氮浓度对菌株Z-5降解氨氮的影响由图4可知,在初始氨氮浓度为100 mg·L-1时,培养2 d氨氮去除率即可达到90%以上,初始氨氮浓度为250、500、750 mg·L-1时,氨氮去除率分别在第3、4、7 d达到90%以上,而当氨氮初始浓度为1 000 mg·L-1时,在培养到第7 d时,氨氮去除率达到69.3%。结果表明,氨氮初始浓度越小,氨氮去除率达到最大所需的时间越短,当氨氮初始浓度为100 mg·L-1时,氨氮去除率于第4 d时达到最高,为96.1%。如图5所示,氨氮初始浓度分别为100、250、500、750、1 000 mg·L-1时,其对应氨氮绝对降解量分别在第2、3、5、7 d时达到最高,分别为96.1、238.2、472.6、702.0、693.1 mg。以上结果说明,氨氮初始浓度越低,氨氮绝对降解量达到最大所需时间越短;初始氨氮浓度在100~750 mg·L-1的范围内时,氨氮初始浓度越高,氨氮绝对降解量的峰值越高,但当氨氮初始浓度提高到1 000 mg·L-1时,其最大氨氮绝对降解量开始下降,因此,菌株Z-5在初始氨氮浓度1 000 mg·L-1以下时,提高氨氮浓度可以提高菌株Z-5的氨氮降解效率。
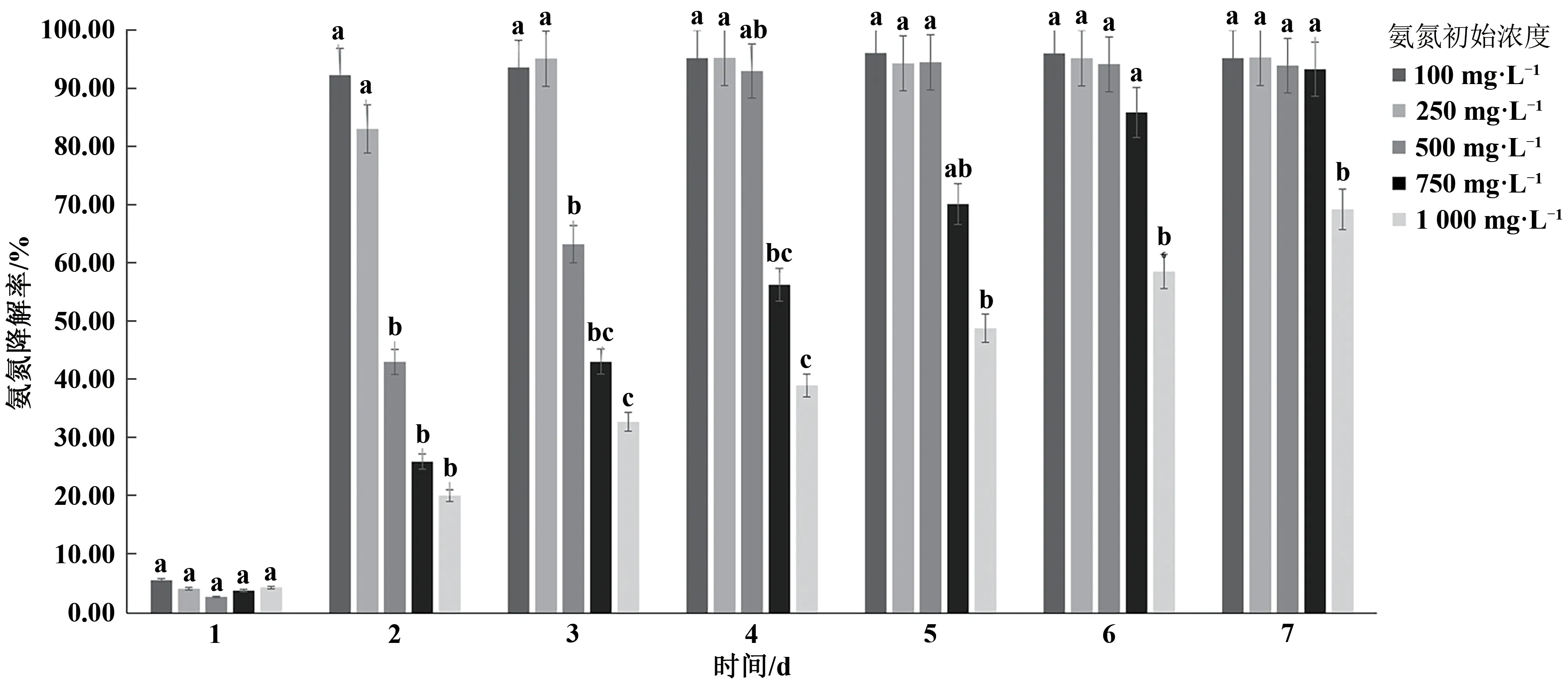
图4 氨氮初始浓度对菌株Z-5氨氮降解率的影响Fig.4 Effect of initial concentration of ammonia nitrogen on ammonia degradation rate of Z-5
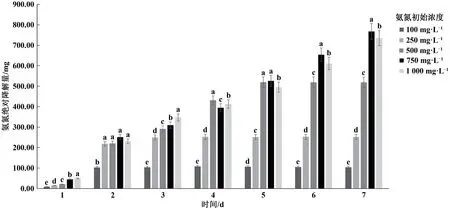
图5 氨氮初始浓度对菌株Z-5氨氮绝对降解量的影响Fig.5 Effect of initial ammonia nitrogen concentration on absolute degradation of ammonia nitrogen by strain Z-5
2.3.3 碳源对菌株Z-5氨氮降解的影响 由图6可知,菌株Z-5最适碳源为红糖,在培养2 d内就可以将氨氮基本完全降解;其次为蔗糖和葡萄糖,在培养3 d后氨氮几乎被完全降解;淀粉作为碳源氨氮降解效果最差,在培养第3 d时氨氮仅去除28.5%。以上结果表明,碳源是微生物生长的能源物质,对微生物的生长发育具有重要作用,合适的碳源不仅能提高氨氮的降解效果,而且能大大降低成本。
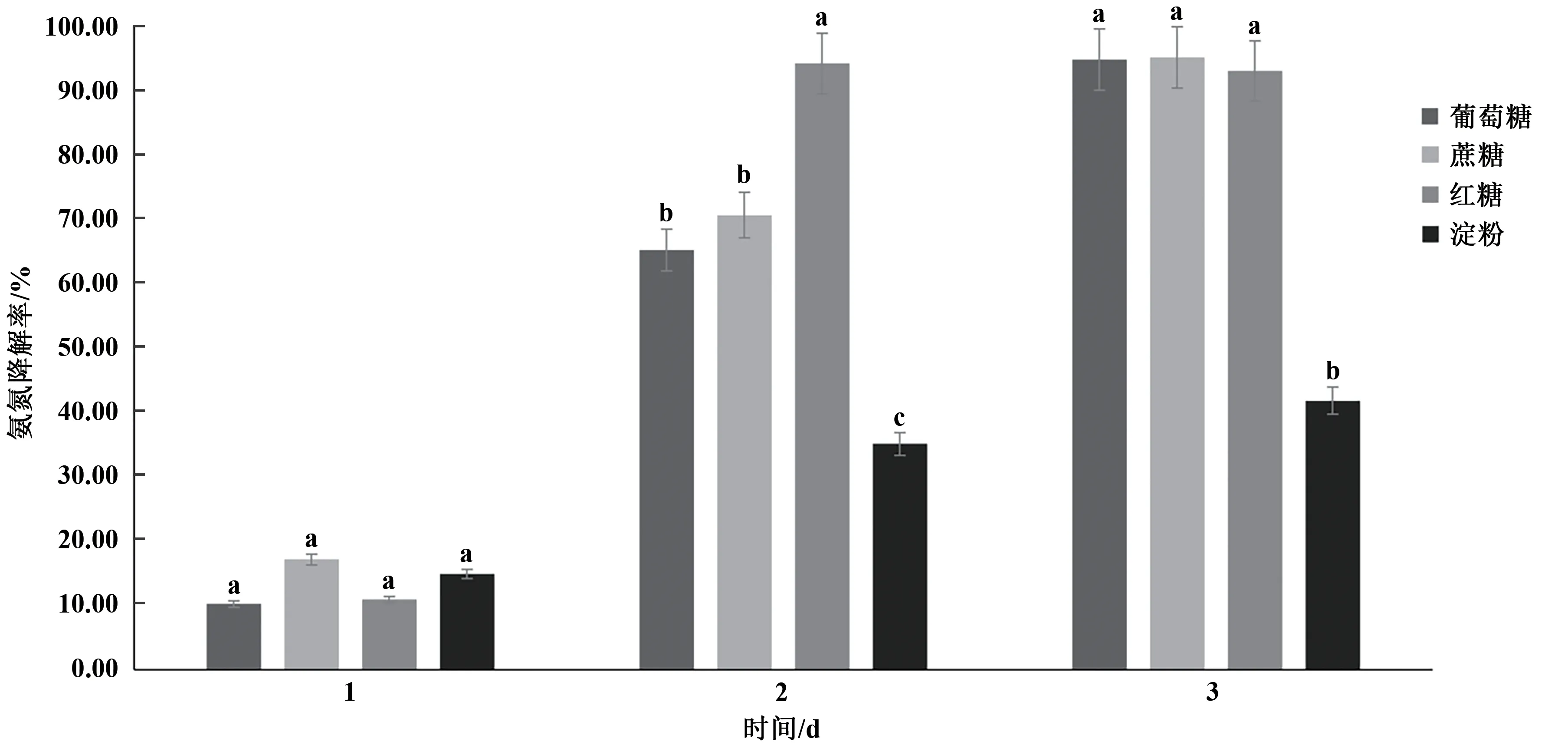
图6 碳源对Z-5菌株氨氮浓度的影响Fig.6 Effect of carbon source on ammonia concentration of Z-5
2.3.4 pH对菌株Z-5氨氮降解的影响由图7可知,在不同pH条件下,随着培养时间的增加,氨氮去除率呈先上升后趋于平稳的趋势。菌株在pH 6.0~8.0时均能很好地发挥脱氮作用,在第4天时其去除率分别为94.97%、94.91%、94.75%,其中当初始pH为8.0时其氨氮去除率在第3天时已达到90.66%,以上结果表明,该菌株更适合中性偏碱的环境,但是在弱酸环境时仍然具有较好的降解效果。
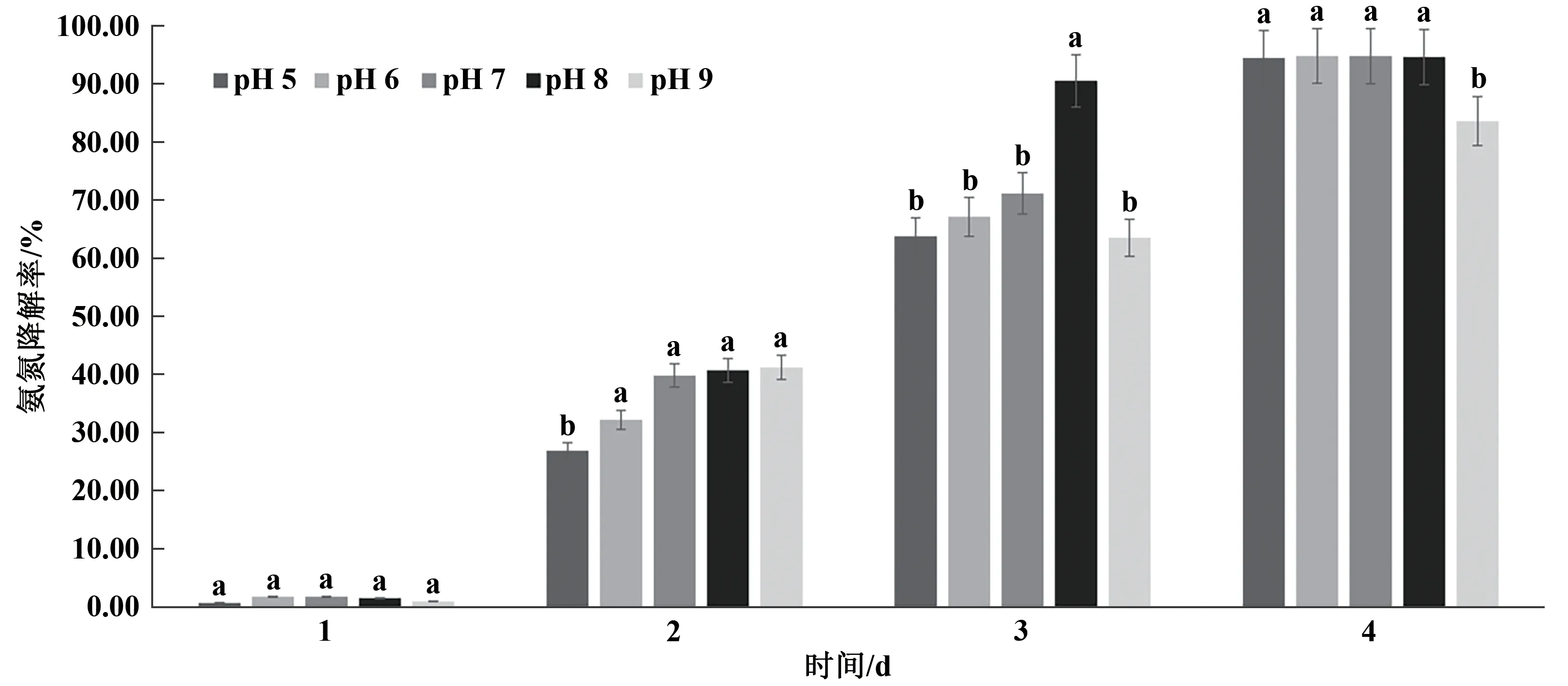
图7 pH对Z-5菌株氨氮降解率的影响Fig.7 Effect of pH on ammonia degradation rate of Z-5
2.4 单因素交叉响应
上述每个单因素指标的计算结果具有片面性,无法表现多种因素的相互影响。为探索多因素的相互影响,用磷酸盐缓冲液和HCl或NaOH调节不同酸碱度和氨氮初始浓度之间的相互影响为例,分析双因素对氨氮降解率的影响,其交互作用的响应面如图8所示,菌株Z-5的初始pH(5.0、6.0、7.0、8.0、9.0)和初始氨氮浓度(100、250、500、750、1000 mg·L-1)的二元分布共包含5×5=25组结构组合,从图中可以看出,随着pH的增加,不同初始氨氮浓度对应的氨氮降解率均先增加,到达最大值后再依次减小;随着初始氨氮浓度的增加,不同pH对应的氨氮降解率均依次减小,并且当初始氨氮浓度为100 mg·L-1和pH为7.0时,其氨氮降解率最高,达到了96.3%,与探究单因素菌株Z-5降解氨氮效果的结果一致。综合单因素的实验结果分析,影响氨氮降解的几个因素主要是氨氮初始浓度、碳源以及pH,故以氨氮降解率为指标,做初始浓度、碳源和pH 3因素3水平正交试验L9(33),正交试验结果见表2。由表2可知,各因素对氨氮降解率的影响主次顺序分别为:氨氮初始浓度、碳源、pH,最优水平为A1B3C3,即氨氮初始浓度为100 mg·L-1,碳源为红糖,pH为7.0,氨氮降解率达到了94.75%。
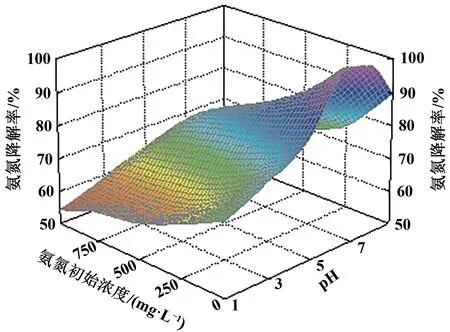
图8 pH和氨氮初始浓度之间的二元分布Fig.8 Bivariate distribution of pH and initial concentration of ammonia nitrogen
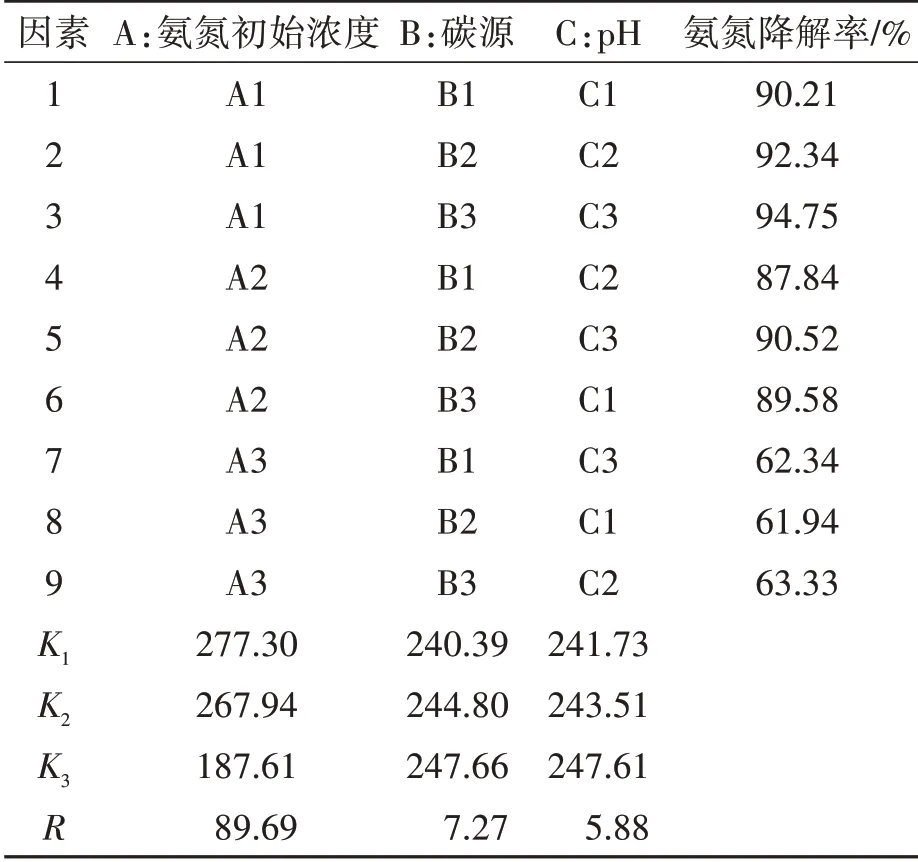
表2 正交试验结果Table 2 The results of orthogonal experiments
3 讨论
研究表明,含有高浓度氨氮的废水如果不经处理直接排放到水库或江河湖海中,会影响人类健康,并且过量的氨氮会破坏水体自净能力,打乱水体环境生态平衡[20]。本研究结果表明,菌株Z-5最适接种量为1.0%,分析原因为,接种量的大小决定了菌种的繁殖速度,接种量过大或过小,都会影响氨氮降解效果。接种量过大会造成溶氧不足,影响产物的合成,随之产生更多的代谢中间产物,不利于菌株生长;过小会延长培养时间,影响氨氮降解速率。吴建江等[21]筛选出一株假单胞菌(Pseudomonassp.)XS76,其最适接种量为4%;王田野等[22]筛选出的一株异养硝化好氧反硝化菌不动杆菌(Acinetobactersp.)SQ2,研究发现其最适接种量为5%。适宜的氨氮浓度可以促进氨氧化菌的生长,提高氨氮去除效率,但过高的氨氮,会抑制氨氧化菌的生长与活性,从而影响其氨氮降解能力[16]。,随着氨氮浓度的增加,菌株Z-5对污水氨氮去除率逐渐下降,在初始氨氮浓度100~750 mg·L-1的范围内,菌株Z-5对氨氮的绝对去除量逐渐增加。分析原因为,氨氮浓度的提高可能会导致C/N比下降造成的;菌株Z-5的最适碳源为红糖,不同的碳源对菌株的氨氮降解能力不同,本研究的碳源分别是葡萄糖、蔗糖、红糖和淀粉,其中葡萄糖、蔗糖和淀粉均属于化合物,而红糖为混合物,总糖分≥85%,含有较多微量元素,如铁、锌、锰、铬等,这些微量元素为菌株降解氨氮的过程中提供了营养物质;菌株Z-5最适pH为7.0,即在中性条件下氨氮降解能力最强。有研究表明,香茅醇假单胞菌(Pseudomonas)WXP-4[9]和寡养不动杆菌(Acinetobactersp.)SYF26[23]pH为7.0时脱氮能力最佳,而喻其林等[24]、朱伟等[25]在鸡粪和生活污水中分离的微生物最适pH分别为7.5、8.0,表明微生物生存环境不同,筛选出的菌种最适pH也存在明显的差异。
本研究对筛选菌株Z-5氨氮降解特性作了初步单因素分析、二元分布以及3因素3水平正交试验,结果表明,当接种量为1%、氨氮初始浓度为100 mg·L-1、碳源为红糖以及pH为7.0时,氨氮降解率最高,达到了94.75%。综上所述,菌株Z-5对低浓度的氨氮具有较高的去除能力,在培养时长足够的条件下对高氨氮废水也具有较强的去除能力,本研究结果为菌株Z-5在实际废水处理中的应用奠定了理论基础,但其他环境影响因素以及多因素交叉影响情况有待进一步分析。

