一个新型臭氧微气泡系统的臭氧液相传质特性研究
胡 珊,NKUDEDE Emmanuel,许小红,张 波,2,吴春笃,毛澍洲
(1. 江苏大学 环境与安全工程学院,江苏 镇江 212013; 2. 江苏大学 常州工程研究院,江苏 常州 213164; 3. 江苏恒泰泳池科技股份有限公司,江苏 常州 213179)
水处理中的臭氧氧化过程一般分为溶解和化学氧化两个步骤,臭氧在水中的溶解性较差,其溶解传质是影响臭氧氧化过程的限速步骤[1].研究表明臭氧气液传质速率与气泡尺寸成反比[2],因此,可以通过减小气泡尺寸来提高气液传质效率.
微气泡为直径小于50 μm的小气泡,与直径几毫米的常规气泡相比,具有界面面积大、气泡密度高、上升速度低和内部压力高的优势,能使臭氧更有效地溶解到溶液中[3],从而使臭氧氧化工艺[4]得到了优化.微气泡的产生方式主要有溶气释气法、超声空化法、化学法、电解法等.超声空化法是利用超声引起液体内部压力变化,液体空化产生微气泡,Moussatoy等[5]采用超声空化法产生平均直径为120 μm的微气泡.化学法是利用化学物质反应生成微气泡.电解法是通过电解水或其他物质产生微气泡.上述3种方法产生的气泡数量较少、反应能耗高.溶气释气法是水处理应用中最常用的方法,该方法产生的气泡直径小、密度大、粒径均匀、上浮稳定[6].
臭氧微气泡技术在污水脱色除臭、杀菌消毒、去除污染物等方面有广泛的研究与应用[7-8].但目前关于臭氧微气泡在水中传质特性方面的研究较少.张静等[9]对微气泡促进臭氧气液传质、改善臭氧氧化效果方面进行探究,结果表明采用微气泡曝气方式,臭氧的气液传质效率是传统毫米级气泡的3.6倍,对酸性大红3R模拟印染废水有较好的处理效果,为工业染料废水的深度处理提供了参考.Chu等[10]研究了臭氧微气泡技术与传统曝气技术处理污泥,结果表明接触时间80 min时,臭氧微气泡技术的臭氧利用率为99%,远大于传统曝气方式的72%.周英豪[11]比较了臭氧微气泡接触和多孔曝气板传统接触方式对臭氧表观传质系数的影响,研究结果表明传统接触方式得到的气泡粒径集中在500~800 μm,是微气泡接触方式得到气泡粒径的10倍,臭氧表观传质系数是传统接触方式的2.4倍.夏志然等[12]研究了地下水中臭氧微纳米气泡和毫米气泡的溶解传质过程,发现微气泡溶解方式的臭氧溶解浓度及速率分别是毫米气泡的5.1、4倍,且微纳米气泡技术降解特征污染物所需的臭氧量更少.
Yausda等[13]报道了微气泡技术可以提高气体的传质速率,但臭氧在溶解过程中会受到气液相流动参数、环境条件的影响.因此,本文利用自行研制的臭氧微气泡产生装置[14-15],系统地研究了不同的水质(pH、水温)和操作条件(气体流量、系统压力)对液相臭氧浓度、臭氧传质系数的影响,以达到通过较少的臭氧投加量来制取高浓度臭氧微气泡水溶液的目的,从而提高臭氧利用率、降低投资和运行成本.
1 材料与方法
1.1 试验装置
试验装置如图1所示,主要由臭氧发生器、气液混合泵、压力溶气罐、柱式反应器以及尾气吸收系统组成.柱式反应器由直径140 mm,高度290 mm的有机玻璃柱加工制成,有效容积为4.3 L.

图1 臭氧微气泡试验装置示意图Fig.1 Diagram of ozone microbubble test device
纯氧作为气源进入臭氧发生器,通过调节电流,使臭氧发生器在不同功率下高压电晕放电产生不同浓度的臭氧气体.臭氧气体由气液混合泵负压进气口吸入,与切线方向进入的循环水在泵中混合并产生高速涡旋.臭氧在高速离心力的作用下与水形成气水混合液进入压力溶气罐,经出口管路上的闸阀调节释放口大小,使高速旋转的气水混合液在适当的压力下从管路上的释放口喷出,产生富含大量微气泡的气水混合液.混合液通入柱式反应器底部,微气泡在反应器中持续上浮至最终消失.水在系统内循环,少量未溶解的臭氧尾气由反应器顶部逸出至吸收系统.试验装置采用的阀门、转换接头均为不锈钢(304)材质,气、液相管路为聚四氟乙烯材质.试验采用臭氧浓度分析仪测定气、液相臭氧浓度,用碘量法[16]进行测定校准.本研究以自来水为原水进行臭氧微气泡系统在不同条件下的气液传质特性试验.
1.2 分析方法
试验中的分析项目、检测方法及仪器型号等如表1所示.

表1 分析项目及测定方法Tab.1 Analysis items and measurement methods
1.3 检测指标及评价方法
1.3.1 臭氧微气泡粒径的估算
Hadamard和Rybczynski推导的球形流体的理论方程[17]推测了球形微气泡从反应器底部缓慢上升的终端速度,如式(1)[18]:
(1)
式中:u为气泡的终端上升速度,单位为m/s;Δρ为空气和水的密度差,单位为kg/m3;g为重力加速度,取值9.8 m/s2;r为气泡半径,单位为m;μ为水的黏度,取值0.102 5 mPa·s;μ′为臭氧的黏度,取值1.56 mPa·s.当臭氧黏度可忽略时,式(1)整理得:
(2)
(3)
1.3.2 臭氧微气泡传质性能的评价
试验采用无传质增强的非稳定态方法对传质系数进行测定[1],采用间歇流式装置(如图1所示),向柱式反应器中补充定量的水,运行气液混合泵产生臭氧微气泡气水混合液.臭氧在向水中传质的同时伴随着分解,考虑到自来水中有机物含量较少,臭氧的衰减主要由于自分解作用,所以传质计算方法符合下式:
(4)

当臭氧向水中的传质速率与溶解臭氧的自分解速率平衡时,dct/dt=0,得下式:
(5)
式中:ce为臭氧在水中的平衡浓度,单位为mg/L.
将式(5)代入式(4),对dct/dt从0→t积分,整理得下式:
(6)
kLa+k即为臭氧的表观传质系数,该系数考虑了液相臭氧浓度受气液传质速率及臭氧分解速率的共同作用.
2 结果与讨论
2.1 臭氧微气泡的粒径估算与测量
试验装置产生微气泡的粒径检测如图2所示.显微镜目视范围内,溶液中富含大量微米级气泡,直径约20~50 μm.

图2 电子显微镜下微气泡的粒径测量图Fig.2 Measurement image of microbubble size under electron microscope
气泡上浮距离取量筒高程0.58 m,观察到的气泡消失时间约为400 s.通过式(2)、(3)能够得出气泡的平均粒径约为42.66 μm,这与显微镜观察到的粒径量级和大小结论相符.
2.2 臭氧微气泡的溶解及传质特性
2.2.1 pH的影响
试验控制臭氧的进气浓度保持在110 mg/L,臭氧进气流量0.06 L/min,系统压力0.19 MPa,水温15 ℃,采用NaOH和HCl溶液(C=1 mol/L)调整水样pH,探究水样在pH 3、5、7和9不同条件下的传质过程.液相臭氧浓度ct的变化结果如图3所示.利用式(6)对不同pH下臭氧的表观传质系数kLa+k进行拟合,进一步分析臭氧的溶解速率,结果如4所示.模型拟合结果用线性拟合系数R2表示,来判断回归方程的拟合程度,该模型拟合结果均大于0.96.随着水样pH由3、5、7至9逐渐增加,表观传质系数kLa+k降低,分别为0.161、0.137、0.116及0.104 min-1.
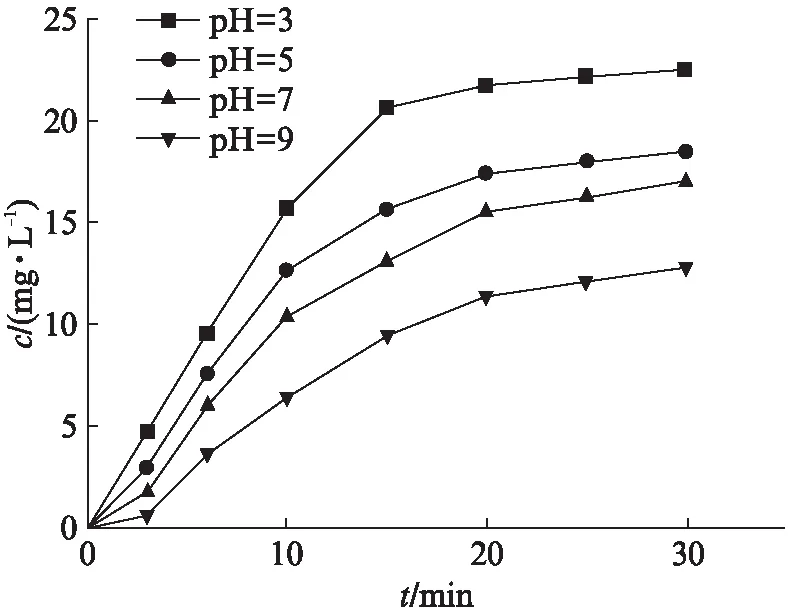
图3 pH对臭氧溶解的影响Fig.3 Effect of pH on ozone dissolution

图4 pH对传质系数的影响Fig.4 Effect of pH on mass transfer coefficient
液相臭氧浓度(ct)随着时间的推移而增加,最终达到稳定状态.反应初15 min液相臭氧浓度迅速上升30 min左右基本达到平衡.当pH为3时,液相臭氧浓度在15 min即可达到20.7 mg/L,而在pH为9时约为9.5 mg/L.这是因为随着溶液pH的增加,水中OH-含量增多,引发自由基链反应,催化臭氧分解[19].这表明当保持臭氧进气流量、浓度、系统压力、水温等因素相同时,液相臭氧浓度及传质速率随pH的降低而增大.
2.2.2 水温的影响
不同水温对臭氧气体的溶解存在影响,如图5所示,在15、20、30和40 ℃下臭氧在水中的溶解度及液相臭氧浓度的变化存在差异.试验控制臭氧进气浓度保持在100 mg/L,进气流量0.06 L/min,系统压力0.20 MPa,水样pH 7.5.当时间为15 min,水温分别为15、20、30及40 ℃时,液相臭氧浓度依次为15.54、13.15、8.96及6.15 mg/L.利用式(6)对不同水温下的表观传质系数(kLa+k)进行拟合,结果如图6所示.模型拟合结果用线性拟合系数R2表示,来判断回归方程的拟合程度,该模型拟合结果均大于0.98.随着水温由15、20、30至40 ℃逐渐升高,表观传质系数降低,分别为0.154、0.135、0.119及0.105 min-1.
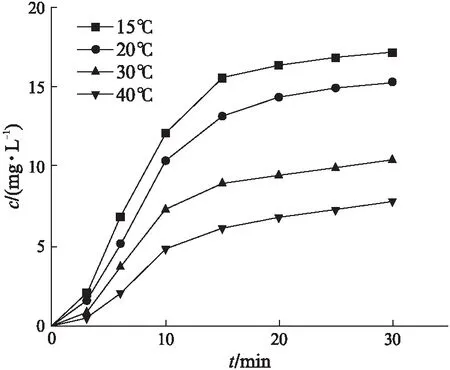
图5 水温对臭氧溶解的影响Fig.5 Effect of water temperature on ozone dissolution

图6 水温对表观传质系数的影响Fig.6 Effect of water temperature on mass transfer coefficient
20 min后液相臭氧浓度的上升幅度较之前减缓,臭氧在水中的溶解服从亨利定律[20],臭氧气体在溶液中的溶解度随其平衡压力的增加而增大.所以随着通气时间的增加,臭氧在水中的平衡压力逐渐减小,其溶解度也随之减小,浓度增加的趋势逐渐变缓,趋于饱和.随着水温的升高,臭氧的自分解速度加快,所以当保持其他因素相同时,降低水温可以有效提升臭氧的溶解度[21-23]及溶解速率,有利于制取高浓度臭氧水,这与Rischbieter等[24]的研究结果基本一致.
2.2.3 进气流量的影响
试验控制臭氧进气浓度保持在100 mg/L,水样pH 7.5,系统压力0.12 MPa,水温15 ℃,进气流量分别调节为0.06、0.10、0.15和0.20 L/min,不同进气量条件下液相臭氧浓度随时间的变化如图7所示.利用式(6)对不同进气流量下的表观传质系数进行拟合,结果如图8所示.模型拟合结果用线性拟合系数R2表示,来判断回归方程的拟合程度,该模型拟合结果均大于0.97.随着进气流量由0.06、0.10、0.15至0.20 L/min逐渐增加,表观传质系数增加,分别为0.111、0.133、0.145及0.165 min-1.

图7 臭氧进气流量对臭氧溶解的影响Fig.7 Effect of ozone inlet flow rate on ozone dissolution

图8 臭氧进气流量对表观传质系数的影响Fig.8 Effect of ozone inlet flow rate on mass transfer coefficient
由图7可知,当进气流量由0.06 L/min逐渐增加时,液相浓度达到饱和的时间分别为18、14、10以及8 min,臭氧进气流量越大,同一时刻液相臭氧浓度ct越高,更快达到饱和.经过30 min,进气流量为0.06 L/min的试验组,单位时间内进入溶液的臭氧量有限,所以臭氧水中溶解浓度显著低于其他3组,仅为11.45 mg/L.但是若气体流量过高,表观传质系数kLa+k值反而会降低,主要原因是随着气体流量的增加,气泡尺寸增大,比表面积减小,同时由于湍流强度增加,部分气泡破裂,导致气泡密度减小,气液传质条件变差[25-27].
2.2.4 压力的影响
试验控制臭氧进气浓度保持在100 mg/L,进气流量0.06 L/min,水温15 ℃,水样pH 7.5,系统压力分别调节为0.12、0.15、0.20和0.25 MPa,不同的压力条件下液相臭氧浓度随时间的变化如图9所示.利用式(6)对不同系统压力下的表观传质系数kLa+k进行拟合,结果如图10所示.模型拟合结果用线性拟合系数R2表示,来判断回归方程的拟合程度,该模型拟合结果均大于0.98.随着系统压力由0.12、0.15、0.20至0.25 MPa逐渐增加,表观传质系数kLa+k增加,分别为0.111、0.129、0.146及0.182 min-1.

图9 系统压力对臭氧溶解的影响图Fig.9 Effect of system pressure on ozone dissolution

图10 系统压力对表观传质系数的影响Fig.10 Effect of system pressure on mass transfer coefficient
液相臭氧浓度在前10 min的运行过程中迅速增大,然后增势变缓,在20~30 min后趋向稳定.当反应系统压力在0.12~0.25 MPa时,随着压力的增加,液相臭氧浓度逐步提高,这是亨利定律在臭氧溶解系统中的体现.
3 结 论
本研究建立了一种新型臭氧微气泡产生系统,考察了pH、水温、进气流量、压力等条件对水溶液中臭氧微气泡溶解特性的影响.结果表明:
1) 建立的该系统有较好的微米级气泡产生效果,气泡平均粒径约为42.66 μm.
2) 低pH、低水温、高进气流量和高的系统压力可以提高臭氧微气泡的溶解传质速率.其中,压力的影响最为显著,当压力由0.12 MPa上升至0.25 MPa,臭氧的表观传质系数kLa+k由0.111 min-1提升至0.182 min-1,提高64%.

