全内镜下腰椎椎间融合术治疗腰椎退行性病变伴腰椎失稳的早期临床疗效
郭时空,高全有,周程沛,袁一方,钱 澍,宋 扬,钱济先,高浩然
(空军军医大学唐都医院骨科,陕西西安710038)
腰椎退行性病变是引起中老年患者腰腿痛的常见病因,其中以腰椎间盘突出症、腰椎管狭窄症发病率较高。在椎间盘退变的基础上,很多患者合并腰椎失稳,最终需要外科手术治疗来缓解临床症状。腰椎椎间融合术是目前公认的治疗腰椎退行性病变伴腰椎失稳的金标准[1]。后路腰椎椎间融合术(posterior lumbar interbody fusion,PLIF)和经椎间孔腰椎椎间融合术(transforaminal lumbar interbody fusion,TLIF)是临床上常用的手术方式,但手术创伤大,术中出血量多,术后易发生顽固性腰痛、血肿、感染等并发症[2-3]。
随着微创脊柱外科的发展,微创经椎间孔腰椎椎间融合术(minimally invasive transforaminal lumbar interbody fusion,MIS-TLIF)已普遍应用于临床,很好地解决了出血量多、软组织损伤大等问题[4-6]。但是,术中仍有很多困扰,如仍有部分肌肉遮挡视野、通道摆放位置欠佳导致对侧减压不够充分等[7]。近年来,脊柱内镜已经受到越来越多的脊柱外科医师的青睐,从最初的单纯髓核摘除,到全内镜下椎管内减压,随着手术技术的不断提高和手术器械的不断完善,其适应证也越来越广泛。已有学者报道全内镜下腰椎椎间融合术(endoscopic lumbar interbody fusion,Endo-LIF)治疗腰椎退行性病变,并取得很好的临床疗效[8-9]。空军军医大学唐都医院骨科自2019年1月至2020年6月采用Endo-LIF治疗腰椎退行性病变伴腰椎失稳22例。现将结果报道如下。
1 资料与方法
1.1 纳入与排除标准
纳入标准:①临床表现为腰痛伴下肢放射痛和(或)间歇性跛行,伴或不伴下肢感觉、肌力障碍;②影像学表现为单节段腰椎间盘突出或腰椎管狭窄,伴腰椎失稳(腰椎过伸过屈位X线示相邻椎体间位移≥3 mm,或上下终板角度变化≥10°[10]),且查体与影像学资料相符;③所有患者经保守治疗至少3个月无效,日常生活严重受影响;④术前检查无明显手术禁忌证。
排除标准:①Ⅱ°及以上腰椎滑脱、重度椎管狭窄[8];②既往曾有腰椎手术史,或有腰椎骨折、肿瘤、感染等其他疾病;③术前检查有明确手术禁忌证。
1.2 一般资料
本组22例,其中男10例,女12例;年龄56~72岁,平均(61.45±4.44)岁。均为单节段手术,其中L3-L42例,L4-L511例,L5-S19例。诊断腰椎间盘突出10例,腰椎管狭窄12例,所有患者均伴有腰椎失稳,临床表现均为不同程度腰痛伴下肢放射痛,其中9例伴间歇性跛行。合并高血压6例,冠心病1例,糖尿病2例,甲状腺功能减退1例。
1.3 手术方法
以L4-L5节段为例(使用器械为Joimax Endo-PLIF镜下融合工具,图1):患者全身麻醉成功后取俯卧位,垫硅胶垫使腹部悬空,调整手术床角度使椎板间隙尽量张开,尽量使椎间隙垂直于水平面。C臂机透视体表定位,定位L4-L5症状侧关节突关节及双侧椎弓根体表投影。术区常规消毒铺巾。沿症状侧关节突关节体表投影处切开皮肤、皮下组织及深筋膜,长约1.5 cm。置入穿刺针,沿穿刺针逐级放入软组织扩张管,放置工作通道。撤除软组织扩张管并放置大通道内镜(iLESSYSDelta镜)。镜下清理关节表面软组织,显露骨性结构,确定L4下关节突及椎板下缘。镜下环钻切除L4下关节突及部分椎板,扩大椎板间隙,显露黄韧带附着部。再使用椎板咬钳或镜下环钻去除部分L5上关节突内侧缘,充分减压骨性侧隐窝。充分止血后确定椎间盘位置,然后更换U形外套管,将神经根推向中央,保护神经组织。显露椎间盘,切开纤维环,摘除髓核组织,使用各种镜下终板处理工具直视下刮除软骨终板,处理椎间隙,直至终板点状渗血。镜下确认神经根被推向中央后撤出内镜。透视下放置融合器试模,确认融合器大小。放置植骨漏斗,置入自体骨粒及同种异体骨粒。透视监视下放置融合器(根据椎间隙大小可选择传统PEEK融合器或可膨胀型融合器),并确认融合器大小及位置。重新放回内镜,镜下再次确认融合器位置合适,神经无卡压。剥离黄韧带附着点,咬除肥厚黄韧带,探查见神经根松解彻底。对于中央管狭窄的患者,可调整工作套管的倾斜角度,完成单侧入路双侧减压,沿棘突根部,对对侧椎板、侧隐窝进行减压。探查硬膜囊及神经根减压彻底后,可撤除大通道内镜及工作通道。再行L4、L5双侧经皮椎弓根螺钉植入术。减压区放置负压引流管1根,逐层缝合各伤口。
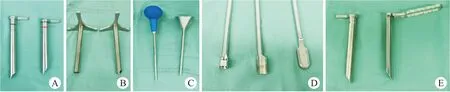
图1 术中所用特殊器械Fig.1 Special instruments used during the operation
1.4 术后处理与随访
术后预防性使用抗生素24 h,常规使用脱水及营养神经药物2~3 d。术后第2天可根据引流量情况拔除引流管。复查X线见内固定无异常后,可佩戴腰围适当下地活动,避免久坐及腰部剧烈活动。术后常规佩戴腰围4~6周。记录手术时间、术中出血量、术后并发症、住院时间等指标。通过门诊、电话或网络随访等方式,收集比较术前、术后1周、术后1个月、术后3个月、术后6个月及末次随访时腰腿痛视觉疼痛模拟评分(visual analogue scale,VAS)和Oswestry功能障碍指数(Oswestry disability index,ODI)末次随访时采用改良MacNab标准进行疗效评定。
1.5 统计学分析
采用SPSS 20.0软件进行数据统计分析。服从正态分布的计量资料用均数±标准差(xˉ±s)表示,术前与术后各时间点比较采用单因素重复测量方差分析法,多重比较采用Bonferroni法。非正态分布的计量资料用中位数(最小值~最大值)表示,术前与术后各时间点比较采用Friedman检验,多重比较采用Wilcoxon符号秩检验。以P<0.05为差异有统计学意义。
2 结 果
22例患者均顺利完成手术,手术时间180~240 min,平均(206.59±15.69)min,术中出血量50~120 mL,平均(92.73±22.29)mL。1例术中出现硬膜囊撕裂,术后患者未诉特殊不适,经严密缝合切口并加压包扎后未做特殊处理。住院时间7~13 d,平均(8.82±1.53)d。22例均获得门诊、电话或网络随访,随访时间6~18个月,平均(10.95±3.34)个月。术后各时间点腰腿痛VAS评分和ODI与术前相比,均明显降低,差异有统计学意义(P均<0.05),术后各时间点腰腿痛VAS评分和ODI两两比较,差异有统计学意义(P均<0.05),结果见表1。末次随访时改良MacNab疗效评定:优17例、良3例、可2例,优良率为90.91%。典型病例见图2。
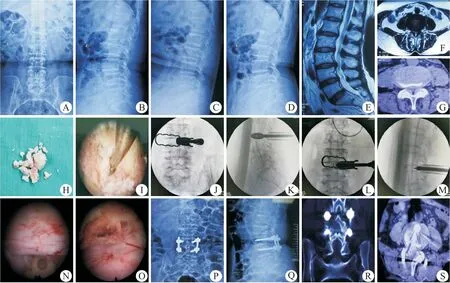
图2 典型病例的术前、术后影像学表现及术中资料Fig.2 Preoperative and postoperative imaging findings and intraoperative data of typical cases

表1 患者术前与术后各随访时间点腰腿痛VAS评分和ODI比较Tab.1 Comparison of VAS scores for lower back pain and leg pain and ODI between preoperative and postoperative followup periods (n=22)
3 讨 论
3.1 Endo-LIF的可行性
腰椎椎间融合术是目前公认的治疗腰椎退行性病变伴腰椎失稳的标准术式,其中PLIF和TLIF使用较为广泛。但不管是后正中入路或者经椎间孔入路,均需不同程度的椎旁肌肉软组织剥离,这就可能导致肌肉的去神经化,进而使术后出现慢性顽固性腰痛等并发症,影响临床疗效。FAN等[11]研究对比了28例行单节段微创PLIF手术和31例行单节段传统开放PLIF手术患者的临床疗效,每组选16例患者行MRI检查评估术后多裂肌萎缩程度,研究结果发现,微创组术后背部疼痛和ODI较开放组均明显下降,微创组多裂肌萎缩程度较少,术中对肌肉的损伤与术后多裂肌萎缩和脂肪浸润显著相关,而多裂肌的退行性变和临床疗效显著相关。近年来,随着微创技术的发展,MIS-TLIF已逐渐取代传统开放后路椎间融合术。MIS-TLIF术中使用可扩张通道经Wiltse入路,很好地避免了椎旁肌的广泛剥离,同时对后柱结构损伤较小。但仍存在一些问题,如术中减压视野有限、无效视野显露过多、对侧减压范围不确切等[7]。
脊柱内镜技术近年来发展迅猛,在单纯减压方面的优势已被众多脊柱外科医师公认[12-13]。随着手术技术的不断成熟和手术器械的不断完善,脊柱内镜技术的临床适应证也越来越广,从最初治疗腰椎间盘突出症,到使用大通道内镜治疗腰椎管狭窄症,均取得了满意的疗效。目前已有学者报道使用内镜辅助腰椎椎间融合术[8-9]。与MIS-TLIF相比,Endo-LIF使用经皮固定通道,更好地减少了对椎旁肌肉的损伤。同时内镜下操作更加精准,按需完成骨性减压,对骨性结构的破坏更少。而且手术在水介质下完成,视野更加清晰,尤其在处理上下终板植骨床时可以清晰地观察植骨床是否准备充分。
3.2 Endo-LIF术中注意事项
3.2.1 手术入路的选择Endo-LIF有经椎间孔入路(endoscopic transforaminal lumbar interbody fusion,Endo-TLIF)和经椎板间隙入路(endoscopic posterior lumbar interbody fusion,Endo-PLIF)两种。Endo-TLIF需充分显露Kambin三角,做好关节突成形,为融合器的置入提供一个安全可靠的通道,否则极易损伤神经根[14]。Endo-PLIF与传统开放PLIF手术解剖类似,医师更加熟悉解剖结构,但术中减压等过程可能对神经根和硬膜囊干扰过多。两种手术技术的适应证不尽相同,对于单侧症状采取经椎间孔入路,对于中央椎管狭窄或双侧根性症状采取经椎板间入路,更有利于减压的操作。无论哪种入路,采取更优的手术策略尤为关键。以Endo-PLIF为例,先显露下关节突内缘与上位椎体下椎板交界处,并向尾端分离显露上关节突内缘与下位椎体上椎板交界处,以上述骨性结构为解剖标志,逐步完成骨性减压。显露黄韧带后切忌不能盲目进入椎管,以免造成神经损伤或者造成椎管内出血,妨碍后续手术进程。我们采取先行椎间融合,再进行椎管减压的步骤,这样的操作优点是保留黄韧带结构,可以保护椎管内神经组织,减少椎管出血,在清晰的内镜视野下完成椎间融合的步骤,最后进行黄韧带切除和椎管减压。
3.2.2 终板处理 传统的椎间融合术在处理椎间隙时无法监视操作的深度,只能依靠术者的手感和经验,一旦突破前纵韧带,极易损伤前方血管,造成严重的并发症[15-16]。此外,使用传统较为锋利的工具(刮刀、绞刀等)处理终板时可能造成终板的损伤,终板切割、融合器沉降等并发症的发生率随之升高[17]。而Endo-LIF是在内镜的监视下完成椎间终板处理,不但安全可靠,而且镜下视野清晰,终板处理得更加精准、彻底,同时可以避免过度处理造成终板损伤,防止术后融合器下沉、融合率降低等并发症[9]。但此技术仍然存在不足:由于工具和通道角度的限制,对于终板处理的广度不如传统手术,植骨床的面积较小,植骨量较少,融合率有待进一步随访。相信随着工具的改进、技术的提高,这一问题能够得到有效解决。
3.2.3 融合器的置入技巧Endo-LIF面临的一个主要问题就是融合器的置入受限于通道的直径,根据工作通道直径不同,Endo-LIF分为普通型和大通道型。传统椎间融合术所使用的融合器对于普通内镜的工作通道而言,相对较大,无法置入。因此,有学者报道只植骨而不使用椎间融合器[18],但该术式面临的主要问题就是脊柱中柱缺乏支撑结构,稳定性无法保证。目前,Endo-LIF临床上常用的融合器主要分为金属可膨胀(或不可膨胀)融合器、PEEK材料不可膨胀融合器及多聚物网状可膨胀融合器等[14]。使用普通外套管时一般采用可膨胀式融合器,其中以金属可膨胀融合器居多,它可以小尺寸经Kambin三角置入椎间隙,而后撑开扩大,从而提高融合器置入的安全性;但是,容易出现融合率下降、融合器损坏等并发症[19]。本研究团队所使用的融合器为PEEK材料不可膨胀融合器,术中使用外径约15 mm的U形外套管,可以保证不同尺寸融合器置入的顺利完成。在放置融合器时使用U形外套管挡开神经根,镜下确认神经根被安全保护后再撤除内镜,同时助手稳定好U形外套管,全程可在术中透视下监视进行,大大降低了神经根损伤的风险。
3.3 本研究的不足之处
本研究属于回顾性组内对照研究,存在一定局限性,下一步将纳入对照组或进行随机对照研究。此外,本研究样本量相对较少,还需要进一步增加样本量,同时随访时间较短,需进一步观察远期疗效及融合率等。
4 总 结
Endo-LIF治疗腰椎退行性病变伴腰椎失稳的早期临床疗效较为满意,具有创伤小、恢复快等优点。

