脊柱内镜下融合技术治疗退行性腰椎疾病的早期疗效
王 放,王永虎,乔 浩,刘东藩,郭 栋,王 瑞,王 栋,李浩鹏,李锋涛
(1.西安交通大学第二附属医院骨二科,陕西西安710004;2.西宁市第二人民医院骨科,青海西宁810003)
退行性腰椎疾病好发于中老年人群,是引起中老年腰腿痛的主要原因之一。随着近年全球老龄化的加剧,退行性腰椎疾病发病率也显著升高,其治疗手段受到广泛关注[1]。患退行性腰椎疾病者不仅疼痛,还常引起脊柱不稳、腰椎滑脱等症状,大多数患者经过保守治疗能缓解或治愈,但仍有一部分患者治疗效果不佳,需行腰椎融合术治疗[2-3]。传统的后路腰椎椎间融合术(posterior lumbar interbody fusion,PLIF)是治疗腰椎失稳症的常用术式,具有腰椎节段适用范围广、减压充分等优点,但也存在术中椎旁肌剥离损伤较重、术后恢复慢等缺点[4]。脊柱内镜技术为腰椎退变性疾病的治疗带来了新的契机,其具有损伤小、术后恢复快等优点,越来越受到脊柱外科医师和患者的青睐[5-7]。基于此,本研究回顾性分析本院31例行脊柱内镜下融合术(endoscopic lumbar interbody fusion,Endo-LIF)治疗退行性腰椎疾病患者的临床资料,评估其应用效果,现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2019年6月至2021年5月本院31例行Endo-P/TLIF治疗的退行性腰椎疾病患者的临床资料。31例患者中男17例,女14例;年龄49~72岁,平 均(60.15±1.72)岁;BMI 18~33 kg/m2,平 均(26.08±0.77)kg/m2,随 访 时 间6~18(14±2.3)个月;单节段腰椎间盘突出症(lumbar disc herniation,LDH)或腰椎椎管狭窄症(lumbar spinal stenosis,LSS)19例(L2/31例,L3/43例,L4/59例,L5/S16例),Ⅰ°腰椎滑脱伴或不伴腰椎不稳9例,盘源性腰疼3例。
1.2 纳入与排除标准
纳入标准:①年龄40~80岁;②符合Hanley有关腰椎退变性不稳的诊断标准(前屈-后伸X线椎体移位>4 mm,或角度变化>11°)或者LDH或LSS患者,有明显症状且经过严格保守治疗无效或者保守治疗期间症状加重者;③有盘源性腰疼,根据中华骨科学会脊柱学组腰背痛手术评分标准小于6分(分值≥16分为优,15~11分为良,10~6分为可,5~0分为差);④接受Endo-P/TLIF治疗;⑤有完整的临床及随访资料;⑥患者及家属签署知情同意书,且获取医院伦理委员会审查通过。
排除标准:①有基础疾病不能耐受麻醉;②病变节段既往手术史;③腰椎畸形或严重的椎间盘钙化、Ⅱ°及Ⅱ°以上腰椎滑脱经皮螺钉难以复位;④体质指数(BMI)>35 kg/m2;⑤伴腰椎创伤、感染或严重骨质疏松;⑥沟通障碍,依从性差。
1.3 手术方法
以单节段腰椎间盘突出症(L4/5)为例:麻醉成功后,患者取俯卧位,用克氏针及C臂机透视定位L4/5间隙并标记,常规消毒铺巾。16G穿刺针穿刺置于L4/5椎间隙棘突右侧,拔除针芯,放置导丝,沿导丝放置工作套管,C臂机下定位工作套管放置良好;连接椎间孔镜,探查显露L4右下关节突和L5右上关节突,用环钻切除部分关节突骨质,显露L4/5间隙右侧黄韧带,咬除部分黄韧带,放置工作套管,可见L5神经根及脊髓,应用髓核钳取出脱出的髓核组织,射频消融残缘的髓核及破碎的纤维环。铰刀及刮勺刮除剩余髓核组织及终板,冲洗椎间隙后应用植骨漏斗植入颗粒骨,放入带自体骨椎间融合器。探查硬脊膜及神经根无明显受压后,取出内镜及工作套管,缝合伤口。X光机引导下于L4/5双侧植入椎弓根螺钉,X线透视示螺钉位置良好,测量双侧钛棒,应用置棒器放入连接钛棒,透视位置良好,螺帽固定,再次透视椎间融合器及钉棒位置良好。生理盐水冲洗双侧伤口,清点手术器械敷料无误后,依次缝合伤口,放置引流皮片,无菌敷料覆盖。
1.4 术后处理
术后常规用二代头孢48 h预防感染,小剂量激素3 d减轻神经根水肿,口服非甾体类止痛药物缓解疼痛,24 h内拔除引流皮片,术后第2天在支具保护下下床活动,术后观察3~5 d无异常后出院。腰部支具保护8周,门诊随诊。
1.5 观察指标
1.5.1 手术相关资料 记录患者术中出血量、透视次数、手术时间、住院时间、术后并发症。
1.5.2 量表评分指标 ①末次随访采用中华骨科学会脊柱学组腰背痛手术评分标准(分值≥16分为优,15~11分为良,10~6分为可,5~0分为差)。优良率=(优+良)/总例数×100%。②以视觉模拟评分(visual analog scale,VAS)评估患者手术前、术后即刻及末次随访疼痛程度。③以Oswestry功能障碍指数(Oswestry disability index,ODI)评价患者手术前、术后即刻及末次随访受疾病影响功能障碍程度。
1.6 统计学分析
数据采用SPSS 18.0软件进行统计学分析,计量资料用xˉ±s表示,手术前后评分的比较采用重复测量方差分析,两两比较采用Bonferroni post hoc检验。P<0.05为差异有统计学意义。
2 结 果
2.1 31例患者围手术期及术后相关指标情况
本组患者手术时间为(134.80±34.98)min,术中出血量(100.13±18.49)mL,平均透视时间(11.67±4.2)min,住院时间(6.65±0.17)d(表1)。术后出现并发症3例:1例患者麻醉苏醒后出现下肢肌力突然减弱,给予急诊切开探查发现血肿压迫神经根,给予清除后放置引流管缝合创面,术后给予小剂量激素、脱水及营养神经等治疗,并加强康复锻炼,下肢症状逐渐缓解;2例患者术后出现颈肩部及颈背部酸痛不适,考虑为类脊髓高压症,与手术时间较长、冲洗盐水刺激等有关,给予卧床休息后好转。手术操作过程和典型病例如图1和图2所示。
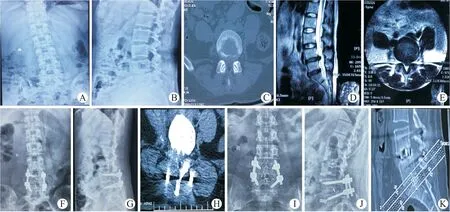
图2 典型病例展示Fig.2 Typical case presentation
表1 31例患者围手术期及术后相关指标Tab.1 Perioperative and postoperative related indicators of the 31 patients (±s)

表1 31例患者围手术期及术后相关指标Tab.1 Perioperative and postoperative related indicators of the 31 patients (±s)
总数(例)31手术时间(min)134.80±34.98术中出血量(mL)100.13±18.49透视时间(min)11.67±4.2住院时间(d)6.65±0.17并发症(例)3
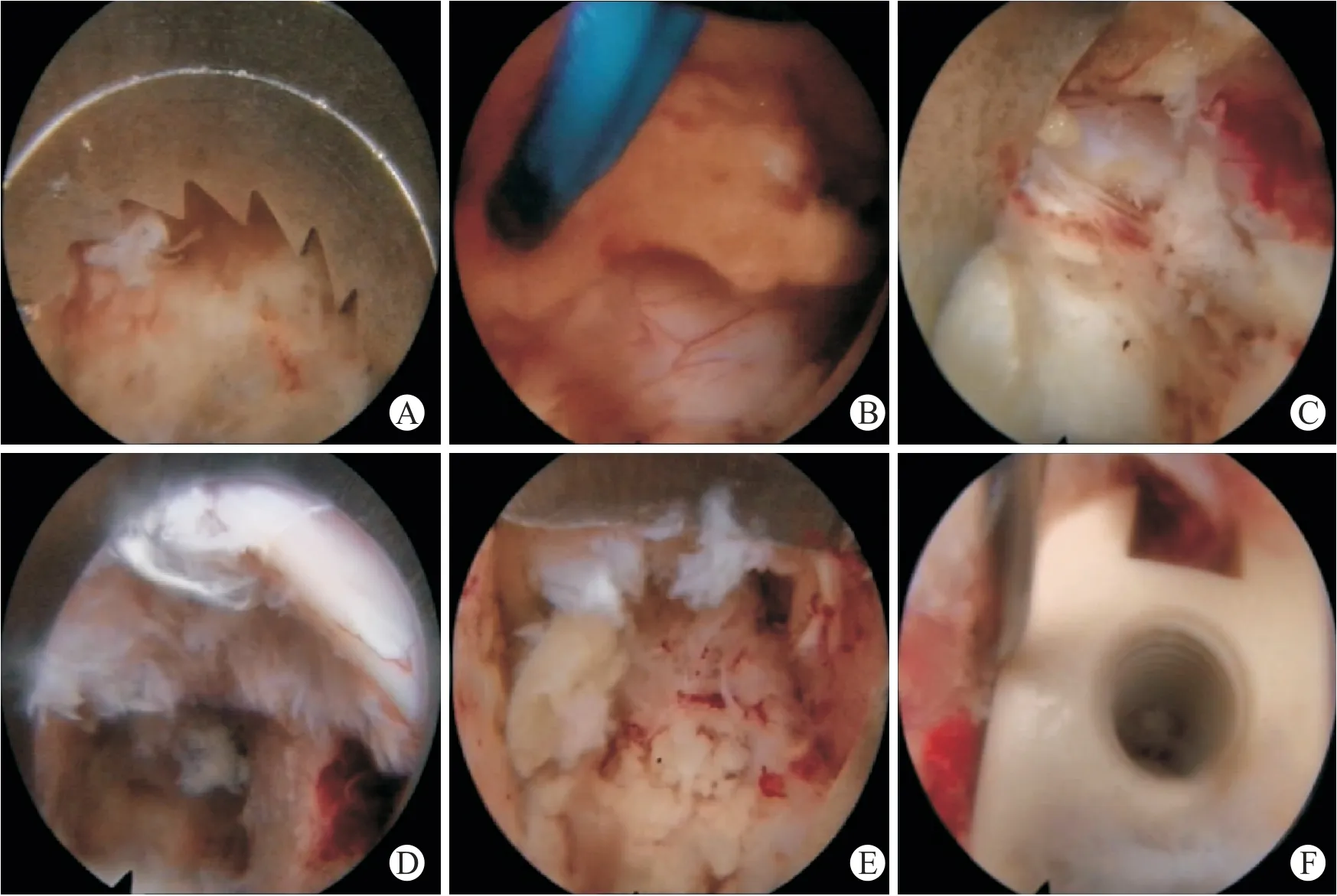
图1 脊柱内镜镜下融合图示Fig.1 Steps of endoscopic spinal interbody fusion
2.2 患者围手术期及术后评分量表指标比较
术后即刻和末次随访时患者VAS疼痛评分和ODI评分均降低(P<0.05),其中末次随访时VAS疼痛评分和ODI评分降低更加明显(P<0.05),差异有统计学意义。根据中华骨科学会脊柱学组腰背痛手术评分标准,优良率达97%(表2、表3)。
表2 脊柱内镜下治疗前后VAS评分和ODI评分的变化Tab.2 Changes in VAS score and ODI score before and after spinal endoscopic treatment (分,±s,n=31)

表2 脊柱内镜下治疗前后VAS评分和ODI评分的变化Tab.2 Changes in VAS score and ODI score before and after spinal endoscopic treatment (分,±s,n=31)
与术前比较,*P<0.05;与术后即刻比较,#P<0.05。
指标VAS疼痛评分ODI评分术前8.10±0.05 62.80±0.20术后即刻4.14±0.05*30.80±0.22*末次随访1.42±0.04*#18.77±0.15*#F 7 221.09 15 504.66 P<0.001<0.001
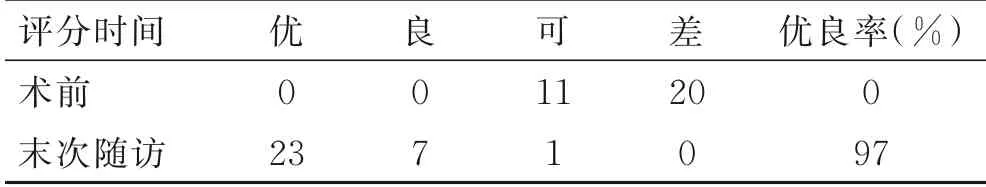
表3 中华骨科学会脊柱学组腰背痛手术评分(分)Tab.3 Surgical score of low back pain in Spinal Group of Chinese Orthopaedic Association
3 讨 论
腰椎退行性疾病是影响老年人群生活质量的常见原因,会导致机械性腰背痛、下肢放射性疼痛及间歇性跛行等症状[8],严重影响日常生活。腰椎椎体间融合术(lumbar interbody fusion,LIF)是治疗腰椎退行性疾病的常规术式之一,具有减轻疼痛、促进功能恢复、恢复腰椎生理性前屈、纠正畸形以及提高生活质量的作用[9]。PLIF术是既往治疗退行性腰椎疾病的主要术式,适用范围广,但术中存在组织剥离广泛、创伤较大等缺点[10]。20世纪90年代以来,科技发展迅猛,脊柱内镜技术得以快速发展,腰椎微创手术在所有脊柱手术量中占据越来越高的比例[11],也越来越受到脊柱外科医师的青睐。对此,本研究就脊柱内镜镜下融合技术对退行性腰椎疾病的疗效展开分析,为临床治疗提高参考依据。
本研究结果显示,脊柱内镜镜下融合技术在治疗退行性腰椎疾病中具有良好的临床效果,且并未发生严重的并发症。与其他类型的腰椎手术相比,Endo-LIF技术最大的优势是微创,除此以外,还有恢复快、住院时间少、费用低等其他优势,具体体现在以下方面:①手术切口小;②手术过程出血量少,且无需使用电凝,对肌肉及软组织影响较小,无需输血治疗;③Endo-LIF较常规手术创伤较小,对于老年人及全身基础情况较差的患者,该技术具有更高的安全性,且可以在手术过程中进行神经监护,术中产生对神经根的刺激时会有报警作用,降低了损伤神经根的可能性[12-13];④减压过程在内镜直视下完成,在骨性终板准备完成后,可在椎间孔镜下再次探查,监测软骨面的准备情况,脊柱外科医师在临床经验的基础上,直视下监测,更有利于完善的软骨下骨面的准备[12,14];⑤促进术后快速康复(enhanced recovery after surgery,ERAS)的进行,有助于减低住院时间及费用[15-17]。
在采用镜下融合技术治疗腰椎退行性病变时,需要注意以下几点:①镜下操作对于术者的解剖要求和微创技术要求较高,在刚开始操作时容易出现镜下“迷路”的现象。因此,建议术者在镜下融合前先熟练掌握经皮椎间孔入路椎间盘切除术(PETD)或经皮椎板间入路椎间盘切除术(PEID),保证术中良好的减压,必要时可在术中采用C臂机透视确认内镜位置。②对于术中出血的处理,镜下操作止血非常重要,建议在入路过程中就应该采用射频电极严密止血;并且通过控制性调节血压和提高冲洗水压力来控制椎管内静脉丛出血,尤其是在切除黄韧带和关节上突时,可以通过涂上骨蜡有效控制骨切除部位出血。③在神经根减压时,一定要注意保护硬膜,因为内镜手术视野有限,一旦发生硬脊膜撕裂,初期修复很困难,而且若术中硬脊膜撕裂未得到恰当有效的处理,则有可能导致持续的脑脊液漏、硬脊膜假性突出(pseudomeningocoele)形成,甚至头痛、恶心、腰痛等,更为严重的并发症包括神经根受压并出现神经损伤的症状、脑膜炎和颅内出血。
本系列研究出现并发症3例,1例患者表现为麻醉苏醒阶段突然出现单侧下肢肌力下降,即刻行术后CT见脊柱螺钉位置良好,与家属商议后决定切开探查,确定为血肿压迫,清理血肿后放置引流管,给予激素冲击、脱水及神经营养治疗并加强康复锻炼后神经症状逐渐缓解;反思此例可能为术中小血管出血,术后没有水压控制,加之感觉术中止血充分未放置引流管导致术后血肿压迫所致,吸取教训后,术后减压侧常规放置引流皮片后,未出现此类事故。术后2例表现为颈部酸困不适、烦躁,其中1例同时存在背部及头部疼痛,询问后表示可耐受,给予卧床休息处理后痊愈;回顾文献将其称之为“类脊髓高压症”,是指由多种脊髓、脊柱及其周围结构的血管性病变导致脊髓引流静脉回流受阻或椎管外静脉血逆流入椎管静脉系统,引起脊髓静脉系统压力增高、循环减慢,进而引发的脊髓功能受损的一组综合征。但本研究病例未出现肌力下降和大小便障碍等神经损伤的表现。目前对于脊髓高压症的发生机制尚不明确。国外学者JOH等[18]研究发现,术中发生颈部疼痛与灌洗液持续灌注引起硬膜外压力增加密切相关;CHO等[19]研究表明,术中持续时间过长和灌洗液输注速度过快,压力过高是引起头颈部疼痛的重要危险因素。而且,本研究随访时间较短,尚不能观察到融合率及远期并发症,未来有待于中长期随访观察其临床疗效及椎间融合效果。
4 结 论
本研究的初步结果显示,脊柱内镜下融合技术能够有效缓解退行性腰椎疾病临床症状,其优良率显著,且具有术中损伤小、术后恢复快等优点,是一种新的、有效的治疗方法。但本研究样本量较小,且本研究设计并非随机对照双盲实验,相关证据不够充分,还需要积累更多的样本量及更长时间的观察来确定脊柱内镜下融合技术在退行性腰椎疾病中的治疗价值。

