经皮椎弓根螺钉与Wiltse入路复位内固定术治疗无神经症状胸腰椎骨折的疗效对比
张波波,宋忠伟,黎巧玲,杨益民
(1.西安交通大学第一附属医院骨科,陕西西安710061;2.西安交通大学第一附属医院护理部,陕西西安710061;3.西安交通大学医学部,陕西西安710061)
脊柱骨折约占全身骨折的5%~6%,其60%没有下肢神经症状,而胸腰椎因其特殊的解剖和生物力学特性,该部位骨折约占全部脊柱骨折的50%[1]。脊柱骨折若治疗不当,可造成腰背部长期慢性疼痛,甚至致残致畸,严重降低患者的生活质量。手术治疗可以恢复脊柱生物力线,缩短卧床时间,减少后期并发症,是脊柱骨折常见治疗方法[2]。胸腰椎骨折传统的手术方式包括:前路手术、后路手术、前后路联合手术等[3]。其中经后路切开复位内固定术可以恢复椎体高度、矫正后凸畸形、恢复脊柱稳定性、实现椎管的间接性减压,因此是无神经症状椎体骨折最常用及经典的手术治疗方法[4]。但手术显露需广泛剥离椎旁肌肉,出血多,软组织损伤大,破坏后柱稳定性,可造成后期腰背部疼痛、无力[5],使临床效果受到一定影响,不利于患者的预后和早期恢复。
随着现代医学的不断发展与进步,外科微创治疗的理念逐渐成为共识,受到了医务人员以及患者的青睐。经皮椎弓根螺钉及Wiltse入路复位内固定术是近年来用于治疗无神经症状胸腰椎骨折的两种最为常用的微创手术方法[6]。微创治疗具有以下优势:手术创伤小,术中出血量少,最大程度避免了椎旁肌的不必要剥离,降低了肌肉和神经损伤,术后腰背部疼痛不适程度明显减轻,这些均有利于术后早期康复锻炼及胸腰椎功能恢复[7]。本研究应用前瞻性随机对照研究的方法评价经皮椎弓根螺钉与Wiltse入路复位内固定术两种方法的临床疗效,以期为患者选用最佳微创治疗方法提供参考。
1 资料与方法
1.1 纳入与排除标准
纳入标准:①胸11-腰2(T11-L2)的单椎体骨折;②受伤时间<2周;③椎体后壁无翻转骨块,椎管占位<50%,无明显下肢及马尾神经症状;④年龄18~60岁。排除标准:①骨质疏松性椎体压缩性骨折;②骨折椎体数≥2;③合并其他疾病难以耐受手术;④AOspine胸腰椎骨折分型为C型。
1.2 研究对象
本研究样 本量的 计算采用N=2(uα+uβ)σ/β的计算公式,检验水准α=0.05,检验效能1-β=0.90。通过公式计算得每组样本数N=51。根据纳入排除标准,共纳入2015年3月至2018年3月间108例无神经症状的胸腰椎骨折患者为研究对象。这108例患者的术前、术中以及术后随访的情况均有详细记录,因此对于本研究来说样本量充足。
按照随机分配原则,采用系统随机化法以个体为单位将108位患者随机分配到两组中,每组各54例。其中男性84例,女性24例;年龄20~57岁,平均44岁;病变椎体:T1112例,T1233例,L148例,L215例;其中单纯压缩骨折24例,爆裂骨折78例,屈曲牵张骨折6例。本研究获得医院伦理委员会审查通过,每位患者或家属均签署知情同意书。
1.3 手术方法
常规术前准备,患者均采用全身麻醉,取俯卧位,过伸牵引后按压手法复位,腹部垫空。
1.3.1 经皮椎弓根螺钉内固定组(A组) 透视下标记病椎及相邻椎体椎弓根皮肤投射点,消毒铺巾,旁开标记点1~1.5 cm,穿刺椎弓根至椎体后壁前3 mm,正侧位透视证实位置良好后,置入导丝,拔除穿刺针,置入合适直径攻丝,攻丝至椎体后壁前方1 cm处,再次透视证实位置良好后,退出攻丝,选择合适直径及长度椎弓根螺钉沿导丝置入。病椎选择长度为3.5 mm的万向螺钉,病椎上下相邻椎体选择长度4.5~5 mm单轴固定螺钉。正侧位透视证实螺钉位置良好后,选择合适长度纵棒并预弯弧度,沿近端螺钉切口经肌肉深层向远端穿入,正侧位透视证实纵棒位置良好后,各椎弓根螺钉外安装入保护套筒,尾帽锁紧一端,依次进行撑开及锁紧剩余螺钉。透视验证骨折椎体复位情况后依次断臂。各切口冲洗并严密止血后,依次缝合(图1)。

图1 经皮椎弓根螺钉复位内固定术的手术情况Fig.1 Surgical situation of minimally invasive percutaneous approach
1.3.2 Wiltse入路组(B组)透视下标记病椎及相邻椎体椎弓根皮肤投射点,以病椎为中心,取后正中切口,依次切开皮肤及皮下组织、腰背筋膜,于腰背筋膜下、肌肉表面向两侧分离,寻找多裂肌与最长肌间隙,手指钝形分开,触及关节突关节,透视明确椎体后,进一步暴露各椎体椎弓根螺钉进钉点,依次开口、加深、攻丝,置入合适长度及直径椎弓根螺钉。病椎选择长度为3.5 mm的万向螺钉,病椎上下相邻椎体选择长度4.5~5 mm单轴固定螺钉。正侧位透视证实螺钉位置良好后,选择合适长度纵棒并预弯弧度,直视下安装纵棒,依次撑开、锁紧。透视验证骨折椎体复位情况后,切口冲洗并严密止血后,依次缝合,关闭切口(图2)。

图2 Wiltse入路复位内固定术的手术情况Fig.2 Surgical situation of Wiltse approach reduction and internal fixation
1.3.3 术后处理所有患者均不放置引流管,术后第3天佩戴支具下地活动,复查正侧位X线片,观察1~2 d,若无特殊情况便办理出院,支具佩戴3个月。术后1个月、3个月、1年以及3年门诊随访,术后1年、3年行腰椎正侧位片评估骨愈合情况,必要时行CT评估后取出内固定。
1.4 观察指标
记录所有患者手术时间、出血量、切口长度、术中透视次数,术中及术后并发症,术后住院时间;术前、术后3 d及每次复查的视觉模拟评分法(visual analogue scale,VAS)评分;X线片测量术前及术后即刻、术后3个月、术后1年以及术后3年椎体前缘高度压缩率(病椎椎体前缘高度/相邻上下椎体前缘高度平均值)及Cobb角,术前及术后3个月、术后1年、术后3年Oswestry功能障碍指数(Oswestry disability index,ODI)。本研究主要研究指标为A组和B组的椎体前缘高度压缩率以及Cobb角,次要研究指标为两组的手术相关指标、VAS评分和ODI值。
1.5 统计学分析
采用SPSS 22.0统计软件。计量资料以±s表示,组间比较采用两独立样本t检验,组内比较采用重复测量设计的方差分析;计数资料的比较采用χ2检验。检验水准α=0.05,P<0.05表示差异有统计学意义。
2 结 果
2.1 两组患者围手术期情况的比较
A组手术时间平均为(89.0±6.6)min,术中平均出血量为(68.6±13.9)mL,术后平均住院时间为(4.9±0.6)d。而B组手术时间平均为(85.9±7.8)min,术中平均出血量为(72.9±13.8)mL,术后平均住院时间为(5.1±0.6)d。两组患者手术时间、术中出血量、术后住院时间均无统计学差异(P>0.05)。A组的术中透视次数平均28次,B组平均透视次数仅为8次(P<0.05);A组的切口总长度平均10 cm,B组切口长度平均为6 cm(P<0.05);两组均未出现术后感染,神经损伤以及椎弓根螺钉断裂等并发症,A组2例患者出现伤口脂肪液化,B组1例患者出现伤口脂肪液化,经过加强换药等处理后伤口均愈合(表1)。

表1 两组患者一般情况和围手术期指标的比较Tab.1 Patient demographics and perioperative indexes in the two groups
2.2 两组患者临床疗效随访情况
术后3 d、术 后1月、术后3月、术后1年以及术后3年随访,两组患者VAS评分及ODI值比较差异无统计学意义(P>0.05);但其均较术前有明显改善(P<0.05,图3)。B组术后、术后3个月、术后1年及术后3年随访的Cobb角以及椎体前缘高度压缩率明显低于A组(P<0.012 5),两组值较术前相比明显降低(P<0.012 5,表2)。

表2 临床疗效指标的比较Tab.2 Clinical efficacy indicators (n=54)
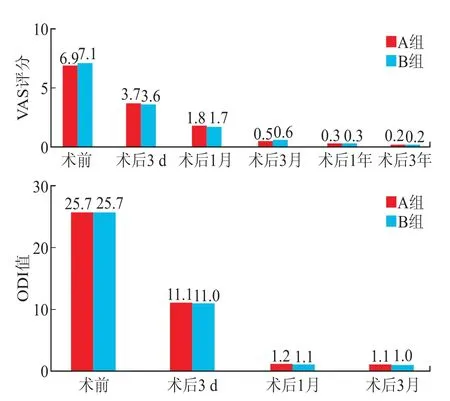
图3 两组VAS评分和ODI值比较Fig.3 Comparison of VAS score and ODI score between the two groups
3 讨 论
对于无神经相关症状的胸腰椎骨折来说,早期手术治疗可以有效地防止受伤椎体的进一步塌陷以及相关并发症的发生。传统的后路手术的流程是切开各层组织,广泛剥离椎旁肌肉至关节突外侧,显露椎弓根进钉点,完成置钉后撑开,完成手术,依次缝合,关闭切口[8],切开的目的主要就是显露进钉点。经皮椎弓根螺钉微创手术的理念就是通过体表穿刺,直接完成置钉,并进一步完成纵棒连接与撑开,从而避免肌肉的剥离。而Wiltse入路虽然也需要切开皮肤、皮下组织,但依然不剥离肌肉,而是沿多裂肌与最长肌间隙触及关节突外缘,仅仅需要显露进钉点即可,完成置钉后的操作过程与传统开放手术一样,操作结束后,肌肉间隙可自然闭合[9]。与传统的手术方式相比,两种微创手术均具有创伤小、出血量少、术后并发症少以及恢复快等优点,并且均可以保护椎旁肌肉和韧带复合体的完整性,有效减轻术后患者腰背部疼痛不适等症状的发生[10]。因此,两种手术方式均有利于减轻手术创伤、促进患者术后恢复。两组均未出现医源性神经损伤和术后感染等相关并发症,术后随访中也均未出现内固定松动,螺钉断裂以及脱出等情况,采用经皮椎弓根螺钉内固定术或Wiltse入路复位内固定术治疗后,患者术后、术后3个月、术后1年以及术后3年的Cobb角、椎体前缘高度压缩率以及VAS评分、ODI值较术前均有明显的改变,说明这两种微创技术均安全有效,对于术后恢复、功能重建以及缓解疼痛、促进患者康复锻炼方面均具有显著的临床效果。
本研究中两组患者的手术时间、术中出血量以及术后住院时间差异无统计学意义,而术中透视次数Wiltse入路组明显少于经皮组。经皮置钉手术的每一步操作均需要完全在透视下验证、调整,而Wiltse入路可在几乎类似于开放手术的视野下完成手术,这样就明显减少了透视次数,透视带来的医患双方的次生辐射损害则相应降低。Wiltse入路切口选择有两种,后正中单一切口和旁开的纵行两切口。PALMER[11]通过200例MRI测量Wiltse间隙距中线的距离:L1/2为7.9 mm,L2/3为10.4 mm,L3/4为16.2 mm,L4/5为28.4 mm,腰5-骶1(L5/S1)为37.8 mm。显示L1节段距中线的距离最短,在L5/S1节段距中线的距离最长,呈“八”字形。故在上腰椎(L1/2),单个正中切口即可行双侧椎旁肌间隙入路手术;而在下腰椎,Wiltse间隙的位置距后正中线较远,建议考虑采用双侧椎旁切口[12]。本研究所纳入的病变椎体均为胸腰段(T11-L2),故在Wiltse入路组均选择了后正中的单一小切口,通过深筋膜下的两侧分离到达多裂肌与最长肌间隙,借助各种拉钩进一步扩大、延伸视野,完成置钉、连棒及撑开。研究数据显示Wiltse入路组切口长度小于经皮组总长度,切口的微创性体现的更加突出。
传统后正中入路对椎旁肌的广泛剥离容易造成多裂肌以及相关神经(脊神经背支)的损伤[13],从而导致患者术后发生腰痛。多项研究结果从不同层面也已证实[14-15],两种微创技术均有效避免了椎旁肌肉的剥离,减少了创伤,最大程度的维持后柱的完整性,患者术后腰部不适的发生率可得到有效的降低,手术满意率明显提升[16]。本研究临床疗效随访结果可知,两组术后VAS疼痛评分和ODI功能指数均无显著的统计学差异,说明两种手术方式对于缓解患者疼痛以及术后恢复方面无明显差异。术后影像学指标显示,B组的术后Cobb角和椎体前缘高度压缩率明显低于A组,说明Wiltse入路对于病椎的高度恢复和纠正后凸畸形有更好的促进作用。经皮置钉组的撑开装置在体外,施加的撑开力无法直接作用于椎体后部,再加之皮肤、筋膜、肌肉组织的阻力,极大地限制了这种撑开的有效性[17]。而Wiltse入路的撑开过程完全相同于开放手术,牵张力量可直接作用于椎体后部,并且没有软组织阻挡,从而可完成更加有效的撑开,达到满意的复位效果。因此,经皮椎弓根内固定技术对伤椎畸形的矫正效果不及Wiltse入路手术,Wiltse入路更有利于减少后期因脊柱生理曲度改变所导致的腰背部疼痛。
综上所述,对于无神经症状的胸腰椎骨折,经皮椎弓根螺钉和Wiltse入路复位内固定都是安全有效的微创治疗方法。相较于经皮椎弓根螺钉内固定术,Wiltse入路复位内固定术可以实现可视化操作,从而减少术中透视次数,降低射线对医患双方的损害;且Wiltse入路手术切口较小,更符合微创理念。Wiltse入路组可以更好的恢复并维持伤椎高度,重塑脊柱生物力线。并且采用常规脊柱后路钉棒系统即可完成,无需特殊手术器械,相比于经皮椎弓根螺钉治疗费用较低,更易于推广普及。因此,选择Wiltse入路治疗无神经症状的胸腰椎骨折可能是一个更好的选择。

