复杂氧化物载氧体的调变策略及在过程强化中的应用
蔡润夏,李凡星
(北卡莱罗纳州立大学化工与生物分子工程系,北卡莱罗纳 罗利 27695-7905,美国)
引 言
随着全球气候变暖加剧,CO2减排已经成为各国发展的重要议题之一[1-2]。高能耗的工业生产过程导致了大量的CO2排放。据统计,2020年全球总CO2排放量中24.2%来源于工业生产[3]。从热力学第一定律上看,许多工业过程经过长期优化已经实现很高的热转化效率,但从第二定律角度却仍然不尽人意,其中尤为甚之的是化工产业[4]。典型的化工过程通常涉及多步流程,每步都会导致不同程度的不可逆,进而造成较高的㶲损失。虽然化学反应步骤普遍被认为是化工过程的决定性因素,化工生产的主要㶲损失却往往产生于分离步骤。例如,深冷空气分离是生产O2和N2的主要方式,但其㶲效率却不足25%[5]。这种极低的㶲效率在涉及分离的化工过程中并非个例:工业精馏的㶲效率通常低于24%[6],而海水淡化过程的㶲效率也低于21%[7]。因此,为了提高系统效率、降低CO2排放,耦合分离反应的过程强化策略备受关注,其中最为典型的就是化学链技术[8-17]。
典型的化学链流程通常利用载氧体将总反应拆分为两个(或多个)子反应,并通过载氧体实现氧气/氧离子的传递,从而实现产物分离、能量梯级利用等目的[18-21]。经过最近二十年的飞速发展,化学链技术已经逐渐从最初的燃料燃烧领域扩展到众多其他化工与能源生产领域,如燃料气化与重整、空气分离、催化脱氢、水裂解等[8,22-30]。由于不同的氧化还原反应中反应物与反应条件等存在着显著的差异,因此,设计与选择合适的载氧体是能否实现不同化学链过程的先决条件。量子化学、高通量计算以及机器学习的发展,使得越来越多新型载氧体被发现,也使得合理设计载氧体性能成为可能(图1)[31-35]。其中,针对不同流程,设计与调变相应载氧体的热力学性质,以期实现不同流程的最优化,是当前最为广泛探索的新领域[33-35]。本文将以化学链空气分离、氧化脱氢和热化学储能三个典型过程为例,阐述化学链过程中载氧体热力学性质的调变策略。
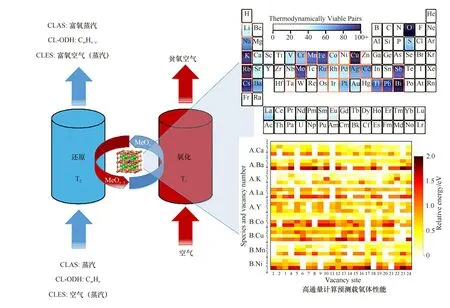
图1 化学链反应系统与载氧体热力学性质的计算预测示意图(右上图引自文献[35])Fig.1 Schematics of a chemical looping reaction system and computationally predicted redox properties of complex oxides(the upper right figure was cited from Ref.[35])
1 典型化学链流程的分析与讨论
氧气是众多化工和电力生产领域的重要原料之一,其主要通过空气分离获得。2021年,全球空气分离市场达到45亿美元,预计2026年底将达到59亿美元[36]。深冷空气分离技术是当前大规模氧气生产技术中最为成熟和最经济有效的方法。但即便如此,生产1kg氧气(95%纯度)仍需消耗0.78 MJ电能,㶲效率不足25%[37]。因此,若能改进现有空气分离技术,将会极大地降低工业流程的运行成本。化学链空气分离技术(chemical looping air separation,CLAS)是一种新兴的氧气生产方式。其利用载氧体的可逆氧化还原反应来实现氧气的吸收与释放[38-40]。由于载氧体对于氧气的吸收和释放具有100%的选择性,CLAS技术相比于传统采用沸石的变压空气分离技术,氧气的产率和纯度都有显著提升[41-42]。此外,CLAS技术的能耗相比于传统的空气分离技术也有显著降低[43-44]。
CLAS技术通常采用变压模式,载氧体在高氧分压条件下吸收氧气,之后在低氧分压条件下释放氧气[45]。任意载氧体的释氧过程可由式(1)表示:

吸氧和释氧过程可以分别用式(2)和式(3)表示[46]:
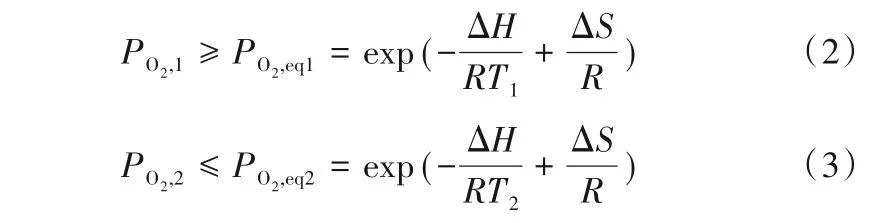
式中,PO2,eq为平衡条件下氧分压;ΔH和ΔS分别为载氧体释氧反应的焓变和熵变。由于高温容易导致金属氧化物烧结,并带来极高的能量损失,中低温运行条件(350~650oC)为CLAS技术的合理运行区间[47]。初步假设:释氧工况下氧分压为0.01 atm(1atm=101325Pa),吸氧工况下氧分压为0.14 atm(加压),且系统运行于恒温条件[43]。
图2所示为计算得到的CLAS技术中适宜采用的载氧体的热力学性质范围,其中典型的载氧体有YBaCo4O7、SrFeO3类复杂氧化物等[5,45,48-51]。从热力学角度,低温分离条件将有利于进一步降低系统能耗。因此,针对CLAS过程,理想的载氧体应具有较小的ΔH和ΔS,但同时需满足吸氧和释氧平衡的制约关系。虽然较低温度下载氧体反应活性会受到影响,近年来复杂氧化物的进展正逐步解决这个问题。相比于最初超过1000oC的运行温度,最新的CLAS载氧体的反应温度区间已显著降低[48]。除了开发适合低温反应、快速动力学性能的载氧体,CLAS技术发展的另一重要方向是商业应用中反应器及系统的设计、优化和大型化。而这也对于载氧体长期的循环稳定性提出了更高的要求[52]。在可预见的未来,相信随着以上问题的逐步解决,CLAS技术有望在氧气生产中占据重要的一席之地。
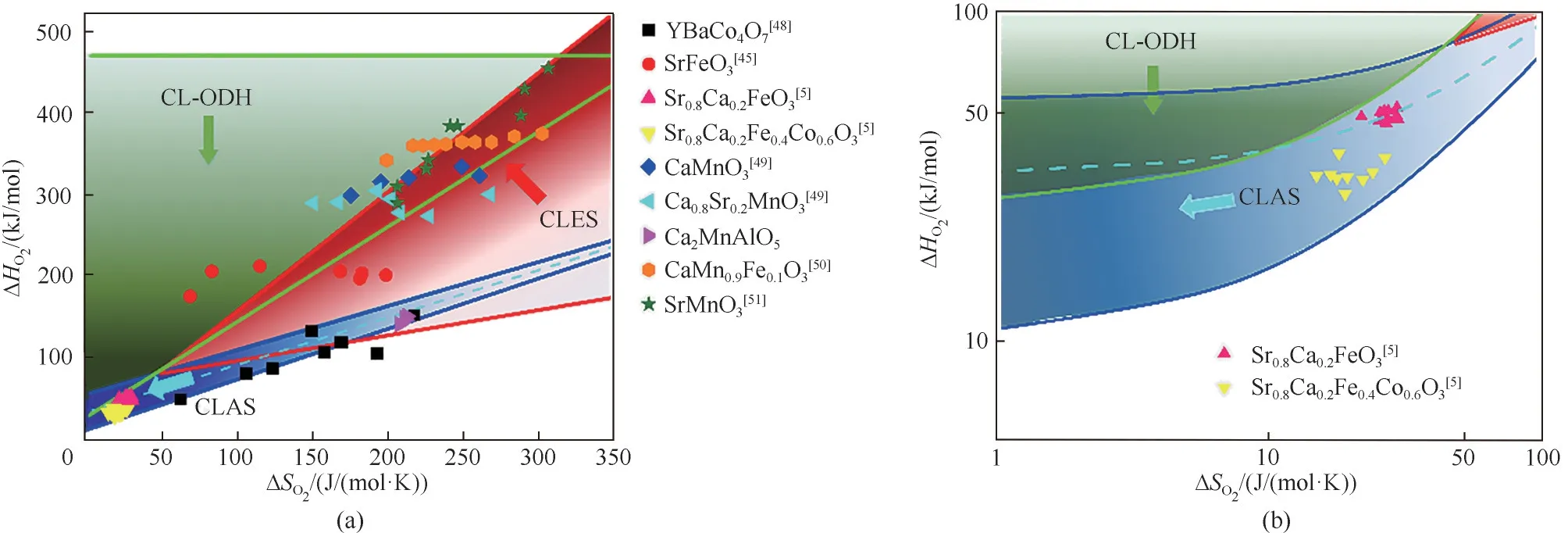
图2 针对不同化学链流程,载氧体热力学性质合适的分布区间:(a)全局视图;(b)低熵、低焓区域放大视图(部分数据点引自文献[5,45,48-51],Ca2MnAlO5数据源于本课题组正在进行的实验工作)Fig.2 Desired thermodynamic properties of complex oxides for different chemical looping process:(a)Overview;(b)Callout view of the low entropy and enthalpy region(Some data points were cited from Refs.[5,45,48-51],data for Ca2MnAlO5were collected from an on-going experimental study in the authors’research group)
许多大宗化学品的生产过程都是受到平衡限制的吸热反应,如乙烯、丙烯、苯乙烯等。这些反应过程都会受益于催化氧化过程[53-54]。CLAS技术可以取代低温空气分离技术,与传统化工过程直接结合,但是简单的耦合仍然会导致较高的投资成本。而近年兴起的化学链氧化脱氢(chemical loopingoxidative dehydrogenation,CL-ODH)技术则更具吸引力,可以直接将氧气分离过程与化学品生产流程相结合[55-61]。以乙烷高温CL-ODH制备乙烯为例,乙烷在高温条件下会裂解生成乙烯和氢气。载氧体在还原室内与燃料接触,选择性燃烧部分氢气,从而为裂解反应提供部分热量,并促进反应平衡向乙烯生成方向移动,随后载氧体在氧化室内与空气反应吸氧则可实现再生[62-68]。
传统乙烷蒸汽裂解过程是强吸热过程,需要通过燃料(如甲烷)燃烧提供额外能量,该过程会导致显著的㶲损失[69-70]。此前研究表明[71],若不考虑传热损失,仅考虑反应所导致的不可逆㶲损失,则理想条件下,乙烷蒸汽裂解的最低㶲损失为48kJ/mol C2H6,而乙烷CL-ODH最低㶲损失为34.6 kJ/mol C2H6。实际过程中,由于CL-ODH两个子反应存在明显的放热或吸热,子反应运行温度的差异也会导致额外的能量损失。通过热力学计算,可以简要比较两种乙烯制备方式的㶲损失,并确定CL-ODH过程中合适载氧体的热力学性质。
假设理想条件为该总反应为热中和,即氢气燃烧释放的热量恰好满足乙烷裂解所需能量,则总反应可由式(4)表示。化学链循环对应的还原子反应和氧化子反应分别如式(5)和式(6)所示:
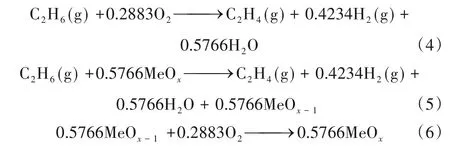
由于总反应热中和,载氧体吸氧的焓变直接影响还原过程和氧化过程的吸、放热,即式(5)和式(6)的吸、放热数值相等。通常而言,CL-ODH过程反应温度在700~900oC。若以800oC为例,为保证系统与热源间的传热,两者需存在传热温差。假设该温差为15oC,即载氧体氧化放热所需冷源温度T1=785oC,氧化脱氢过程吸热所需热源温度T2=815oC,环境低温热源为40oC。此外,假设热量输入和回收效率η1=95%,卡诺循环不可逆系数η2=75%,则系统换热的总㶲损失为:
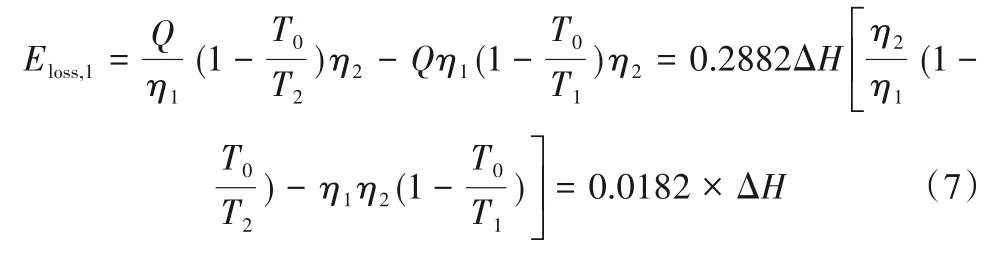
这表明若ΔH越大,则CL-ODH过程系统传热所导致的额外㶲损失越高。初步假设理想条件下乙烷蒸汽裂解㶲损失(48kJ/mol C2H6)的90%为最大允许㶲损失,则可以获得ΔH的上边界。但另一方面,过低的ΔH会导致材料热敏感性过强,且高温吸氧困难。为了保证载氧体在高温条件下能够吸收氧气,式(6)同样需要满足式(1)。假设操作区间在700~900oC,吸氧工况氧分压为0.2 atm,则可以获得CL-ODH过程载氧体的热力学性质的合适区间。如图2所示,CL-ODH过程适宜的载氧体典型代表之一是CaMnO3类复杂氧化物。以上计算也表明,温度控制是CL-ODH过程的重要挑战之一。这一方面表现为当前载氧体运行温度仍普遍较高,另一方面也表现为两个子反应的温差控制。此外,载氧体对于烯烃的选择性和单程收率、超长期循环稳定性等也是未来需要进一步优化和验证的重点方向[23,55]。
近年来兴起的基于载氧体的化学链热化学储能(chemical looping thermochemical energy storage,CLTES)技术,是直接利用载氧体吸氧和释氧过程能量的另一重要应用[72]。可再生能源能从根本上降低化石燃料使用、减少CO2排放,但其不稳定与间歇性的特点限制了其在电网中的比例[73]。储热技术能提供大规模、长时间的能量储存,并可直接与太阳能等中高温热源结合,是解决可再生能源的时空分布不均问题的重要途径之一[74]。现有最主流的储热技术为熔融盐储热[75]。但熔融盐的凝固风险、较窄的操作区间以及对储罐腐蚀等问题成为该储热技术发展的重要瓶颈之一[76]。基于载氧体的化学链热化学储能(CL-TES)技术具有较高能量密度,且可以打破传统熔融盐中低温运行壁垒,实现更高的能量利用效率,因此,近年来受到越来越多的关注[46,77-78]。
CL-TES技术通常采用变温运行模式,在高温条件T2下通入空气或蒸汽,载氧体在释放氧气的同时吸收热量。之后将系统降温至T1同时通入空气,载氧体在吸收氧气的同时释放热量[79]。吸氧(释放能量)和释氧(储存能量)过程仍可以用式(2)和式(3)表示。由于变温运行会导致较高的㶲损失,若载氧体能在较窄的温度区间内实现放热与吸热(即吸氧和释氧)过程,则可以实现较高的系统效率。同样假设热量输入和回收效率η1=95%,卡诺循环不可逆系数η2=75%,取式(2)和式(3)等式作为边界条件,则载氧体吸氧和释氧过程的吸、放热如式(8)和式(9)所示:
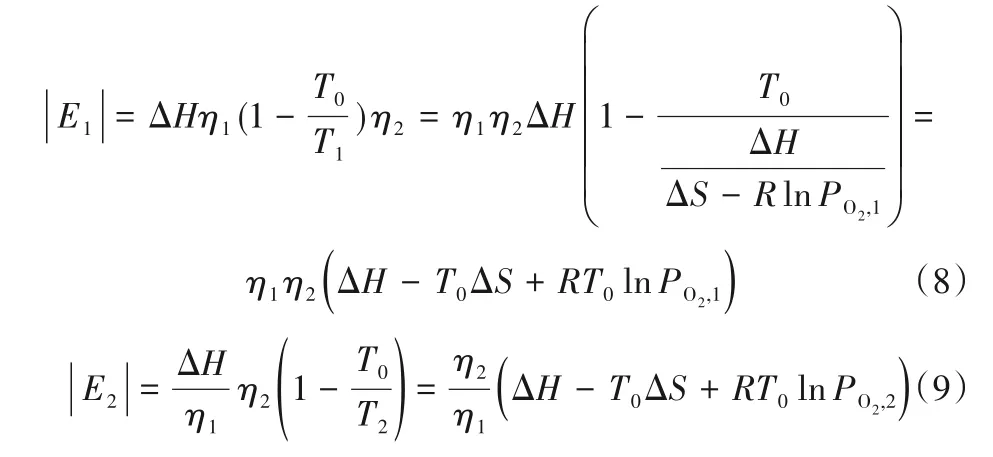
定义效率η3为:
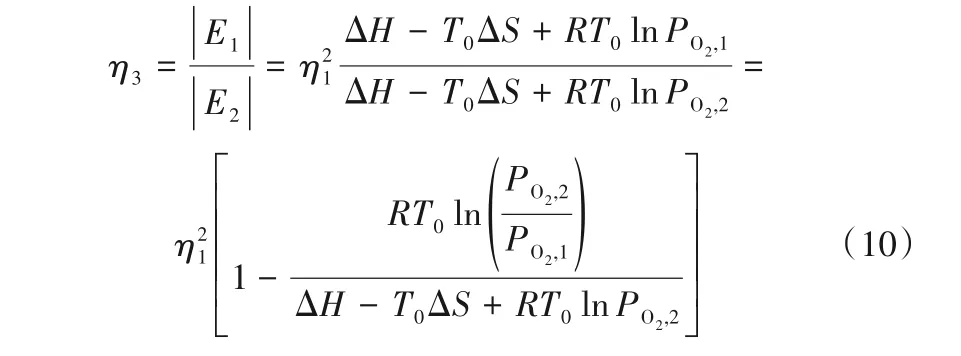
式中,T0为低温热源温度;E1表示放热过程中回收的㶲;E2表示吸热过程中需要补充的㶲。由于CL-TES过程希望能够储存更多能量,理想的载氧体应具有较大ΔH。而根据式(8)和式(10)可以发现,相同ΔH条件下,ΔS越小,则载氧体做功越多,效率越高。但是过小的ΔS却会导致释氧温度过高。假设环境温度T0=40oC,低温氧气平衡分压PO2,1=0.03 atm,且η3≥0.80 。若针对最简单的空气释氧过程,为保证高温顺利释氧,假设高温氧气平衡分压PO2,1=0.5 atm,释氧温度T2≤1000oC。如图2所示,CLTES过程载氧体ΔH和ΔS的合适区间与CL-ODH过程载氧体的有所重叠。这主要是由于两种流程均需要在较高温度条件下运行,该区间的典型代表也是CaMnO3类的载氧体。但尽管如此,CL-TES过程更倾向于选择低熵变、高焓变的材料,以实现更高的循环效率。
对于CL-TES过程,载氧体需要首先具备与热源相匹配的运行温度区间和较高储能密度。变温运行模式也对于载氧体的循环稳定性和热交换效率提出了很高的要求。此前CL-TES过程所采用的载氧体主要为单一金属氧化物和简单混合氧化物,但鉴于复杂氧化物(如钙钛矿型氧化物)循环稳定性上的优越性,近些年复杂氧化物的研究愈发受到关注。此外,载氧体经济性、储能系统设计和优化等也有待未来进一步解决[80-81]。
在过去的几十年里,化学链载氧体的开发飞速发展,逐渐从最初的单一过渡金属氧化物到现今的复杂氧化物,使得载氧体的调变性和适应性都显著提升。尽管复杂氧化物,如钙钛矿等表现出很好的潜力,但其巨大的设计空间也同样给研究者们带来了巨大的挑战。通过实验试错来探索合适载氧体的传统方法可以用于复杂氧化物的开发,但却会消耗大量的人力与时间。另一方面,基于密度泛函理论(DFT)的计算方法从最初就展现出计算复杂氧化物载氧体氧化还原性质的巨大的潜力[82-85]。近期对于复杂氧化物计算的研究成果表明,虽然要用到一些简化假设,但DFT及相关计算已能够在前文所述温度区间内相对快速地估算氧空位生成的焓变、熵变及预测相变情况。尽管考虑到复杂氧化物的复杂性,例如磁排序、过渡金属的电子自相互作用和缺陷相互作用等DFT计算具有固有的局限性,但这些计算工具对于指导复杂氧化物的选择和设计具有指导意义。还需特别指出的是,高通量DFT计算能够覆盖大量具有相关热力学参数的材料,这可能可以应用于机器学习算法以进一步扩展材料设计空间。此外,诸如p轨道中心和净电子电荷之类的电子描述符也已被证明对有效预测载氧体性质具有潜在的作用[32]。再加上从基础层面和实验数据修正的模型改进,通过计算辅助,可预期研发出远超现有材料性能的新型载氧体材料。以CLAS过程为例,如图3所示,DFT能够作为一种有效的手段指导和优化SrxA1-xFeyB1-yO3-δ载氧体性质[32]。氧空位生成结合能ΔEV和净电子电荷Δe线性相关,且两者均与氧容量和氧气传递能垒存在明显的相关性。因此,可以通过净电子电荷Δe更为快速地筛选不同掺杂情况下的复杂氧化物,从而获得氧容量较高、氧气传递能垒较低的高性能载氧体。
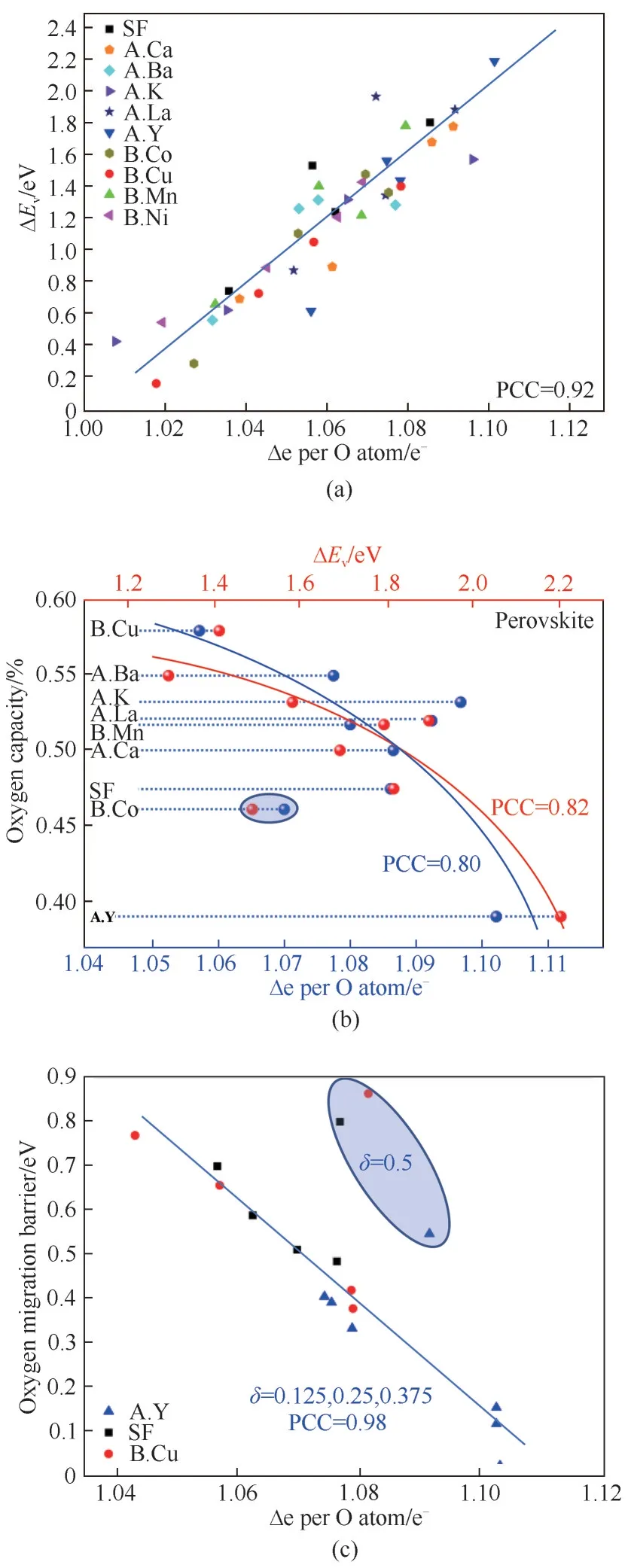
图3 DFT指导和优化CLAS流程中SrxA1-xFeyB1-yO3-δ载氧体性质:(a)载氧体ΔEv和Δe存在线性关系;(b)实验测得700°C、1%~20%氧分压变压运行得到的氧容量与ΔEv和Δe有很强的关联性;(c)氧气传递能垒也与Δe相关[32]Fig.3 DFT was used for the design and optimization of SrxA1-xFeyB1-yO3-δ oxygen sorbents in the CLAS process:(a)Linear relationship betweenΔEv andΔe was observed;(b)Experimental oxygen capacity at700°C within1%-20% PO2swing as functions of ΔEv andΔe;(c)Oxygen migration barrier as a function ofΔe per O atom[32]
以上关于复杂氧化物合适热力学性质的讨论,当与这些有效的计算手段相结合后,就可以指导复杂氧化物的理性选择。除了热力学性质,动力学性质例如氧空位传导率和表面反应的能垒也可以用于辅助载氧体的筛选。当然,以上分析为了获得更为直观的结论,简化了反应系统,也未考虑反应动力学等因素的影响。实际针对某一特定过程载氧体的调变策略,应进行更为细致的分析。
2 结论与展望
针对化学链空气分离、氧化脱氢和热化学储能三个典型过程热力学分析表明,由于不同化学链过程的反应物与反应条件显著不同,载氧体的调变策略也存在显著差异。CLAS过程理想的运行温度较低,因此载氧体的ΔH和ΔS均较小。CL-ODH过程系统的传热㶲损失随着载氧体的ΔH增大而增加,但过小的ΔH会导致载氧体吸氧再生困难,因此合适的载氧体应是低ΔH、高ΔS。载氧体的ΔH增大可以提升CL-TES过程的储热能力,并且ΔS越小系统循环效率越高,因此理想的载氧体应为高ΔH、低ΔS。尽管本文的分析做了相应简化以获得更为直观的结论,但以上讨论已经表明了载氧体热力学性质调变的必要性与可行性。许多现有的载氧体已经在这些化学链过程中显示出很好的潜力,但仍然有广阔的空间可以显著改善复杂氧化物的性质。可以预见,若能结合高通量计算,可针对特定化学链流程关键反应中载氧体的行为进行调变,从而扩大相关流程的运行范围、提高系统运行效率并显著降低排放。

