基于Nano-Fe3O4/Nafion修饰玻碳电极用于海水基的铅离子传感器研究
王 聪, 邱成军, 曲 伟, 庄 远, 牙富东, 严怡柔
(1.北部湾大学 机械与船舶海洋工程学院, 钦州 535011; 2.北部湾大学 电子与信息工程学院,钦州 535011; 3.广西大学 计算机与电子信息学院, 南宁 530004)
0 引 言
重金属离子在水中具有富集性和强毒性,会随着工业废水和生活污水排放量的增加,给整个海洋生态系统带来严重威胁[1-2]。其中Pb2+是一种高毒性重金属离子,会对生物神经系统造成损害,也能引起部分器官衰竭[3-4]。考虑到它的危害,世界卫生组织(WHO)和美国环境保护局(EPA)规定海水中Pb2+的最高含量为50 μg·L-1[5],超过此浓度海洋生物和人类健康将面临严重威胁。因此,检测海水中Pb2+的含量尤为重要。
电化学溶出伏安法因其操作简便、灵敏性高、响应速度快的优势,备受研究人员的广泛关注[6]。其中差分脉冲溶出伏安(DPSV)法因其响应速度快、背景电流低等优点,成功用于多种环境下Pb2+的检测分析。如文献[6-9]通过DPSV法分别实现了矿山废水、湖水以及饮用水中痕量Pb2+的测定。但目前对海水进行检测的相关报道较少,这是因为海水基体环境复杂、干扰性强[10]。而多组分的修饰电极具有良好的协同和耦合作用,在灵敏度、选择性和稳定性方面都要优于单组分修饰电极,适合用于铅离子含量低、基体干扰强的检测[11-12]。软磁材料四氧化三铁(Fe3O4)是一种尖晶石类铁氧体,在电子领域、生物领域以及医学领域等展现出了良好的应用价值。而纳米级的四氧化三铁(Nano-Fe3O4)表现出的超顺磁性使其在修饰电极上增加电极的导电性,加快电极与溶液反应时电子的传输速率;其小尺寸效应表现出了体积小和比表面积大的特点[13]。全氟磺酸又名Nafion,是一种金属阳离子交换剂,具有防污性能,其膜带负电荷,可作为天然屏障阻止带负电荷粒子的相互作用[14]。本文研究了一种多组分的纳米复合材料修饰电极构建的Pb2+传感器,利用Nafion作为分散剂分散在Nano-Fe3O4中,Nafion不仅可以作为分散剂与成膜剂,还可以实现重金属离子的萃取,提高检测的灵敏度[15]。通过滴涂法在玻碳电极(GCE)表面实现Nano-Fe3O4/Nafion复合膜的修饰,基于DPSV法实现铅离子传感器对海水中Pb2+高灵敏度的检测。
1 实验部分
1.1 仪器与试剂
本实验基于上海辰华仪器公司生产的CHI 830D电化学分析仪进行操作;采用标准三电极体系:工作电极为3 mm的GCE,辅助电极为铂丝,参比电极为饱和甘汞电极。通过Sigma HD型扫描电子显微镜(SEM)拍摄修饰电极的形貌。pH计、磁力搅拌器和电子天平购于上海力辰仪器科技有限公司。
实验过程使用的药品分别为分析纯(AR)的无水乙醇、氯化铁、硫酸亚铁、乙酸钠、N,N-二甲基甲酰胺(DMF),优级纯(GR)的氯化钾、冰乙酸,质量分数为5%的Nafion(乙醇与水混合液)以及100 μg·mL-1的Pb2+标准溶液(1%硝酸)等药品。实验用水为电阻率达到18.0 MΩ·cm的超纯水。
1.2 修饰溶液的制备
利用电子天平分别称取3.244 g氯化铁和8.344 g硫酸亚铁,放入烧杯中,加入100 mL超纯水,超声20 min;再加20 mL浓氨水,在恒温50 ℃下,通过磁力搅拌器剧烈搅拌1 h,倾去上层清液,冲洗至中性,抽滤并在干燥箱内干燥;在研钵中研磨成粉末,就得到了Nano-Fe3O4。将Nafion经无水乙醇稀释到0.5%,称取10 mg Nano-Fe3O4粉末与25 μL Nafion一起放入烧杯中,利用DMF定容至10 mL,超声30 min以上,使其分散均匀,即可得到Nano-Fe3O4/Nafion修饰电极溶液。
1.3 Pb2+传感器的制备
分别用0.3和0.05 μL的Al2O3粉末对裸GCE进行抛光;然后再经超纯水、无水乙醇冲洗电极;最后将裸GCE在H2SO4(0.5 mol·L-1)溶液中活化,用循环伏安法(CV)进行扫描,直至得到稳定的CV曲线,用超纯水冲洗电极,晾干即可。用移液器精确移取5 μL Nano-Fe3O4/Nafion修饰溶液均匀地滴加到GCE上,并置于红外灯下烘烤,待溶液挥发后即可得到Nano-Fe3O4/Nafion/GCE,一层致密的薄膜粘附在GCE表面,表明Pb2+传感器构建成功。
1.4 实验测量
配制0.1 mol·L-1pH 4.5的HAc-NaAc支持电解质溶液,将一定量的铅离子标准溶液加入到支持电解质溶液中,通N2除氧10 min。将Nano-Fe3O4/Nafion/GCE、铂丝电极、饱和甘汞电极浸入溶液中。在搅拌的作用下,利用电化学分析仪的恒电位(I-t)法进行富集,电位-1.1 V,时间180 s;利用DPSV法记录Pb2+的溶出曲线,操作参数:起始、终止电位分别为-0.9和-0.3 V,电位增量0.05 V,其他参数为仪器默认参数。
2 结果与讨论
2.1 Nano-Fe3O4的形貌表征
通过扫描电子显微镜(SEM)技术表征了本文制备的Nano-Fe3O4微观形貌结构。如图1(a)所示,在Mag=50 kx放大倍数下可以发现Nano-Fe3O4呈球形或近球形;进一步放大,在Mag=100 kx倍数下,如图1(b)所示,直径大约为30~40 nm,尺寸大小均一,分布均匀,颗粒感好,形貌良好。

图1 Nano-Fe3O4 SEM图: (a) Mag=50.00 kx; (b) Mag=100.00 kxFig.1 SEM images of Nano-Fe3O4: (a) Mag=50.00 kx; (b) Mag=100.00 kx
2.2 Nano-Fe3O4/Nafion/GCE的电化学表征
为了验证Nano-Fe3O4/Nafion修饰材料是否被成功修饰在传感器的电极上,在0.1 mol·L-1KCl溶液中(含0.01 mol·L-1[Fe(CN)6]3-/4-)进行了不同电极的CV测试。如图2所示,对比裸GCE (曲线a)和Nano-Fe3O4/Nafion/GCE (曲线b),可以发现Nano-Fe3O4/Nafion/GCE的Fe3+/Fe2+的氧化还原峰明显大于裸GCE的,说明Nano-Fe3O4/Nafion被成功修饰到了电极表面,增加电极的比表面积,改善了电极的电化学性能。为了精确地求出不同电极的电活性面积,根据Randles-Sevcik方程[16],利用下式:
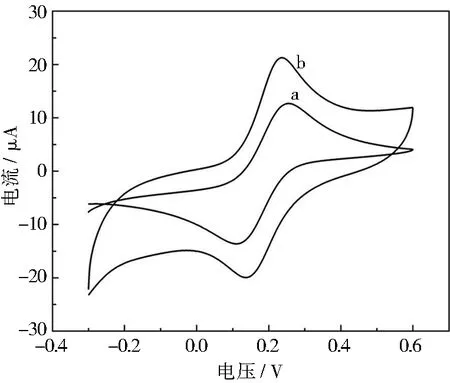
图2 Nano-Fe3O4/Nafion/GCE与 裸GCE的CV对比图Fig.2 Comparison of CV between Nano-Fe3O4/ Nafion/GCE and bare GCE
Ip=2.69×105AD1/2n2/3γ1/2C
(1)
式中:Ip为电流峰值,A;A为有效电极面积,cm2;D为扩散系数,cm2·s-1;n为参与反应的电子数;γ为电位变化速率,V·s-1;C为浓度,mol·cm-3。将D=7.6×10-6cm2·s-1,n=1,C=10 mmol·L-1代入上式计算可得Nano-Fe3O4/Nafion/GCE、裸GCE的电活性面积分别为0.010 8和0.008 4 cm2。进一步说明了Nano-Fe3O4/Nafion有效地增加GCE的电活性面积,提高了传感器的导电性能。
电极在进行电化学反应时,可分为表面过程控制和扩散过程控制,为了验证Nano-Fe3O4/Nafion/GCE的电极表面特性,将Nano-Fe3O4/Nafion/GCE置于KCl、[Fe(CN)6]3-/4-溶液中,进行不同扫速的CV测试,得到如图3(a)所示的CV图。随着扫速的增加,峰电流在增大,且峰电流Ip与扫速V1/2成一定的线性关系,如图3(b)所示,表明Nano-Fe3O4/Nafion修饰的Pb2+传感器的电极反应由扩散过程控制。

图3 (a) 不同扫速下Nano-Fe3O4/Nafion/GCE的CV图; (b) 峰电流Ip与扫速V1/2图Fig.3 (a) CV diagram of Nano-Fe3O4/Nafion/GCE at different scanning speed; (b) relationship of peak current and scanning speed
Pb2+在不同修饰电极上的响应效果如图4所示。采用DPSV法在50 μg·L-1Pb2+溶液中对Nano-Fe3O4/Nafion/GCE与裸GCE进行溶出伏安曲线对比,可以看出,Nano-Fe3O4/Nafion/GCE的Pb2+溶出峰电流要明显大于裸GCE的,这是由于Nano-Fe3O4/Nafion材料独特的性能,提高了电极表面的电子传输速率,更利于Pb2+的吸附,因此,Nano-Fe3O4/Nafion/GCE展现出了更高的灵敏度与峰电流。

图4 Nano-Fe3O4/Nafion/GCE(曲线a)与裸GCE(曲线b) 在50 μg·L-1 Pb2+溶液中的DPSV曲线Fig.4 DPSV curves of Nano-Fe3O4/Nafion/GCE (curve a) and bare GCE (curve b) in 50 μg·L-1 Pb2+ solution
2.3 Pb2+传感器检测的实验条件优化
2.3.1 支持电解质的影响
不同的支持电解质会直接影响Pb2+传感器溶出曲线基线的平稳、峰形的大小以及重现性。如图5所示,分别在含有50 μg·L-1Pb2+的HAc-NaAc、HCl、KCl(均为0.1 mol·L-1、pH 5.0)三种不同支持电解质内对Nano-Fe3O4/Nafion/GCE进行了DPSV测试,通过对比基线、峰电流的大小以及峰形确定了HAc-NaAc作为Pb2+传感器检测Pb2+的支持电解质。
2.3.2 富集电位影响
最优的富集电位可以加速目标金属离子的富集,提高Pb2+传感器检测的准确性[17]。在-0.8 ~1.2 V范围进行富集电位的优化结果如图6所示。可以看出,随着电位的增大,峰电流也在增大。当电位为-1.1 V时,峰电流信号达到最大值。继续增加富集电位,峰电流反而下降,由于传感器的修饰电极表面会有析氢现象,导致修饰电极表面已经被富集的Pb2+会脱落。因此,选取-1.1 V作为富集电位。
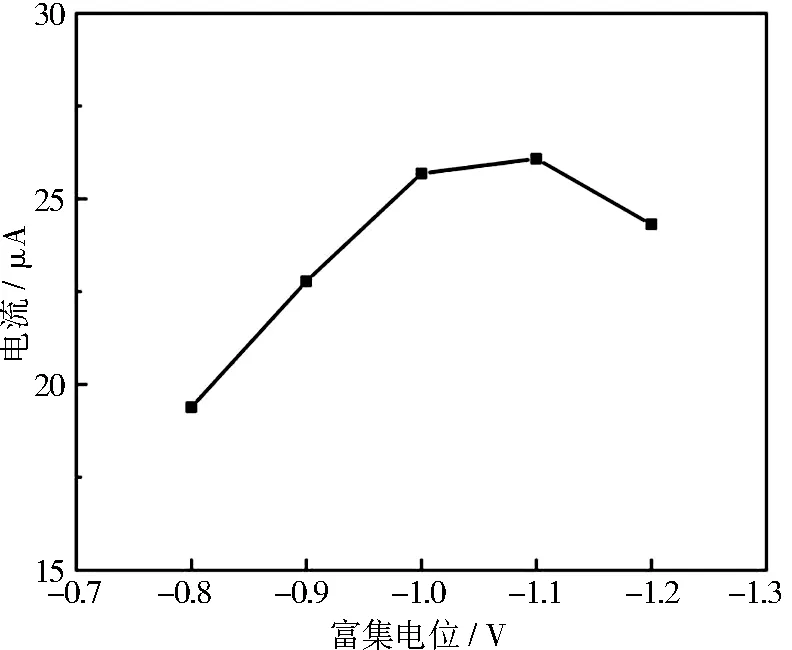
图6 富集电位对Pb2+溶出峰电流的影响Fig.6 Effect of accumulation potential on the peak current of Pb2+ dissolution
2.3.3 HAc-NaAc电解质pH的影响
当pH过低时,溶液中的H+与Pb2+存在竞争关系(即析氢可能会干扰沉积富集过程),pH过高时,Pb2+可能会水解形成金属氢氧化物和络合物等,从而减少溶液中金属离子的量[18]。于是考察了不同pH的HAc-NaAc支持电解质溶液对峰电流的影响,如图7所示。HAc-NaAc电解质的pH从4.0变化到5.0时,峰电流不断增大。在5.0处最大,当pH继续增大,峰电流反而呈下降趋势。因此,HAc-NaAc缓冲溶液的pH选择5.0。
2.3.4 Nano-Fe3O4浓度的影响
由于Nano-Fe3O4浓度过高,会导致背景电流过大,相反浓度过低会影响电极对Pb2+的吸附能力。优化了Nano-Fe3O4浓度对Pb2+溶出峰的影响,如图8所示。可以看出,当Fe3O4浓度为4 mg·mL-1时,Pb2+的峰电流值最大。因此,Nano-Fe3O4浓度选择4 mg·mL-1。
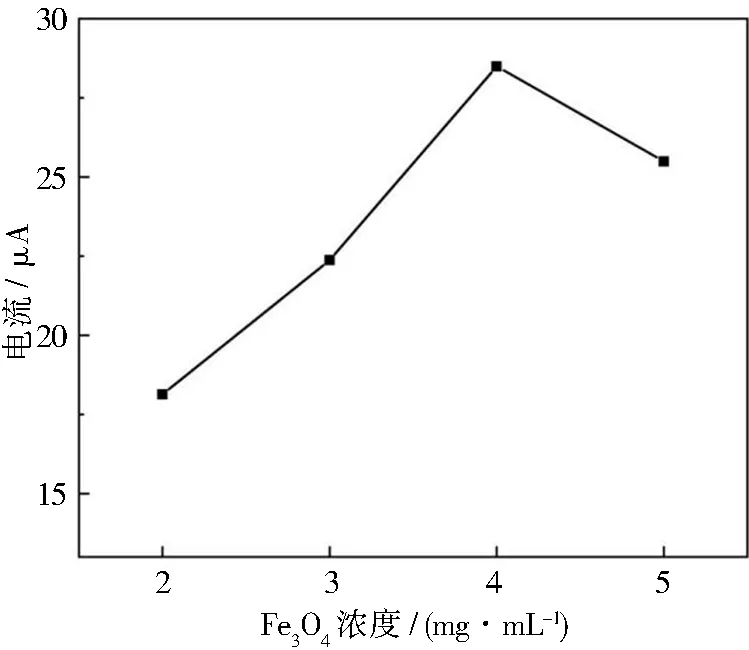
图8 Nano-Fe3O4浓度对Pb2+溶出峰电流的影响Fig.8 Effect of Fe3O4 concentration on the peak current of Pb2+ dissolution
2.3.5 富集时间的影响
由于Nano-Fe3O4的吸附能力会随着时间的增加而增加,直至达到饱和。对富集时间进行了优化,结果如图9所示,峰电流随着富集时间的延长而变大,当富集时间大于300 s后,峰电流增长缓慢,考虑到灵敏度与效率等因素,选取300 s作为富集时间。
2.4 标准曲线
通过建立标准曲线有助于准确分析传感器对铅离子检测的可行性与准确性。配制一系列不同浓度的Pb2+标准溶液,将Nano-Fe3O4/Nafion/GCE插入到标准溶液当中,在搅拌的条件下富集300 s。通过DPSV法检测不同Pb2+浓度下的响应电流信号,绘制浓度与Pb2+溶出峰电流的关系图,如图10(a)所示,得到相应的线性回归方程如图10(b)所示,线性回归曲线y=0.241+0.699c,相关系数R2=0.993 73,检出限为0.5 μg·L-1(3σ/m,σ为空白溶液标准偏差,m为方程斜率)。

图10 (a)Nano-Fe3O4/Nafion/GCE对不同浓度Pb2+的溶出伏安图; (b)相应的线性回归曲线Fig.10 (a) Dissolution voltammogram curves of Nano-Fe3O4/Nafion/GCE to different concentrations of Pb2+; (b) corresponding linear regression curve
2.5 Pb2+传感器的抗干扰性
为了评估Pb2+传感器在海水基中的检测性能,通过添加不同干扰离子来研究传感器对Pb2+检测的抗干扰性。如图11所示,在30 μg·L-1的Pb2+标准溶液中分别加入了150倍的K+、Cl-、Na+干扰离子,发现上述浓度的干扰离子对Pb2+的峰电流无显著影响,峰电流变化率都在10%以内,说明该铅离子传感器具有良好的抗干扰性。
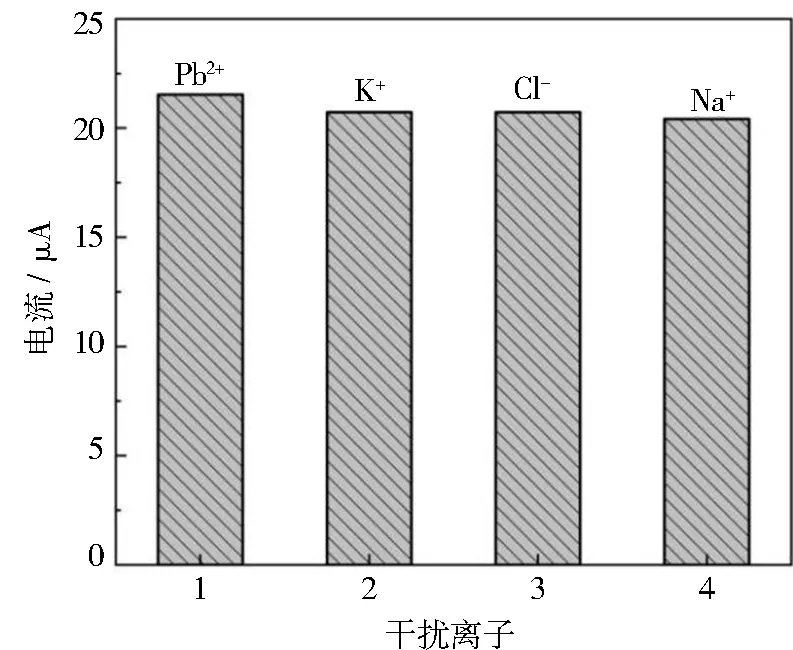
图11 Nano-Fe3O4/Nafion/GCE对30 μg·L-1 Pb2+ 中加入150倍K+、Cl-、Na+的峰电流影响Fig.11 Effect of Nano-Fe3O4/Nafion/GCE pairs after adding 150 times K+, Cl-, Na+ to 30 μg·L-1 Pb2+
2.6 Pb2+传感器的重现性
在实际应用中,重现性是表征传感器实用性的重要指标。为了验证本文传感器的重现性,在相同实验条件下制备了5支Nano-Fe3O4/Nafion/GCE对5 μg·L-1Pb2+溶液进行测定,结果如图12所示,计算得到了其相对标准偏差(RSD)为5.93%,表明该传感器的重现性良好。
2.7 样品分析
分别采集了茅尾海2处不同地点的海水样品,静置3 d,经0.45 μL微孔滤膜过滤和紫外线预处理后,利用Pb2+传感器对所采集的海水进行Pb2+浓度的测定,并通过加标回收实验对海水样品进行回收率的检测,结果如表1所示。加标回收率90.0%~99.3%,表明该传感器可应用于实际样品中Pb2+浓度的检测。

表1 实际样品中Pb2+浓度的检测Table 1 Detection of Pb2+ concentration in actual samples
为了进一步评估本文研制的Nano-Fe3O4/Nafion/GCE铅离子传感器的性能,其结果与近年来报道的基于不同材料修饰GCE制备的检测铅离子的传感器性能对比结果如表2所示。所制作的Nano-Fe3O4/Nafion/GCE铅离子传感器在检测限要低于BOC/GCE[19]铅离子传感器,高于PGA/cCNSs/GCE[20]、p-Tyr/Bi/GCE[21]、PtNFs/GCE[22]、Ergo-MWNTs-L-Cys/GCE[23]铅离子传感器,但仍可应用于海水中μg·L-1(ppb)级别Pb2+的检测[24],并且低于WHO与EPA规定的50 μg·L-1[5]。同时,所研制的铅离子传感器在灵敏度上要高于BOC/GCE、p-Tyr/Bi/GCE、PtNFs/GCE、Ergo-MWNTs-L-Cys/GCE的铅离子传感器,表明该传感器灵敏度高、响应快速、稳定性好,可应用于海水中不低于ppb级别的铅离子检测。

表2 不同Pb2+传感器的性能分析对比Table 2 Performance comparison of different Pb2+ sensors
3 结 论
将比表面积大、电子传输速率快的Nano-Fe3O4与Nafion混合作为敏感材料,采用滴涂法将Nano-Fe3O4/Nafion成功修饰到GCE上,构建了用于检测Pb2+的传感器。通过SEM、CV法对修饰电极进行了表征,并对实验条件进行优化改进。得出了富集电位为-1.1 V、支持电解质pH为5.0、Fe3O4浓度为4 mg·mL-1及富集时间为300 s的最优条件,该传感器所得到的DPSV响应电流与Pb2+浓度在5~80 μg·L-1内呈正比,检出限为0.5 μg·L-1(3σ/m)。在外加干扰离子的环境内,Pb2+传感器表现出了一定的抗干扰性,同时,重现性良好,可用于实际海水中Pb2+的检测,对海洋环境与人类健康的保护具有良好的应用价值。

