湿法炼锌溶液中铜的选择性吸附机理及行为
林晓坦,李存兄,夏 力,熊甲成,吉文斌,张兆闫,张耀阳,唐嘉莉
(昆明理工大学 冶金与能源工程学院,云南 昆明 650093)
0 引 言
铜是重要的战略有色金属,而我国约70%的铜资源依赖进口[1].湿法炼锌所用锌精矿中常伴生0.09%~1.05%的铜[2],每年进入锌冶炼系统的铜资源量为64 250 t左右,这部分铜资源的高效回收对提高有价金属综合回收率及缓解铜资源紧张局面具有重要意义.现阶段我国大约90%的锌采用焙烧→浸出→净化→电积工艺流程生产[3-4],在此工艺流程中铜主要集中于酸性浸出液,因此酸性浸出液中铜的选择性分离与富集极为关键.
目前,湿法冶金领域酸性溶液中铜的分离富集方法包括:溶剂萃取法、硫化沉淀法、旋流电积脱铜法等[5-7].溶剂萃取法选择性好,萃取效率高,且成本低,但引入的有机物会严重影响湿法炼锌溶液的后续处理工序[8];硫化沉淀法具有工序简单,沉淀物稳定等优点,但湿法炼锌溶液中存在大量的Zn2+,锌铜同时沉淀,选择性分离困难[9];旋流电积法具有电流效率高,产品质量好等优点,但适合处理Cu2+浓度高的溶液[10].采用上述工艺分离富集湿法炼锌含铜溶液时存在有机物污染严重、选择性分离困难、成本高等问题,而树脂吸附法具有清洁高效、工艺简单、能耗低等优点.
湿法炼锌酸性浸出液中存在大量的Fe3+、Zn2+、Mg2+等金属离子,采用树脂吸附法分离Cu2+的关键在于筛选可在酸性溶液中将Cu2+选择性分离的大容量树脂.国内科研工作者采用功能基为亚胺二乙酸的螯合树脂开展了不同体系中铜的选择性分离与富集研究.张慧等[11]研究了Cu2+、Zn2+、Ni2+等5种离子在D751型螯合树脂上的吸附量与溶液pH值的关系,证明了在低于3的任一pH值下,Cu2+与亚胺二乙酸基生成的螯合物比Zn2+与该功能基生成的螯合物稳定;刘步云等[12]针对酶促反应的茶氨酸体系具体考察了D401型螯合树脂对Cu2+的去除效果,证明亚胺二乙酸基树脂在较宽的 pH 范围内对 Cu2+均具有很好的选择吸附性;曹焕义等[13]针对氨基酸生产过程中产生的含铜废水的水质和水量,设计了D851型螯合树脂回收废水中Cu2+的二级吸附工艺.众多学者的研究表明亚胺二乙酸基螯合树脂对Cu2+的吸附量大、选择性好、可循环利用且成本较低,具有工业应用的基础[14-15].前人采用亚胺二乙酸基螯合树脂开展了氨基酸生产废水、茶氨酸体系溶液等多种体系中Cu2+的分离与富集研究,但使用该功能基树脂回收湿法炼锌酸性浸出液中Cu2+的研究未见报道.为提高锌冶炼过程中铜的回收率,本文开展了亚胺二乙酸基螯合树脂从湿法炼锌酸性浸出液中分离富集铜的工艺研究.通过静态实验研究了不同条件下亚胺二乙酸基螯合树脂吸附Cu2+、Zn2+的等温线和动力学等行为机理,并探索了高浓度硫酸锌溶液中树脂对Cu2+的选择吸附性能,考察了解吸剂的解吸效果,结果将为湿法炼锌溶液中铜的选择性回收及树脂工艺的选择提供理论依据和技术支撑.
1 实验部分
1.1 实验材料
配置溶液使用的化学试剂均为分析纯.主要试剂:硫酸铜(CuSO4·5H2O,天津风船化学试剂,w%≥99%);硫酸锌(ZnSO4·7H2O,天津恒兴化学试剂,w%≥99.5%);浓硫酸(H2SO4,四川西陇科学有限公司,96%~98%).
本实验采用的树脂为亚胺二乙酸基螯合树脂,其物理化学性能如表1所示.
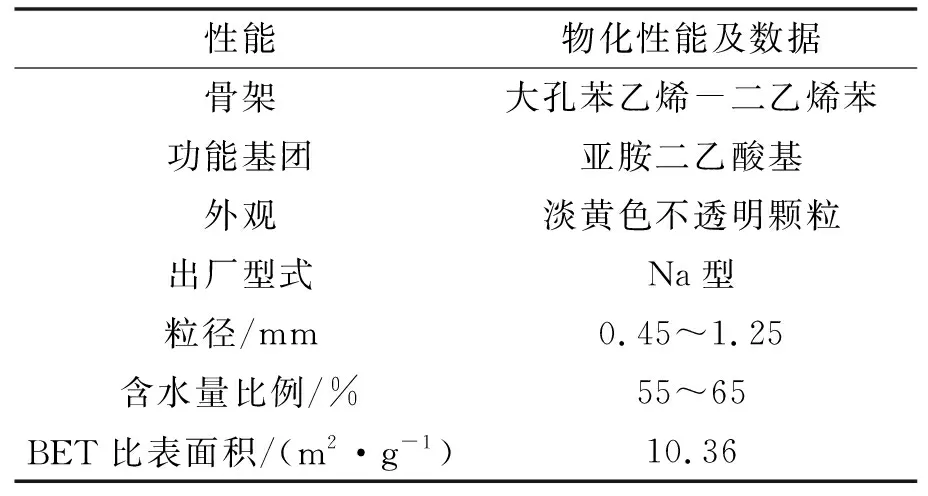
表1 树脂的物理化学性能
1.2 实验原理与流程
树脂吸附原理为Cu2+取代亚胺二乙酸功能基中的Na+且与N原子的孤对电子进行螯合,其化学反应如图1所示.

图1 反应原理图Fig. 1 Schematic diagram of reaction
采用稀H2SO4溶液进行负载金属离子树脂的解吸,解吸原理为H+重新取代功能基上的Cu2+.树脂吸附-解吸实验流程与官能团微观结构演变规律如图2所示.
1.3 实验方法1.3.1吸附实验
用去离子水清洗亚胺二乙酸基螯合树脂,去除新树脂携带的机械杂质及破碎树脂小颗粒.溶液体积与干树脂质量之比为50 mL/g.将定量树脂与配置的吸附前液于密闭小瓶中混合,随后在振荡器上恒温震荡若干分钟.过滤负载金属离子树脂,检测溶液中Cu2+或Zn2+剩余浓度.
根据公式(1)~(4)计算吸附率、吸附量、Cu2+(Zn2+)的分布系数、Cu2+和Zn2+的分离系数[16-17]:
(1)
(2)
(3)
(4)
式中:E为树脂对金属离子的吸附率,%;Qe为树脂的金属离子吸附量,mg/g;Ke为分布系数,mL/g;αCu/Zn为Cu2+与Zn2+之间的分离系数;C0为溶液中金属离子初始浓度,mg/L;Ce为溶液中平衡金属离子浓度,mg/L;V为溶液体积,L;m为干树脂质量,g.
1.3.2解吸实验
用去离子水清洗负载Cu2+树脂,至洗水的pH值为中性且无金属离子存在.将不同质量分数的稀H2SO4溶液与负载Cu2+的树脂于密闭小瓶中混合,置于振荡器上恒温震荡若干分钟进行解吸.检测解吸后液中Cu2+浓度.
根据公式(5)计算解吸率,进而选择最佳解吸剂浓度及解吸时间.
(5)
式中:D为解吸率,%;ma为解吸到硫酸溶液中的金属离子质量,mg;mr为树脂负载金属离子质量,mg.
1.4 分析检测
使用全自动比表面及孔隙度分析仪(型号麦克ASAP2460)测定树脂的比表面积;采用傅里叶红外变换光谱仪(型号Bruker ALPHA)测定新树脂和负载金属离子树脂的红外光谱;使用钨灯丝扫描电镜(型号VEGA3 GM)观察树脂吸附前后的形貌变化;使用雷磁pH计(型号PHSJ-4A)检测溶液pH值.
2 结果和讨论
2.1 树脂表征
2.1.1 扫描电镜分析
将亚胺二乙酸基螯合树脂喷铂后粘在导电胶带上,对其形貌结构进行SEM观察.新树脂、负载Cu2+树脂放大50 000倍的SEM图像分别如图3(a)、(b)所示.
由图3(a)可观察到新树脂的表面均匀布满了许多形状各异的孔道,孔道相互交叉且互通,可供分子进出,有利于吸附过程的进行.由图3(b)可观察到吸附之后树脂的形貌与新树脂差异明显,表面大部分孔的开口及空腔被薄膜覆盖,说明树脂已负载Cu2+.

(a)新树脂 (b)负载Cu2+的树脂图3 树脂SEM图Fig. 3 SEM image of resin: (a) the new resin; (b) the resin loaded with Cu2+
2.1.2 红外光谱分析

(a)新树脂红外光谱图;(b)负载Cu2+树脂红外光谱图;(c)负载Zn2+树脂红外光谱图图4 树脂的红外光谱图Fig. 4 Infrared spectrogram of resin: (a) the new resin; (b) the resin loaded with Cu2+;(c) the resin loaded with Zn2+
本研究采用傅里叶红外变换光谱仪测定树脂化学结构,新亚胺二乙酸基螯合树脂、负载Cu2+树脂、负载Zn2+树脂的红外光谱图如图4所示.
由图4(a)可知,新树脂的红外光谱在3 453.56 cm-1和1 630.68 cm-1处有两个明显的特征峰;3 453.56 cm-1处是羟基伸缩振动形成的一个较宽的吸收峰;1 630.68 cm-1处是羧酸根离子的反对称伸缩振动形成的峰[18].由图4(b)、图4(c)可知,3 453.56 cm-1处的峰和1 630.68 cm-1处的峰依旧存在,而负载Cu2+的树脂和负载Zn2+的树脂分别在615.43 cm-1和618.36 cm-1处出现两个新峰,根据盛芬龄等学者的研究[19]可知,这一带的吸收峰反映了N-Me(Me代表金属元素)的振动,说明树脂吸附金属离子后N与Cu2+或Zn2+发生配位,形成螯合物.
2.2 不同因素对吸附性能的影响
在湿法炼锌企业产出的含铜酸性浸出液中Zn2+对 Cu2+的选择性吸附影响最为显著,本文首先探究了亚胺二乙酸基螯合树脂对Cu2+、Zn2+的吸附行为.分别在Cu-SO3-H2O、Zn-SO3-H2O体系溶液中研究了溶液初始酸度、溶液初始Cu2+或Zn2+浓度、接触时间对亚胺二乙酸基螯合树脂吸附性能的影响.
2.2.1初始酸度的的影响
利用1 g干树脂分别在50 mL的 Cu-SO3-H2O和Zn -SO3-H2O体系溶液中进行了初始酸度对吸附率E影响的实验研究.溶液初始Cu2+或Zn2+浓度为300 mg/L,在室温、振荡频率为150 r/min、接触时间为120 min条件下的实验结果如图5(a)所示.测量Cu-SO3-H2O体系溶液吸附前后的pH值,结果如图5(b)所示.
由图5(a)可知,树脂对Cu2+和Zn2+的吸附率随初始酸度的升高而显著降低;溶液含H2SO4浓度为0.01 mol/L时,树脂对Cu2+和Zn2+的吸附率均很高,分别为98.88%和97.94%;溶液含H2SO4浓度为0.6 mol/L时,树脂对Cu2+和Zn2+的吸附率分别降低至为20.67%和4.5%,且溶液含H2SO4浓度为0.1 mol/L时,树脂对Cu2+的吸附率比Zn2+高55.33%,吸附率差值达到最大.由图5(b)可知,吸附后溶液的pH值升高,酸度降低,且随着溶液初始酸度增大,吸附后溶液酸度降低趋势更加明显.由此可知亚胺二乙酸基螯合树脂的吸附性能随酸度升高而变差,是由H+与Cu2+竞争活性位点造成的[20],所以低酸浓度的弱酸性体系有利于树脂吸附的进行.

(a)初始酸度对吸附率的影响 (b)溶液pH值的变化图5 初始酸度对吸附率的影响和溶液pH的变化图Fig. 5 Influence of initial acidity on adsorption rate and change in pH of the solution:(a)influence of initial acidity on adsorption rate;(b)change in pH of the solution
2.2.2 初始Cu2+、Zn2+浓度的影响
利用1 g干树脂分别在50 mL的 Cu-SO3-H2O和Zn-SO3-H2O体系溶液中进行了初始Cu2+、Zn2+浓度对吸附量Qe影响的实验研究.溶液初始H2SO4浓度为0.01 mol/L,在室温、振荡频率为150 r/min、接触时间为120 min条件下的实验结果如图6所示.
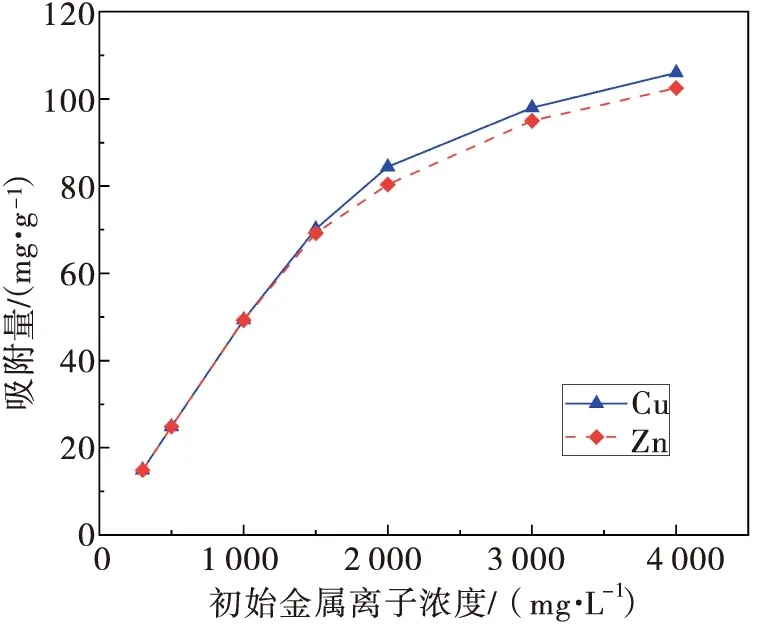
图6 初始Cu2+或Zn2+浓度对吸附量的影响Fig. 6 Influence of initial Cu2+ or Zn2+ concentration on adsorption capacity
由图6可知,亚胺二乙酸基螯合树脂对Cu2+或Zn2+的吸附量随初始金属离子浓度的增加而显著升高;初始Cu2+或Zn2+浓度均为4 000 mg/L时,树脂对Cu2+、Zn2+的吸附量均达到最大值,分别为106 mg/L和102.5 mg/L,说明亚胺二乙酸基螯合树脂对Cu2+和Zn2+的吸附性能均较强.在本研究浓度范围内树脂对Cu2+的吸附量略高于Zn2+,但两种离子的吸附量增长曲线基本一致,因此无法根据单一金属离子体系溶液中不同初始离子浓度条件下的吸附结果判断树脂对Cu2+、Zn2+吸附效果的差异,后续将研究二元竞争金属离子体系中Cu2+和Zn2+浓度对树脂选择性吸附性能的影响.
2.2.3接触时间的影响
利用1 g干树脂分别在50 mL的 Cu-SO3-H2O和Zn -SO3-H2O体系溶液中进行了接触时间对吸附量Qe影响的实验研究.溶液初始H2SO4浓度为0.01 mol/L,在室温、振荡频率为150 r/min、溶液初始Cu2+或Zn2+浓度为4 000 mg/L条件下的实验结果如图7所示.
由图7可知,亚胺二乙酸基螯合树脂对Cu2+、Zn2+的吸附量随接触时间的增加而增加;树脂与溶液接触120 min后对Cu2+、Zn2+的吸附量基本不再增加,分别达117.92 mg/g和 106.8 mg/g.因此接触120 min后,树脂对Cu2+、Zn2+的吸附趋于平衡.
2.3 吸附等温线
Langmuir模型和Freundlich模型是用来描述吸附达到平衡时溶液中金属离子浓度与树脂吸附量之间关系的常用模型[21],两个模型对应的吸附等温方程式分别由公式(6)和公式(7)表示[22]:
(6)
(7)
式中:qe是平衡吸附容量,mg/g;qm是饱和吸附容量,mg/g;Ce是溶液中平衡金属离子浓度,mg/L;KL是与吸附自由能相关的Langmuir常数;KF是与吸附容量相关的Freundlich常数;n是代表与吸附线性度偏差的Freundlich吸附常数.
用Langmuir和Freundlich等温方程对2.2.2节吸附实验结果进行线性回归,吸附等温线如图8(a)、(b)所示,拟合参数如表2所示.由图8和表2可知,Freundlich模型拟合相关系数R2更大,分别为0.987 6和0.998 1,说明亚胺二乙酸基螯合树脂对Cu2+和Zn2+的吸附符合Freundlich模型,树脂对Cu2+和Zn2+的吸附均为多分子层吸附,即同时存在物理吸附和化学吸附[23];Freundlich方程中吸附常数KF反应了树脂吸附能力的强弱,树脂吸附Cu2+过程的KF值更高,为36.44,证明树脂对Cu2+的吸附性能更强.利用吸附性能的强弱差异,亚胺二乙酸基螯合树脂可在湿法炼锌溶液中将Cu2+与Zn2+等杂质离子分离.
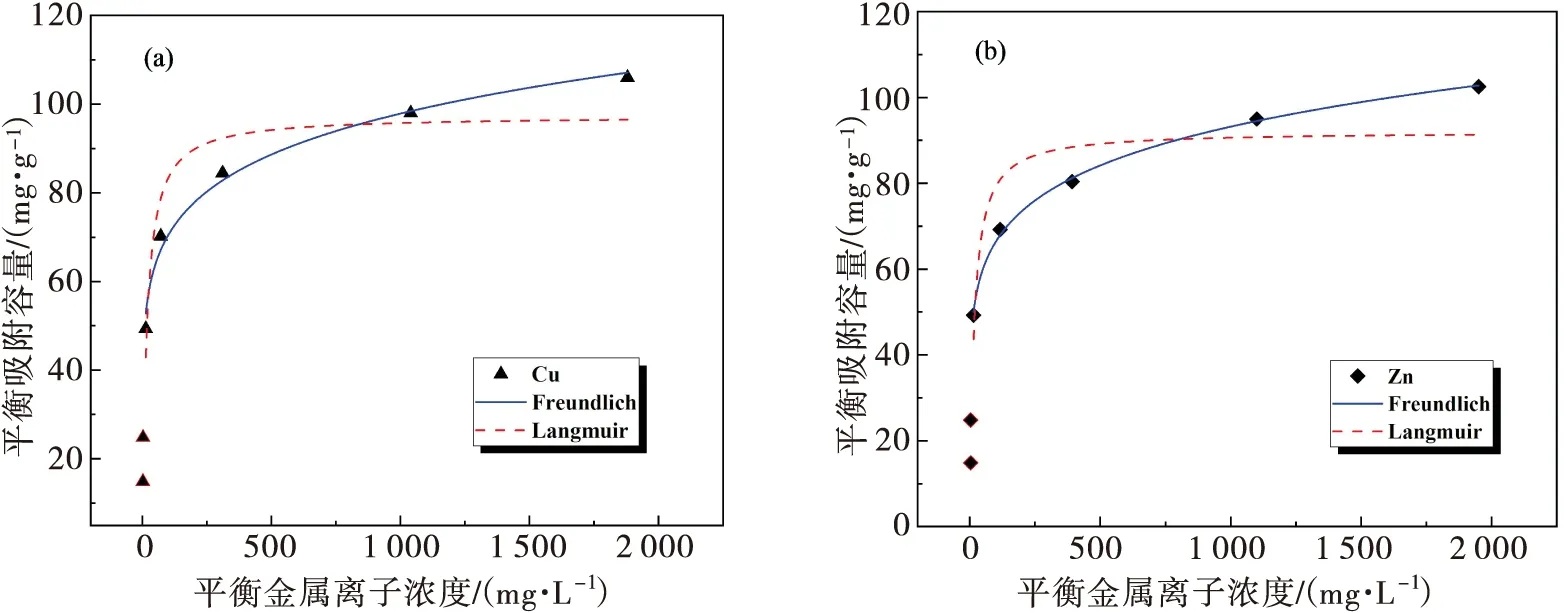
(a) Cu2+ (b) Zn2+图8 Freundlich和Langmuir吸附等温线Fig. 8 Freundlich and Langmuir adsorption isotherms:(a) Cu2+;(b) Zn2+
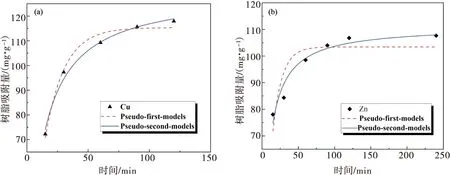
(a) Cu2+ (b) Zn2+ 图9 准一级和准二级动力学模型Fig. 9 Pseudo-first-order and pseudo-second-order dynamics modes:(a) Cu2+;(b) Zn2+

表2 Freundlich、Langmuir等温方程拟合参数
2.4 吸附动力学
吸附动力学模型在一定程度上可反映出吸附过程的主要控制步骤及内在机理.固体吸附剂对溶液中溶质的吸附动力学过程常用准一级动力学模型、准二级动力学模型来描述;离子交换过程一般需要经过膜扩散、颗粒扩散、化学反应3个步骤,常用动边界模型来判断反应的速率控制步骤[24].
2.4.1 准一级与准二级动力学模型
为了研究亚胺二乙酸基螯合树脂的吸附机制,采用准一级、准二级动力学模型对第2.2.3节吸附实验结果进行拟合.准一级、准二级动力学方程分别由公式(8)和公式(9)表示[25]:
qt=qe-qee-K1t
(8)
(9)
式中:qe是平衡吸附容量,mg/g;qt是吸附t时间的树脂吸附量,mg/g;K1是准一级反应速率常数;K2是准二级反应速率常数.
拟合结果如图9及表3所示.由图9和表3可知,准二级模型描述树脂吸附Cu2+和Zn2+过程的相关系数R2更大,分别为0.991 0和0.945 9,说明亚胺二乙酸基螯合树脂对Cu2+、Zn2+的吸附反应近似于准二级反应,树脂吸附Cu2+和Zn2+的机制主要为化学吸附[26];准二级动力学速率常数K2可反应吸附速率的快慢,树脂吸附Cu2+的速率常数更高,为2.807,因此较于Zn2+树脂吸附Cu2+的速率更快.
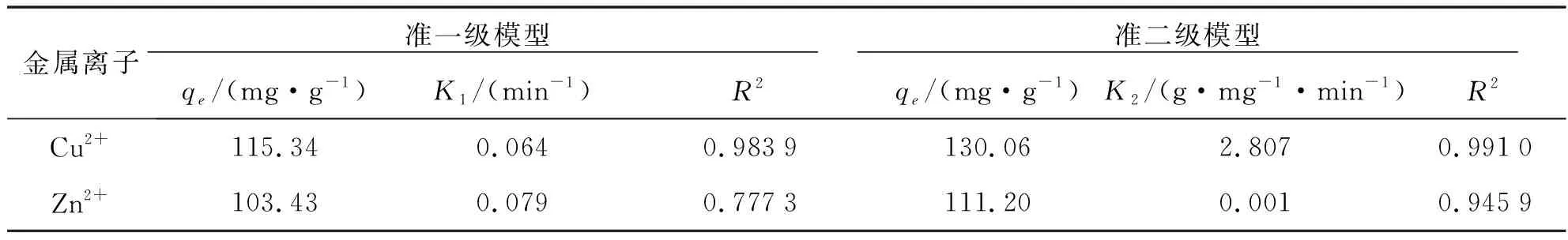
表3 准一级、准二级动力学方程拟合参数
2.4.2 动边界模型
为了分析亚胺二乙酸基螯合树脂对Cu2+、Zn2+吸附过程的速率控制步骤,采用动边界模型对2.2.3节的实验结果进行拟合.膜扩散、颗粒扩散和化学反应速率为控制步骤的模型方程分别由公式(10)~(12)所示[27]:
ln(1-F)=-kt
(10)
(11)
(12)

拟合结果如图10所示.由图10可知,在亚胺二乙酸基螯合树脂吸附Cu2+、Zn2+的过程中,膜扩散速率控制方程的线性相关系数R2最大,分别为0.997 4和0.999 4,因此树脂吸附Cu2+、Zn2+过程的速率控制步骤为膜扩散.

(a)膜扩散 (b) 颗粒扩散 (c)化学反应 图10 速率控制步骤模型拟合Fig. 10 Model fitting of rate control steps: (a) membrane diffusion ;(b) particle diffusion ;(c) chemical reaction
2.5 选择性吸附
上述研究已证明在不同条件下的单金属离子体系中,亚胺二乙酸基螯合树脂对Cu2+的吸附效果均强于Zn2+;分布系数反映了金属离子被树脂吸附的能力,分离系数反映了两种离子的分离效果[28];为了探索两种离子共存情况下树脂对Cu2+的选择吸附性,在Cu-Zn-SO3-H2O二元竞争金属离子体系中开展了锌铜初始浓度比对Cu2+的分布系数(KeCu)、Zn2+的分布系数(KeZn)、Cu2+和Zn2+之间的分离系数(αCu/Zn)影响的实验研究.溶液初始H2SO4浓度为0.3 mol/L、溶液初始Cu2+浓度为300 mg/L、振荡频率为150 r/min、接触时间为120 min,利用1 g干树脂在50 mL溶液中进行选择性吸附实验的结果如图11所示.

图11 Cu-Zn-SO3-H2O体系中的选择性吸附结果Fig. 11 Selective adsorption results in Cu-Zn-SO3-H2O system
由图11可知,Cu2+的分布系数随着锌铜初始浓度比的增加在44.792~52.128 mL/g范围内波动;Zn2+的分布系数随着锌铜初始浓度比的增加由2.347 mL/g升高至9.1 mL/g;在本研究浓度比范围内Cu2+的分布系数明显高于Zn2+的分布系数,说明二元金属离子体系中树脂对Cu2+的吸附性能相比于Zn2+依旧更强;Cu2+和Zn2+之间的分离系数随锌铜浓度比的升高而降低,在锌铜浓度比为25时最大,为18.867,因此尽可能地提高湿法炼锌溶液中Cu2+浓度、降低Zn2+浓度有利于Cu2+的选择性吸附.
2.6 树脂的解吸
首先利用1 g干树脂在50 mL的 Cu-SO3-H2O体系溶液中进行吸附实验,溶液初始H2SO4浓度为0.01 mol/L,初始Cu2+浓度为300 mg/L,在室温、振荡频率为150 r/min、接触时间为120 min的条件下吸附;随后分别用不同质量分数的稀H2SO4溶液解吸15 min,解吸结果如图12所示.
由图12可知,Cu2+的解吸率随解吸剂浓度的增加而增加,当稀H2SO4溶液浓度为12%时Cu2+的解吸率达88.27%;考虑实际工业生产中解吸液酸度过高会增加后期含铜溶液处理成本,故选择10%的稀H2SO4溶液进行了后续解吸时间的影响实验.

图12 解吸剂浓度对解吸率的影响Fig. 12 Influence of desorption concentration on desorption rate
在上述吸附-解吸条件下,解吸时间对Cu2+解吸率的影响结果如图13所示.由图13可知,在本研究时间梯度内,Cu2+的解吸率在90.5%~93.1%范围波动;解吸时间为30 min时,解吸率达到最大值93.1%.

图13 解吸时间对解吸率的影响Fig. 13 Influence of desorption time on desorption rate
3 结 论
通过以上研究,可得出以下结论:
1)在Cu-SO3-H2O、Zn-SO3-H2O的单一金属离子体系中,亚胺二乙酸基树脂对Cu2+和Zn2+均有很强的吸附能力,但树脂对Cu2+的吸附量更大,吸附率更高;溶液含H2SO4浓度为0.01 mol/L时,树脂对Cu2+和Zn2+的吸附率分别为98.88%和97.94%;溶液含H2SO4浓度为0.1 mol/L时,树脂对Cu2+的吸附率比Zn2+高55.33%,吸附率差值达到最大;可利用树脂对两种离子吸附性能的差异将其分离.
2)亚胺二乙酸基螯合树脂对Cu2+和Zn2+的吸附均为多分子层吸附,吸附机制主要是化学吸附,离子交换过程速率控制步骤为膜扩散.
3)在Cu-Zn-SO3-H2O的二元竞争离子体系中,Cu2+的分布系数明显高于Zn2+的分布系数,树脂可将Cu2+高效地选择性分离,且Cu2+和Zn2+之间的分离系数随锌铜浓度比升高而降低,提高Cu2+浓度、降低Zn2+浓度有利于提高树脂对Cu2+的选择性分离效果.用质量分数为10%的稀H2SO4溶液解吸30 min,Cu2+的解吸率为93.1%,有望使用亚胺二乙酸基螯合树脂高效回收实际湿法炼锌工业系统酸性浸出液中的铜.

