复方紫草温敏凝胶的制备与质量评价
徐 科,吴赟杰,李金洋,赵君晰,张泽瀚,梁晓霞
(四川农业大学动物医学院天然药物研究中心,成都 611130)
皮肤[1-2]作为人体与外界的主要物理屏障,经常受到不同程度的伤害,因而皮肤创伤是对我们医疗系统的巨大挑战,大至手术创伤,小至口腔溃疡,无一不给患者造成了长期的医学(如疼痛、瘙痒、活动范围缩小)和心理社会损害,也给社会带来极大的负担。更有甚者如糖尿病引发的难治性溃疡还可能导致患者的截肢[3]。因此,开发一款高效、稳定、持久且既能保护创面又能促进皮肤修复的创伤愈合药物在医学应用领域具有重要意义。
紫草[4],又名新疆紫草,药用历史悠久。同时紫草在各类创伤愈合和修复中也有大量应用实例:“紫草润肌膏”使用紫草、当归等药材进行组方治疗火烫,发泡腐烂;“紫草膏”中使用紫草、当归白芷等药材进行组方,治疗热疮;“紫云膏”中使用紫草、当归和冰片等药材进行组方治疗水火烫伤,溃烂化脓;《新疆中草药手册》中使用紫草、当归和黄柏等药材进行组方达到化腐生肌。综上所述,用于皮肤创伤治疗的处方中使用频率较高的药材包括紫草、当归、黄柏、白芷和冰片等。因此本研究结合多个经典方剂,并在古方剂的基础上加减配伍与用量,拟定了紫草复方(紫草∶当归∶黄柏∶白芷∶冰片=5∶4∶2∶2∶0.5)。方中紫草[5]凉血热、生新血,解毒生肌,对烧伤创面有积极作用,为君药;当归[6]为“血中圣药”,长期用于滋补气血,同时能促进新鲜肉芽组织生长,为臣药;黄柏[7]、白芷[8]抗菌燥湿、消肿止痛,为佐药,冰片[9]清热止痛,同时增加皮肤渗透作用,为使药。该组方能参与创伤修复的全过程,既可缓解早期临床症状体征,又可促进创面早日愈合。
温敏凝胶[10-12](hermosensitive gels)是一类在室温下的为聚合低黏度水溶液状态,但随着环境温度的升高(如达到生理温度)可发生溶胶-凝胶转变的一种新型给药剂型,目前温敏凝胶在人类多种疾病治疗方面已经得到广泛应用。泊洛沙姆[13-14](Poloxamer)是聚环氧乙烷-聚环氧丙烷-聚环氧乙烷(PEO-PPO-PEO)形式的三嵌段共聚物。中心PPO嵌段是疏水的,而侧PEO嵌段是亲水的,从而产生表面活性性质,因具有精细可调的溶胶-凝胶转变温度而表现出良好的热凝胶性。基于泊洛沙姆的多种产品已经进入药物市场,但仍是进一步研究和商业开发的潜在领域,目前P407和P188是两种最常用的温敏材料[15],多将其配合进行使用。
本研究采用现代制药技术,将疗效确切的紫草复方与温敏凝胶相结合,制成一种温度敏感型外用凝胶制剂,在筛选出最佳处方后对所制得凝胶的各种体外参数进行了表征,例如:紫草素含量、性状、pH值、黏度、胶凝温度、胶凝时间、稳定性试验、保湿率和微生物限度等,旨在为各种创伤的愈合提供更好的新选择。
1 材料和方法
1.1 试验材料
ESJ200-4A分析天平(苏州安泰空气技术有限公司);B-220恒温水浴锅(上海亚荣生化仪器厂);pH酸度计(重庆塞恩斯仪器有限公司);NDJ-5S黏度计(上海昌吉地质仪器有限公司);UV-1102紫外可见分光光度计(中国天美科学仪器有限公司);GTOP-1588恒温培养箱(浙江拓普仪器有限公司);DT-131电子温度计。新疆紫草(Arnebiaeuchroma(Royle)Johnst)、当归(Angelicasinensis(Oliv.)Diels)、黄柏(Phellodendri Chinensis Cortex)、白芷(Angelica dahurica(Fisch.ex Hoffm.)Benth.et Hook.f.)、冰片(成都市药材公司)。泊洛沙姆407(P407,德国BASF公司)、泊洛沙姆 188(P188,德国 BASF公司);甘油(成都市科龙化工试剂厂);紫草素对照品(成都曼斯特生物科技有限公司);水为蒸馏水;其余试剂均为分析纯。
1.2 药液的制备
采用水煎法[16-17],根据组方量(紫草∶当归∶黄柏∶白芷=5∶4∶2∶2)称取药材,总量为195 g,第一次加8倍水煎煮1 h,倒出水提液,再加6倍水煎煮1 h,合并两次水提液,混合均匀,浓缩至195 mL,再往水提液中加入7.5 g冰片,备用。
1.3 温敏凝胶制剂工艺研究
1.3.1 温敏凝胶的制备
采用“冷法”[18-19]来制备基于泊洛沙姆的温敏凝胶,准确称取处方量的P407和P188,加入适量蒸馏水,搅拌均匀,置于4℃冰箱内24 h以上,直到P407和P188完全溶解,使其充分溶胀后得到澄清溶液,若凝胶中含有其他辅料,可根据其用量的多少在温敏凝胶基质加入前溶于蒸馏水中,再按上述步骤制备。
1.3.2 胶凝温度的测定
采用倾斜法[20],取5 mL左右凝胶于小西林瓶中,开启水浴锅使水浴持续缓慢升温,每升高1℃恒温10 min,每15 s倾斜一次西林瓶,倾斜角度约90℃,待凝胶不再流动时插入电子温度计(精确到0.1℃)记录温度计的读数,即为胶凝温度。每个样品重复测量3次,取平均值。
本研究的复方紫草温敏凝胶设计为皮肤创伤外用制剂,因此胶凝温度应高于环境温度(室温),低于皮肤温度(33.5±0.5)℃,故将温敏凝胶的最佳胶凝温度设置为33℃[21]。
1.3.3 单因素实验
(1)P407含量对胶凝温度的影响
据文献报道[22]P407浓度低于15%时失去胶凝能力。因此,本试验中,以P407的质量与蒸馏水的质量比(W/W)为考察因素,精密称取P407,按1.3.1的方法配制5组质量百分浓度分别为16%、18%、20%、22%和24%的P407溶液,按1.3.2的方法测定胶凝温度。
(2)P188含量对胶凝温度的影响
以P188的质量与蒸馏水的质量比(W/W)为考察因素,在1.3.3.1确定的P407含量(18%)的基础上,精密称取P188,按1.3.1的方法配制5组质量百分浓度分别为2%、4%、6%、8%和10%的P188溶液,按1.3.2的方法测定胶凝温度。
(3)甘油含量对胶凝温度的影响
以甘油的质量与蒸馏水的质量比(W/W)为考察因素,在1.3.3.2确定的P188含量(2%)的基础上,精密称取甘油,按1.3.1的方法配制5组质量百分浓度分别为4%、6%、8%、10%和12%的甘油溶液,按1.3.2节方法测定胶凝温度。
1.3.4 正交试验
根据单因素实验结果,综合分析,选择P407、P188和甘油作为3个考察因素,以胶凝温度作为考察指标,每个因素选择3个水平,按L9(3)3设计正交试验,优化制备工艺。
1.3.5 复方紫草药液含量的筛选
以复方紫草药液的质量与蒸馏水的质量比(W/W)为考察因素,根据1.3.4的结果,确定泊洛沙姆P407的含量(16%)、泊洛沙姆 P188的含量(2%)、甘油的含量(4%),精密称取复方紫草药液,按1.3.1的方法配制5组质量百分浓度分别为4%、6%、8%、10%和12%的含药凝胶溶液,按1.3.2节方法测定胶凝温度。
1.3.6 复方紫草温敏凝胶的优化制备工艺
取蒸馏水60 g,加入精密称取的P407计16 g,P188计2 g,溶散均匀后,加入甘油4 g,复方紫草药液8 g,并补足蒸馏水至100 g,混合均匀,充分润湿,置于4℃冰箱过夜,充分溶胀,即得复方紫草温敏凝胶。
1.4 复方紫草温敏凝胶剂的质量评价
1.4.1 紫草素含量
由于本研究制备的复方紫草温敏凝胶中,紫草为君药,且紫草的有效成分为其萘醌类成分(羟基萘醌总色素),故参照《中华人民共和国药典》2020版一部[23]药材与饮片中紫草的含量测定,照紫外-可见分光光度法(通则0401),以左旋紫草素(C16H16O5)计本研究制备的复方紫草温敏凝胶中萘醌类成分(羟基萘醌总色素)并对其进行含量测定。
(1)确定测定波长
准确称取5 mg紫草素对照品,用乙醇溶解并定容于100 mL容量瓶中,摇匀得浓度为50 mg/L的对照品溶液。在200~800 nm的波长范围内对紫草对照品溶液进行全波长扫描。
(2)绘制标准曲线
精密量取1.0 mL紫草素对照品溶液,置于10 mL容量瓶中,加入乙醇溶液定容并摇匀配制成浓度为5 mg/L的紫草素溶液,同法依次配制出浓度分别为10、15、20、25、30、35、40、45 和 50 mg/L 的紫草素溶液,置于1 cm石英吸收池中,以相同的乙醇溶液做空白,在波长为513 nm处测定吸光度后绘制标准曲线方程。
(3)紫草素的含量的确定
精密称定1.0 g复方紫草温敏凝胶,加入精密称量的乙醇10 mL,超声溶解离心后制备供试品溶液[24],在波长为513 nm处测定其吸光度,将其吸光度值代入标准曲线公式中,即得复方紫草温敏凝胶中紫草素含量。
1.4.2 性状
取“1.3.6”项制备的复方紫草温敏凝胶适量分别在室温条件下与33℃左右的皮肤表面观察凝胶的性状。
1.4.3 pH值
《中华人民共和国药典》2020版四部[25]通则中规定,凝胶剂一般应检查其pH值,故按照《中华人民共和国药典》2020版四部附录0631中的方法,取“1.3.6”项制备的复方紫草温敏凝胶20 mL置于烧杯中,使用4和7的酸碱度缓冲液校准数字酸度计后将玻璃电极充分浸入制剂样品中,然后用数字酸度计直接测定复方紫草温敏凝胶的pH值,平行重复3次。
1.4.4 黏度
黏度是反映凝胶流变学性能的重要参数,因此采用NDJ-5S型旋转黏度计,按《中华人民共和国药典》2020版四部附录0633,参照旋转黏度计测定法[26-28],利用与黏度计接触的恒温水浴调节样品的温度,测定不同温度下“1.3.6”项制备的复方紫草温敏凝胶黏度(η),平行重复3次。
1.4.5 胶凝温度
取适量“1.3.6”项制备的复方紫草温敏凝胶于西林瓶中,置于恒温水浴锅中缓慢升温,升温速度为1℃/min,每15 s倾斜一次西林瓶,倾斜角度约90°,待凝胶不再流动时用电子温度计测定凝胶的温度,温度计的读数即为胶凝温度。平行重复3次。
1.4.6 胶凝时间
取适量“1.3.6”项制备的复方紫草温敏凝胶于西林瓶中,放置在33℃下的恒温水浴锅中内,每15 s倾斜一次西林瓶,倾斜角度约90℃,记录西林瓶中的液体不再流动时的时间即为凝胶化时间。平行重复3次。
1.4.7 稳定性试验
(1)离心试验
取适量“1.3.6”项制备的复方紫草温敏凝胶于离心管中,观察2 000 r/min离心20 min后凝胶的外观形态变化。平行重复3次。
(2)低温试验
取适量“1.3.6”项制备的复方紫草温敏凝胶于带塞西林瓶中,放入4℃冰箱内,分别在0、15和30 d取样。分别从凝胶的外观性状、pH值和胶凝温度等方面考察其制剂的稳定性。
(3)高温试验
取适量“1.3.6”项制备的复方紫草温敏凝胶于带塞西林瓶中,放入60℃恒温干燥箱内,分别在0、15和30 d取样。分别从凝胶的外观性状、pH值和胶凝温度等方面考察其制剂的稳定性。
1.4.8 保湿率
取适量“1.3.6”项制备的复方紫草温敏凝胶,均匀涂布于载玻片上,精密称量复方紫草温敏凝胶在干燥前的质量(m1)后,将该玻片置于33°C的恒温密封干燥器中,放置24 h后取出,精密称定复方紫草温敏凝胶干燥至恒定的质量(m2),根据公式:保湿率=m1/m2,计算其保湿率。平行重复3次。
1.4.9 微生物限度
《中华人民共和国药典》2020版四部通则中规定,凝胶剂一般应照非无菌产品检查其微生物限度,依据《中华人民共和国药典》中的微生物计数法(通则1105)、控制菌检查法(通则 1106)和非无菌药品的微生物限度标准(通则1107)对“1.3.6”项制备的复方紫草温敏凝胶进行检查。
1.5 数据处理
采用Microsoft Excel 2016进行数据整理,采用IBM SPSS Statistics 23.0和Graph Pad Prism8.0软件进行统计学分析和图形绘制。
2 结果与分析
2.1 单因素试验结果
2.1.1 P407含量对胶凝温度的影响
P407含量对胶凝温度的影响结果见图1a。根据图1a可知,胶凝温度随P407含量的增加而降低。这可能是与P407在水中的胶凝机制有关[29]。P407的水溶液显示出热可逆性质,其特征是存在溶胶-凝胶转变温度,当低于此温度时,P407呈现液体状态,但当高于此温度时,P407由溶液状态变为半固体的凝胶状态。这种热凝胶化是共聚物不同链段之间相互作用的结果,随着温度的升高,由于疏水PPO嵌段的脱水,P407共聚物分子聚集成胶束,这些胶束是球形的,有脱水的聚氧乙烯核与水合膨胀的聚氧乙烯链外壳,对于足够浓缩的样品,这种胶束化之后便是凝胶化,这种凝胶化归因于胶束的有序堆积。
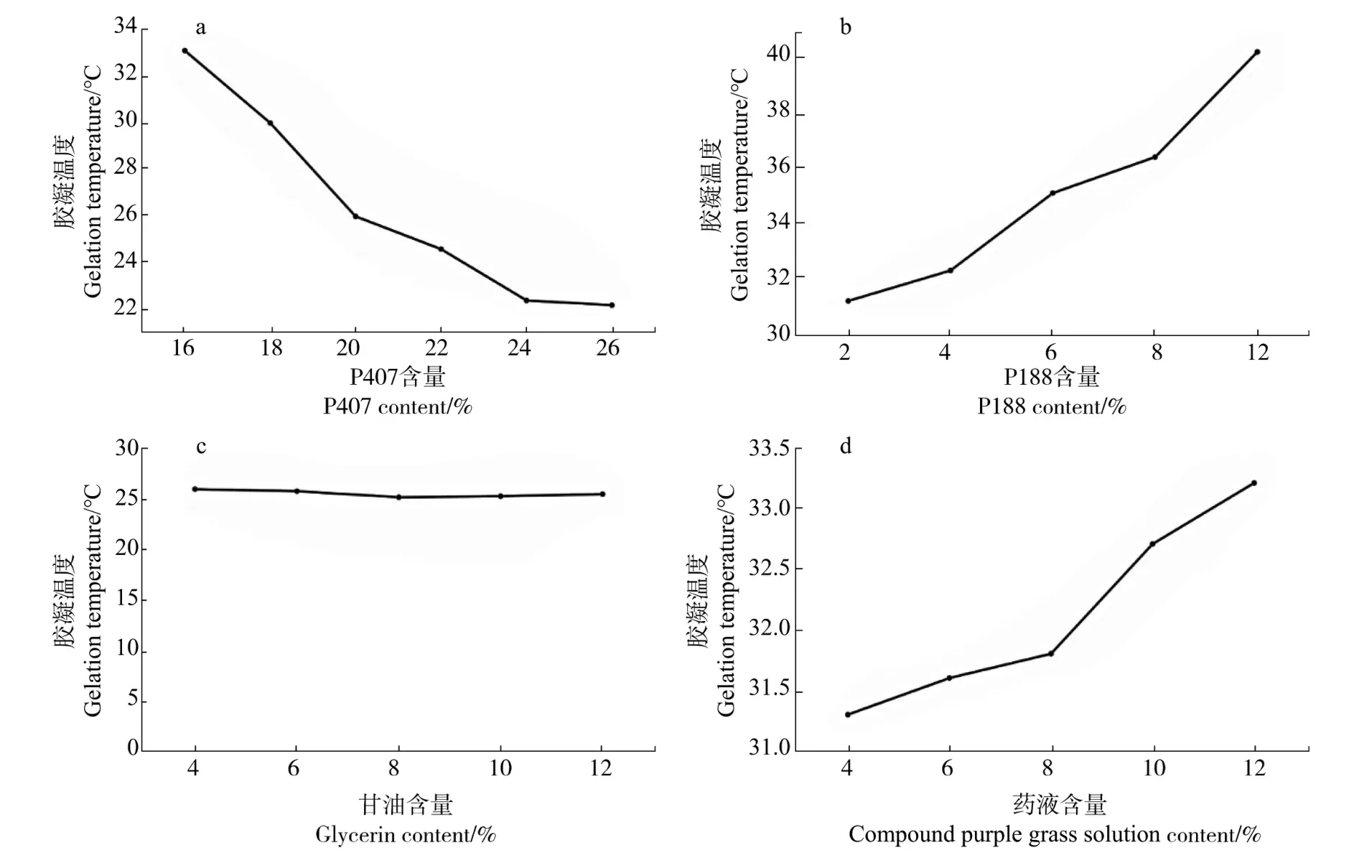
图1 P407(a)、P188(b)、甘油(c)以及复方紫草药液(d)含量对胶凝温度的影响Figure 1 P407(a),P188(b),glycerin(c),compound purple grass solution(d)on gelation temperature
根据P407含量对胶凝温度影响的试验结果并结合实际需要,选择更接近人体皮肤温度的3个P407含量(16%、18%和20%)作为正交试验因素水平,同时选择目前最优的P407含量(18%)作为P188含量对胶凝温度影响试验的研究基础。
2.1.2 P188含量对胶凝温度的影响
P188含量对胶凝温度的影响结果见图1b。根据图1b可知,在确定含量的P407(18%)条件下,胶凝温度随P188含量的增加而升高。在P407中加入适量的P188后,其胶凝温度发生改变,其原因可能是P188的亲水性PEO嵌段/疏水性PPO嵌段的比为8∶2,亲水基团比例相对增加,疏水基团比例相对减少,从而提高了整个凝胶体系的胶凝温度[30]。
根据P188含量对胶凝温度影响的试验结果并结合实际需要,选择更接近人体皮肤温度的3个P188含量(2%、4%、6%)作为正交试验因素水平,同时选择目前最优的P188含量(2%)作为甘油含量对胶凝温度影响试验的研究基础。
2.1.3 甘油含量对胶凝温度的影响
甘油含量对胶凝温度的影响结果见图1c。根据图1c可知,在确定含量的P407(18%)和P188(2%)条件下,胶凝温度随甘油含量的增加而略微降低。
根据甘油含量对胶凝温度影响的试验结果并结合实际需要,选择更接近人体皮肤温度的3个甘油含量(4%、6%、8%)作为正交试验因素水平。
2.2 正交实验结果
正交试验的因素水平见表1,正交试验结果见表2,方差分析见表3。
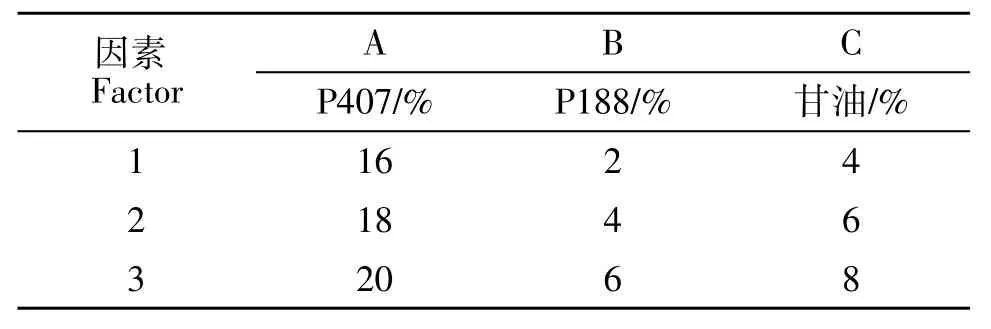
表1 正交试验因素水平表Table 1 Level of factors for orthogonal test
表2 正交实验结果(±SD,n=3)Table 2 Orthogonal test results(±SD,n=3)

表2 正交实验结果(±SD,n=3)Table 2 Orthogonal test results(±SD,n=3)
试验号Test number Gelation temperature/℃P407/% P188/% 甘油/%因素Factor 胶凝温度1 16 2 4 32.07±0.12 2 16 4 6 33.50±0.10 3 16 6 8 34.23±0.12 4 18 2 6 30.33±0.15 5 18 4 8 31.67±0.15 6 18 6 4 33.30±0.10 7 20 2 8 29.87±0.06 8 20 4 4 30.47±0.06 9 20 6 6 31.73±0.15

表3 方差分析Table 3 Analysis of variance
本试验期望该制剂能在高于环境温度(室温),且低于皮肤温度(33.5±0.5)℃时由原来的可流动的溶液变成半固体凝胶,因此该凝胶的最适胶凝温度应不大于(33.5±0.5)℃(即≤33℃),且越接近33℃越适宜,因此根据表2正交实验结果直观分析可知,凝胶最佳配比的组合为A1B1C1,即:16%P407+2%P188+4%甘油。根据表3方差分析可知,3个因素对胶凝温度的影响大小为:P407含量>P188含量>甘油含量,P407含量对胶凝温度的影响最大,P188和甘油对胶凝温度起调节作用。
2.3 复方紫草药液含量的筛选结果
复方紫草药液含量的筛选结果见图1d。根据图1d可知,随着复方紫草药液含量的增加,胶凝温度不断上升,综合考虑药物用量对胶凝温度的影响及成品外观,选择加药量为8%。
2.4 复方紫草温敏凝胶剂的质量评价结果
2.4.1 紫草素含量
在200~800 nm的波长范围内对紫草对照品溶液进行全波长扫描,最终结果显示,紫草素在(513±1)nm的波长处有最大吸收峰。以乙醇溶液做空白,在波长为513 nm处测定不同浓度紫草素对照品溶液的吸光度,得到标准曲线方程:A=0.107 2C+0.008 1(r2=0.999 4,n=10),结果表明紫草素浓度(C)与吸光度(A)的线性关系良好(图2)。将复方紫草温敏凝胶的吸光度值代入标准曲线公式中,即得复方紫草温敏凝胶中紫草素浓度为116.595 mg/L。
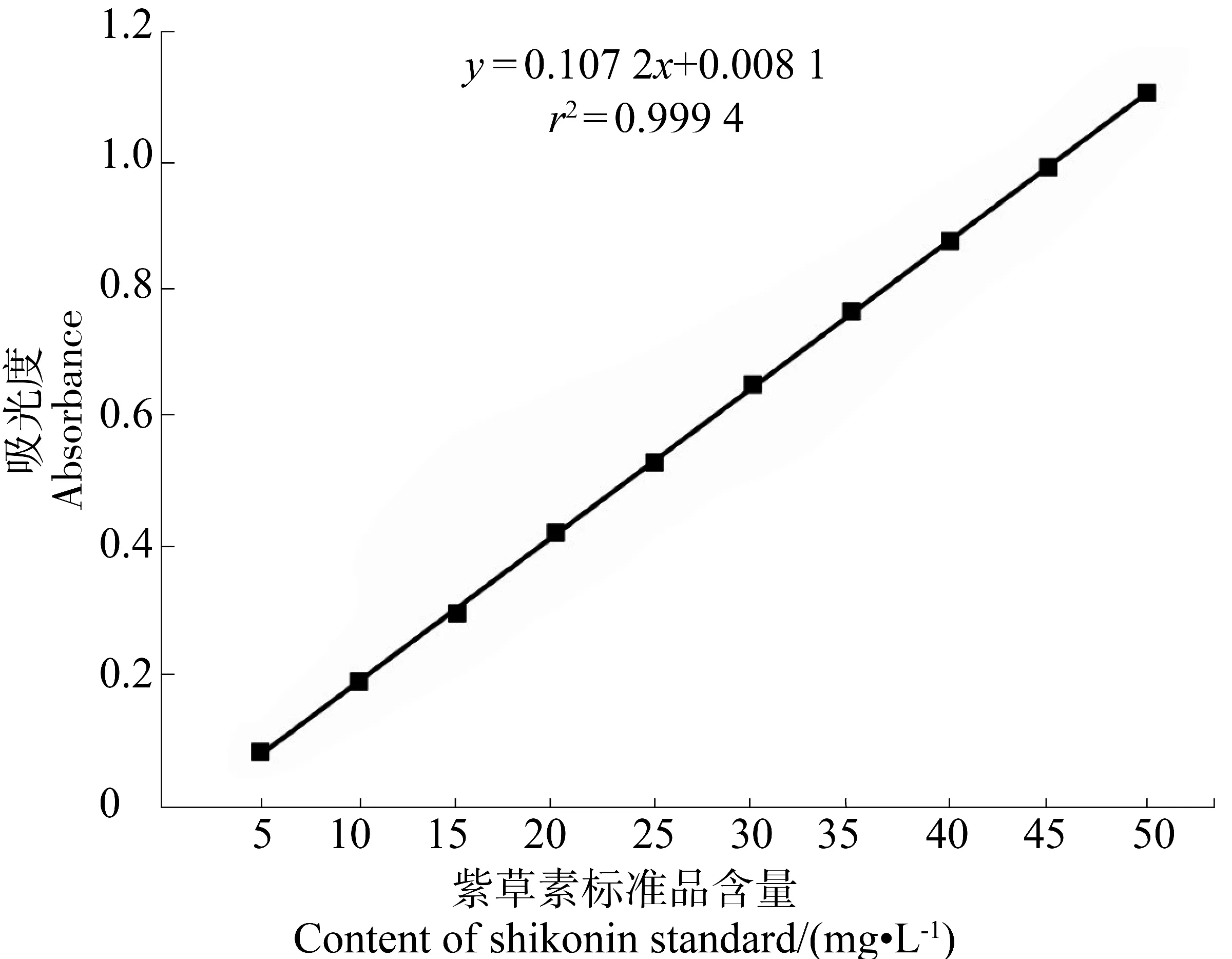
图2 紫草素标准曲线Figure 2 The standard curve of shikonin
2.4.2 性状
“1.3.6”项制备的复方紫草温敏凝胶在室温条件下为棕绿色均匀的凝胶溶液,涂抹于33℃左右的皮肤表面,结果转变为棕绿色半固体凝胶。
2.4.3 pH值
“1.3.6”项制备的复方紫草温敏凝胶的pH值为4.80±0.5,适合涂抹于皮肤表面。
2.4.4 黏度
“1.3.6”项制备的复方紫草温敏凝胶黏度测量结果见表4。结果表明复方紫草温敏凝胶在室温下黏度较低,具有良好的流动性,经过升温,在模拟皮肤表面温度33℃下发生变,形成黏度较大的半固体凝胶状态。

表4 不同温度下凝胶的黏度Table 4 Viscosity of gels at different temperatures
2.4.5 胶凝温度
“1.3.6”项制备的复方紫草温敏凝胶的胶凝温度为(32.8±0.3)℃,当涂抹于皮肤表面能较好黏附于皮肤表面,胶凝温度良好。
2.4.6 胶凝时间
“1.3.6”项制备的复方紫草温敏凝胶的胶凝时间为(45±4)s,当涂抹于皮肤表面能较好黏附于皮肤表面,胶凝时间良好。
2.4.7 稳定性试验
(1)离心试验
“1.3.6”项制备的复方紫草温敏凝胶经离心试验后结果显示凝胶仍保持均匀澄清,均未出现分层现象。
(2)低温试验
“1.3.6”项制备的复方紫草温敏凝胶低温试验结果见表5。结果表明,复方紫草温敏凝胶在低温条件下较为稳定,可长期贮存。

表5 低温试验结果Table 5 Low temperature test results
(3)高温试验
“1.3.6”项制备的复方紫草温敏凝胶高温试验结果见表6。结果表明,复方紫草温敏凝胶在高温条件下各方面均出现一定的变化,不可长期贮存。
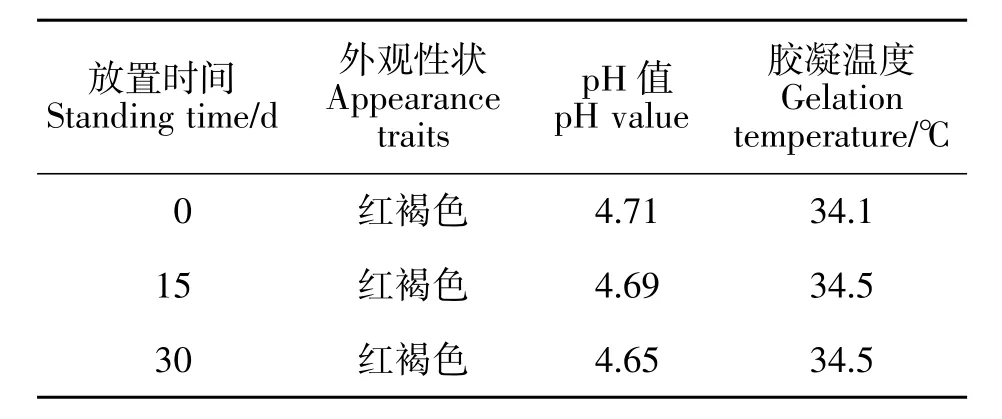
表6 高温试验结果Table 6 High temperature test results
2.4.8 保湿率
“1.3.6”项制备的复方紫草温敏凝胶的保湿率为(96.74±0.71)%,表明其保湿性良好,有利于在皮肤上涂展。
2.4.9 微生物限度
“1.3.6”项制备的复方紫草温敏凝胶的微生物限度结果见表7,结果符合药典标准。

表7 微生物限度的检测结果Table 7 Detection of microbial limits
3 讨论
近年来,在国内外学者的共同努力下,创伤修复的研究已经取得了重大进展,但目前的创伤治疗剂型仍以喷剂、膏剂、酊剂和粉剂为主。其中,喷剂给药量小,故需多次使用,十分麻烦,同时生产容器时成本较高;膏剂的吸收效果不好,经常要使用透皮吸收促进剂,且常因透气性不好加速感染;酊剂很容易挥发,必须反复涂抹,且其含有大量酒精易刺激新生皮肤,增加患者痛苦并易留下瘢痕,治疗效果不甚理想。而温敏凝胶可以很好解决上述问题,该制剂在常温状态下为自由流动的液体状态,当接触到温度的升高时,会转变为半固体状态凝胶,对创面具有保护作用,使用方便,不对创面产生刺激,同时具有延缓药物释放,延长药物作用时间,提高生物利用度。因此本研究利用复方紫草的改善局部创面组织的血液循环、抗炎、抗菌、加快肉芽组织生成和细胞趋化因子表达等功效,促进创口愈合,同时结合温敏进行质量凝胶的缓释及伤口保护作用,“强强联合”制成一种治疗创伤的外用制剂。
在大多数报道的基于泊洛沙姆的研究中在原位凝胶,P407单独用作胶凝剂,这导致了两个主要缺点:首先,P407适合使用的浓度范围非常窄,大约为16%~20%(W/W)。当浓度小于15%(W/W)时,无论温度如何,制剂都不能形成凝胶。如果高于20%(W/W),临界温度将低于20℃,给使用和储存带来不便;第二,由于凝胶的稠度较低且抗稀释性较差,对药物从形成的凝胶中释放的控制有时不够充分,这意味着凝胶的强度随着体液的渗透而急剧下降。因此,配方的相变温度可以通过简单地添加另一种泊洛沙姆(P188)来调节,P188具有比P407更高的PEO与PPO嵌段比,在研究中与P407结合使用,可以上调制剂的相变温度,从而提高P407的使用上限,同时解决由于单一种类的泊洛沙姆形成的胶束有很多问题,例如胶凝温度不理想、载药量低和凝胶溶液不稳定等。
根据本研究的单因素试验结果可知,处方中P407和P188含量对复方紫草温敏凝胶的凝胶化温度具有显著影响,凝胶化温度随P407含量的增加而降低;在P407含量一定时,凝胶化温度随着P188含量的增加而升高,凝胶化温度随甘油和复方紫草药液含量的变化改变不大。
4 结论
本研究通过正交试验进行处方优化,制备得到一款复方紫草温敏凝胶,其最优处方为:16%P407+2%P188+4%丙三醇+8%复方紫草药液,其凝胶化温度为(32.8±0.3)℃。制剂质量评价显示:复方紫草温敏凝胶的紫草素含量、状、pH值、黏度、胶凝温度、胶凝时间、稳定性试验、保湿率和微生物限度等各方面性质较为稳定。

