基于固载腐植酸凝胶光子晶体的镉离子可视化传感研究
李荣振,南 境,余莉萍*,肖文理
(1.天津大学理学院,天津 300350;2.新疆工程学院化学与环境工程学院,新疆 乌鲁木齐 830052)
凝胶光子晶体将光子晶体的周期性长程有序结构固定在水凝胶中,是一类既具有光子带隙性能又对外界环境变化具有响应性的新型材料[1]。凝胶光子晶体具有信号自表达特性,能把环境变化引起水凝胶体积的膨胀或收缩通过光子带隙变化表现出来,有时还可以引起光子晶体结构颜色发生变化,从而实现裸眼可视检测[2]。凝胶光子晶体传感器具有响应速度快、灵敏度高和选择性好的优点,已应用于多种物质的传感,如温度[3]、湿度[4]、压力[5]、pH值[6]、磁场[7]、电场[8]和化学物质[9]等,还可以用于结构生色[10]和色谱芯片[11]等。依据识别基团与目标化合物之间的作用方式(如分子印迹、共价键合或配位作用等)设计合成具有特定识别能力的凝胶光子晶体、实现目标化合物的快速传感和定量检测是目前凝胶光子晶体在分析检测领域的发展方向。
重金属离子如Pb2+、Cu2+、Cd2+等难以被生物降解,对环境和人体健康都有很大的威胁[12-14],会通过食物链富集进入到人体,造成慢性中毒;过量的Cd2+会损害肾小管,减缓骨骼的新陈代谢。腐植酸广泛存在于自然界中,其结构中含有丰富的羧基、羰基和酚羟基,具有较高的反应活性,对包括Cd2+在内的环境中的金属离子具有强烈结合能力[15]。如果将腐植酸引入到水凝胶前驱体溶液中,填充入光子晶体,制得具有特定响应性的凝胶光子晶体,可以实现检测水溶液中金属离子的目的。
基于此,作者制备固载腐植酸的凝胶光子晶体,利用腐植酸与Cd2+的配位作用,结合凝胶光子晶体的自表达传感机制,构建一种新颖的Cd2+传感方法,考察pH值、平衡时间、离子强度等对固载腐植酸凝胶光子晶体响应Cd2+的影响,建立固载腐植酸凝胶光子晶体光子带隙与Cd2+浓度的关系,以实现对Cd2+的可视化可逆传感。
1 实验
1.1 试剂与仪器
冰醋酸、醋酸钠、浓硫酸、双氧水、硝酸钾、聚苯乙烯(PS)、过硫酸铵(APS)、丙烯酰胺(AMD)、丙烯酸(AAC)、N,N′-亚甲基双丙烯酰胺(BIS)、腐植酸(HA)等试剂均为分析纯,天津科威公司;实验用水为二次蒸馏水。
Nova NanoSEM 430型场发射扫描电镜,FEI公司;JKHQ-D1型光纤光谱仪,天津津科浩强科技有限公司;FE20K型pH 计,德国梅特勒-托利多公司;DZG-4018型电热真空干燥箱,天津天宇实验仪器有限公司;BT-125D型电子天平,德国赛多利斯科学仪器有限公司。
1.2 固载腐植酸凝胶光子晶体的制备
先采用乳液聚合法制备粒径(210 nm左右)均匀的聚苯乙烯微球乳液。然后,按照微球乳液与水体积比为1∶15的比例将一定质量的聚苯乙烯微球乳液加入到盛有二次蒸馏水的烧杯中,超声振荡混合均匀,得到聚苯乙烯胶体溶液。再将用浓硫酸/双氧水处理过的载玻片插入到聚苯乙烯胶体溶液中,在43 ℃水浴中进行垂直自组装。随着水分的不断蒸发,聚苯乙烯微球在载玻片上逐层沉积,自组装成光子晶体模板。最后,将光子晶体模板置于80 ℃烘箱中干燥2 h后,备用。
取3.0 g丙烯酰胺、0.08 gN,N′-亚甲基双丙烯酰胺、0.09 g过硫酸铵、1.6 mL丙烯酸,溶解在4 mL腐植酸溶液(0.01 g腐植酸溶于4 mL 1×10-5mol·L-1NaOH溶液中)中,充分混合后制成前驱体溶液。然后,将前驱体溶液滴加在覆盖有光子晶体模板的载玻片上端,通过毛细力渗透填充到光子晶体模板的空隙中。再在55 ℃下热引发聚合反应6 h,得到固载腐植酸的凝胶光子晶体。
1.3 光子晶体的结构表征
采用场发射扫描电镜(SEM)观察光子晶体模板及固载腐植酸凝胶光子晶体的表面形貌,电压5 kV。采用光纤光谱仪在垂直光子晶体表面的方向记录光子带隙。
1.4 传感实验
采用醋酸-醋酸钠缓冲溶液调节实验溶液的pH值。根据不同实验目的,将固载腐植酸凝胶光子晶体在4 mL相应的溶液中浸泡10 min后,记录光子带隙。考察传感影响条件时,保持Cd2+溶液浓度为1×10-7mol·L-1,每换一次条件记录一次光子带隙。考察固载腐植酸凝胶光子晶体对不同浓度Cd2+的响应,考察顺序从低浓度到高浓度进行。
2 结果与讨论
2.1 固载腐植酸凝胶光子晶体的结构和光学性质
采用垂直沉积法自组装所得的光子晶体模板和固载腐植酸凝胶光子晶体的SEM照片如图1所示。

图1 光子晶体模板(a)和固载腐植酸凝胶光子晶体(b)的SEM照片Fig.1 SEM images of photonic crystal template(a) and HA-immobilized hydrogel photonic crystal(b)
由图1可知,光子晶体模板呈面心立方结构;固载腐植酸凝胶光子晶体在经过填充和聚合后,光子晶体的面心立方结构被固定于凝胶体系中,填充和聚合过程都没有破坏模板的光子晶体结构。
2.2 固载腐植酸凝胶光子晶体的传感条件优化
2.2.1 pH值
理论上,pH值既影响腐植酸与Cd2+的配位作用,也影响凝胶光子晶体的溶胀性能。采用醋酸-醋酸钠缓冲溶液调节Cd2+溶液pH值分别为3.0、3.5、4.0、4.5、5.0、5.5、6.0,以不含Cd2+溶液为空白对照,考察固载和未固载腐植酸凝胶光子晶体在不同pH值的1×10-7mol·L-1Cd2+溶液中的光子带隙变化(Δλ),结果如图2所示。

图2 固载和未固载腐植酸凝胶光子晶体在不同pH值Cd2+溶液中的光子带隙变化Fig.2 Photonic bandgap variation of HA-immobilized and HA-unimmobilized hydrogel photonic crystals in Cd2+ solution with different pH values
由图2可知,未固载腐植酸的凝胶光子晶体的光子带隙在不同pH值Cd2+溶液中的变化很小;而固载腐植酸的凝胶光子晶体的光子带隙在pH值为3.0~5.5的Cd2+溶液中的变化较明显,在pH值为5.5~6.0时变化不大。表明固载腐植酸凝胶光子晶体的响应性来自于固载其中的腐植酸对Cd2+的配位作用;在pH值为5.5~6.0时,腐植酸与Cd2+的配位作用以及凝胶光子晶体的响应性都达到了稳定状态。因此,后续实验均在pH值为5.5的Cd2+溶液中进行。
2.2.2 平衡时间
先将固载腐植酸凝胶光子晶体在pH值为5.5的缓冲溶液中浸泡15 min,达到溶胀平衡;然后将其置于pH值为5.5的1×10-7mol·L-1Cd2+溶液中,每隔1 min测定一次光子带隙,连续测定30 min,结果如图3所示。

图3 固载腐植酸凝胶光子晶体在1×10-7 mol·L-1 Cd2+溶液中的光子带隙与时间的关系Fig.3 Relationship between photonic bandgap of HA-immobilized hydrogel photonic crystal and time in 1×10-7 mol·L-1 Cd2+ solution
由图3可知,固载腐植酸凝胶光子晶体的光子带隙在9 min以前变化很快,但在9 min以后变化很小。表明,在实验条件下固载腐植酸凝胶光子晶体对Cd2+的响应性在9 min内就能达到稳定。因此,后续传感平衡时间定为10 min。
2.2.3 离子强度
配制浓度(mol·L-1)分别为0、1×10-5、1×10-4、1×10-3、0.01、0.1、1.0的KNO3溶液,分别加入到pH值分别为3.0、3.5、4.0、4.5、5.0、5.5、6.0的1×10-7mol·L-1Cd2+溶液中,测定固载腐植酸凝胶光子晶体在溶液中的光子带隙,考察离子强度对传感的影响,结果如图4所示。
由图4可知,在不同pH值Cd2+溶液中,KNO3浓度对固载腐植酸凝胶光子晶体传感Cd2+的影响均很小。表明,对传感低浓度Cd2+来说,1.0 mol·L-1以下离子强度的KNO3溶液的影响可以忽略不计。
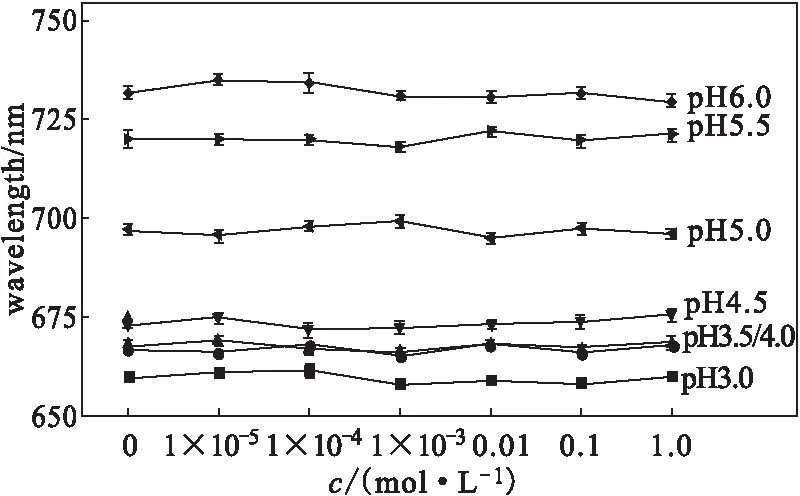
图4 加入不同浓度KNO3溶液后,固载腐植酸凝胶光子晶体在不同pH值Cd2+溶液中的光子带隙Fig.4 Photonic bandgap of HA-immobilized hydrogel photonic crystal in Cd2+ solution with different pH values after adding KNO3 solution with different concentrations
2.3 固载腐植酸凝胶光子晶体对Cd2+的传感性能
2.3.1 Cd2+的可视化传感
在优化的传感条件下,将固载腐植酸凝胶光子晶体浸于不同浓度的Cd2+溶液(pH值5.5)中,10 min后测定光子带隙,结果如图5所示。
由图5可知,当Cd2+溶液浓度从1×10-12mol·L-1逐渐增加到1×10-5mol·L-1时,固载腐植酸凝胶光子晶体的光子带隙逐渐红移,从最初的651 nm移至745 nm,光子带隙与浓度之间具有相关性;当Cd2+浓度继续从1×10-5mol·L-1增加到1×10-2mol·L-1时,光子带隙不再随着Cd2+浓度的增加发生明显移动。

Cd2+溶液浓度(mol·L-1)从左至右依次为:blank、1×10-12、
其中,当Cd2+浓度从1×10-10mol·L-1增加到1×10-5mol·L-1时,肉眼可以观察到固载腐植酸凝胶光子晶体的结构颜色发生明显变化,从最初的黄色逐渐变为橙色,最后变为红色(图6),实现了简便快捷可视化检测水溶液中Cd2+浓度。

图6 固载腐植酸凝胶光子晶体在不同浓度Cd2+溶液中的颜色变化
2.3.2 传感选择性
将固载腐植酸凝胶光子晶体分别浸泡在pH值为5.5的相同浓度的Al3+、Zn2+、Cu2+、Fe3+、Pb2+、Cd2+等金属离子溶液中,发现其光子带隙变化(Δλ)差别较大(图7),分别为11 nm、23 nm、31 nm、40 nm、58 nm、86 nm。其中,在Cd2+溶液中的光子带隙变化最大,说明固载腐植酸凝胶光子晶体对pH值为5.5的Cd2+的选择性最强。可能是因为腐植酸中的羧基(pKa=4~6)在pH值为5.5时起主要作用,与Cd2+配位稳定常数相对较大。
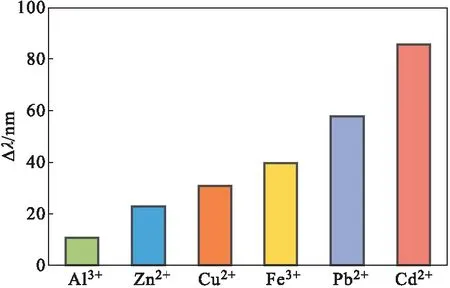
图7 固载腐植酸凝胶光子晶体在不同金属离子溶液中的光子带隙变化Fig.7 Photonic bandgap variation of HA-immobilized hydrogel photonic crystal in different metal ions solution
2.3.3 传感可逆性
通过可逆循环实验研究固载腐植酸凝胶光子晶体的传感可逆性。先将固载腐植酸凝胶光子晶体浸泡在pH值为5.5的缓冲溶液中记录光子带隙波长;再浸泡在1×10-7mol·L-1Cd2+溶液中测定传感后的波长;然后置于0.1 mol·L-1盐酸中浸泡5 min,破坏腐植酸与Cd2+的配位作用;最后用大量的二次蒸馏水冲洗彻底,使其恢复至空白状态后浸泡在pH值为5.5的缓冲溶液中记录波长,结果如图8所示。

图8 固载腐植酸凝胶光子晶体响应Cd2+的可逆性Fig.8 Reversibility of HA-immobilized hydrogel photonic crystal in Cd2+ solution
由图8可知,固载腐植酸凝胶光子晶体在经过5个循环后依然保持着光子带隙性质,且不同状态下的光子带隙的重复波长范围都在±5 nm内波动。表明固载腐植酸凝胶光子晶体对Cd2+的响应是一个可逆的过程,固载腐植酸凝胶光子晶体可以多次重复使用。
3 结论
利用腐植酸与Cd2+的配位作用,构建了一种新颖、快速、灵敏度高的Cd2+凝胶光子晶体传感器,能够检测1×10-12~1×10-2mol·L-1浓度范围内Cd2+。当Cd2+浓度在1×10-10~1×10-5mol·L-1范围时,可以肉眼观察到固载腐植酸凝胶光子晶体的结构颜色随Cd2+浓度变化而发生明显变化,实现了水溶液中Cd2+浓度的可视化检测。

