热脱附—气相色谱—质谱法测定环境空气中挥发性有机污染物
宋 洲, 吉义平, 钟 旭, 唐泽彪, 周宇齐, 罗火焰, 郭燕飞
(1.湖北省地质实验测试中心,湖北 武汉 430034; 2.资源与生态环境地质湖北省重点实验室(湖北省地质局),湖北 武汉 430034;3.湖北华祥地质环境检测科技有限公司,湖北 武汉 430000)
环境空气中的挥发性有机污染物(VOCs)主要包括烯烃、烷烃、芳香烃、醛酮、酯和醚等[1],是大气光化学反应的重要反应物,也是大气污染物臭氧和颗粒物的重要前体物[2-5]。由于VOCs来源多样[6]且具有强的挥发性,因此其普遍存在于环境空气中[7]。研究表明,部分VOCs具有致癌、致突变性[8],已被中国列为空气四大污染物之一。因此,有必要建立环境空气中VOCs准确的测定方法。
环境空气中VOCs的采集方法包括气袋法[9]、吸附管法[10]和罐采样法[11]等,其中吸附管法采样适用浓度范围广,可重复多次使用[12],已被纳入中国环境标准HJ 644—2013和HJ 734—2014中,分别对环境空气和固定污染源废气中VOCs进行采样。朱晓平等[13]研究了不同填料不锈钢采样管对环境空气中67种VOCs的捕集情况,发现Tenax TA和Carbograph 1 TD组合填料采样管效果较好。冯丽丽等[7]在分析环境空气中23种VOCs时采用了Tenax TA的吸附管;邓桂凤等[14]在分析环境空气中35种VOCs时选择了填料为Graphitised Carbon Black和Carbonised Molecular Seive的吸附管。由此可见,吸附管填料的选择是VOCs分析的关键。此外,程伟[15]在研究室内空气中16种VOCs的测定时发现,标准系列管的制备条件不同,容易导致目标物测定结果的相对标准偏差偏大,进而影响目标物的准确测定。然而在标准HJ 644—2013和HJ 734—2014中并未对此进行量化,给实际检测工作造成不便。
因此,本研究针对环境空气中35种VOCs,考察了不同填料不锈钢采样管的捕集效果,优化了标准系列管的制备条件,探讨了热脱附条件的影响,通过加标回收实验考察了方法的准确度,以期对HJ 644—2013标准中相关关键步骤参数进行量化,从而更方便指导实际样品的检测工作,满足环境空气中35种VOCs准确测定的需求。
1 实验部分
1.1 主要仪器
Agilent 7890B气相色谱-5977A质谱联用仪(美国Agilent公司);TD-100自动热脱附系统(英国Marks公司);JH-1活化仪(北京中惠普分析技术研究所);GSP-300FT-2采样器(日本GASTEC株式会社)。
1.2 试剂与材料
毛细管色谱柱:DB-624(30 m×0.25 mm×1.4 μm,美国Agilent公司)。不锈钢采样管:1#、Tenax GR(60/80) / Carbograph 1 TD(60/80),美国Camsco公司;2#、Carbograph 1 TD(40/60) / Carboxen 1000(40/60),英国Marks公司;3#、Tenax TA / Carbograph 1 TD / Carboxen 1003,英国Marks公司;4#、Tenax GR(35/60) / Carbograph 1 TD(40/60),英国Marks公司;5#、Carbograph 2(40/60) / Carbograph 1(40/60) / Carboxen 1000 (40/60),上海安谱实验科技股份有限公司。微量注射器:10 μL,G4513-80209,美国Agilent公司。35种VOCs混标:1,1-二氯乙烯、1,1,2-三氯-1,2,2-三氟乙烷、氯丙烯、二氯甲烷、1,1-二氯乙烷、顺式-1,2-二氯乙烯、三氯甲烷、1,1,1-三氯乙烷、四氯化碳、1,2-二氯乙烷、苯、三氯乙烯、1,2-二氯丙烷、顺式-1,3-二氯丙烯、甲苯、反式-1,3-二氯丙烯、1,1,2-三氯乙烷、四氯乙烯、1,2-二溴乙烷、氯苯、乙苯、间-二甲苯、对-二甲苯、邻-二甲苯、苯乙烯、1,1,2,2-四氯乙烷、4-乙基甲苯、1,3,5-三甲基苯、1,2,4-三甲基苯、1,3-二氯苯、1,4-二氯苯、苄基氯、1,2-二氯苯、1,2,4-三氯苯和六氯丁二烯,质量浓度均为2 000 mg/L,甲醇介质;3种内标混标:1,4-二氯苯-d4、氯苯-d5、氟苯,质量浓度均为2 000 mg/L,甲醇介质;上述产品均购于上海安谱实验科技股份有限公司。甲醇(色谱纯),美国Fisher试剂公司。
1.3 样品采集
采样前,参照不锈钢采样管使用说明对其进行老化,同时抽取20%的采样管进行空白检验,合格后方可使用,否则应重新老化。采样时,将采样管连接到采样泵上,以流量100 mL/min采集20 min。采样后,立即用密封帽密封,4℃保存,7 d内分析完毕。
1.4 样品分析
1.4.1标准系列管的制备
将35种VOCs混标经甲醇逐级稀释,得到质量浓度分别为5、10、20、50和100 mg/L的标准系列使用溶液,其中内标的质量浓度均为50 mg/L。通过Marks CSLR液体加标装置向已经老化好的5支采样管中分别加入1 μL不同浓度的标准系列使用液,得到分析物浓度分别为5、10、20、50和100 ng,内标物浓度均为50 ng的标准系列管。
1.4.2热脱附条件
干吹时间:0.5 min;预吹扫时间:0.5 min;采样管解吸温度:300℃;解吸时间:3 min;采样管解吸分流比:1∶3.5;冷阱初始温度:-28℃;冷阱解吸温度:280℃;解吸时间:3 min;冷阱解吸分流比:1∶42.7;流路温度:150℃;吹扫气体:高纯氦气,流量为20.0 mL/min。
1.4.3气相色谱—质谱条件
载气:高纯氦气;色谱柱流量:1.2 mL/min;隔垫吹扫关闭,不分流进样;程序升温:初温30℃,保持3.2 min,以11℃/min升至200℃,保持3 min。EI电离源;离子化能量:70 eV;离子源温度:230℃;四极杆温度:150℃;传输线温度:250℃;测定方式:全扫描;溶剂延迟时间:0 min;扫描质量范围:35~270 amu;35种VOCs的保留时间及特征离子如表1所示。
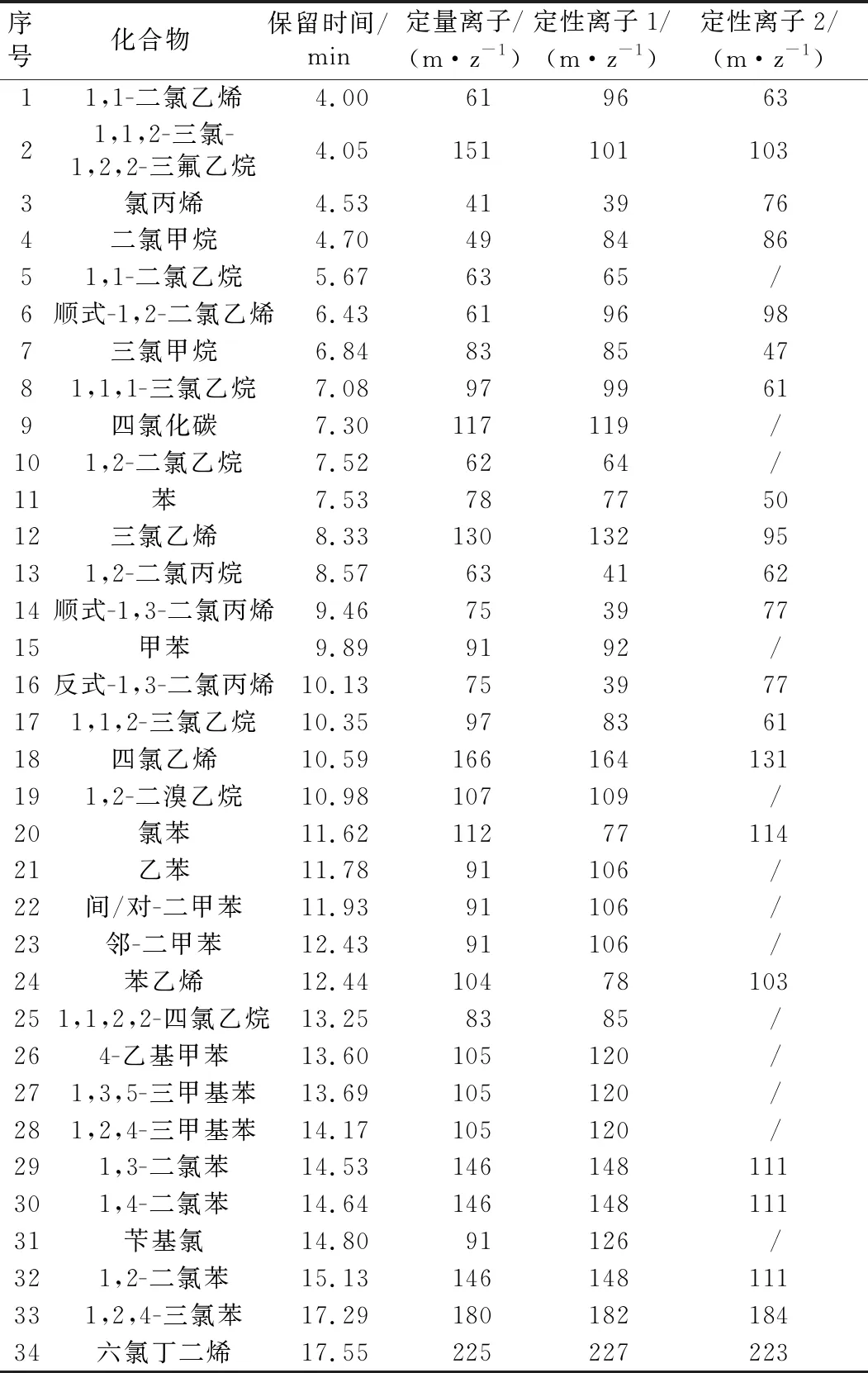
表1 35种VOCs的保留时间及特征离子Table 1 Retention times and characteristic ions of 35 volatile organic compounds (VOCs)
2 结果与讨论
2.1 采样管的选择
热脱附—气相色谱—质谱法测定环境空气中挥发性有机污染物的流程示意如图1所示。由图1可知,被测组分以迁移的方式吸附在干净的采样管中,然后样品管加热并反吹,用惰性气体将目标物带入冷阱,接着冷阱快速地加热以使待测组分进入气相色谱—质谱联用仪进行测定。

图1 样品测试流程示意图Fig.1 The schematic diagram of sample test process
针对35种VOCs,考察了1.2节中5种不锈钢采样管的捕集情况,结果发现大部分物质捕集效果相当,仅1,1-二氯乙烯、1,1,2-三氯-1,2,2-三氟乙烷、氯丙烯、1,1,1-三氯乙烷、四氯化碳和苄基氯等的响应存在显著差异,结果如图2所示。由图2可知,4#采样管捕集效率最高,经热脱附仪解吸后进入气相色谱—质谱联用仪测定的响应最高。因此,在后续研究中选择4#不锈钢采样管进行35种VOCs的采样分析。
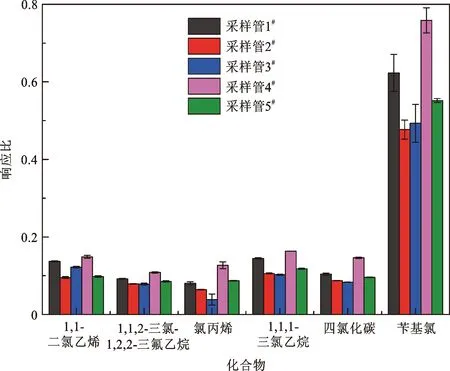
图2 VOCs经不同采样管捕集后的响应Fig.2 The response of VOCs captured by different sampling tubes
不同采样管填料信息如表2所示。目前常用的填料有多孔聚合物Tenax TA、石墨化碳黑、碳分子筛等。由于目标VOCs种类较多,需要使用多种吸附剂填料组成的采样管进行样品采集。Tenax GR是由石墨化碳黑与Tenax TA聚合物共沉淀而得,适用于低分子量和低沸点有机物的捕获。因此,采样管1#和4#的效果优于3#的。与4#相比,采样管1#填料的粒径更小,比表面积更大,对目标物吸附力更强,容易导致解吸效率降低,因此,采样管4#的捕集效率优于1#的。石墨化碳黑和碳分子筛组合具有较强的吸附能力,适用于较高挥发性化合物,但其亲水性强,不适宜潮湿环境,且有一定的活性,对卤代烃等采集效果不理想。因此,采样管2#和5#的效果低于4#的。综上分析,多孔聚合物与石墨化碳黑为填料的采样管捕集效果占优。
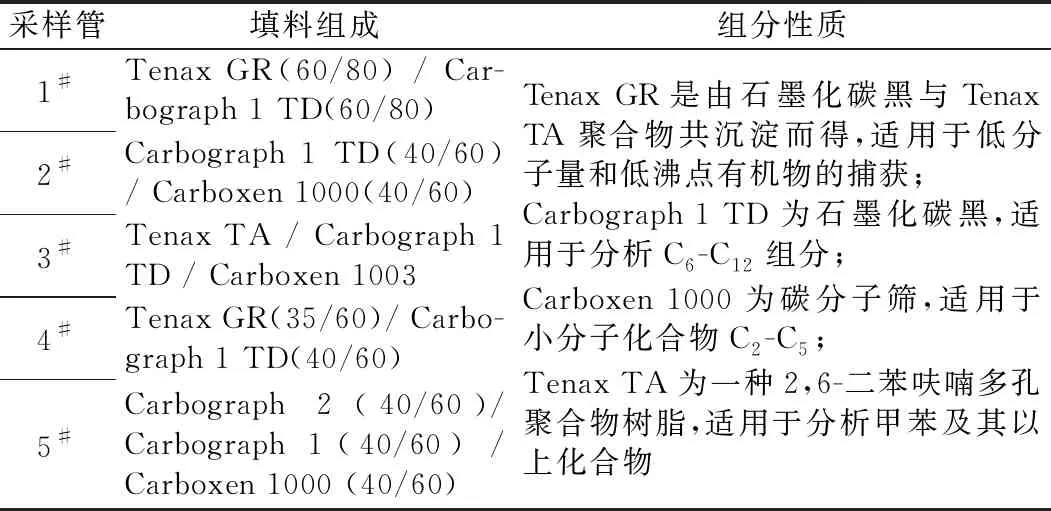
表2 不同采样管填料信息Table 2 The packing information of different sampling tubes
2.2 热脱附条件优化
2.2.1干吹时间
采样管在加热解吸之前需要通过干吹除去采样管与管路中的水分以及氧化性气体,以免影响后续测定。笔者考察了在氦气流量20.0 mL/min的条件下,不同干吹时间对35种VOCs响应的影响,结果发现,仅1,1-二氯乙烯、1,1,2-三氯-1,2,2-三氟乙烷、氯丙烯、二氯甲烷、三氯甲烷、甲苯、四氯乙烯、乙苯、间/对-二甲苯、邻-二甲苯、苯乙烯、4-乙基甲苯、1,3,5-三甲基苯和1,2,4-三甲基苯的响应受干吹时间的影响(图3)。随着时间从0.5 min延长至2.0 min,响应均出现降低的趋势,这可能是由于过长的干吹导致目标组分随水分一起流失。因此,在后续研究中选择干吹时间为0.5 min。
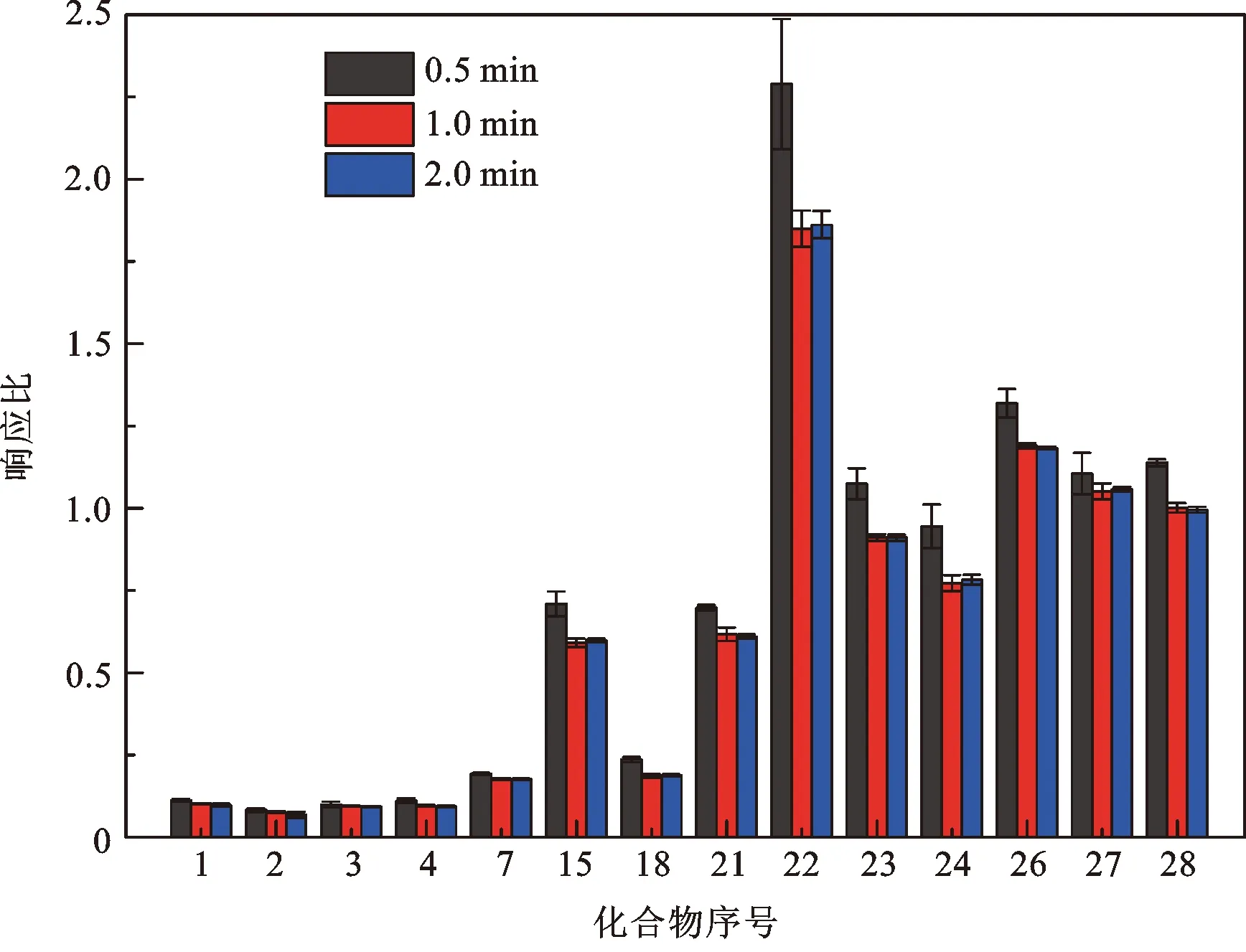
图3 干吹时间对VOCs响应的影响(化合物序号如表1所示)Fig.3 The effect of dry purge time on the response of VOCs
2.2.2采样管解吸条件优化
笔者考察了采样管的解吸温度与时间对35种VOCs响应的影响,由图4-a可知,1,1-二氯乙烯、1,1,2-三氯-1,2,2-三氟乙烷、氯丙烯、1,1,1-三氯乙烷、四氯化碳、苄基氯、1,2,4-三氯苯和六氯丁二烯的响应受解吸温度影响明显,在300℃下解吸响应最高。在此温度下,随着解吸时间从1 min增至3 min,1,1,2-三氯-1,2,2-三氟乙烷、1,1,1-三氯乙烷、四氯化碳、乙苯、1,3,5-三甲基苯、1,2,4-三甲基苯、苄基氯、1,2-二氯苯和1,2,4-三氯苯的响应增加,1,1-二氯乙烯和1,2-二氯乙烷的响应降低;进一步延长解吸时间至7 min时,上述目标物响应均无明显变化。综合考虑,选择解吸时间为3 min。
2.2.3冷阱种类选择
笔者考察了普通冷阱和TO-15冷阱对35种VOCs的捕集情况,结果发现1,1-二氯乙烯、1,1,2-三氯-1,2,2-三氟乙烷、二氯甲烷、1,1-二氯乙烷、三氯甲烷、苯、顺式-1,3-二氯丙烯、甲苯、四氯乙烯、氯苯、乙苯、间/对-二甲苯、4-乙基甲苯和苄基氯的响应在TO-15冷阱上占优(图5),响应可提高1.22~159倍。这主要是由于VOCs种类繁多且性质各异,相比普通冷阱仅使用单一填料而言,TO-15冷阱使用复合填料能够满足不同性质VOCs捕集的需求,因而能够显著提高VOCs的响应。
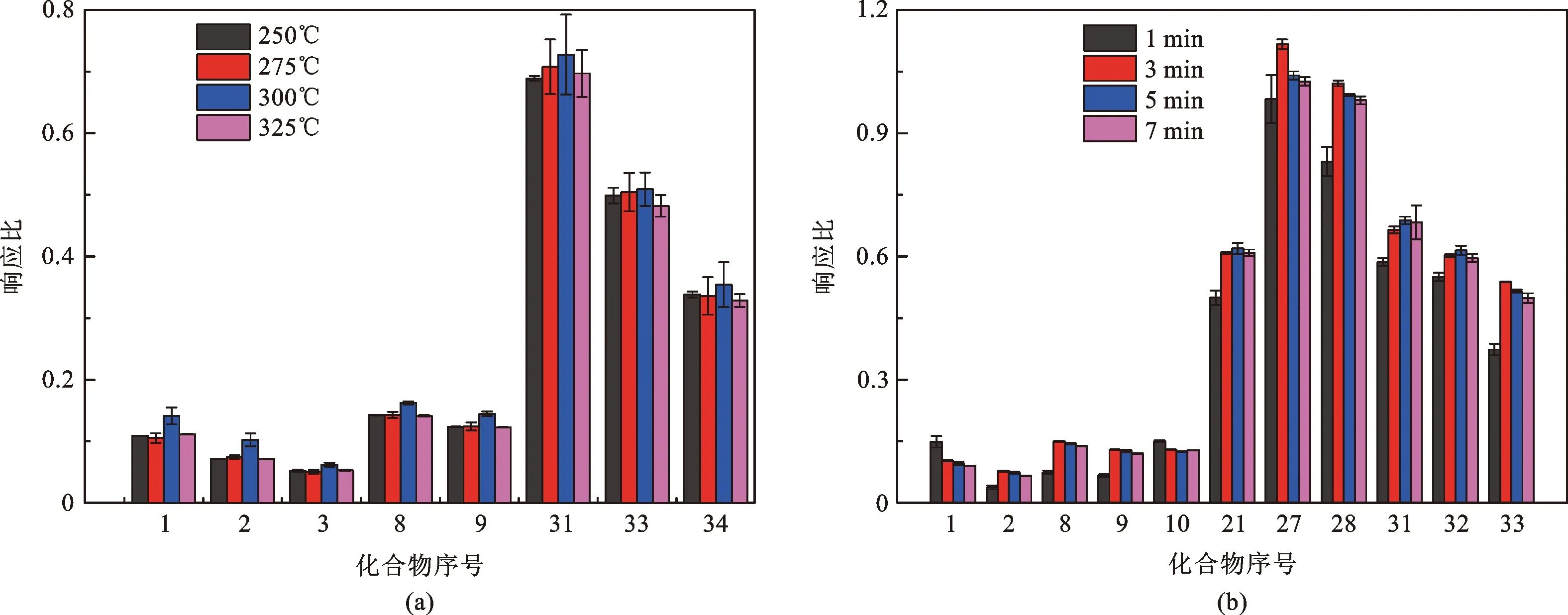
图4 采样管解吸温度(a)和时间(b)对VOCs响应的影响(化合物序号如表1所示)Fig.4 The effect of sampling tube desorption temperature (a) and time (b) on the response of VOCs

图5 VOCs经不同冷阱捕集后的响应(化合物序号如表1所示)Fig.5 The response of VOCs trapped by different cold traps
2.2.4冷阱解吸温度与时间
由于目标物从采样管解吸出来比较慢,导致色谱峰展宽,降低检测灵敏度。因此,需要将目标物先转移至冷阱,再通过冷阱快速地升温解吸,以获得良好的色谱峰型与灵敏度。为此,笔者考察了冷阱解吸温度与时间对35种VOCs响应的影响。由图6-a可知,受解吸温度的影响,1,1-二氯乙烯、氯丙烯、顺式-1,3-二氯丙烯、甲苯、间/对—二甲苯、邻—二甲苯、苯乙烯和1,3,5-三甲基苯的响应在280℃下最高。在该温度下解吸3 min时,1,1-二氯乙烯、氯丙烯、1,1-二氯乙烷、三氯甲烷、顺式-1,3-二氯丙烯、甲苯、反式-1,3-二氯丙烯、间/对—二甲苯、邻—二甲苯、苯乙烯、4-乙基甲苯、1,3,5-三甲基苯、1,2,4-三甲基苯和六氯丁二烯的响应占优。综合上述分析,选择冷阱解吸温度280℃和时间3 min。
2.3 方法学性能研究
2.3.1标准样品上样条件优化
按照1.4.1节中标准系列管的制备方法,对1 μL不同浓度的标准系列使用液的进样时间进行了优化,结果如图7所示。由图7可知,不管是快速注射(1 s),还是慢速注射(匀速,时间分别为10 s、20 s和30 s),35种VOCs的响应变化不大。因此,从节省制备时间考虑,选择进样时间1 s制备标准系列管。
在标准系列使用液注入后,通过氮气吹扫以除去溶剂甲醇。35种VOCs中14种化合物受氮气吹扫流量的影响较大,结果如图8所示。由图8可知,随着氮气吹扫流量的增加,1,1-二氯乙烯、1,1,2-三氯-1,2,2-三氟乙烷、氯丙烯、二氯甲烷、三氯甲烷、甲苯、四氯乙烯、乙苯、间/对—二甲苯、邻—二甲苯、苯乙烯、4-乙基甲苯和1,2,4-三甲基苯等的响应呈现先增加后降低的趋势,在60 mL/min时达到最大。这主要是由于氮气吹扫流量过小时,溶剂甲醇去除不彻底,影响后续冷阱捕集效率,从而导致响应降低;氮气吹扫流量过大时,在去除溶剂甲醇的同时,目标化合物亦会随之损失,同样会导致响应降低。因此,选择氮气吹扫流量60 mL/min制备标准系列管。

图6 冷阱解吸温度(a)和时间(b)对VOCs响应的影响(化合物序号如表1所示)Fig.6 The effect of cold trap desorption temperature (a) and time (b) on the response of VOCs
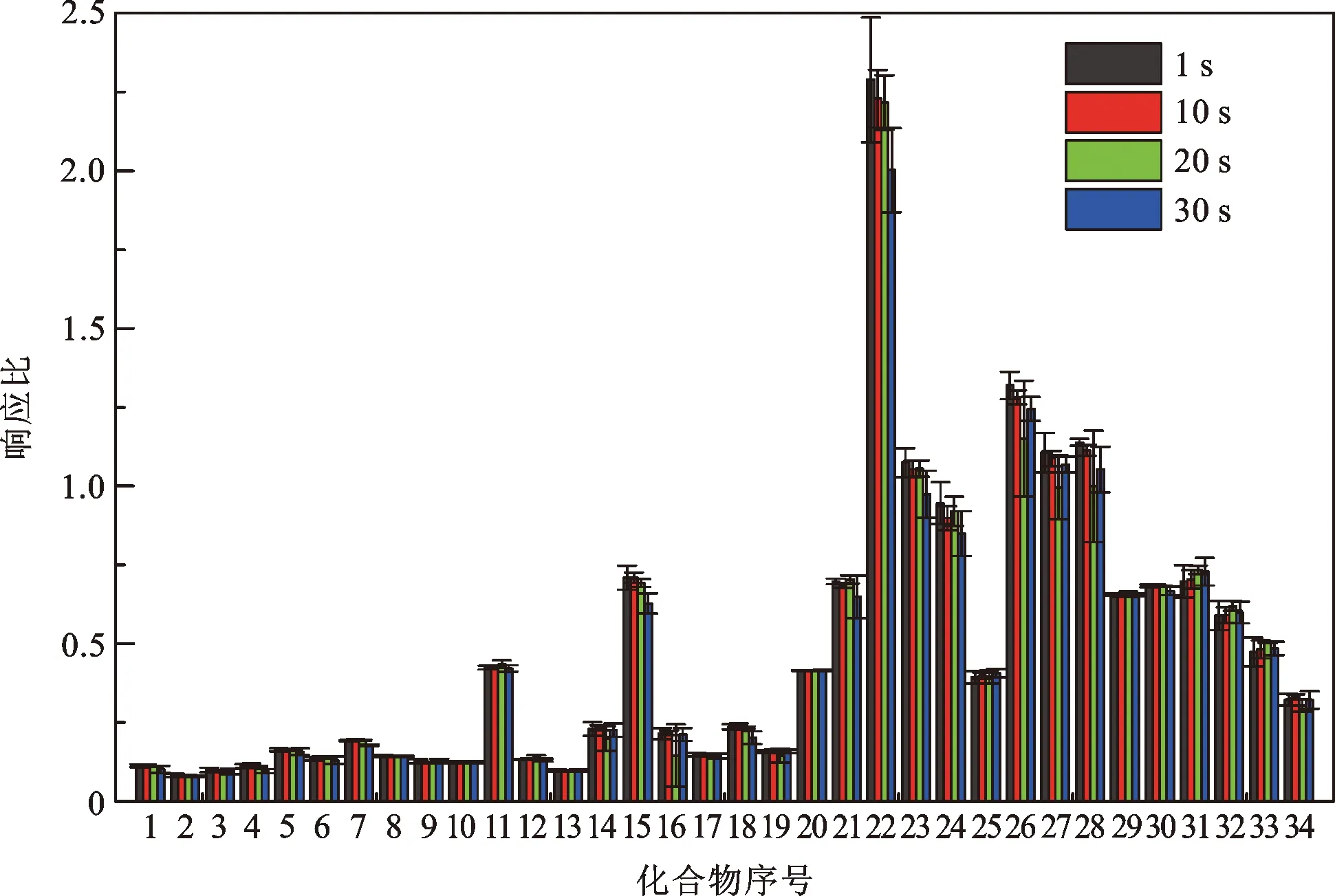
图7 进样时间对标准系列管制备的影响(化合物序号如表1所示)Fig.7 The effect of injection time on the preparation of standard series tubes
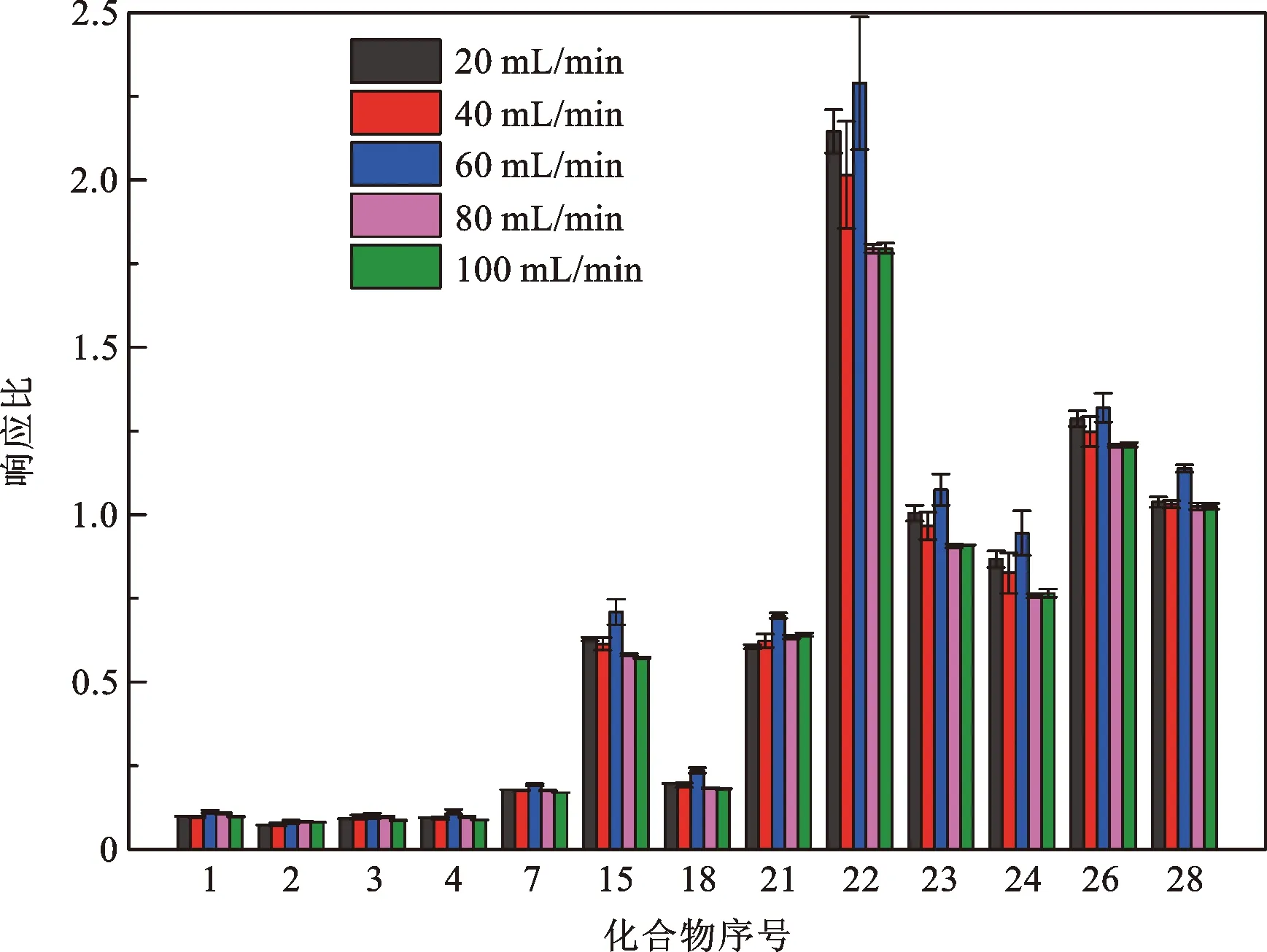
图8 氮气流量对标准系列管制备的影响(化合物序号如表1所示)Fig.8 The effect of nitrogen flow on the preparation of standard series tubes
在氮气吹扫流量60 mL/min的条件下,比较了不同吹扫时间下35种VOCs响应变化情况,结果发现1,1-二氯乙烯、1,1,2-三氯-1,2,2-三氟乙烷、氯丙烯、二氯甲烷、1,1-二氯乙烷和顺式-1,2-二氯乙烯等的响应有变化,如图9所示。由图9可知,氮气吹扫30 s,上述6种VOCs响应最高,这得益于在该条件下溶剂甲醇高效去除的同时避免了目标物过度吹扫损失。因此,后续选择氮气吹扫时间为30 s。
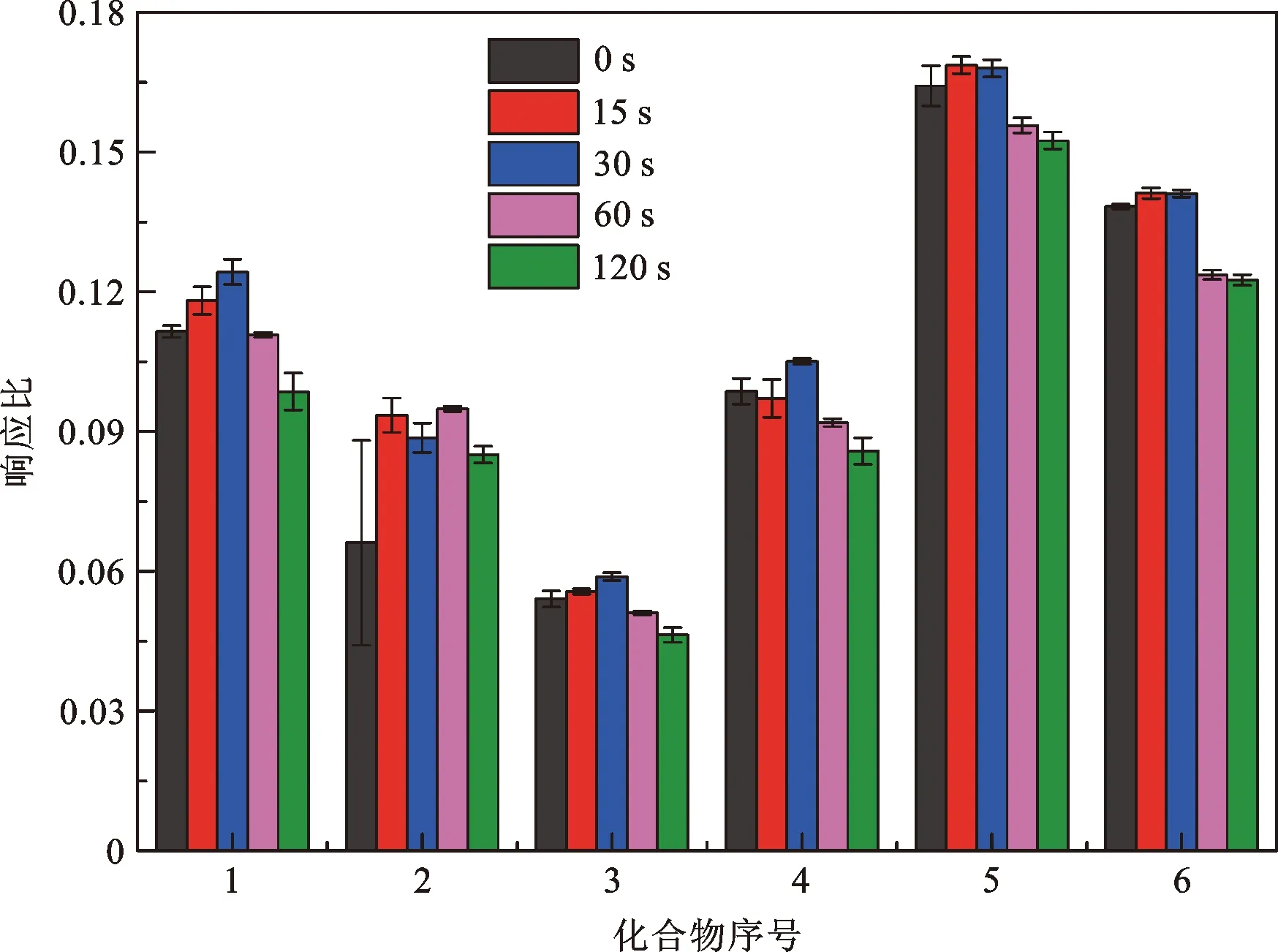
图9 氮气吹扫时间对标准系列管制备的影响(化合物序号如表1所示)Fig.9 The effect of nitrogen purge time on the preparation of standard series tubes
2.3.2线性范围、检出限和定量下限
在1.4.3节中的条件下,35种VOCs的总离子流色谱图如图10所示。由图10可知,35种VOCs的分离效果良好,峰型尖锐且对称,除了间/对-二甲苯无法分开定量外,其余物质均能独立定量分析。
按照1.4.3节中的条件对1.4.1节制备的标准系列管进行分析,以目标物浓度与内标物浓度的比值(X)为横坐标,以其定量离子峰面积的比值(Y)为纵坐标进行线性回归分析,结果如表3所示。由表3可知,在浓度为5~100 ng(其中间/对-二甲苯为10~200 ng)范围内,各目标物的相关系数r在0.999 1~0.999 9,线性关系良好。
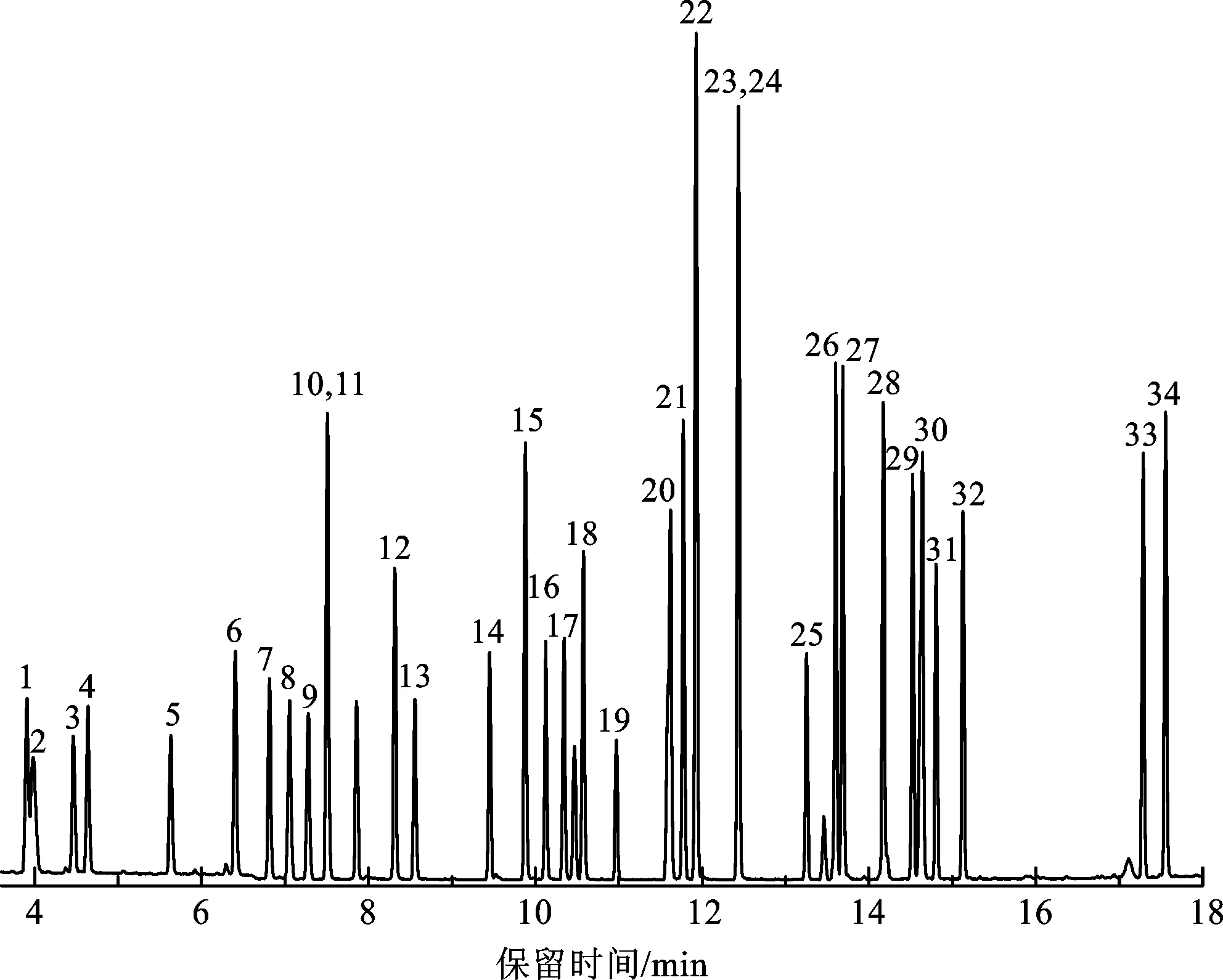
图10 35种VOCs的总离子流色谱图(化合物序号如表1所示)Fig.10 Total ion chromatogram of 35 volatile organic compounds (VOCs)
根据《环境监测分析方法标准制订技术导则》(HJ 168—2020)的规定,通过连续测定7个接近于方法检出限的浓度考察了本方法的检出限,通过4倍检出限换算得到方法定量下限。按照1.4.1节中样品制备和1.4.3节中分析条件,得到在采样体积为2 L时,35种VOCs的方法检出限为0.06~0.55 μg/m3,定量下限为0.24~2.20 μg/m3。
2.3.3准确度试验
按照1.4.1节中的方法制备加标量分别为5、20、100 ng(其中间/对-二甲苯为10、40、200 ng)的样品各6份,所得平均加标回收率和相对标准偏差如表4所示。由表4可知,35种VOCs的回收率范围为78.0%~116%,相对标准偏差的范围为0.25%~4.51%,表明本方法具有较高的准确度,能够满足实际环境空气样品测定的需求。
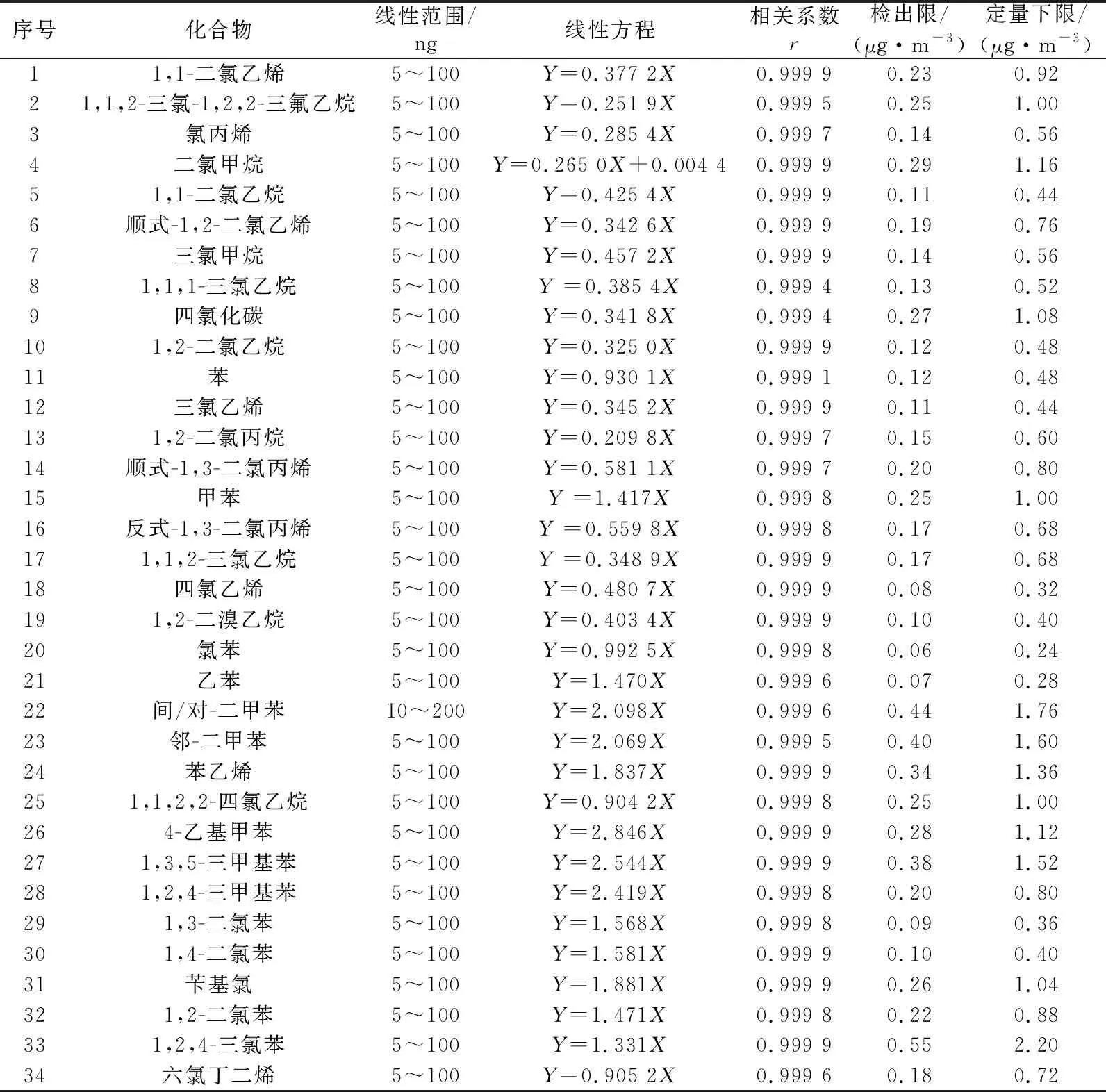
表3 35种VOCs的线性范围、线性方程、相关系数、检出限及定量下限Table 3 Linear ranges,linear equations,correlation coefficients,method detection limits,and minimum quantitative detection limits of 35 volatile organic compounds (VOCs)
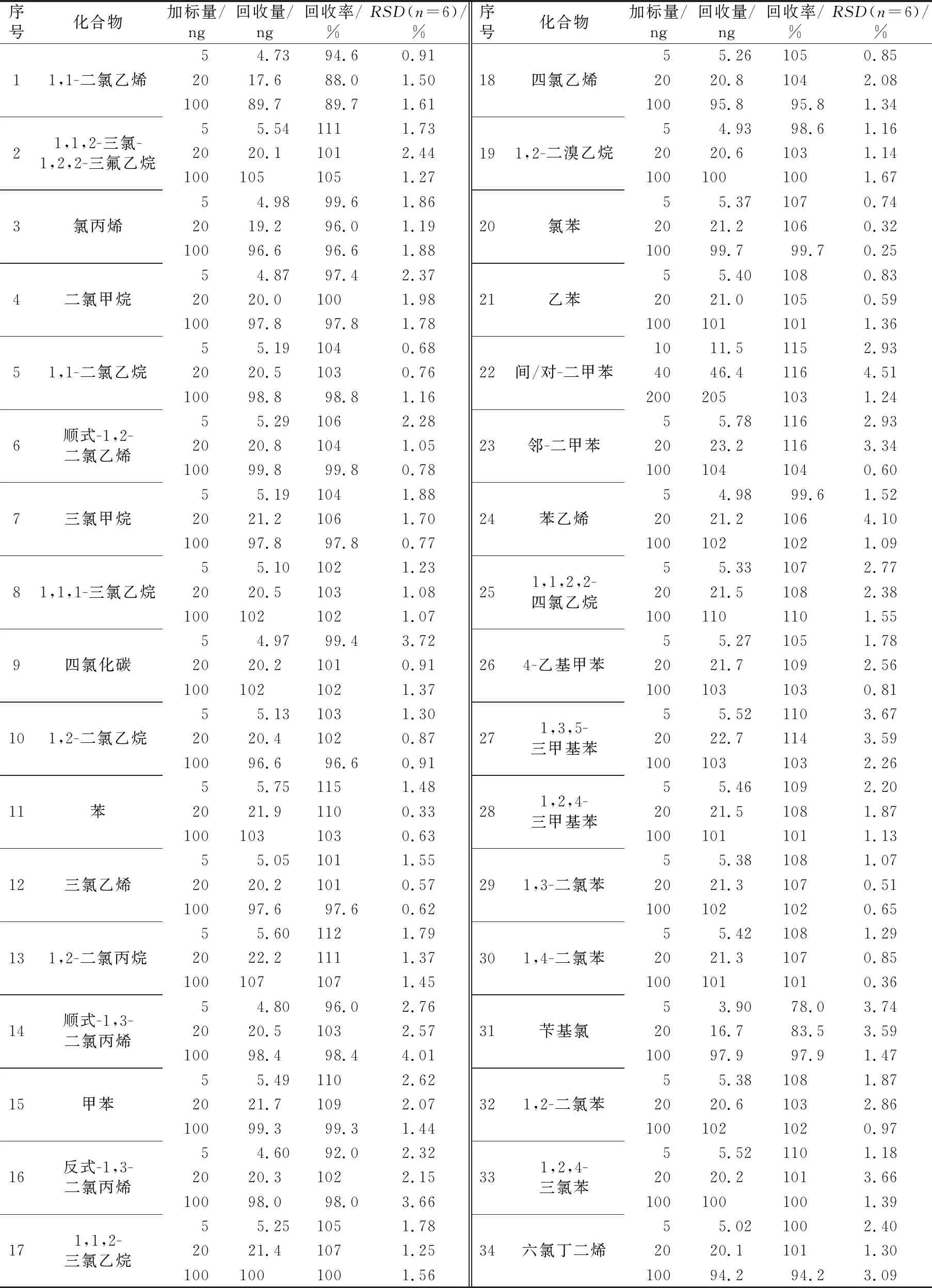
表4 35种VOCs的加标回收试验结果Table 4 Standard addition recovery test results of 35 volatile organic compounds (VOCs)
2.4 实际样品测定
采用所建立的方法对3个半挥发性有机污染物前处理车间中的空气进行分析,结果如表5所示。由表5可知,3个前处理室中检出了20种VOCs,其中卤代烃的浓度普遍较高,其次为苯系物的,氯苯类浓度较低。尤其是3#前处理室,二氯甲烷和三氯甲烷的浓度可分别高达119 μg/m3和178 μg/m3,这主要与该室水样前处理需要用到二氯甲烷和三氯甲烷作为溶剂有关。尽管1#前处理室未直接使用二氯甲烷和三氯甲烷,但其依然有一定程度检出,这也表明VOCs因其强的挥发性,在环境空气中广泛存在。因此,在样品挥发性和半挥发性组分分析时,一定要进行物理分区,避免所用溶剂对挥发性组分测定的干扰。
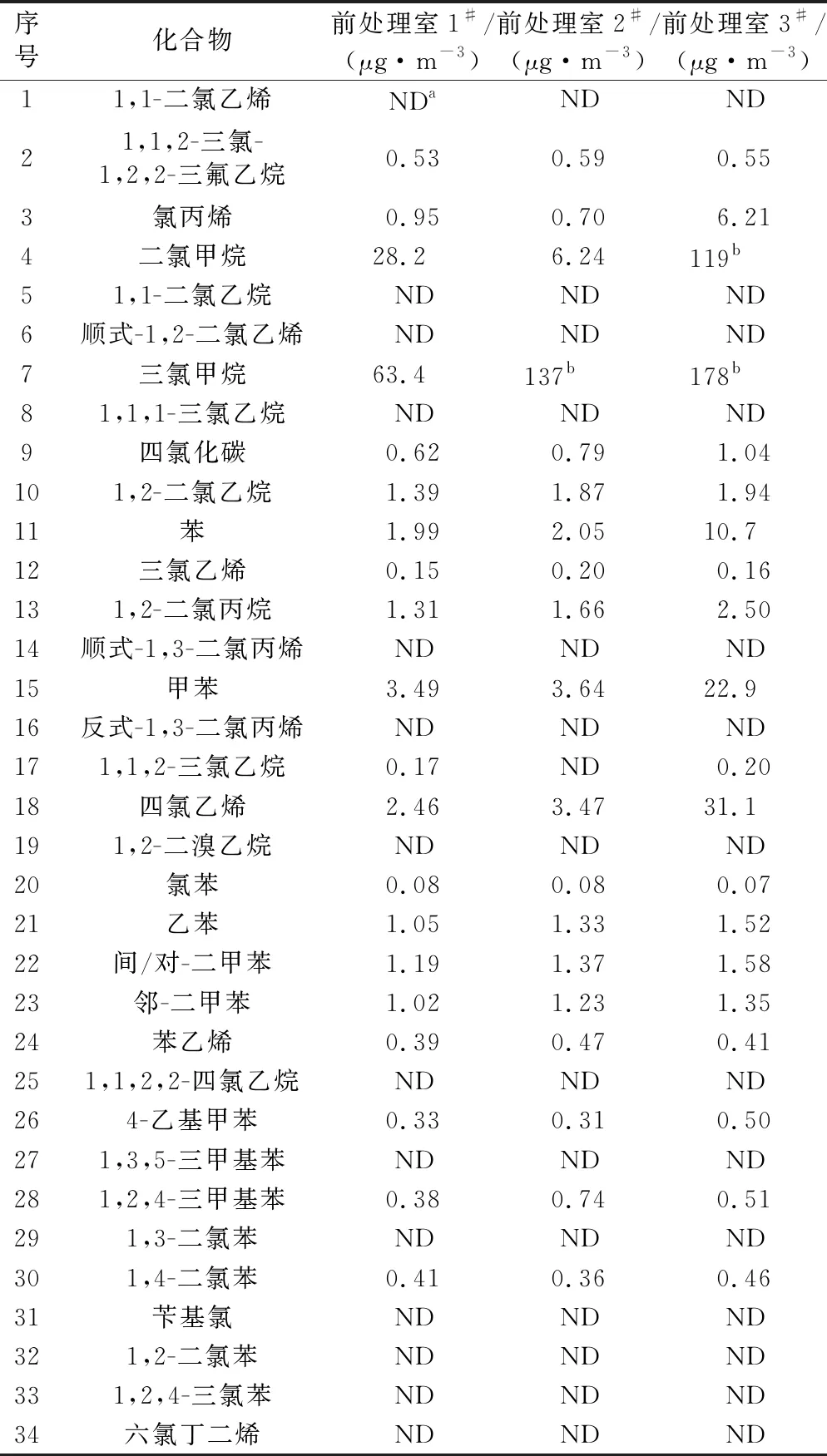
表5 实际样品中35种VOCs测定结果Table 5 Determination results of 35 volatile organic compounds (VOCs) in practical samples
3 结论
本文通过对采样管类型、标准系列管制备条件、热脱附条件等的优化,建立了热脱附—气相色谱—质谱法测定环境空气中35种VOCs的分析方法。结果发现,填料为Tenax GR(35/60) / Carbograph 1 TD(40/60)的不锈钢采样管(4#)可高效捕集目标VOCs,经过TO-15专用冷阱进行二级热脱附后,在获得尖锐对称峰型的同时可提高目标物的响应。在优化的条件下,当采样体积为2 L时,35种VOCs的方法检出限为0.06~0.55 μg/m3,低于标准HJ 644—2013的检出限(0.3~1.0 μg/m3),能够满足实际环境空气样品中VOCs的准确测定。

