达芬奇机器人手术在儿童动脉导管未闭中的应用研究
应力阳 刘喜旺 谭 征 俞建根 舒 强
动脉导管未闭(patent ductus arteriosus,PDA)是常见的先天性心脏病之一,约占先天性心脏病的5%~10%[1]。由于PDA存在左向右分流,导致持续肺血流增加,左心前负荷增加,易造成心功能不全、感染性心内膜炎等,需要手术治疗。目前PDA手术方式包括开胸手术结扎、经皮穿刺封堵、胸腔镜下结扎等。这些方法存在创伤大、需要置入封堵器、视野不清晰等弊端。达芬奇机器人辅助下结扎PDA有创伤小、恢复快、无需封堵器等优点。本研究回顾性分析达芬奇机器人辅助胸腔镜下行PDA结扎术患者的临床资料,总结经验如下。
材料与方法
一、临床资料
以2020年8月至2021年4月在浙江大学医学院附属儿童医院行达芬奇机器人辅助胸腔镜下PDA结扎术的35例患者作为研究对象。部分患者存在反复呼吸道感染,心前区听诊闻及持续性机器样隆隆杂音,15例仅闻及收缩期杂音。术前超声提示动脉导管未闭,左向右分流。胸片显示肺血增多,左心增大。心电图提示5例左心室高电压。1例因超声提示降主动脉偏细,行CT血管成像排除狭窄。所有患者术前诊断和手术指征均明确。其中男18例,女17例,年龄1.2~7.1岁,中位年龄2.6岁;体重9.5~37.0 kg,中位体重14.0 kg;PDA直径0.15~0.56 cm,中位直径0.30 cm;手术时间40~120 min,中位时间60 min;术后住院时间1~6 d,中位时间2 d;费用51 703~62 577元,中位费用54 018元。
二、手术方法
患者采取气管插管全身麻醉,将气管插管置入右侧主支气管,单肺通气,建立动脉血压监测及颈内中心静脉置管。术前置入食道超声,右侧卧位,右腋下垫高,固定体位。腋中线第五肋间置入镜孔,人工气胸压力维持4 mmHg,肩胛中线第六肋间及腋前线第四肋间置入操作孔,在腋前线第七肋间置入辅助孔(图1)用于牵拉暴露及置入结扎线。置孔后连接第四代达芬奇机器人的机械臂,定位调整机械臂,置入马里兰钳及卡地亚钳,打开纵膈胸膜及主动脉外膜上至左锁骨下动脉,下至动脉导管下窗2 cm处,将迷走神经及其分支喉返神经夹在纵膈胸膜和主动脉外膜之间(图2),辅助孔牵拉外膜,暴露动脉导管组织,钝性游离下窗,避免损伤迷走神经喉返支,再分离上窗,将马里兰钳从动脉导管下窗背面到达上窗,带两道7号丝线,降低收缩压至60 mmHg左右结扎动脉导管(图3)。常规将气管插管回退至主支气管双肺通气,同时食道超声复查动脉导管无残漏,排完胸腔积气后缝合置孔处皮肤,于手术室常规撤离呼吸机后送普通病房。术后常规复查心脏超声及胸片。
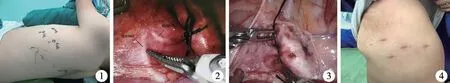
图1 达芬奇机器人辅助腔镜技术治疗儿童PDA的术前置孔 图2 达芬奇机器人辅助腔镜技术治疗儿童PDA 注 黑色线:术中的迷走神经及喉返神经 图3 达芬奇机器人辅助腔镜技术治疗儿童PDA术中结扎动脉导管 图4 达芬奇机器人辅助腔镜技术治疗儿童PDA患者术后1个月皮肤切口Fig.1 Preoperative foramen placing Fig.2 Vagus nerve and recurrent laryngeal nerve(indicated by black lines)Fig.3 Intraoperative ligation of PDA Fig.4 Skin incision 1 month later
结 果
35例均顺利在达芬奇机器人辅助下完成手术,无一例转开胸手术,手术时间20~84 min,平均50.54 min;术中出血2~3 mL,未留置胸腔引流管,平均住院费用5.4万,术中食道心脏超声复查未见残余分流。术后1~6 d出院,出院前复查超声心动图、胸片均未见异常,出院时切口愈合良好(图4)。1例术后1个月门诊复查超声心动图,发现动脉导管残漏0.12 mm,该例患者术前动脉导管直径0.56 cm,术中结扎动脉导管2道,复查食道超声及术后1 d复查超声未见残漏,术后6个月复查动脉导管残漏仍存在。1例术后喉返神经损伤致声音嘶哑、喝水呛咳等,随访3个月后好转。
讨 论
动脉导管是胎儿时期正常血液循环的一部分,是连接降主动脉和肺动脉之间的正常通道。新生儿出生后血氧分压上升,动脉导管组织收缩,造成出生后24h功能性关闭,并在数月至1年内解剖性关闭。足月儿PDA的发病率为0.057%,而早产儿发生动脉导管未闭的概率较足月儿更高[1,2]。动脉导管组织连接降主动脉与肺动脉,收缩期及舒张期均存在大量左向右分流,分流量的大小与动脉导管直径和两侧压差呈正相关,大型动脉导管导致肺循环血流量增加,左心前负荷增加,体循环有效循环血量减少,从而导致肺动脉高压及左心功能不全。部分患者出生后动脉导管直径小,临床症状不明显,但随着年龄增大,会出现出汗、反复肺部感染、感染性心内膜炎等临床症状。
目前PDA治疗方案有以下几种:①后外侧或腋下切口PDA结扎或切断缝合术;②非甾体抗炎药物治疗;③内科介入PDA封堵术;④胸腔镜下PDA结扎术;⑤达芬奇机器人辅助腔镜下PDA结扎术。后外侧后腋下切口结扎PDA存在创伤大、恢复慢、切口瘢痕形成等问题,但适合于各种PDA的治疗,包括大型PDA、窗型PDA等[3];药物治疗只适合于早产儿PDA的治疗[4];内科介入PDA封堵术存在放射性、封堵器长期存在体内、术后溶血以及核磁共振检查受限等弊端[5-8];而胸腔镜下PDA结扎术存在术中转开胸、视野不清晰、游离和套扎PDA困难、术后肋间疼痛等弊端[9-12]。
与传统腔镜相比,第四代达芬奇机器人手术系统具有以下优势:①清晰准确的三维立体视野定位更准确。②操控者手部和腕部的动作可被实时转化为精确的机械动作。③手术器械可在腕处转弯,弯曲及旋转的程度远超过人手的极限。颤抖滤除和直觉式运动可让操作更稳定、自然。④操作者无需上手术台,节省空间,避免主刀医生和助手间的拥挤以及对手术视野的阻挡。⑤良好的三维视野和简化的配合方式以及符合人体工程学设计的医生操作台能最大程度减少医生的疲劳。目前达芬奇机器人已广泛应用于成人泌尿外科、胸外科、妇产科、普外科、心脏外科等,随着微创技术的发展,达芬奇机器人甚至可以应用于头颈外科[13-15]。但达芬奇机器人应用于小儿外科时间较短,与成人相比,小儿体腔空间狭小,传统的手术操作受到限制,腔镜手术的进步已经逐步解决了这个问题,但是对局限性病灶的精准操作,仍存在不足。而达芬奇机器人可在有限的空间内进行精细操作,减少手术副损伤,在提高疗效的同时最大限度地减轻患者痛苦。达芬奇机器人应用于小儿心脏外科相对较迟,最早是由EL Bret在2002年报道机器人辅助下PDA切断缝合,波士顿儿童医院Suematsu[17]在2005年报道了达芬奇机器人辅助下PDA结扎术。
本组病例采用达芬奇机器人辅助腔镜下动脉导管结扎术,术中置孔位置选择非常重要,置孔位置不佳导致手术视野不佳、操作困难以及机械臂之间对抗。本组病例采用四孔法,术中能有效避开左上肺叶的视野干扰,同时在分离结扎动脉导管时更加安全。手术均在右侧单肺通气下进行,人工气胸压力维持在4 mmHg,视野放大倍数可根据术中病情、视野需要及手术操作者习惯调整,术中将动脉导管上下窗分离后可以清晰地显示动脉导管、迷走神经及其喉返分支,结扎时可以顺利避开喉返神经。本组有1例出现声音嘶哑、喝水呛咳等喉返神经损伤症状,考虑可能与早期未能有效分离纵隔胸膜及主动脉外膜,结扎动脉导管时损伤喉返神经有关,因此后面的手术尽可能将两层组织分离,将迷走神经及其喉返分支夹在两层膜之间,避免神经损伤。机器人Endowrist功能可以有效安全地游离动脉导管后壁,高清视野使深部打结更加快速安全有效。1例术后1个月门诊复查心脏超声发现动脉导管残漏,考虑动脉导管粗大,结扎动脉导管不够紧,导致1个月后出现动脉导管残漏,后期对于粗大的动脉导管予结扎三道防止残漏,术中也常规需要食道超声及经胸超声评估是否存在残漏。
达芬奇机器人辅助下动脉导管结扎术有以下技术要求:①机械臂操作时无力量反馈,游离动脉导管后壁时需要特别小心,需通过视线和对器械的位置感来避免动脉导管组织后壁的损伤,结扎动脉导管时需密切观察丝线的紧张度,防止用力过度导致丝线断裂。②该手术需由具有多年开胸结扎动脉导管经验的医师主刀,可在紧急状态下行开胸动脉导管结扎术。本组主刀医师均有十余年心脏外科治疗经验,术中无一例大出血、丝线断裂及转开胸病例。本组病例早期因缺乏经验,故选择年龄>2岁且体重>10 kg的患者进行手术治疗,随着病例资料积累,年龄<2岁者甚至婴儿都可以选择达芬奇机器人手术治疗。
除治疗动脉导管未闭外,目前达芬奇机器人还可以应用于血管环、双主动脉弓的手术治疗,但机器人辅助下体外循环治疗儿童先天性心脏病的病种受限,因为外周建立体外循环需要达到一定的年龄及体重,国内只应用于大龄患者房间隔缺损、室间隔缺损的手术治疗[18,19]。另外,达芬奇机器人辅助腔镜治疗动脉导管平均手术费用达5.4万,费用偏高,且未进入医保报销,对于经济水平相对低下的家庭还有相当的负担。

