主流促排方案在多囊卵巢综合征患者中辅助助孕的结局比较
曾汝君,陈晗笑,秦 朗,曾 珣
(四川大学华西第二医院妇产科生殖医学中心,四川大学华西第二医院出生缺陷与相关妇儿疾病教育部重点实验室,四川 成都 610041)
全世界范围内不孕症的患病率约为15%[1],中国育龄期女性不孕症发病率可达25%[2,3]。多囊卵巢综合征(polycystic ovarian syndrome,PCOS)是一种常见的导致女性不孕的生殖内分泌疾病,育龄期女性中患病率为8%~13%[4],2018年我国接受辅助生殖技术的不孕夫妇中,排卵障碍的发生率约为11.2%[5]。对于这部分患者,体外受精-胚胎移植(in vitro fertilization and embryo transfer,IVF-ET)是诱导排卵失败后的重要治疗方法。为了减轻患者的负担、缩短妊娠等待时间,我们倾向于让接受IVF-ET的患者进行新鲜胚胎移植。但是,PCOS这种卵巢高储备的患者可能在控制性卵巢刺激(controlled ovarian stimulation,COS)期间出现卵巢高反应,卵巢过度刺激综合征(ovarian hyperstimulation syndrome,OHSS)的风险增加,并影响胚胎移植时机。因此个体化的促排方案十分必要的。本研究回顾性分析了四川大学华西第二医院生殖医学中心2018~2020年接受不同COS方案的PCOS患者的结局,旨在探讨哪种COS方案可使PCOS患者的最大获益,以期为临床医生选择促排方案提供依据。
1 资料与方法
1.1 一般资料回顾性纳入2018年1月1日至2020年12月31日在四川大学华西第二医院生殖医学科接受IVF/ICSI治疗的PCOS患者共317例。纳入标准:①2003年鹿特丹标准诊断为PCOS的患者,即以下3项标准中满足2项:稀发排卵或无排卵,高雄表现或高雄激素血症,卵巢多囊样改变,并且排除其他可能引起高雄激素及排卵异常的疾病;②不孕患者,不孕症诊断标准为有规律性生活、未避孕未孕一年及以上;③对于接受多次IVF治疗的患者,仅纳入该患者第一个周期的实验室指标和妊娠结局;④临床资料完整。排除标准:①男性因素不孕;②子宫因素不孕;③夫妻双方或者一方染色体异常;④复发性流产病史的女性;⑤接受胚胎植入前遗传学诊断/胚胎植入前遗传学筛查者。所有患者均知情同意并签署知情同意书,本研究经四川大学华西第二医院伦理委员会审核并批准。
1.2 基线信息从电子病历系统中提取了患者的基线信息,包括年龄、身高、体重、体重指数(body mass index,BMI)。实验室检验指标包括:睾酮(testosterone,T)、黄体生成素 (luteinizing hormone,LH)、卵泡刺激素(follicle-stimulating hormone,FSH)、窦卵泡数(antral follicle count,AFC)、抗苗勒管激素(Anti-Mullerian hormone,AMH)。性激素和AFC均在患者月经周期的2~4天进行测量。性激素和AFC均在患者月经周期的2~4天进行测量。
1.3 方法根据COS方案的不同,分为①拮抗剂固定方案组[6](n=227):外源性促性腺激素(gonadotrophin,Gn)从月经第2~3天开始施用,根据患者年龄、BMI、AFC等因素决定Gn剂量,在使用Gn6~8天添加GnRH-拮抗剂,至扳机日;②卵泡期长方案组(n=32):在月经周期第2~3天,阴道B超了解AFC情况,无直径>10 mm卵泡时肌肉注射长效GnRH-a(达菲林,益普生生物制药公司,法国)3.75 mg,28天后查血性激素及B超,根据患者年龄、BMI、AFC等决定Gn剂量,并根据血性激素及B超情况调整Gn用量。当2个及以上优势卵泡直径≥18 mm或3个及以上优势卵泡直径≥17 mm时,注射绒促性素注射液(8000~10000 IU,丽珠,中国)进行扳机。若患者存在OHSS高风险,选择低剂量注射用绒促性素注射液(4000~5000 IU)、注射用绒促性素注射液(2000 IU)联合GnRH 激动剂(0.2 mg)或GnRH 激动剂(0.2 mg)进行扳机。扳机后36~38小时取卵,行IVF或ICSI。如果患者扳机日孕酮水平高或存在OHSS高风险,则取消新鲜周期移植及全胚冷冻。
记录每个患者的初始Gn剂量、Gn天数、总Gn剂量、扳机日直径≥14 mm的卵泡数、雌激素(estradiol,E2)、孕酮(progesterone,P)、LH、扳机日子宫内膜厚度、卵巢敏感指数(ovarian sensitivity index,OSI)、获卵数。根据《人类辅助生殖技术临床数据质控专家共识》,判断患者的卵巢反应性。
1.4 观察指标根据形态学评估卵裂期胚胎和囊胚的质量。比较两组患者获卵MII率、2PN率、卵裂率、D3优质/可利用胚胎率、取消周期率、囊胚形成率、优质/可利用囊胚率等指标的差异。胚胎移植后2周检测血hCG,并在胚胎移植后4周行阴道超声检查确定临床妊娠。随访所有患者的新鲜周期胚胎移植的临床妊娠率、OHSS发生率等妊娠结局指标。
1.5 统计学方法应用 SPSS 22.0统计学软件进行数据分析。符合正态分布的计量资料以均值±标准差表示,比较采用t检验;不符合正态分布的计量资料以中位数和四分位间距表示,比较采用Mann-WhitneyU检验;计数资料用频数和百分比描述,比较采用卡方检验或Fisher精确检验。采用Logistic回归分析影响PCOS不孕患者临床妊娠率的因素。P<0.05为差异有统计学意义,
2 结果
2.1 两组患者基线资料和卵巢刺激情况比较两组患者一般临床资料、体外授精方式比较差异无统计学意义(P>0.05),见表1。与拮抗剂固定方案组比较,卵泡期长方案组Gn天数更长,扳机日LH更低(P<0.05),但两组患者扳机日大卵泡数目、E2、P和子宫内膜厚度比较,差异无统计学意义(P>0.05)。拮抗剂固定方案组OSI显著高于卵泡期长方案组(P<0.05)。见表2。

表1 两组患者基线资料比较

表2 两组患者卵巢刺激情况比较
2.2 两组患者实验室指标及临床结局比较两组患者MII率、2PN率、卵裂率、D3优质/可利用胚胎率、取消移植周期率、囊胚形成率、优质/可利用囊胚率、卵巢反应、临床妊娠率比较,差异均无统计学意义(P>0.05)。见表3。拮抗剂固定方案组发生重度OHSS 13例(5.73%),卵泡期长方案组发生重度OHSS 4例(12.50%),见表4。
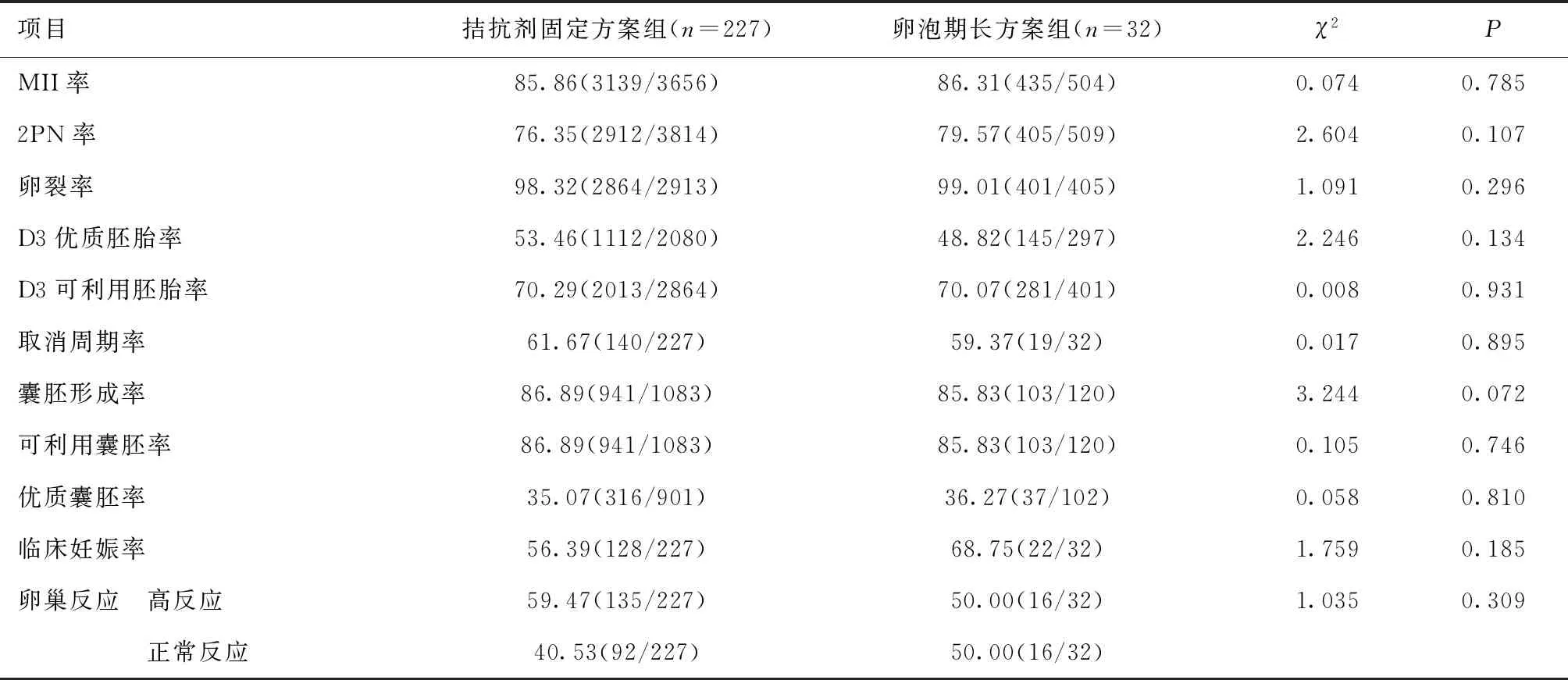
表3 两组患者实验室指标及临床结局比较 [%(n)]

表4 两组患者的OHSS结局比较
2.3 不同BMI的PCOS患者促排卵结果比较将患者按照BMI≥24 kg/m2和BMI<24 kg/m2进行分组比较后,结果发现无论超重与否,两种方案的实验室指标及临床结局差异均无统计学意义(P>0.05)。BMI≥24 kg/m2患者卵泡期长方案的2PN率、D3可利用胚胎率高于拮抗剂固定方案(P<0.05);BMI<24 kg/m2患者拮抗剂固定方案的D3可利用胚胎率高于卵泡期长方案(P<0.05)。在所有使用拮抗剂固定方案的患者中,BMI≥24 kg/m2和BMI<24 kg/m2两组在MII率、卵裂率、D3优质胚胎率、囊胚形成率、优质囊胚率、临床妊娠率、OHSS发生率差异均无统计学意义(P>0.05)。但BMI <24 kg/m2的拮抗剂固定方案的新鲜周期移植取消率和可利用囊胚率高于BMI≥24 kg/m2(P<0.05)。见表5。

表5 不同BMI的PCOS患者促排卵结果比较 [%(n)]
2.4 COS患者辅助助孕结局的影响因素分析Logistic多因素回归分析表明,年龄是PCOS患者行辅助生殖新鲜周期临床妊娠率的影响因素(P<0.05),见表6。
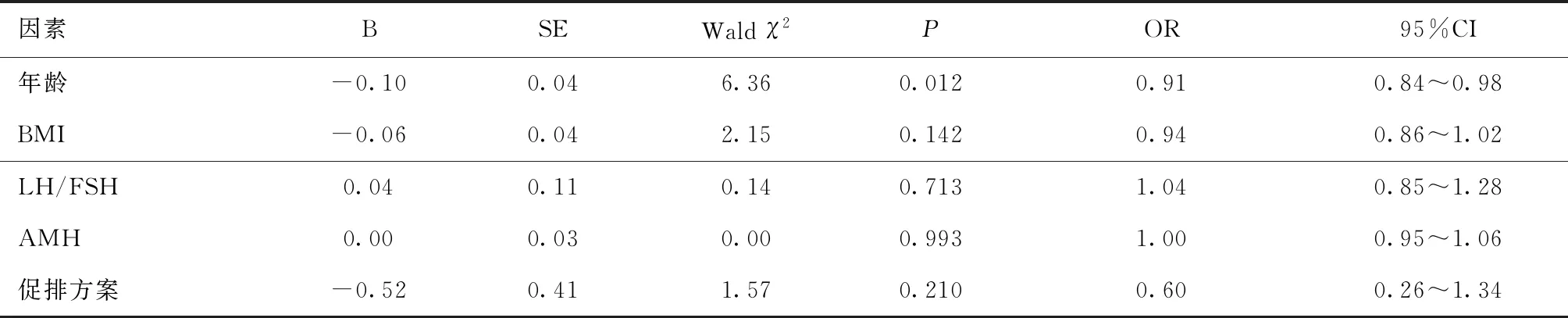
表6 多囊卵巢综合征患者的妊娠影响因素分析
3 讨论
本研究主要探讨了不同促排卵方案在PCOS患者中的应用,结果显示,卵泡期长方案Gn使用时间及总量增加,新鲜周期临床妊娠结局稍优于拮抗剂方案,但OHSS发生率也高于拮抗剂方案。且PCOS患者年龄影响其行辅助生殖的新鲜周期临床妊娠率。
目前PCOS患者常用的促排卵方案是激动剂方案和拮抗剂方案[7]。本研究发现卵泡期长方案的Gn使用时间和总量更多,优质囊胚率、新鲜周期妊娠率也更高。拮抗剂方案无需进行降调节,可减少促排卵时间和药物剂量。卵泡期长方案通过充分的垂体降调节改变了PCOS患者体内HPO轴的紊乱状态,改善卵泡对促排卵药物的反应性,改善卵子质量,这与非PCOS人群中的研究结果是一致的[8]。另外,GnRH激动剂降调节能提高子宫内膜胞饮突水平,抑制炎症反应,低雌激素水平可使内膜整合素表达水平升高,从而提升内膜容受性[9]。在正常反应人群中,与拮抗剂方案相比,激动剂方案的患者新鲜周期胚胎移植妊娠率更高,但累积妊娠率无显著差异[10]。在高反应人群中,拮抗剂方案在临床妊娠和继续妊娠方面不劣于激动剂方案[11]。拮抗剂方案新鲜周期胚胎移植妊娠率较低,一是因为拮抗剂可与子宫内膜细胞的GnRH受体结合,并且影响颗粒细胞芳香化酶活性,从而影响内膜容受性;二是拮抗剂存在溶黄体作用,且部分患者可能应用激动剂扳机,影响黄体功能[12]。
本研究多数为早发型OHSS,并且在卵泡期长方案中更高。2020年ESHRE指南建议对于卵巢高反应风险者,应用拮抗剂方案以减少OHSS风险[13]。根据体重进行了亚组分析,BMI≥24 kg/m2和BMI<24 kg/m2两组的辅助生殖结局无明显差异,但在D3可利用胚胎率方面,超重患者可能从卵泡期长方案获益,非超重患者则可能从拮抗剂固定方案获益。孔慧娟等报道对于肥胖的PCOS患者,卵泡期长效方案在累积活产率方面更具优势[14]。
本研究存在以下局限性:第一,本研究系回顾性研究,无法对纳入患者的基线水平进行控制;其次,本研究的随访时间有限,未统计累积妊娠情况和累积活产情况。还需要更多大样本、多中心的随机对照研究来进一步探究和验证。
综上,拮抗剂方案是目前PCOS患者的常用促排方案,可以减少促排卵的时长、促排卵药物的应用并降低OHSS发生的风险。在缩短妊娠等待时间方面,卵泡期长方案可通过更加充分的垂体降调节,改善性激素紊乱及子宫内膜容受性,获得比拮抗剂方案更好的新鲜周期移植临床妊娠结局,但在应用时需警惕OHSS风险。

