无针注射甘精胰岛素对2型糖尿病的控糖效果及胰岛β细胞功能的影响*
时永强,丁 燕,丁丽萍
(宁夏回族自治区石嘴山市第二人民医院内分泌科 753000)
糖尿病是一种以胰岛功能减退、胰岛素抵抗为特征的慢性终身性疾病,可能引起高血糖、脂肪及蛋白质等一系列代谢紊乱综合征,严重影响患者身体健康及生活质量[1]。糖尿病在国际上通常分为1型糖尿病、2型糖尿病、妊娠期糖尿病及其他特殊类型糖尿病4种类型,其中2型糖尿病约占糖尿病总人数的95%[2]。血糖的控制是首要问题,胰岛素治疗作为当前临床用于糖尿病治疗的重要方式,有着较好的控糖效果,但鉴于当前临床胰岛素注射方式多样,不同注射方式可能影响患者控糖效果[3]。无针注射器作为一种不同于传统注射针头穿刺皮肤给药的新型注射装置,可通过压力产生高压将药物以喷射方式注入皮下,其已在疫苗接种、手汗症患者治疗、美容药物注射等方面有了较为广泛的应用,可能有比传统有针注射更高的应用价值[4]。本研究探讨无针注射甘精胰岛素对2型糖尿病的控糖效果及胰岛β细胞功能的影响。
1 资料与方法
1.1 一般资料
选取2018年10月至2020年10月在本院住院的100例2型糖尿病患者为研究对象,分为无针组和有针组,每组50例。纳入标准:(1)参照《中国2型糖尿病防治指南》[5]诊断标准;(2)年龄30~70岁;(3)病程大于或等于3年,且每天接受稳定的甘精胰岛素治疗大于或等于1年。排除标准:(1)近6个月内发生严重心血管事件;(2)治疗期间同时应用激素或免疫抑制剂,且存在免疫力缺陷或低下;(3)既往有肝肾功能不全病史;(4)合并严重水电解质紊乱、良恶性肿瘤、血液系统疾病;(5)因精神疾病或其他原因无法配合本次研究;(6)1型糖尿病、妊娠期糖尿病或其他类型糖尿病。本研究经医院伦理委员会批准(20180420-3),患者及家属知情同意。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性,见表1。

表1 患者一般资料比较
1.2 方法
基础治疗:所有患者在入院后进行全身检查,同时对其进行宣教,使其规范生活方式,能更好地配合治疗;分组治疗前先给予患者胰岛素强化治疗3 d,均于三餐前30 min进行腹部皮下注射,注射剂量0.5 IU·kg-1·d-1,3 d后进行分组治疗,以3个月为1个疗程,治疗1个疗程后对疗效进行评价。有针组:采用胰岛素笔注射甘精胰岛素(珠海联邦制药股份有限公司,国药准字S20160009,生产批号20161223),起始剂量与强化治疗后基础胰岛素剂量相同,3 d后根据血糖水平进行调整。无针组:采用无针注射器(中国北京快舒尔公司,QS-M型)注射甘精胰岛素,起始剂量为强化治疗后基础胰岛素剂量的70%,3 d后根据血糖水平进行调整。
1.3 观察指标
(1)比较两组治疗前后血糖水平及胰岛素用量。分别抽取两组治疗前后空腹、餐后2 h静脉血5 mL,离心后采取葡萄糖氧化酶偶联比色法检测空腹血糖(FPG)及餐后2 h 血糖(2hPG)水平。(2)比较两组治疗前后胰岛β细胞功能。将患者治疗前后空腹静脉血离心后采用全自动化学发光法检测空腹胰岛素(FINS)、C肽(CP)水平,并计算胰岛素抵抗指数(HOMA-IR),数值越高表明其胰岛素抵抗越严重;采用免疫抑制透射比浊法检测血清糖化血红蛋白(HbA1c)水平。(3)比较两组患者治疗前后血糖波动情况,选择动态血糖监测仪在治疗前后分别测定患者血糖水平,每次测量均连续监测3 d,每天8个时间段(早餐前30 min、早餐后2 h、午餐前30 min、午餐后2 h、晚餐前30 min、晚餐后2 h、睡前30 min、凌晨3点),根据血糖动态监测结果计算两组血糖标准差(SD)、血糖波动幅度(MAGE)、日间血糖平均绝对差(MODD)。(4)比较两组治疗期间不良反应发生情况,主要包括疼痛[6]、注射处皮肤反应[7]、漏液、低血糖。检测仪器采用ADVIA 2400全自动生化仪(德国西门子股份公司),MMT-722动态血糖监测仪(美国美敦力公司)。
1.4 统计学处理
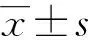
2 结 果
2.1 两组治疗前后血糖水平及胰岛素用量比较
无针组治疗后FPG、2hPG、胰岛素用量均明显低于有针组,差异有统计学意义(P<0.05),见表2。
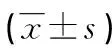
表2 两组治疗前后血糖水平及胰岛素用量比较
2.2 两组治疗前后血糖波动情况
两组治疗后SD、MAGE、MODD水平明显低于治疗前,差异有统计学意义(P<0.05)。两组治疗前后各指标组间比较差异无统计学意义(P>0.05),见表3。
2.3 两组治疗前后胰岛素β细胞功能比较
无针组治疗后HbA1c水平明显低于有针组,差异有统计学意义(P<0.05)。两组治疗后FINS、CP水平明显高于治疗前,HOMA-IR明显低于治疗前,差异有统计学意义(P<0.05),见表4。
2.4 两组不良反应发生情况
无针组不良反应总发生率14.00%明显低于有针组32.00%,差异有统计学意义(P<0.05),见表5。
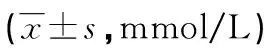
表3 两组治疗前后血糖波动情况
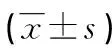
表4 两组治疗前后胰岛素β细胞功能比较
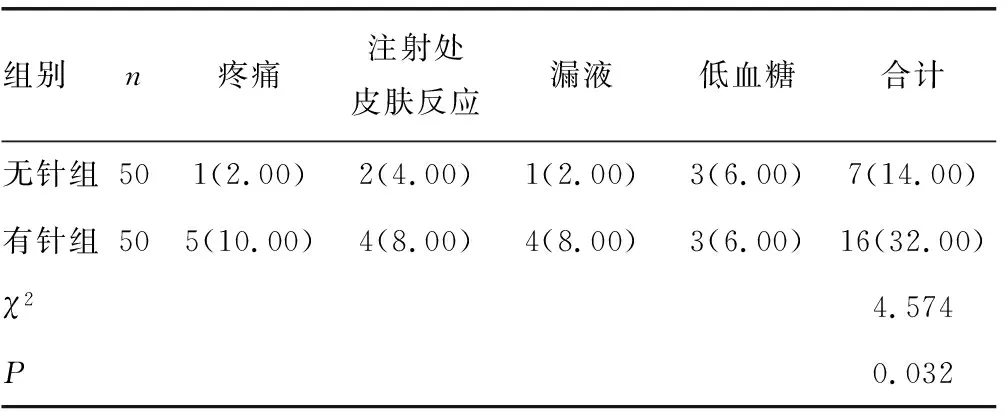
表5 两组不良反应发生情况[ n(%)]
3 讨 论
随着社会经济发展,人们生活方式改变,我国糖尿病患病率逐步升高。据 WHO预测,到2025年全世界糖尿病患者将达到3亿人,因而加强对糖尿病患者有效治疗方案的研究已成为临床重要课题[8]。目前无针注射技术已基本成熟,涉及各个领域,并取得了一定研究成果,也有不少研究证实无针注射速效及短效胰岛素能有效控制餐后血糖[9-10]。但目前对于其是否有长期、稳定的降糖效果还未可知。
本研究显示,无针组治疗后FPG、2hPG、胰岛素用量均明显低于治疗前及有针组,提示无针注射器可在长期有效控糖的同时减少胰岛素注射量,节省了医疗成本。两组均在分组治疗前进行3 d强化治疗,使血糖控制在一定水平。机体的血糖水平一般受术后胰岛功能的影响,当胰岛素与其受体结合后会使得细胞膜的葡萄糖通道打开,让细胞外的葡萄糖转运到细胞内,再把葡萄糖变成糖原的形式储存起来,从而降低机体血糖水平。无针注射将甘精胰岛素喷射入皮肤后药物会因为高速射流使胰岛素瞬间穿透皮肤,在皮下以类圆锥形均匀分布,从而增加吸收面积,药物沿机体缝隙均匀分布吸收更快,药物利用率更高,而甘精胰岛素在注射入人体后通过模拟人体胰岛素功能,促使组织、细胞对葡萄糖的摄取和利用增加,加速葡萄糖合成为糖原,进而减少患者血液中葡萄糖浓度,且因为无针操作下药物的高利用性,注射入机体的胰岛素能更好地促进葡萄糖转化,从而使得血糖控制效果更好[11]。而传统胰岛素笔注射会使药物在皮下形成一个直径约为5 mm的不规则水滴,被周围毛细血管吸收的时间会更长,药物利用率相对较低,因而对血糖的控制效果略弱于无针注射。糖尿病患者多为肥胖,脂肪组织血流降低会延迟传统注射时胰岛素的吸收,但无针注射使得药物在皮下呈弥散方式吸收,通过加大吸收面积来提高机体对药物的吸收速度,有效减少后期胰岛素注射剂量[12],这与王莹等[13]的研究相一致。
无针组治疗后HbA1c水平明显低于治疗前及有针组,两组治疗后FINS、CP水平明显高于治疗前,HOMA-IR水平明显低于治疗前,提示无针注射在改善血糖的同时不会影响胰岛素β细胞正常功能的恢复。HbA1c可反映患者2~3个月平均血糖变化,无针注射后患者平均水平明显更低,表明无针注射甘精胰岛素有更长期、稳固的治疗效果[14]。CP作为一种具有31个氨基酸的内源性多肽,其前体胰岛素原的肽链在胰岛中断裂形成CP和FINS,因而对FINS水平表达有协同作用。甘精胰岛素注入人体后可模拟生理性基础胰岛素分泌,具有平稳、无峰值的特点,从而促进患者胰岛β细胞功能的恢复,两种注射方式并不影响其对胰岛β细胞功能的改善效果。
两组治疗后SD、MAGE、MODD水平明显低于治疗前,两组治疗前后SD、MAGE、MODD水平组间比较差异无统计学意义(P>0.05)。血糖波动可加速并发症发展,损害胰岛素分泌功能,但本研究显示无针注射并没有明显增加血糖波动的发生,这可能是由于无针注射被喷射入皮下,可缓慢稳定发挥作用,保持原有代谢特征,从而更加稳定地控制血糖[15]。
无针组不良反应总发生率14.00%明显低于有针组32.00%。无针注射喷出的射流极细,在皮肤表面留下的创伤比传统胰岛素笔更小,因此对神经末梢的刺激更小,疼痛感减轻,且注射后短时间的停留能增加胰岛素吸收,减少漏液的发生。注射后偶有红点、瘀斑,但弥散后可尽快吸收,不会增加不良反应,这与谢晓敏等[16]的研究相符。
综上所述,无针注射甘精胰岛素可改善2型糖尿病患者血糖水平,减少胰岛素注射量,提高药物利用率,在改善胰岛β细胞功能的同时减少不良反应发生,值得临床推广。

