MFe2O4(M=Zn、Co、Ni)/CdS纳米花球的制备及其光催化性能
邵 敏,梅益成,刘志英,徐炎华,李忠玉,4,徐 松
(1.南京工业大学 土木工程学院,江苏 南京 211800;2.常州大学 环境与安全工程学院,江苏 常州 213164;3.南京工业大学 环境科学与工程学院,江苏 南京 211800;4.常州大学 先进催化与绿色制造协同创新中心,江苏 常州 213164;5.常州大学 石油化工学院 江苏省绿色催化材料与技术重点实验室,江苏 常州 213164)
近年来,随着社会经济的快速增长,能源短缺和环境污染问题已经成为制约可持续发展的关键因素。光催化技术凭借其二次污染少、催化活性高以及操作方便等优点,被认为是一种高效、绿色和有前景的解决方案。半导体光催化剂可以有效地利用太阳光,分解水产氢、降解有机物以及将CO2转化为可再生燃料,具有广阔的应用前景[1-4]。目前,常用的可见光半导体光催化材料有AgPO4[5]、Ag3VO4[6]、Bi2WO6[7]、Bi2MoO6[8]、Fe2O3[9]、CdS[10]。
CdS是一种具有较窄带隙(2.4 eV)的直接带隙半导体,可以吸收波长<520 nm的太阳光,广泛应用于光催化领域。但是,光生电子-空穴对的快速重组,导致了CdS光催化效率低下和光腐蚀现象的发生。为了克服这些缺陷,常将CdS与能带结构不同的半导体材料进行复合,形成异质结,如CeO2/CdS[11]、TiO2/CdS[12]、ZnFe2O4/CdS[13]、SnO2/CdS[14]、BiPO4/CdS[15]、MoS2/CdS[16],以促进电子-空穴对的分离和转移,从而提高其光催化活性。Wang等[12]采用水热法合成介孔锐钛矿型TiO2/CdS中空微球,对可见光激发产生的光生电子和空穴能够有效地分离,100 min内对罗丹明B和苯酚的去除率分别为94%和85%,表现出优异的光催化活性;Fang等[13]将ZnFe2O4纳米颗粒负载到CdS纳米棒上形成异质结,在可见光照射下催化还原Cr(Ⅵ),取得了较好的效果,120 min的还原效率为90%。侯美顺等[17]将p-NiFe2O4窄带隙半导体与n-CdS宽带隙半导体复合,制备光催化剂p-NiFe2O4/n-CdS,在固定床微反应器中降解亚甲基蓝(MB),并探讨了NiFe2O4质量分数、流速、MB溶液初始浓度和pH对降解性能的影响,结果表明复合光催化剂对MB的降解率达88.5%,是CdS的1.8倍。
尖晶石铁氧体在光、热、电、磁等方面表现出许多新奇的特性,近年来受到人们的普遍关注[18-20]。铁氧体化学性质稳定,利于磁性分离,而且禁带宽度窄,可以响应可见光。但单独使用却效率低下,因而多采用改性、掺杂或与其他半导体材料复合的方法来提高其光催化效率[21-22]。
本文采用水热法将MFe2O4(M=Zn、Co、Ni) 铁氧体纳米颗粒负载于CdS纳米花球(CdS NSPs)的表面,形成MFe2O4(M=Zn、Co、Ni)/CdS复合材料,探索其结构和光学性质,并以染料孔雀石绿(MG)和MB为降解对象考察其光催化性能。
1 实验部分
1.1 材料的制备
参考文献[23]制备CdS NSPs。将0.006 4 mol Cd(CH3COO)2·2H2O和0.016 0 mol NH2CSNH2溶于80 mL去离子水中,在室温下快速搅拌30 min后,装入100 mL聚四氟乙烯内衬的反应釜中,140 ℃加热24 h。将获得的黄色沉淀用去离子水和无水乙醇反复洗涤,离心分离(转速5 000 r/min),干燥后研磨成粉末,即得CdS NSPs。
采用水热法[24]制备MFe2O4(M=Zn、Co、Ni)/CdS复合材料。取0.1 g CdS NSPs置于60 mL去离子水中,超声1 h使CdS充分分散,得到混浊液。称取适量 M(NO3)2·6H2O (M=Zn、Co、Ni)和FeCl3·6H2O加入上述混浊液,并磁力搅拌使其完全溶解。随后逐滴加入10 mL NaOH溶液(3 mol/L),快速搅拌10 min后,装入100 mL聚四氟乙烯内衬的反应釜中,于180 ℃加热15 h。将产物洗涤、干燥、研磨,即得MFe2O4(M=Zn、Co、Ni)/CdS复合材料。根据MFe2O4(M=Zn、Co、Ni)与CdS的质量比分别为0.1∶1、0.2∶1、0.3∶1,复合材料分别记为0.1MFe2O4(M=Zn、Co、Ni)/CdS、0.2MFe2O4(M=Zn、Co、Ni)/CdS、0.3MFe2O4(M=Zn、Co、Ni)/CdS。
1.2 材料的表征
采用D/max2500PC型X线衍射仪(XRD)测试样品的晶相;红外吸收光谱由NicoletiS 50型傅里叶变换红外光谱(FT-IR)仪进行检测;JSM-6360LA型扫描电子显微镜(SEM)和JEM-2100型透射电子显微镜(TEM)用于观测样品的形貌;采用Cary Eclipse型荧光分光光度计对样品进行荧光光谱(PL)测试。紫外-可见漫反射光谱(UV-vis)由UV-3600型分光光度计测试。瞬态光电流响应曲线和电化学阻抗谱均采用RST型电化学工作站进行测试,电解液为0.2 mol/L的Na2SO4。
1.3 光催化活性实验
光催化反应在比朗EL-GHT-V型光化学反应仪中进行。称取30 mg样品,均匀分散到装有50 mL MG或MB溶液(质量浓度为20 mg/L)的比色管中。先将比色管置于黑暗处搅拌30 min进行暗反应,以达到吸附-脱附平衡。随后,在1 kW的氙灯照射下进行光催化反应,每隔20 min取样2 mL。将取出的混浊液以10 000 r/min速度离心3 min,用UV-1800PC型紫外-可见分光光度计测定上清液的吸光度,根据MG或MB的浓度-吸光度标准曲线,计算染料浓度。
2 结果与讨论
2.1 XRD表征
图1为0.2MFe2O4(M=Zn、Co、Ni)/CdS和CdS NSPs的XRD图谱。由图1可见:CdS NSPs衍射图谱中的特征峰与六方相CdS(JCPDS No. 41-1049)相匹配,在24.8°、26.5°、28.2°、43.7°、47.8°和51.8°等位置对应(100)、(002)、(101)、(110)、(103)和(112)等晶面,与文献[25]相符。0.2MFe2O4(M=Zn、Co、Ni)/CdS复合材料的衍射图不仅具有CdS的特征峰,同时还出现了尖晶石铁氧体的相应衍射峰,与ZnFe2O4(JCPDS No. 22-1022)[26]、CoFe2O4(JCPDS No. 22-1086)[27]、NiFe2O4(JCPDS No. 10-0325)[28]标准卡片相一致。3种复合材料都表现出较为尖锐的衍射峰,且没有其他杂峰,说明复合材料具有较高的结晶度。从图1右侧的细节图可以看到,由于尖晶石铁氧体中金属离子的不同,其复合材料(311)、(440)晶面对应的特征峰出现了偏移,而CdS(102)晶面对应的特征峰却没有发生变化。
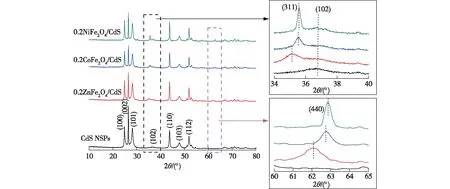
图1 CdS NSPs、0.2ZnFe2O4/CdS、0.2CoFe2O4/CdS和0.2NiFe2O4/CdS的XRD图谱Fig.1 XRD patterns of CdS NSPs, 0.2ZnFe2O4/CdS, 0.2CoFe2O4/CdS and 0.2NiFe2O4/CdS
纳米材料的平均晶粒尺寸可通过Debye-Scherrer方程[29](式(1),适用范围为1~100 nm)计算得到。
(1)
式中:d为平均晶粒尺寸;K为形状因子,取0.9;λ为X线波长;β为衍射峰的半高宽;θ为衍射半角。0.2MFe2O4(M=Zn、Co、Ni)/CdS复合材料中尖晶石铁氧体的平均晶粒尺寸根据对应材料的(311)晶面衍射峰进行计算,结果见表1。由表1可得:复合材料中的铁氧体按照平均晶粒尺寸由小到大排列的顺序为ZnFe2O4(7.13 nm)、CoFe2O4(18.34 nm)、NiFe2O4(45.12 nm)。

表1 0.2MFe2O4(M=Zn、Co、Ni)/CdS中铁氧体的平均晶粒尺寸
2.2 SEM和TEM分析
SEM和TEM可以用于观察纳米材料的大小和形貌,结果见图2。由图2(a)和2(b) CdS NSPs的SEM和TEM照片可见:CdS为直径约270 nm的球状,大小均一,表面粗糙,呈花球状。由图2(c)和2(d)可见:ZnFe2O4的纳米颗粒均匀分布在CdS纳米花球的表面,ZnFe2O4纳米颗粒的粒径较小,约7 nm;高分辨透射影像(HRTEM)揭示了ZnFe2O4和CdS之间接触点的信息,CdS的晶格间距为0.344 nm,对应(002)晶面;ZnFe2O4的晶格间距为0.483 nm,对应(111)晶面[30]。由图2(e)和2(f) 可见:0.2CoFe2O4/CdS晶格条纹的间距为0.340 nm,对应CdS的(002)晶面;间距为0.319和0.259 nm的条纹分别对应CoFe2O4的(220)和(311)晶面[27]。由图2(g)和2(h)可见:0.2NiFe2O4/CdS中铁酸镍的颗粒尺寸较大,约40~50 nm,与从XRD中获得的晶粒尺寸基本一致;从0.2NiFe2O4/CdS的HRTEM照片可以观察到CdS的晶格间距为0.347 nm,对应(002)晶面;NiFe2O4的晶格间距为0.290 nm,对应其(220)晶面[20]。

图2 CdS NSPs的SEM和TEM照片及0.2MFe2O4(M=Zn、Co、Ni)/CdS的TEM和HRTEM照片Fig.2 SEM and TEM inages of CdS NSPs, TEM and HRTEM images of 0.2MFe2O4(M=Zn,Co,Ni)/CdS
2.3 红外光谱
图3为CdS NSPs和0.2MFe2O4(M=Zn、Co、Ni)/CdS的FT-IR图谱。由图3可见:在500~650 cm-1范围内,0.2MFe2O4(M=Zn、Co、Ni)/CdS复合材料均可观察到一个指纹峰,由铁氧体四面体M-O团簇的拉伸振动产生[31-32],而纯CdS则没有该峰。对于0.2ZnFe2O4/CdS,在555 cm-1处观察到这一M-O团簇的拉伸振动峰,当用Co2+和Ni2+替换Zn2+时,这一拉伸振动峰向频率更高的方向漂移,振动峰值分别在600和607 cm-1左右,左侧的细节图中可以明显看到振动峰值的变化。这是由于振动频率的变化与胡克定律[33]相关,由胡克定律可以得出,振动频率与力常数成正比,与折合的原子质量成反比。与Co2+和Ni2+相比,ZnFe2O4结构中Zn2+的分子量较大,导致了Zn2+掺杂的0.2ZnFe2O4/CdS的振动频率明显较小,即相应的振动峰值较小。
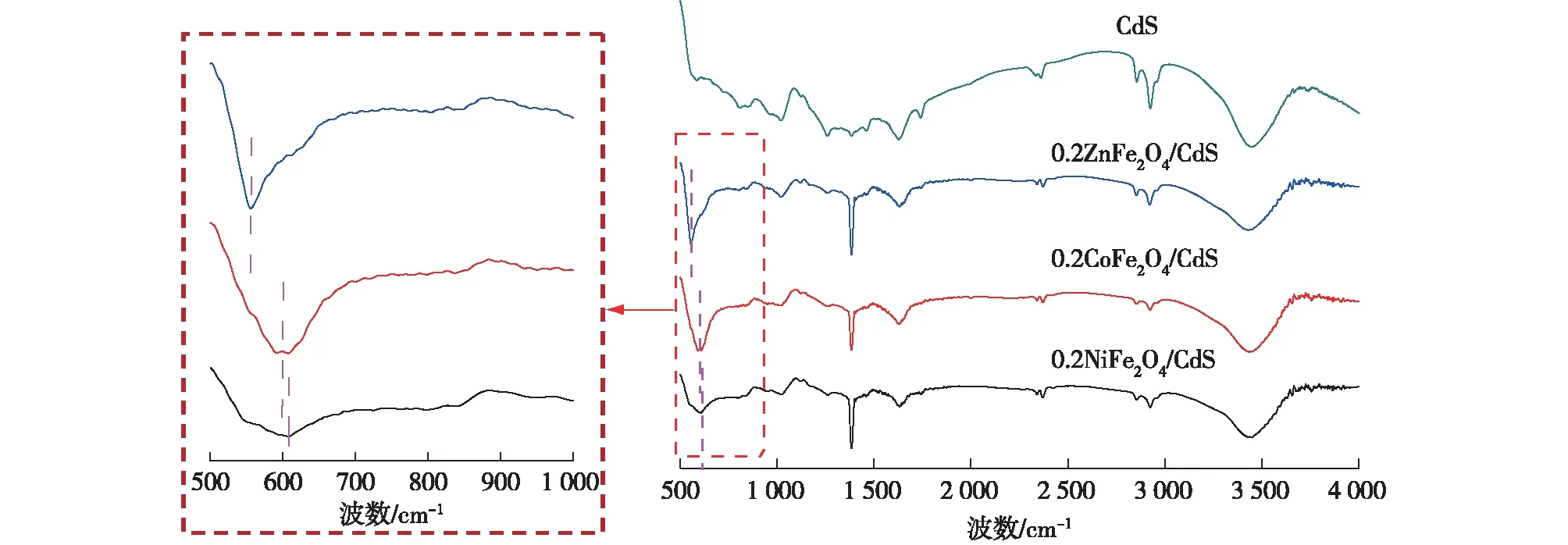
图3 0.2ZnFe2O4/CdS、0.2CoFe2O4/CdS、0.2NiFe2O4/CdS和CdS NSPs的FT-IR图谱Fig.3 FT-IR spectra of 0.2ZnFe2O4/CdS, 0.2CoFe2O4/CdS, 0.2NiFe2O4/CdS and CdS NSPs
2.4 紫外-可见漫反射光谱
采用UV-vis光谱对样品的光学性质进行分析,图4为0.2MFe2O4(M=Zn、Co、Ni)/CdS和CdS NSPs的UV-vis光谱。由图4可见:CdS的吸收带边约为570 nm,0.2ZnFe2O4/CdS、0.2CoFe2O4/CdS、0.2NiFe2O4/CdS复合材料在可见光525~725 nm波长范围内具有明显的光吸收性能,这表明将铁氧体纳米颗粒负载到CdS NSPs的表面,有利于提升材料对可见光的吸收,对光催化反应具有重要意义。
为估算光催化材料相应的带隙能量,根据Tauc方程[34]绘制(αhv)2~hv关系曲线,结果见图5(图中α为吸光度,hv为入射光子能量)。通过对图5中曲线的直线部分做切线得出:CdS NSPs的带隙为2.36 eV,0.2ZnFe2O4/CdS、0.2CoFe2O4/CdS、0.2NiFe2O4/CdS的带隙分别为2.29、2.32和2.28 eV。与纯铁氧体ZnFe2O4(1.90 eV)、CoFe2O4(1.19 eV)、NiFe2O4(1.56 eV)[17,35-36]的带隙值相比,复合材料的带隙出现红移,这可能是由界面缺陷和复合材料形成子带隙能级等原因造成的[37]。
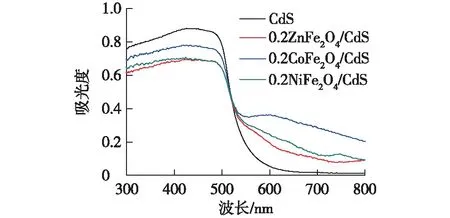
图4 0.2ZnFe2O4/CdS、0.2CoFe2O4/CdS、0.2NiFe2O4/ CdS和CdS NSPs的UV-vis图谱Fig.4 UV-vis spectra of 0.2ZnFe2O4/CdS, 0.2CoFe2O4/CdS, 0.2NiFe2O4/CdS and CdS NSPs
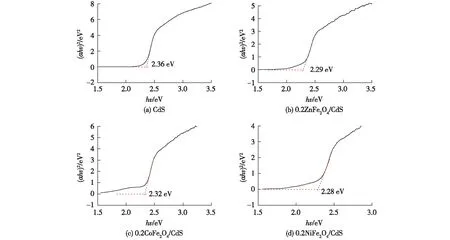
图5 CdS NSPs、0.2ZnFe2O4/CdS、0.2CoFe2O4/CdS和0.2NiFe2O4/CdS的带隙图Fig.5 Band gaps of CdS NSPs, 0.2ZnFe2O4/CdS, 0.2CoFe2O4/CdS and 0.2NiFe2O4/CdS
2.5 荧光光谱分析
荧光光谱通常是由于表面态载流子的重组而产生,经常用于衡量光催化材料中光生电子和空穴的分离能力。CdS NSPs和0.2MFe2O4(M=Zn、Co、Ni)/CdS在激发波长为250 nm时产生的荧光光谱见图6。由图6可见:CdS NSPs在560和588 nm处产生两个强峰,之后出现了一系列较弱的峰。0.2MFe2O4(M=Zn、Co、Ni)/CdS的荧光光谱和CdS NSPs比较相似,其最强峰主要出现在588 nm处。产生较强PL峰的原因是激发态电子和空穴复合而产生的荧光,弱峰则归因于材料表面缺陷部位的空穴与捕获电子的复合[38]。
由图6还可以看出:CdS NSPs产生的荧光强度最大,随着ZnFe2O4、NiFe2O4以及CoFe2O4的负载,荧光强度逐渐降低,按照荧光发射强度由强到弱排列的顺序为CdS、0.2ZnFe2O4/CdS、 0.2NiFe2O4/CdS 、0.2CoFe2O4/CdS。
半导体材料受到可见光的辐射,产生光诱导的电子-空穴对。光诱导电子向CdS迁移,而空穴则向MFe2O4(M=Zn、Co、Ni)转移,从而导致电子与空穴分离。因此,由于CdS和铁氧体MFe2O4(M=Zn、Co、Ni)之间快速的电荷转移,降低了材料中电子-空穴对的复合率,导致复合材料的荧光强度要低于CdS NSPs[14]。
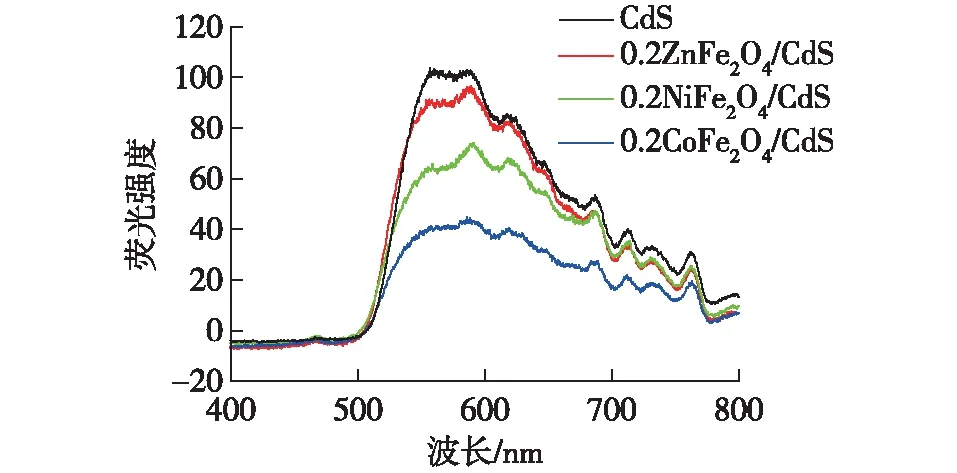
图6 0.2NiFe2O4/CdS、0.2ZnFe2O4/CdS、0.2CoFe2O4/CdS以及CdS NSPs的PL图谱Fig.6 Photoluminescence spectra of 0.2NiFe2O4/CdS, 0.2ZnFe2O4/CdS, 0.2CoFe2O4/CdS and CdS NSPs
2.6 瞬时光电流曲线与电化学阻抗谱
瞬时光电流曲线和电化学阻抗谱可以进一步说明光催化材料中光生载流子的激发、分离、转移和重组,0.2MFe2O4(M=Zn、Co、Ni)/CdS以及CdS NSPs的瞬时光电流曲线和阻抗谱见图7。由图7(a)可得:在光源关闭时,工作电极的光电流很小,而光照后,样品的光电流都出现不同程度的响应,按响应由大到小排列的顺序为0.2ZnFe2O4/CdS、0.2CoFe2O4/CdS、0.2NiFe2O4/CdS。0.2ZnFe2O4/CdS的光电流最大,大约是CdS的3倍。这说明CdS与MFe2O4(M=Zn、Co、Ni)之间形成的异质结能有效提高载流子的分离能力,表现出较强的光电流响应信号。电化学阻抗谱在高频区域的半圆半径可以反映电解质与半导体之间的电子转移过程,较大的半径则意味着较低的电荷转移效率。由图7(b)可得:相比于CdS,复合材料的半圆半径较小,其中0.2ZnFe2O4/CdS的半圆半径最小,说明其电荷转移的效率最高。瞬时光电流曲线和阻抗谱都证明了复合材料能够对光生载流子进行有效的分离和转移,抑制界面电子和空穴的二次复合。
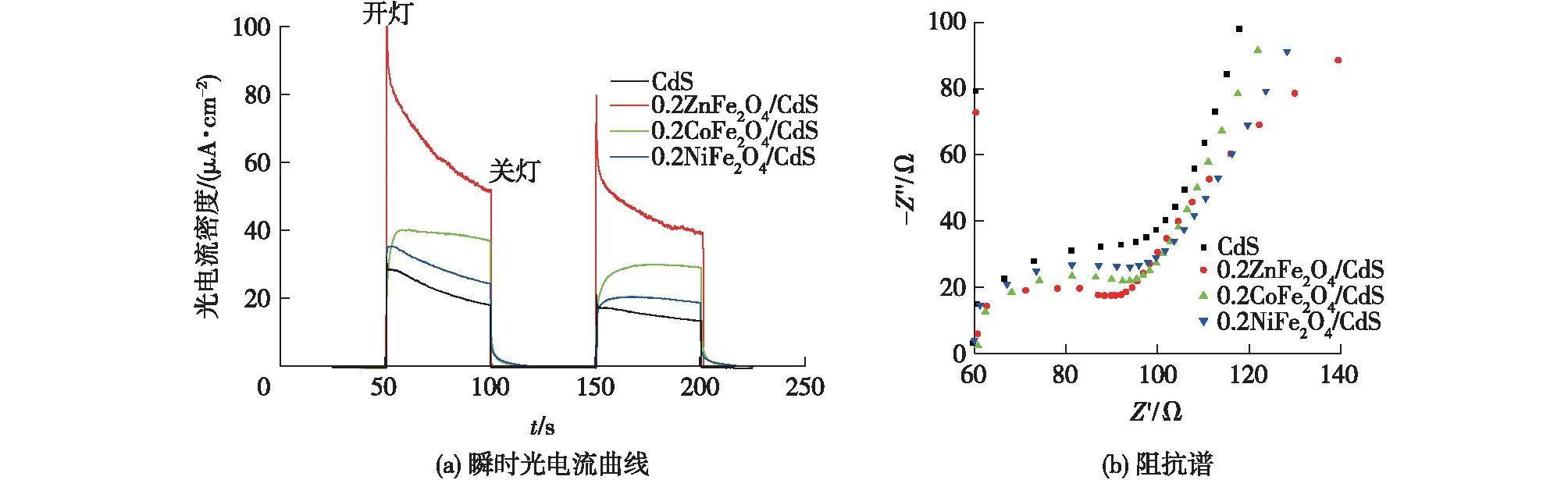
图7 0.2MFe2O4(M=Zn、Co、Ni)/CdS以及CdS NSPs的瞬时光电流曲线和阻抗谱Fig.7 Transient photocurrent response curses and electrochemical impedance spectra of 0.2MFe2O4(M=Zn,Co,Ni)/CdS and CdS NSPs
2.7 光催化活性实验
2.7.1 最佳复合比例的确定
以MG为降解对象,分别考察不同复合比例的MFe2O4(M=Zn、Co、Ni)/CdS的光催化活性,结果见图8,其中c0和ct分别为染料的初始浓度和光照t时间后染料的浓度。由图8可见:3种复合材料对MG的降解效率均高于单一的CdS NSPs和铁氧体,表现了较高的催化活性;MFe2O4(M=Zn、Co、Ni)与CdS质量比为0.2∶1的异质结对MG的降解效率远高于相同比例的混合物。结合紫外-可见漫反射光谱和荧光光谱,可以看出CdS和铁氧体形成的异质结增强了对可见光的吸收,有效地分离了电子-空穴对,从而提高了对污染物MG的降解效率。此外,从图8还可以看出:异质结中铁氧体在CdS上的负载比例同样影响MG的降解效率,铁氧体负载量过低或过高都会影响催化剂的活性,实验结果表明,当铁氧体MFe2O4(M=Zn、Co、Ni)与CdS的质量比为0.2∶1时,3种复合材料都对MG表现出最好的光催化活性。
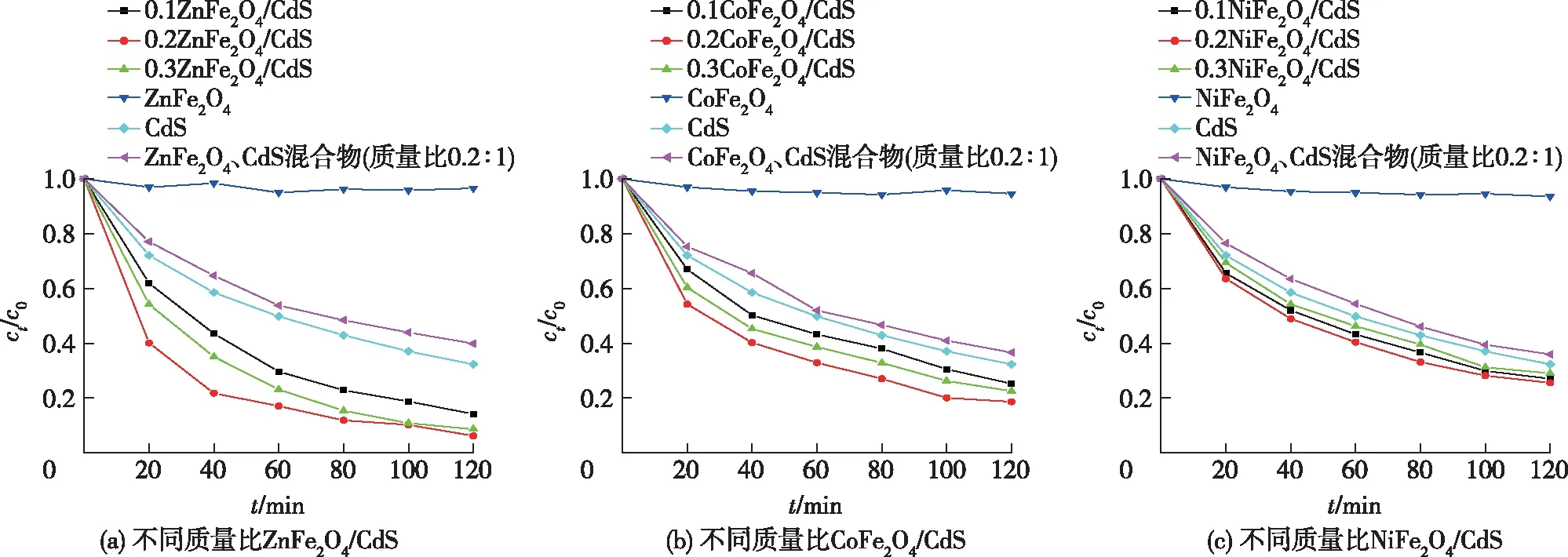
图8 不同质量比例MFe2O4(M=Zn、Co、Ni)/CdS对MG的降解曲线Fig.8 Degradation curves of MG degraded with different mass ratios of MFe2O4 (M=Zn, Co, Ni)/CdS
2.7.2 光催化活性的比较
为进一步探讨不同种类铁氧体的负载对复合材料光催化活性的影响,选取催化活性最佳的0.2MFe2O4(M=Zn、Co、Ni)/CdS,比较其对MG和MB的降解效果。图9给出了CdS NSPs和0.2MFe2O4(M=Zn、Co、Ni)/CdS降解MG和MB的降解曲线及动力学曲线。从图9(a)和9(c)中可以看出:3种复合材料中,0.2ZnFe2O4/CdS复合材料的催化活性要显著高于0.2CoFe2O4/CdS和0.2NiFe2O4/CdS;在120 min内,0.2ZnFe2O4/CdS对MG的去除率可以达到94%,对MB的去除率达到89%。由表1中3种复合材料中铁氧体的晶粒尺寸可知,ZnFe2O4的平均晶粒尺寸最小,一般来说,晶粒尺寸越小,表面活性位点就越多,对应的催化活性也越高,与上述实验结果相一致。
为了进一步研究复合材料的光催化性能,运用一级反应动力学模型[3]进行拟合,见式(2)。
ln(c0/ct)=kt
(2)
式中:k为反应速率常数。
由图9(b)和9(d)动力学拟合结果可知:CdS NSPs和0.2MFe2O4(M=Zn、Co、Ni)/CdS对MG的反应速率常数分别为0.009 0、0.020 9、0.013 3、0.010 9 min-1,对MB的反应速率常数分别为0.007 7、0.017 7、0.012 6、0.009 5 min-1。因此,本文中,复合材料对MG和MB的反应速率都明显高于CdS NSPs;3种复合材料作为光催化剂时,0.2ZnFe2O4/CdS对两种染料的反应速率高于其他两种复合材料,是最佳的可见光催化材料。各复合材料在染料降解上表现出的光催化活性,与前面的电化学表征结果是一致的。
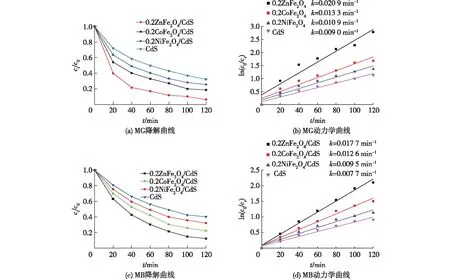
图9 0.2MFe2O4(M=Zn、Co、Ni)/CdS和CdS NSPs对MG、MB的降解曲线以及动力学曲线Fig.9 Degradation curves and kinetic curves of MG and MB degraded by 0.2MFe2O4/CdS (M=Zn, Co, Ni) and CdS NSPs
2.7.3 催化剂的稳定性
稳定性是评价催化材料的一个重要参数。以0.2ZnFe2O4/CdS为代表,MG为降解对象,进行4次循环实验,结果见图10。由图10可见:催化剂经过4次循环后,0.2ZnFe2O4/CdS对MG的降解效率未有明显下降,去除率可以达到87%,说明0.2ZnFe2O4/CdS仍具有较高的光催化活性。实验结果说明,0.2ZnFe2O4/CdS具有较好的光催化稳定性。
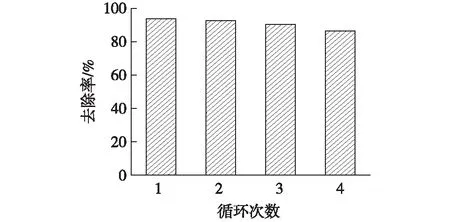
图10 0.2ZnFe2O4/CdS光催化降解MG的循环实验Fig.10 Cyclic experiments of 0.2ZnFe2O4/CdS for the photocatalytic degradation of MG
2.7.4 降解机制
CdS为n型半导体,其导带(CB)电位和价带(VB)电位分别为-0.58和1.77 eV,禁带宽度为2.35 eV[17];ZnFe2O4、CoFe2O4、NiFe2O4为p型半导体,ZnFe2O4的CB和VB电位分别为-1.5和0.4 eV,禁带宽度为1.90 eV[35];CoFe2O4的CB和VB电位分别为-0.71和0.48 eV,禁带宽度为1.19 eV[36];NiFe2O4的CB和VB电位分别为-1.18和0.38 eV,禁带宽度为1.56 eV[17]。因此,p型半导体MFe2O4(M=Zn、Co、Ni)的CB和VB电位都比n型CdS的更负,二者复合之后形成了p-n异质结[39],其能带结构见图11。当MFe2O4(M=Zn、Co、Ni)和CdS在可见光的照射下产生光生电子(e-)和空穴(h+),来自MFe2O4(M=Zn、Co、Ni)CB的激发电子流到CdS的CB上,而CdS中的空穴则向MFe2O4(M=Zn、Co、Ni)的VB移动,即光生电子和空穴沿相反方向迁移,这降低了重组的可能性,提高了电荷分离的效率,从而提升了光催化活性。
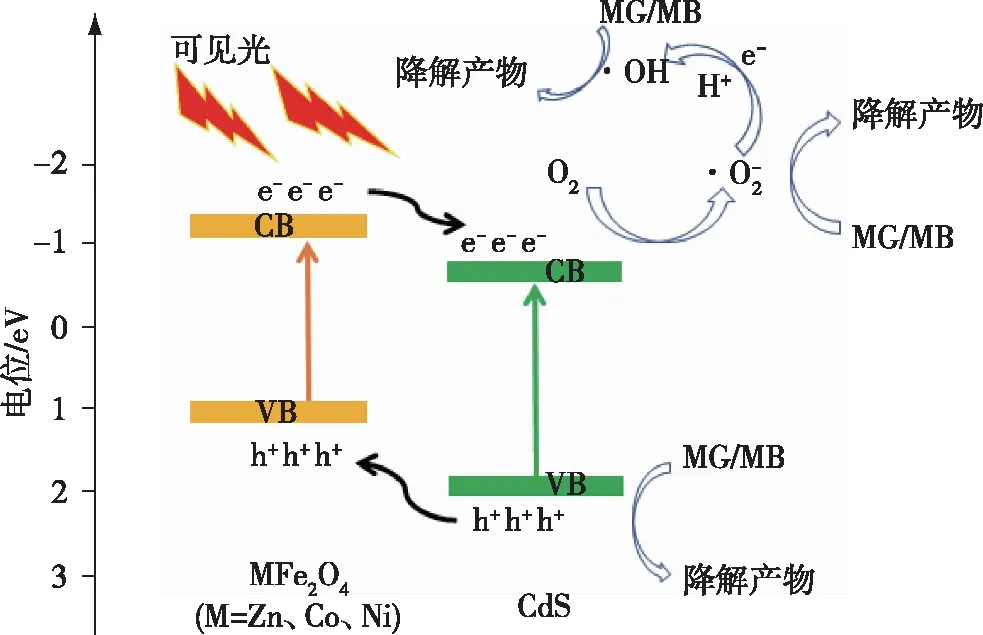
图11 光催化反应机制Fig.11 Mechanism of the photocatalytic reaction
3 结论
1)通过水热法成功制备了MFe2O4(M=Zn、Co、Ni)/CdS纳米复合材料,MFe2O4(M=Zn、Co、Ni)纳米颗粒负载在CdS纳米花球表面,形成p-n异质结,能够对光生载流子进行有效的分离、迁移,抑制了电子和空穴的复合,表现出较高的光催化活性。
2)复合材料对可见光的吸收增强,在525~725 nm有明显的光响应;当3种铁氧体与CdS的质量比为0.2∶1时,复合材料在降解MG时表现出最好的降解效果。
3)0.2MFe2O4(M=Zn、Co、Ni)/CdS纳米复合材料对MG和MB染料降解活性明显高于CdS NSPs,3种复合催化剂中,0.2ZnFe2O4/CdS的降解效率最高。在可见光照射下,0.2ZnFe2O4/CdS 在120 min内对MG的去除率达到了94%,对MB的去除率达到了89%。

