响应面法优化沙拉沙星/β -环糊精包合物制备工艺与稳定性评价
姜兴粲,李 冰,杨 敏,张继瑜,*
(1.农业农村部兽用药物创制重点实验室,甘肃 兰州 730050; 2.甘肃省新兽药工程重点实验室,甘肃 兰州 730050; 3.中国农业科学院 兰州畜牧与兽药研究所,甘肃 兰州 730050)
沙拉沙星(sarafloxacin,SAR)是一种具有4-喹诺酮环结构的喹诺酮类广谱抗菌药物,具有较强的抗菌活性[1-2]。沙拉沙星适用于革兰氏阴性菌、革兰氏阳性菌及霉形体引起的各种感染,特别对家禽的慢性呼吸道病、大肠埃希菌感染、传染性鼻炎等疗效显著;猪可用于红痢、白痢、黄痢、丹毒等;牛用于巴氏杆菌、布氏杆菌感染等;羔羊用于痢疾、大肠杆菌感染等,均有良好的疗效。沙拉沙星的常见剂型为粉剂,具有溶解度差、药物性质不稳定等缺点。分子包合技术具有提高溶解度和稳定性、改善生物利用度的优点。分子微胶囊技术是以壁材包裹芯材,从而实现对芯材保护的一种加工方法。经过包合后,不仅可以改善芯材的物理性质,还可以使芯材免受光、热等极端环境的影响。β-环糊精(β-cyclodextrin,β-CD)做为一种优良的药用辅料可用于沙拉沙星的包合过程,弥补沙拉沙星不稳定的缺点,达到对其进行优化的目的[3-4]。
响应面方法(response surface methodology,RSM)是一种数学和统计技术,用于建立经验模型,对于优化生产条件具有重要意义。RSM可以减少分析的次数,快速筛选出设定指标下的工艺参数,具有成本低、用时短等特点[5-6]。喷雾干燥是将溶液雾化到热干介质中使之干燥的技术。雾化产生的液滴能够在很短的停留时间内有效地将水蒸发在干燥室中。沙拉沙星耐热不耐光,可以采用高温喷雾干燥来提高干燥效率,干燥过程最终将液体包合物转化为固体粉末,从而易于运输和储存,可以更高效地推广到临床使用中[7-9]。基于以上因素,本研究采用响应面法优化包合作用条件和喷雾干燥工艺参数,以期为广谱抗菌药沙拉沙星的广泛应用提供参考。
1 材料与方法
1.1 材料与仪器
1.1.1 试验材料
沙拉沙星(含量>98%,批号为20180111),购自广州杨叶生物科技有限公司;β-环糊精(β-CD,批号为20180309)、四丁基溴化铵(AR级,含量为99%,批号为20180119),购自上海源叶生物科技有限公司;沙拉沙星标准品(批号为20180113),购自中国兽医药品监察所;磷酸(HPLC级,含量为98%,批号为20180311),购自美国Kermel公司;乙腈(GR级,含量为99.98%,批号为20171009),购自美国Fisher Chemical公司;氢氧化钠(含量>96%,批号为20161113),购自西安化学试剂厂;甲醇(GR级,含量>99.98%,批号为20171201)。
1.1.2 试验仪器
1290型高效液相色谱仪、数控超声波清洗器(型号为KQ3200DE)、优普超纯水制造系统、紫外分光光度计,购自美国Agilent Technologies公司;天平(型号为BSA423S-CW),购自德国Sartorius公司;可控温磁力搅拌器,购自德国IKA公司;离心式喷雾干燥机(型号为LPG-Ⅴ),购自湘宏设备科技有限公司。
1.2 沙拉沙星/β-环糊精包合物制备工艺优化
研究中制备工艺主要分为包合工艺与干燥工艺两步。将原料药用适量碳酸钠溶解后加入到饱和的β-环糊精水溶液中,恒温恒速搅拌直至β-环糊精充分包合原料药。当增加β-环糊精比例、提高包合温度或延长包合时间均可以提高包合物制剂的包合率[3,10]。采用响应面模型的Box-Behnken设计法对制备沙拉沙星/β-环糊精(SAR/β-CD)包合物微胶囊的制备工艺进行优化[11]。以包合率(Y)为效应值,选取SAR与β-CD的摩尔比(A)、包合温度(B)、包合时间(C)作为3个因素,因素水平如表1所示。利用Box-Behnken中心组合设计原理,对三因素二水平进行响应面分析,以包合率为指标进行筛选(表1)[5-6]。包合率计算公式如下:包合率(%)=包合物中的药量/加入的总药量×100。
1.3 沙拉沙星/β-环糊精包合物干燥工艺条件优化
1.3.1 单因素试验
分别以干燥度为指标,对进气温度(℃)和蠕动泵转速(r·min-1)进行单因素试验,观察不同进气温度(D)和不同蠕动泵转速(E)条件对干燥度的影响。干燥度计算公式如下:干燥度(%)=制剂中的水分质量/制剂的总质量×100%。
1.3.2 响应面试验
采用响应面模型Central-composite设计法对制备SAR/β-CD包合物微胶囊的喷雾干燥条件进行优化[11]。响应面法对喷雾干燥工艺的评价标准为:干燥度≤98%,0分;干燥度>98%,100分。蠕动泵的转速(r·min-1)和进口空气温度(℃)对材料的干燥度有显著影响。在单因素试验的基础上,采用响应面优化法设计正交试验因素和水平,如表2所示[7-9]。
1.4 液相色谱检测
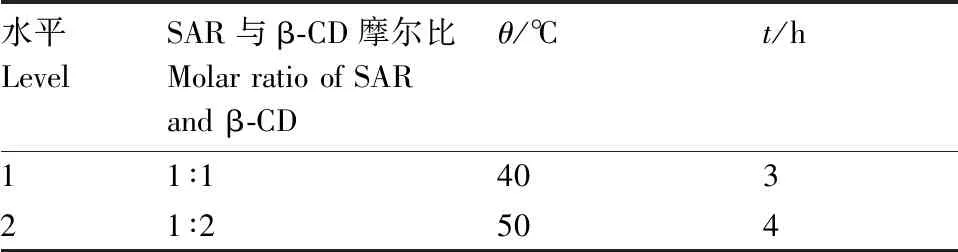
表1 包合物制备工艺正交试验因素和水平
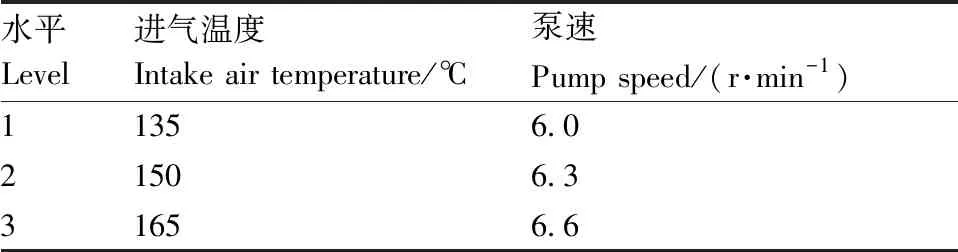
表2 喷雾干燥工艺正交试验因素和水平
1.4.1 色谱条件
称取9.94 mg沙拉沙星标准品于100 mL容量瓶中,加适量0.1 mol·L-1氢氧化钠溶解,配制成质量浓度为99.40 mg·L-1的标准储备液,4 ℃冷藏储存备用。使用前,用流动相逐级稀释成适当浓度的标准工作液。配制适当质量浓度的沙拉沙星标准品溶液,在紫外分光光度计200~800 nm范围内扫描,并在高效液相色谱仪上逐步验证。对比乙腈-磷酸水溶液体系和乙腈-2%四丁基溴化铵(13∶87,V/V)这2种流动相体系中的响应值、对称度等性能参数[12]。
1.4.2 线性范围与检测限、定量限
制备质量浓度分别为9.94、19.88、29.82、39.76、49.70、59.64、69.58、79.52、89.46、99.40 mg·L-1的梯度标准溶液,用于液相色谱检测。应用外标法以峰面积为纵坐标,沙拉沙星浓度为横坐标,绘制标准曲线。进样分析后计算信噪比,当信噪比=3(S/N≥3)时,该浓度为检测限(method detection limit,MDL),信噪比=10(S/N≥10)时,该浓度为定量限(limit of quantitation,LOQ)。
1.4.3 精密度与回收率试验
分别配制不同批次低(29.82 mg·L-1)、中(59.64 mg·L-1)、高(99.40 mg·L-1)浓度的沙拉沙星标准溶液,进行高效液相色谱检测,计算方法精密度。制备添加空白辅料的不同批次低(29.82 mg·L-1)、中(59.64 mg·L-1)、高(99.40 mg·L-1)浓度的沙拉沙星标准溶液,进行高效液相色谱检测,进行回收率试验。
1.4.4 SAR/β-CD包合物载药量测定
取适量的纯净水,加入准确称量的SAR/β-CD包合物,在25 ℃下振荡12 h达到平衡,过滤注入高效液相色谱仪进行检测,检测进行3次重复。SAR/β-CD包合物的载药量计算公式如下:载药量=(测得包合物中盐酸沙拉沙星的质量/包合物的总质量)×100%。
1.4.5 SAR/β-CD包合物溶解度测定
将过量的SAR/β-CD包合物和沙拉沙星原药分别加入超纯水中,在(25±2)℃下搅拌12 h,以达到稳定状态,过滤后注入高效液相色谱仪进行检测,检测进行3次重复[12-14]。
1.5 SAR/β-CD包合物干燥损失试验
参照《中华人民共和国兽药典》(2015版),称取SAR/β-CD包合物1.00 g左右,混合均匀,置于供试品相同条件下干燥至恒重的扁形称量瓶中,精密称定,在105 ℃干燥箱中干燥至恒重。由减失的质量和取样质量计算供试品的干燥损失。
1.6 高温稳定性试验
参照《中华人民共和国兽药典》(2015版),取供试品置于密封洁净容器中,在60 ℃条件下放置10 d,于第5天和第10天取样,检测制剂的有效物质相对标示量的含量、杂质量及有关物质量。若供试品发生显著变化(如含量下降5%),则在40 ℃下同法进行试验。
1.7 强光照稳定性试验
参照《中华人民共和国兽药典》(2015版),取供试品置于装有日光灯的光照箱中,将最小包装的产品单层排列,于(4 500±500)lx条件下放置10 d,在第5天和第10天取样检测,检测制剂的有效物质相对标示量的含量、杂质量及有关物质量。
1.8 高湿稳定性试验
参照《中华人民共和国兽药典》(2015版),取供试品置于恒湿密闭容器中,于25 ℃、相对湿度(90±5)%条件下放置10 d,于第5天和第10天取样进行检测。若供试品吸湿后质量增加5%以上,则应在25 ℃、相对湿度(75±5)%条件下进行试验。
1.9 生物稳定性试验
物理混合物和SAR/β-CD包合物在模拟胃液(25 ℃,pH=1.5)中溶解。每隔12 h采集样本,滤过后注入高效液相色谱仪测定[15-16]。每次试验3次重复。
2 结果与分析
2.1 包合试验参数的优选
用响应面模型建立过程模型的方差分析见表3。由表可知,该模型的P值为0.000 4,极显著(P<0.01),表明该模型回归显著。
响应面图可反映交互作用的影响程度,趋近于椭圆形表明显著[17]。通过Design-Expert软件分析得到最优试验参数为:β-环糊精与沙拉沙星摩尔比1.83∶1,搅拌温度47.84 ℃,搅拌时间3.76 h。经过多次验证试验表明,当β-环糊精与沙拉沙星摩尔比为2∶1,搅拌温度50 ℃,搅拌时间4 h时,包合率最大,能满足生产与应用需求。
2.2 干燥工艺条件优化
如图2所示,干燥工艺中,进风温度与干燥度成正比,蠕动泵转速与干燥度成反比。
用响应面模型建立的过程模型的方差分析见表4。由表4可知,该模型的P值为0.000 7,极显著(P<0.01),表明该模型回归显著。
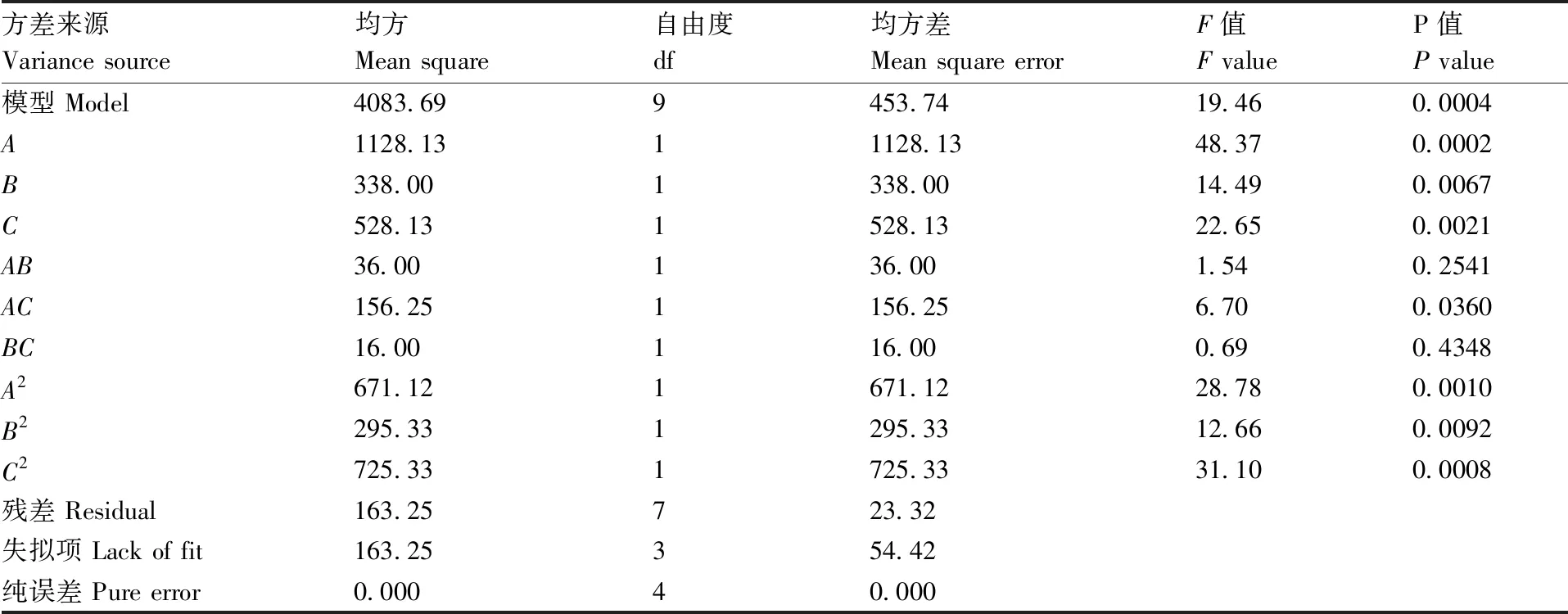
表3 回归模型的方差分析
通过Design-Expert软件分析得到最优试验参数为:进气温度约为162 ℃,蠕动泵转速约为6.3 r·min-1[17-18]。经过多次验证试验表明,进气温度为160 ℃、蠕动泵转速为6.3 r·min-1的条件下干燥的包合物具有良好的流动性,能满足生产与应用需求。
2.3 液相色谱检测
试验发现,沙拉沙星在280 nm时有明显的吸收峰,灵敏度与对称度良好。确定的色谱条件为:色谱柱Agilent ZORBAX SB-C18柱(4.6×150 mm),柱温30 ℃;流动相:乙腈-2%四丁基溴化铵(13∶87,V/V),检测波长280 nm,进样量5 μL。采用该液相色谱条件进行标准溶液检测。结果表明,沙拉沙星质量浓度在9.94~99.40 μg·mL-1范围内,线性关系优良,回归方程为Y=34.66X-15.867,相关系数(R2)为0.999 9。检测限为0.004 μg·mL-1(S/N≥3),定量限为0.066 μg·mL-1(S/N≥10)。
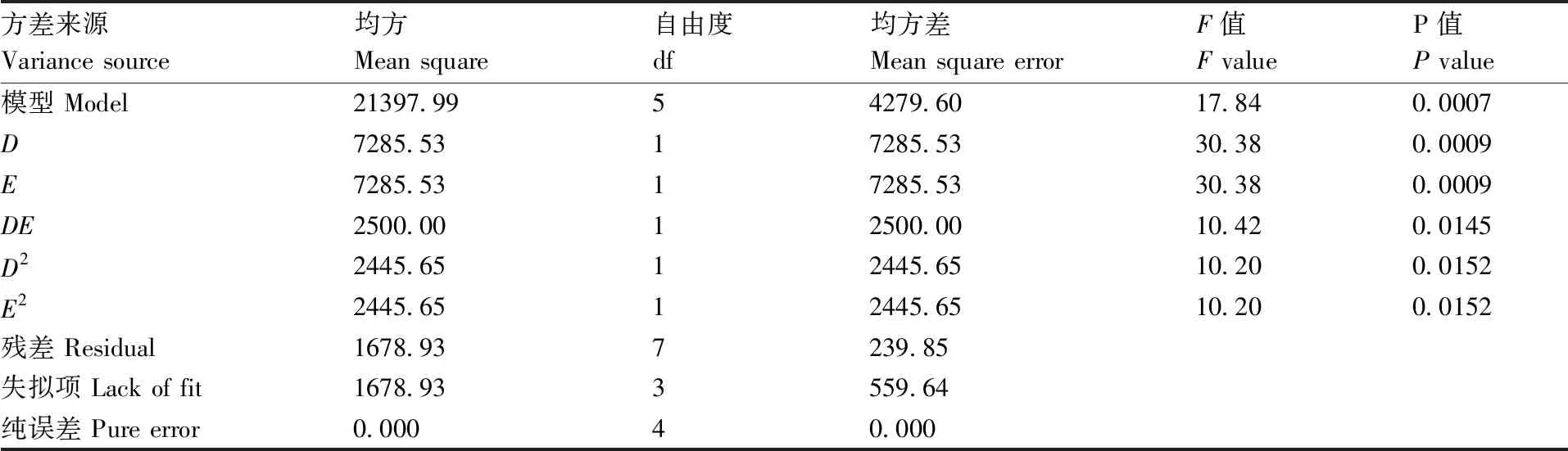
表4 回归模型的方差分析
精密度试验中,高浓度(89.46 μg·mL-1)沙拉沙星平均响应值为3 058 mAU*s,标准偏差2.50;中浓度(59.64 μg·mL-1)的平均响应值为2 046 mAU*s,标准偏差13.44;低浓度(29.82 μg·mL-1)的平均响应值为1 035 mAU*s,标准偏差1.70。高浓度(89.46 μg·mL-1)的回收率平均值为100.21%,RSD 0.15%;中浓度(59.64μg·mL-1)的回收率平均值为99.17%,RSD 0.04%;低浓度(29.82 μg·mL-1)的回收率平均值为101.67%,RSD 0.15%。
2.4 SAR/β-CD包合物干燥损失试验结果
如表5所示,在筛选出的喷雾干燥工艺参数下制备的沙拉沙星包合物含水量小于2%,符合规定。
2.5 SAR/β-CD包合物载药量及溶解度
如表6所示,3批次沙拉沙星包合物制剂载药量的平均值90.33%;平均溶解度为14.69 mg·mL-1。
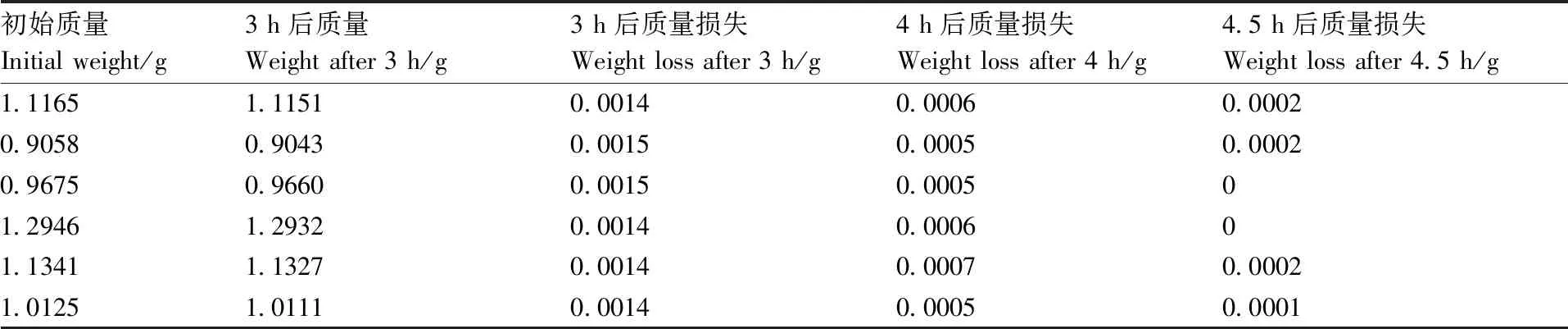
表5 干燥质量损失试验结果
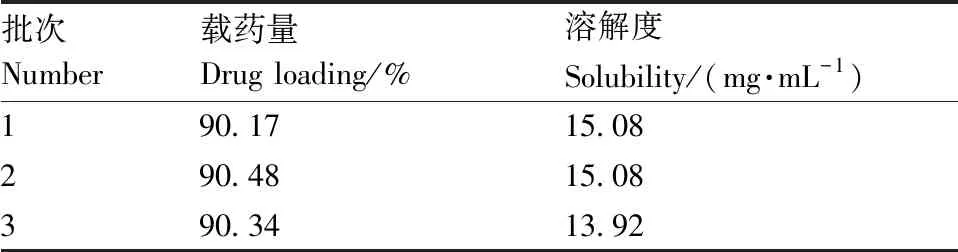
表6 载药量及溶解度
2.6 高温稳定性试验结果
如表7所示,SAR/β-CD包合物在60 ℃下保存5 d和10 d后,单一杂质含量小于0.5%,总杂质量与有关物质量均小于1%。
2.7 强光照稳定性试验结果
如表8所示,在强光照条件下暴露5 d和10 d后,单一杂质含量小于0.5%,总杂质量与有关物质量均小于1%。

表7 SAR/β-CD包合物高温稳定性试验

表8 SAR/β-CD包合物强光照稳定性试验
2.8 高湿稳定性试验结果
如表9所示,SAR/β-CD包合物在25 ℃、相对湿度(90±5)%时吸湿率大于5%。在25 ℃和相对湿度(75±5)%时,SAR/β-CD包合物的吸湿率和增重率均小于5%。3批药物的单杂质含量、总杂质含量和有关物质含量均小于1%。
2.9 生物稳定性试验结果
在pH 1.5的溶液中,初始48 h内,物理混合物和SAR/β-CD包合物中的沙拉沙星浓度减少量相似。但是,从48 h到120 h,SAR/β-CD包合物的沙拉沙星浓度下降幅度明显小于物理混合物的浓度。120 h时,物理混合液中游离沙拉沙星的浓度下降了46%,而SAR/β-CD包合物中的沙拉沙星浓度仅下降了17%。
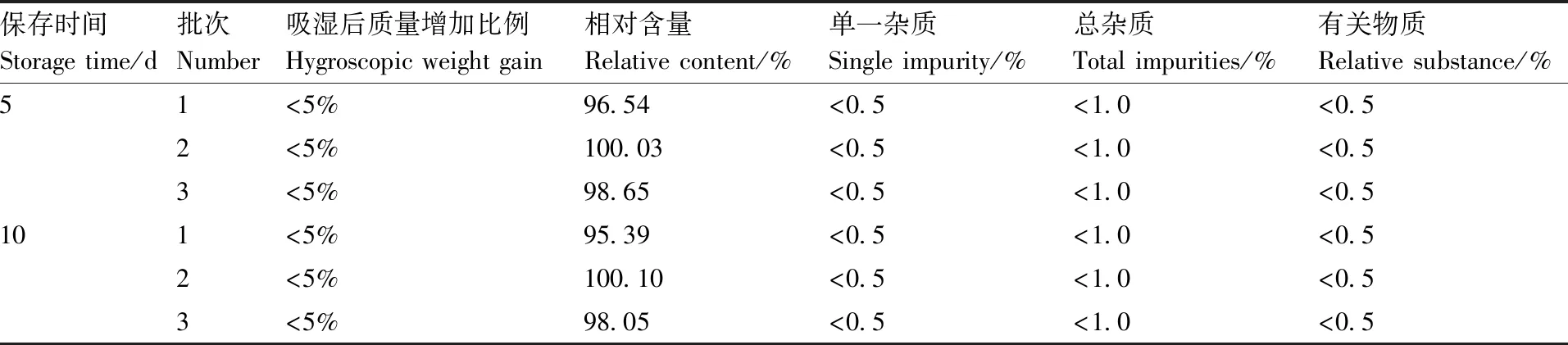
表9 SAR/β-CD包合物高湿稳定性试验
3 讨论
饱和水溶液法制备沙拉沙星/β-环糊精包合物,其工艺过程简单、高效,相对于超声法具有成本低廉,易于实现工业化生产的特点。研究中以包合率为评分指标,应用响应面法对包合工艺进行优化并完成了多次验证试验,最终筛选出最优的物料处方配比和制备工艺为:搅拌温度50 ℃,搅拌时间4 h,沙拉沙星与β-环糊精摩尔比为1∶2,包合过程对环境友好,无有害物质产生。相对于冷冻干燥法速度慢、成本高,而喷雾干燥法具有生产效率高,产品特性恒定,全程自动可控,适合大规模生产的优点。本研究应用响应面法对喷雾干燥工艺进行优化并完成了多次验证试验,以干燥度为评价指标,筛选出喷雾干燥工艺的试验参数为进气口温度160 ℃,泵速6.3 r·min-1,获得的沙拉沙星/β-环糊精包合物制剂含水量较低,流动性好,便于运输和储存。本研究使用高效液相色谱法测定沙拉沙星包合物制剂的载药量与溶解度,经验证,测定沙拉沙星包合物含量的高效液相色谱方法学研究数据良好,3种质量控制浓度的回收率平均值都大于90%且小于110%,满足试验要求。用此种方法检测的3批次沙拉沙星包合物制剂平均溶解度为14.69 mg·mL-1,表明包合物制剂性质优良,满足实际需求[12,14]。通过对此种新型制剂的稳定性试验,结果表明,沙拉沙星/β-环糊精包合物在60 ℃高温或高湿度或强光照条件下放置10 d后,供试品各检测项未发生显著变化,证明3个批次药物的各检测项均符合规定。在模拟胃酸溶液的生物稳定性实验中,沙拉沙星包合物制剂的稳定性同样明显高于未进行过包合作用的简单物理混合物,说明制成包合物新制剂后沙拉沙星的光不稳定性得到改善[16,19]。
沙拉沙星是由美国雅培公司研制的动物专用的第三代氟喹诺酮类抗菌药物,对多数革兰氏阴性菌、革兰氏阳性菌及霉形体均表现出良好的抗菌作用。在市场上具有广阔的应用前景,临床推广潜力巨大。但是,市售的药物主要是沙拉沙星普通粉剂,这种剂型对提高原料药溶解度的效果不明显,仍然有理化性质不稳定,遇光颜色变深,甚至发生强光下部分药物分解的现象。此次研究通过响应面法优化沙拉沙星/β-环糊精包合物的制备工艺,建立的响应面法模型具有显著性,成功得到了沙拉沙星包合物新剂型,其制备工艺过程简单高效、成本低廉,且符合环保要求,弥补了原有的缺点,既提高了药物的溶解度,又达到了大幅度提高药物稳定性的目的,证明了此种包合物新剂型的优势,对生产实践具有重要的指导意义。

