油茶壳热解反应动力学和热力学研究
周园芳,欧阳少波 ,熊道陵,张彩霞,薛茹萍,王 君
(1.江西理工大学材料冶金化学学部,江西 赣州 341000;2.商洛学院化学工程与现代材料学院,陕西 商洛 726000)
0 引 言
随着化石能源的不断消耗,寻找新的可再生替代能源尤为迫切[1]。与太阳能、风能、水力发电及地热能等其他可再生能源相比,生物质在满足世界能源需求中占比最大[2]。在农业生产过程中,会产生大量的农林废弃物,可作为生物能源利用。生物质作为能源,在世界范围内具有巨大的潜力,其不仅仅是1种可再生能源,同时也可以有效减少环境污染的问题[3]。油茶是我国1种特有的典型经济农作物,主要分布在浙江、江西、湖南等地,种植面积达3.5×106hm2,年产油茶果560多万t[4]。油茶壳是油茶果生产茶油的副产物,约占整个茶果鲜重的50%~60%,其资源量十分丰富[5]。一般油茶壳作为农林废弃物直接焚烧或丢弃处理,不仅浪费资源,同时也会释放大量的污染物导致环境污染问题。因此,如何有效地安全处理油茶壳,将其转化为生物燃料回收能源,对于实现油茶壳资源化利用具有重要意义。
目前,生物质制备生物燃料主要通过热化学转化技术实现,包括热解、气化和燃烧等技术[6],其中,热解技术是生物质资源化利用最具有前景的技术之一[7]。通过热解过程,生物质可转化为合成气、生物燃油和半焦等产物[8]。合成气和生物燃油,其热值较高,可作为能量回收利用,生物燃油也可进一步提炼转化为发动机燃料,替代汽油、柴油,或其他化学物质[9]。半焦可制备碳材料[10]、电容器[11]、燃料电池[12]等。热解过程较为复杂,涉及脱水、解聚、裂解、重整、再聚合、缩合及碳化等反应。目前研究人员已对木屑、秸秆、玉米棒、橄榄仁、椰壳等热解过程进行了相关研究[13-17]。对油茶壳热解特性相关的研究相对较少,张党权等[4]利用Py-GC/MS联机技术,对新鲜油茶壳在590 ℃热解温度,He气氛下的热解液体产物进行GC/MS分析,结果发现热解产物中含有名贵生物医药、名贵香料成分等46种化合物。许细薇等[18]以云南腾冲红花油茶壳为原料,利用热重对油茶壳热解特性进行分析,并采用Ozawa法和Friedman法对其热解动力学进行探讨,发现随着热解转化率的增加,活化能分别在(139~270) kJ/mol和(151~302) kJ/mol,但未涉及热解过程中的热力学。在笔者前期工作中,探讨了油茶壳与低阶煤共热解特性,根据动力学分析发现共热解过程存在协同效应,根据一级Arrhenius定律,采用Coats-Redfern(CR)法拟合计算,油茶壳在热解温度225 ℃~350 ℃之间时,对应活化能为(37.37~44.08) kJ/mol[19]。
为更进一步探讨油茶壳热解过程的动力学和热力学,以下选择江西赣南地区所产油茶壳为原料进行相应试验,利用热重分析技术(TGA)对其热解特性进行详细研究,并采用3种不同动力学模型对其热解动力学和热力学进行探讨,为油茶壳热化学转化过程提供理论基础。
1 实验部分
1.1 实验原料
选取江西赣南地区所产油茶壳为实验原料,由赣州某油茶公司提供的油茶壳经浸泡洗涤后,在120 ℃烘干12 h,之后利用粉碎机破碎至150 μm以下。其工业分析和元素分析结果见表1。
由表1中的分析结果可以看出,油茶壳中挥发分较高,其值为65.47%;元素分析结果中O含量较高,其值为44.56%;导致高位热值较低,仅为17.62 kJ/g[19]。

表1 油茶壳工业分析及元素分析Table 1 Proximate and ultimate analyses of camellia oleifera shell
1.2 实验仪器
实验所用的主要仪器设备及辅助仪表等见表2。其中,工业分析按GB/T 212—2008进行检测,主要涉及的设备为马弗炉和烘箱,元素分析由元素分析仪测定;热重分析仪主要对油茶壳热失重进行分析,全自动量热仪用于油茶壳热值测定。
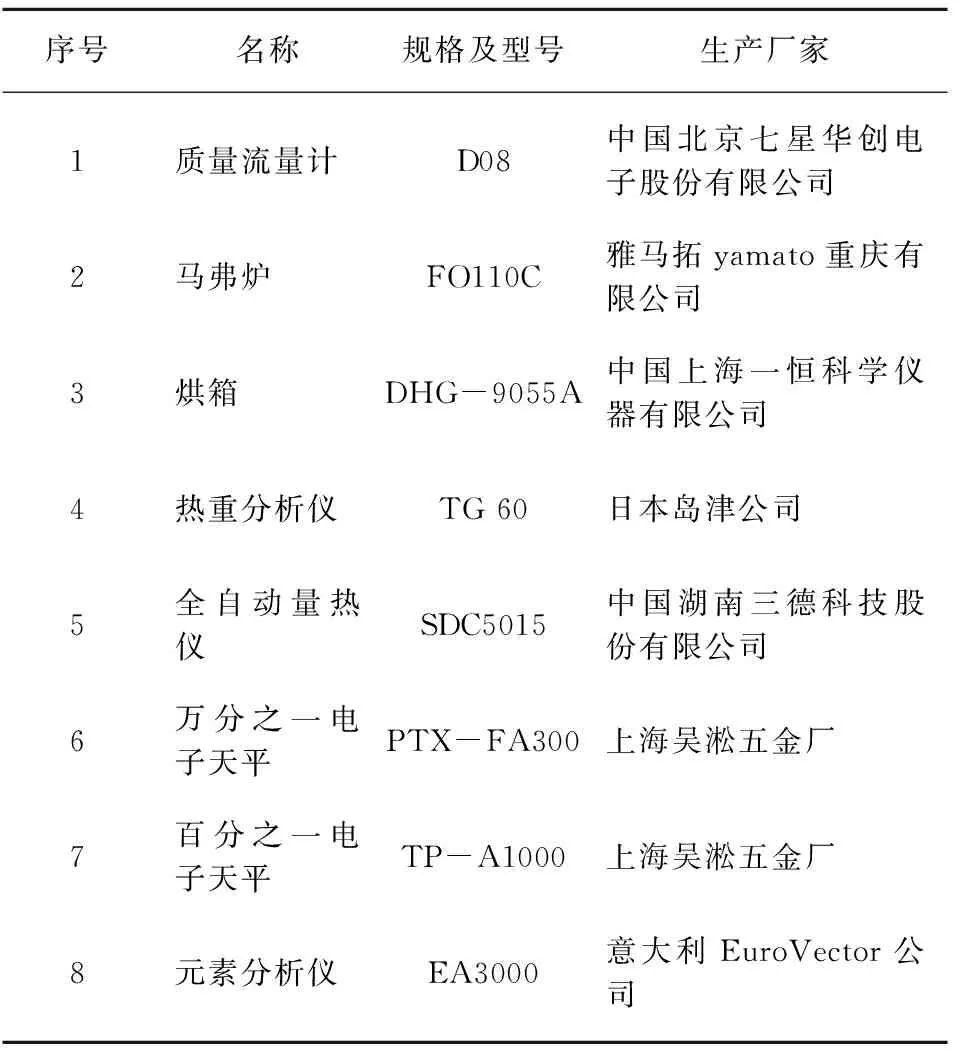
表2 研究油茶壳热化学转化所用的实验仪器及设备Table 2 Experimental apparatus and equipments for thermochemical conversion of camellia oleifera shell
1.3 热重分析实验
采用TG 60系列差热—热重同步分析仪对油茶壳样品进行热重分析,测定样品重量随温度的变化,记录样品质量和温度值并绘制热重(TG)曲线,热重曲线对温度或时间的一阶导数即微商热重(DTG),由此绘制的微商热重值和温度或时间的曲线称为微商热重(DTG)曲线[20-21]。
取处理后的油茶壳约10 mg样品放入Al2O3坩埚中,称重后放入加热炉中吊盘内。采用氮气作为载气,使热分解在无氧状态下进行,并利用流量控制计保持氮气气氛流量为75 mL/min。设定热重分析仪终温为800 ℃,加热速度分别为5 ℃/min、10 ℃/min、15 ℃/min和20 ℃/min。
1.4 动力学模型
假设热解过程中的各种反应为同时且独立进行,根据质量作用定律,生物质热解反应动力学方程详见式(1):
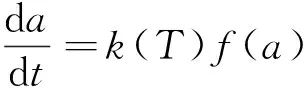
(1)
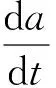
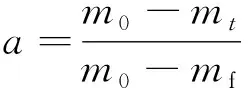
(2)
其中,m0、mt和mf分别表示固体起始时候、在t时刻和反应最终时候的质量。
根据Arrhenius方程,反应速率常数k可表示为式(3)的形式:
k=Ae(-Ea/RT)
(3)
其中,A指前因子(frequency factor),Ea为反应活化能,R为普遍化气体常数,T为温度。
根据式(1)和(3),可得到:
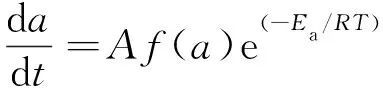
(4)
其中,f(a)是转化率的函数,其表达式见式(5)[22-23]:
f(a)=(1-a)n
(5)
在非等温条件下,温度T与时间t关系式如式(6):
T=T0+βt
(6)
其中,T0为起始温度,β为升温速率。
由此反应速率可以表达成式(7),即采用转化率对温度求导。
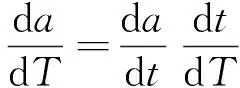
(7)
由式(6)可得到式(8):
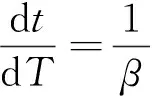
(8)
其中,da/dT是非等温过程反应速率,da/dt是等温过程反应速率。
将式(4)和式(8)代入式(7),可得式(9)的反应速率表达形式:
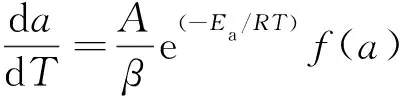
(9)
对式(9)分离变量,并积分可得式(10):
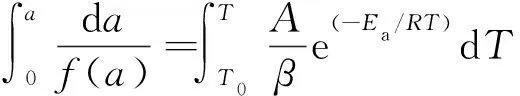
(10)
一般情况下,在低温条件的反应速率较低,因此式(10)可以近似为式(11)[23]:
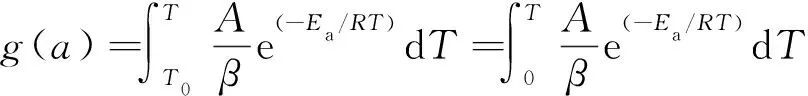
(11)
在式(11)右侧可根据Doyle近似而引入式p(u)[24],可得式(12):
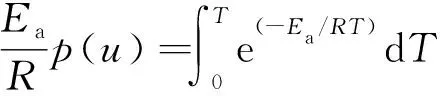
(12)
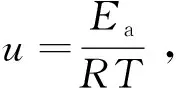
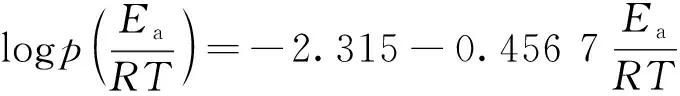
(13)
将式(12)代入式(11),可得式(14):
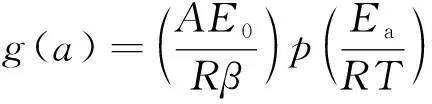
(14)
对式(14)求对数形式,可得式(15):

(15)
并将式(13)代入(15),可得Ozawa-Flynn-Wall(OFW)模型,其表达式为式(16)或(17):

(17)
由此可知,根据OFW模型,通过lnβ或logβ对1/T作图,根据斜率可求出活化能(Ea),再利用活化能(Ea)和截距即可求出指前因子(A)[25]。
对式(4)两侧取自然对数,可得式(18),即为Friedman(FM)模型。

(18)
根据FM模型,通过ln[da/dt] 对1/T作图,根据斜率可以求出活化能Ea,利用截距即可求出指前因子A[26]。
对于Kissinger-Akahira-Sunose(KAS)模型,其表达式如式(19)所示:

(19)
根据式(19),通过ln[β/T2] 对1/T作图,根据斜率可以求出活化能(Ea),利用活化能(Ea)和截距即可求出指前因子(A)[27]。
针对此次试验过程,假设热解反应级数n=1,则f(a)=1-a和g(a)=-ln(1-a),后续数据处理过程全部按一级动力学进行模拟分析。
1.5 热力学函数计算
根据OFW模型等转化率法[22],利用活化能(Ea)计算指前因子(A)、焓变(ΔH)、吉布斯自由能变(ΔG)和熵变(ΔS)等热力学参数。指前因子(A)、焓变(ΔH)、吉布斯自由能变(ΔG)和熵变(ΔS)的数学表达式分别见式(20)、(21)、(22)和(23)[7,28]。

(20)
ΔH=Ea-RTa
(21)

(23)
其中,KB为玻尔兹曼常数(1.381×10-23J/K),h为普朗克常数(6.626×10-34J·s),Tm为DTG曲线峰值温度,Ta为转化率a时对应的温度。
2 结果与讨论
2.1 热失重曲线分析
在不同升温速率5 ℃/min、10 ℃/min、15 ℃/min和20 ℃/min下,油茶壳热失重曲线如图1所示,其中TG为失重曲线,DTG为失重率曲线。
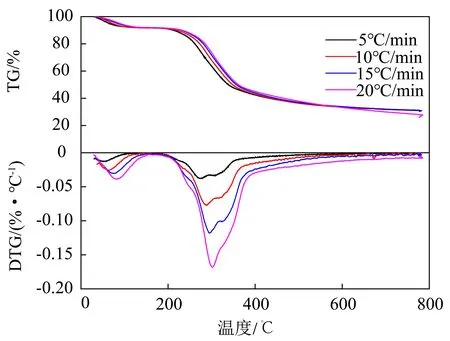
图1 不同升温速率下油茶壳热解TG/DTG曲线Fig.1 TG/DTG diagram of camellia oleifera shell at different heating rates
从图1中可看出,油茶壳热失重过程主要发生在200 ℃~500 ℃之间,当温度达到500 ℃时其失重率在65%左右,同样,失重率随升温速率增加稍有降低。在热失重区间,从DTG曲线可观察到4个失重峰,在0~150 ℃的失重峰为脱水失重峰,该过程主要是物理过程。一般对于生物质而言,主要由纤维素、半纤维素和木质素构成,由于三者的结构差异,其热解特性会有所区别,油茶壳热解过程与其他生物质具有相同的失重特性曲线[17,29-30],随着温度的升高,半纤维素、纤维素和木质素会逐渐裂解。其中,在200 ℃~320 ℃有2个失重峰,对应于半纤维素的热解;320~400 ℃失重峰为纤维素的特征峰,对于木质素,其热解峰不明显,热解温度跨越范围很广,700 ℃以后也能观察到木质素的分解,但分解量较少[30]。对比不同升温速率对应的TG和DTG曲线,升温速率的变化不会改变热分解模式,但会影响热解温度范围和热失重速率。同时,升温速率的增加会导致TG曲线会向高温方向偏移,尤其DTG曲线中最高失重峰值对应温度明显向右偏移,导致在相同失重率的情况下,需要更高的热解温度。通常将该种现象称为热滞后现象,在其他文献综述也存在相同的现象[11-14]。升温速率对热分解过程主要有以下2个方面的影响:①升温速率增加,达到热解温度时间缩短,但挥发份的停留时间不足,为了达到充分热分解需要更高的温度;②升温速率过高会导致原料颗粒内外的温度梯度增加,降低热分解过程传热效率。
2.2 热解过程动力学分析
利用KSA模型、OFW模型和FM模型该3种不同动力学模型对热重曲线进行分析研究,150 ℃之前主要为干燥失水物理过程,因此不在此进行讨论,而主要关注200 ℃~500 ℃的热解过程,对其热重曲线进行拟合计算,线性拟合结果如图2所示,拟合动力学参数列于表3。结合图2和表3的数据可知,KSA模型拟合结果中活化能(Ea)在123.75~180.99 kJ/mol,且随着转化率的增加,整体呈逐渐增加的趋势,平均活化能为151.17 kJ/mol,指前因子(A)在1.42×1011~1.42×1014min-1范围内,相关系数在0.963~0.998;利用OFW模型拟合,其活化能(Ea)在125.88 kJ/mol~182.24 kJ/mol之间,变化趋势也与KSA模型活化能趋势一致,平均活化能为152.83 kJ/mol,与KSA模型计算结果基本相同,指前因子(A)在2.62×1011min-1~1.94×1014min-1范围内,整体结果比KSA模型结果偏大,相关系数在0.967~0.998;通过FM模型对油茶壳热失重曲线拟合结果,分析可知,活化能(Ea)在128.20~191.50 kJ/mol,平均活化能为162.68 kJ/mol,相较KSA模型和OFW模型拟合结果稍有偏高,而随转化率的增加,活化能变化趋势与KSA模型、OFW模型相一致,相关系数在0.955~0.997。笔者主持的此次研究工作结果与其他文献中油茶壳热解动力学参数结果对比见表4,对于不同模型所得结果存在一定的差异,不同产地的原料热解特性并不相同。
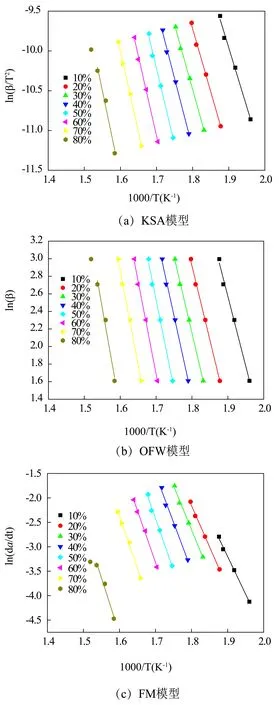
图2 KSA模型、OFW模型和FM模型的拟合动力学曲线Fig.2 KAS ,OFW and FM plots from the degradation of camellia oleifera shell at different conversions
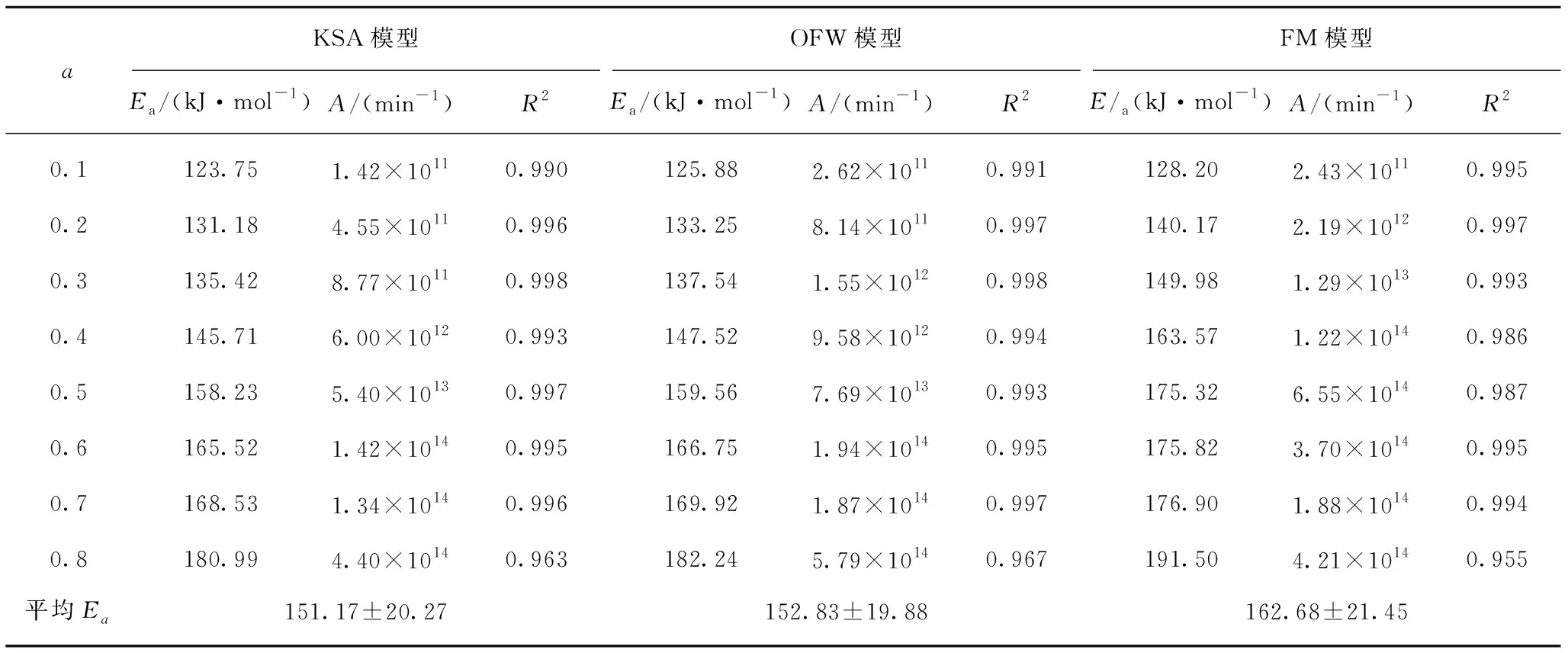
表3 KSA模型、OFW模型和FM模型拟合动力学参数结果Table 3 Kinetic parameters calculated at different conversions from decomposition of camellia oleifera shell using various models

表4 其他文献中油茶壳热解动力学参数Table 4 A comparative study showing kinetic parameters calculated in this work with reported studies
通过表3可见3种模型对应的活化能随转化率变化情况,活化能变化趋势基本相同,随转化率增加,活化能呈不断增加趋势,说明随转化率增加,生成的固体产物反应活性对温度越敏感,而初始活化能较低,主要是由于生物质热解初始时,半纤维素中存在大量的弱键—支链羰基和羧基,容易发生断裂;随转化率增加,主要是木质素热分解和半焦的碳化,其中强键的断裂,需要消耗更多的能量,表现为更高的活化能[31]。同时,也可知FM模型结果较其他两模型结果偏高,通过分析3种模型的计算原理,可以容易理解造成该现象的原因,KSA模型和OFW模型存在一些假设和近似,而FM模型不存在假设与近似[32]。由此,FM模型计算结果更为精确,更接近热解过程中的实际活化能。
2.3 热解过程热力学分析
利用OFW模型对不同升温速率下热解过程热力学状态函数进行分析,结合热解动力学所得表观活化能(Ea),分别计算热力学状态函数A、ΔH、ΔG和 ΔS,计算结果列于表5。
根据Eyring过渡态理论,结合公式(20)可以计算指前因子(A)的数值,在对表面积的影响进行修正后,在阿伦尼乌斯方程中,固相反应的指前因子A的取值范围很广,可达106s-1或107s-1。对于典型的准一级反应指前因子,其值在104s-1~1018s-1[33]。当指前因子在102~104s-1之间时为吸附过程控制,在107~1011s-1时为扩散过程控制,在1010~1013s-1时为表面反应控制,1013~1016s-1之间为脱附过程控制[34]。由表4中的结果计算所得的指前因子在108s-1~1016s-1之间,随转化率增加,在此范围内需经历扩散过程、表面反应和脱附过程等控制步骤。
焓变(ΔH)是反应产物和反应物间的能量差,其变化趋势与表观活化能相一致。从表5可见,ΔH值随着转化率的增加而不断增加,可升至120 kJ/mol~180 kJ/mol。ΔH为正值,说明热解过程为吸热反应,随着反应的进行则需消耗更多的热量。在等转化率的情况下,随着升温速率的增加则其焓变值稍有降低,但变化不明显,因此,在升温速率5 ℃/min~20 ℃/min的条件下,不会明显改变热解过程的热效应。
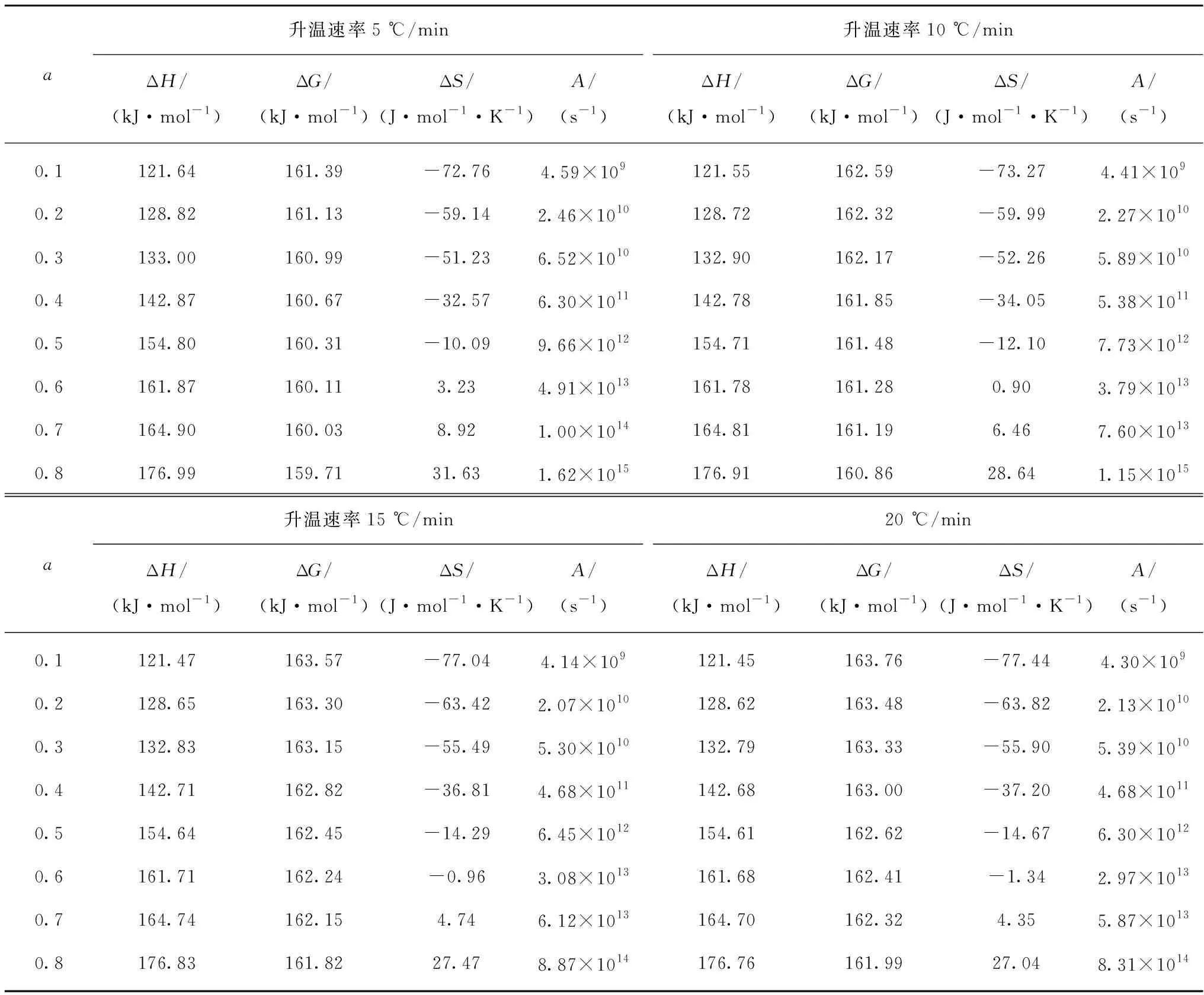
表5 OFW模型对应不同升温速率下油茶壳热解过程热力学状态函数Table 5 Thermodynamic parameters during the pyrolysis process of camellia oleifera shell at different heating rates using OFW model
吉布斯自由能变(ΔG)显示了反应物消耗和产物生成过程中体系总能量增加。在热解过程中,ΔG变化并不明显,随反应的进行稍有降低,对应于升温速率5 ℃/min、10 ℃/min、15 ℃/min和20 ℃/min时,ΔG分别由161.39 kJ/mol降至159.71 kJ/mol、162.59 kJ/mol降至160.86 kJ/mol、163.57 kJ/mol降至161.82 kJ/mol和163.76 kJ/mol降至161.99 kJ/mol,相同的参数对应于稻秸秆为164.59 kJ/mol、米糠为167.17 kJ/mol和鸡粪175.29 kJ/mol[7]。在等转化率的情况下,升温速率的增加,ΔG不断增加,说明反应更难进行,需要升高温度使反应发生,与热重曲线结果相一致;等转化率时,升温速率越快,所需温度越高,主要是由于升温速率升高,易在颗粒表面和内部形成温度梯度,颗粒内部反应需要更高的温度。
熵变(ΔS)是体系微观状态混乱程度的度量,低熵值意味着材料经过某种物理或化学处理过程后,使其达到接近自身热力学平衡的状态,该情况下的材料反应活性较低,需增加反应时间;而高熵值表明材料远离其自身热力学平衡的状态,反应活性较高,反应速率较快[33]。从表5中可知,ΔS随着转化率的增加,由负值逐渐增加变成正值。ΔS为负值说明与反应物相比,键解离生成的产物微观结构混乱度降低;ΔS为正值,说明产物微观结构的混乱程度增加[7]。从结果分析,热解过程熵变随转化率的增加,热解体系逐渐从有序度增加向混乱程度增加方向转变,使产物向熵增方向进行,体系达到更加稳定的状态,与热解半焦的无定型石墨化结构相一致。在升温速率5 ℃/min和10 ℃/min时,ΔS变化趋势相同,转化率为0.6时,变为正值;升温速率15 ℃/min和20 ℃/min时,对应的ΔS变化趋势相同,转化率为0.7时,变为正值。在等转化率下,熵变随加热速率增加呈不断降低趋势,说明产物的混乱程度降低,可能是由于转化率相同的条件下,加热速率增加对应的处理温度升高,使产物的石墨微晶结构更加有序。
3 结 论
利用热重分析技术,通过改变升温速率以探讨油茶壳的热解特性,分析油茶壳热解过程反应动力学和热力学特性,得出以下相关结论:
(1)油茶壳热解过程主要包括脱水、半纤维素、纤维素和木质素热解等过程,随着升温速率的增加,热失重曲线存在明显的滞后现象,等转化率情况下的热解温度偏高,同时失重峰的峰值温度向高温偏移。
(2)利用KSA模型、OFW模型和FM模型对油茶壳热解动力学进行分析,3种模型计算得到表观活化能分别在123.75 kJ/mol~180.99 kJ/mol、125.88 kJ/mol~182.24 kJ/mol和128.20~191.50 kJ/mol,且活化能随转化率的增加而不断增大。KSA模型和OFW模型计算结果基本相同,FM模型计算结果要高于前两者的计算结果。
(3)利用OFW模型对热力学函数进行分析,指前因子(A)、ΔH和ΔS分别在108s-1~1016s-1、120 kJ/mol~180 kJ/mol、(-78~32)J/(mol·K)之间,随转化率的增加,三者均呈不断增加的趋势;在等转化率的情况下,与升温速率呈正相关性;ΔG在159 kJ/mol~164 kJ/mol,相同升温速率下ΔG随转化率的增加稍有降低,但不明显;而在等转化率的情况下,随着升温速率的增加则ΔG也随之增加。

