冠状动脉CT血管成像联合基于CT的血流储备分数预测阻塞性冠心病主要不良心脏事件的价值
庞智英 杨飞 苏亚英 刘峰 汤林梦 崔书君
1河北北方学院研究生院(河北张家口 075000);2河北北方学院附属第一医院放射科(河北张家口 075000)
冠状动脉粥样硬化性心脏病(coronary artery disease,CAD)已成为严重威胁人类生命健康的心血管疾病之一,容易并发多种不良心脏事件,因此寻求一种经济、有效的CAD 早期筛查手段,及时进行临床干预和管理,备受业内人士关注。冠脉CT 血管成像(coronary CT angiography,CCTA)作为诊断CAD 最常用的无创影像技术,仅可单纯评估冠脉狭窄程度,并不能准确反映冠脉血流动力学的改变。目前基于CT 的血流储备分数(CT derived fractional flow reserve,CT-FFR)作为一种可同时提供冠脉形态学和功能学信息的无创CT 心脏功能学成像技术,可准确评估冠脉狭窄引起的血流动力学改变[1],近年来逐渐用于指导CAD 患者的诊疗策略和血运重建的实施及评估患者预后,已成为临床研究的新热点[2]。本研究旨在探讨CT-FFR、冠脉狭窄程度、临床心血管危险因素及三者联合应用对阻塞性CAD 患者发生主要不良心脏事件(major adverse cardiac events,MACE)的评估、预测价值,从而为CAD 患者干预管理及预防MACE 提供一种无创、有效的评估方法。
1 资料与方法
1.1 研究对象收集从2017年1月至2018年6月于河北北方学院附属第一医院行CCTA 检查且结果显示为一支或多支冠脉中重度狭窄(50%~90%)的阻塞性CAD 患者133 例,其中男105 例,女28 例。阻塞性CAD 定义为冠脉狭窄≥50%。排除标准:临床怀疑急性冠状动脉综合征的患者;先前行经皮冠状动脉介入治疗(PCI)或冠状动脉旁路移植术(CABG)的患者;CCTA 图像存在严重钙化、伪影及噪声;CT-FFR 分析失败。
1.2 临床心血管危险因素收集包括年龄、性别、高血脂症病史、糖尿病史、高血压史、心血管疾病家族史、吸烟史、左心室射血分数(left ventricular ejection fraction,LVEF)、体质量指数(body mass index,BMI)。
1.3 CCTA 扫描方案与图像分析采用佳能320排动态容积CT(Aquilion One)进行扫描。扫描前应用双筒高压注射器,以速率为5.5 mL/s 注射等渗对比剂碘克沙醇(320 mgI/mL),随即立即以相同速率注入0.9%氯化钠溶液30 mL。扫描参数:管电压100 kV;管电流为自动毫安。监测设定在降主动脉中央层面,采用SureStart 软件自动触发扫描,触发域值为280 HU。选取冠脉血管显示最清楚的时相进行重建。由本科室两位有经验的影像诊断医师对CCTA 图像进行分析,观察最狭窄冠脉分支并测定其狭窄程度。若血管分支同时存在中度狭窄(≥50%且<70%)及重度狭窄(≥70%且<90%),则定义该患者的冠脉狭窄程度为重度狭窄。
1.4 CT-FFR 分析使用基于深度学习的软件深脉分数进行CT-FFR 分析,将患者的CCTA 图像上传至科亚医疗有限公司的影像平台,软件会自动计算各支冠状动脉血管的CT-FFR 值,测量位置选取在斑块远端2~3 cm 的位置。本研究依据多项CT-FFR 相关临床研究结果[3-4],将其临界值设为0.80。若存在多支病变时,只要有一支血管病变的无创CT-FFR 为阳性,则代表该患者为阳性病例。
1.5 研究终点及随访通过病历系统查阅、电话等方式对患者进行随访。以CCTA 检查日期作为随访起点,以MACE 作为终点,MACE 主要包括心源性死亡、非致死性心肌梗死、因不稳定心绞痛住院及接受靶血管血运重建。根据是否发生MACE将患者分为MACE 组和非MACE 组
1.6 统计学方法使用SPSS 25.0 和MedCalc 15.0统计学分析软件。计量资料符合正态分布时比较用独立样本t检验;不符合时则用Mann-WhitneyU检验。计数资料比较采用χ2检验。采用Kaplan-Miere 法绘制生存曲线并通过Log-rank 检验进行分析。应用Cox 生存回归模型分析MACE 的独立危险因素,建立3 个预测MACE 的模型:模型1(CT-FFR)、模型2(CT-FFR 联合冠脉狭窄程度)、模型3(CT-FFR 联合冠脉狭窄程度和临床心血管危险因素)。通过ROC曲线下面积(AUC)计算3个预测模型对MACE 的预测效能。P<0.05 为差异有统计学意义。
2 结果
2.1 两组间临床资料的比较本研究最终随访133 例患者,平均年龄为(61.4 ± 8.5)岁,其中男性占76.7%。中位随访时间为44(32,48)个月,发生MACE 者31 例,其中心源性死亡1 例,非致死性心肌梗死3 例,因不稳定心绞痛住院4 例,接受靶血管血运重建23 例。与非MACE 组相比,MACE 组患者的糖尿病发生率更高、左心室射血分数降低(P<0.05),两组间其他指标差异无统计学意义(P>0.05)。见表1。
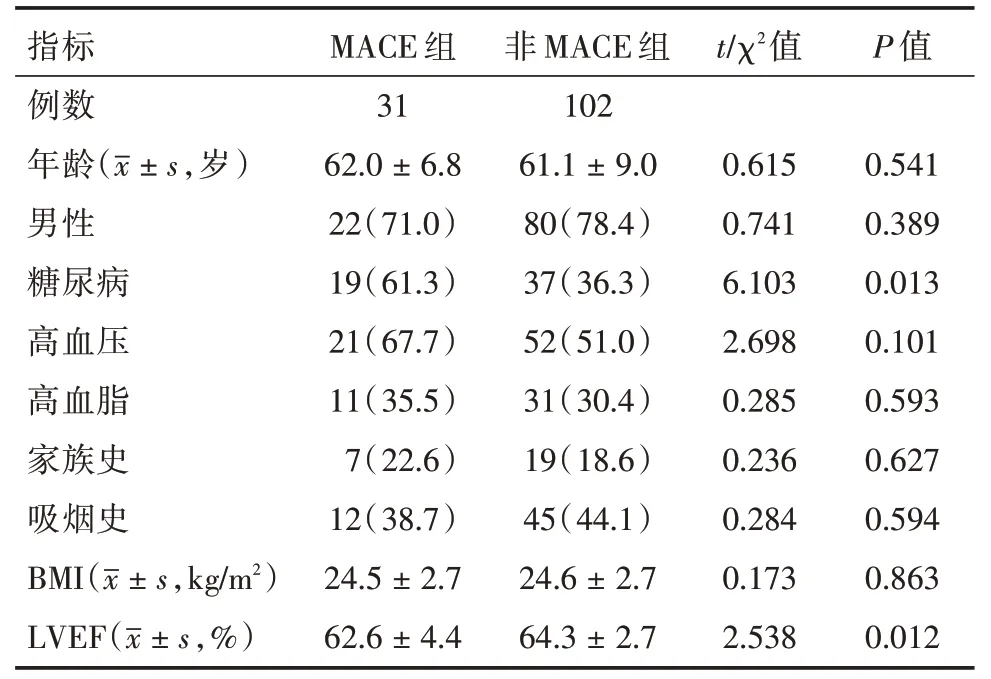
表1 两组间临床资料的比较Tab.1 Comparison of clinical data between the two groups例(%)
2.2 两组间冠脉基线资料的比较与非MACE 组相比,MACE组冠脉狭窄程度更重、CT-FFR值≤0.80所占比例更高(基于患者和血管水平),差异有统计学意义(P<0.05),见表2。CCTA和CT-FFR 图像见图1。
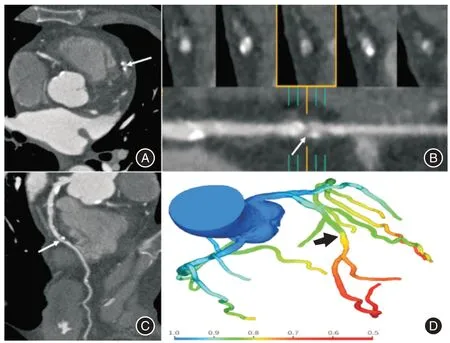
图1 CCTA 及CT-FFR 示意图Fig.1 Schematic diagram of CCTA and CT-FFR
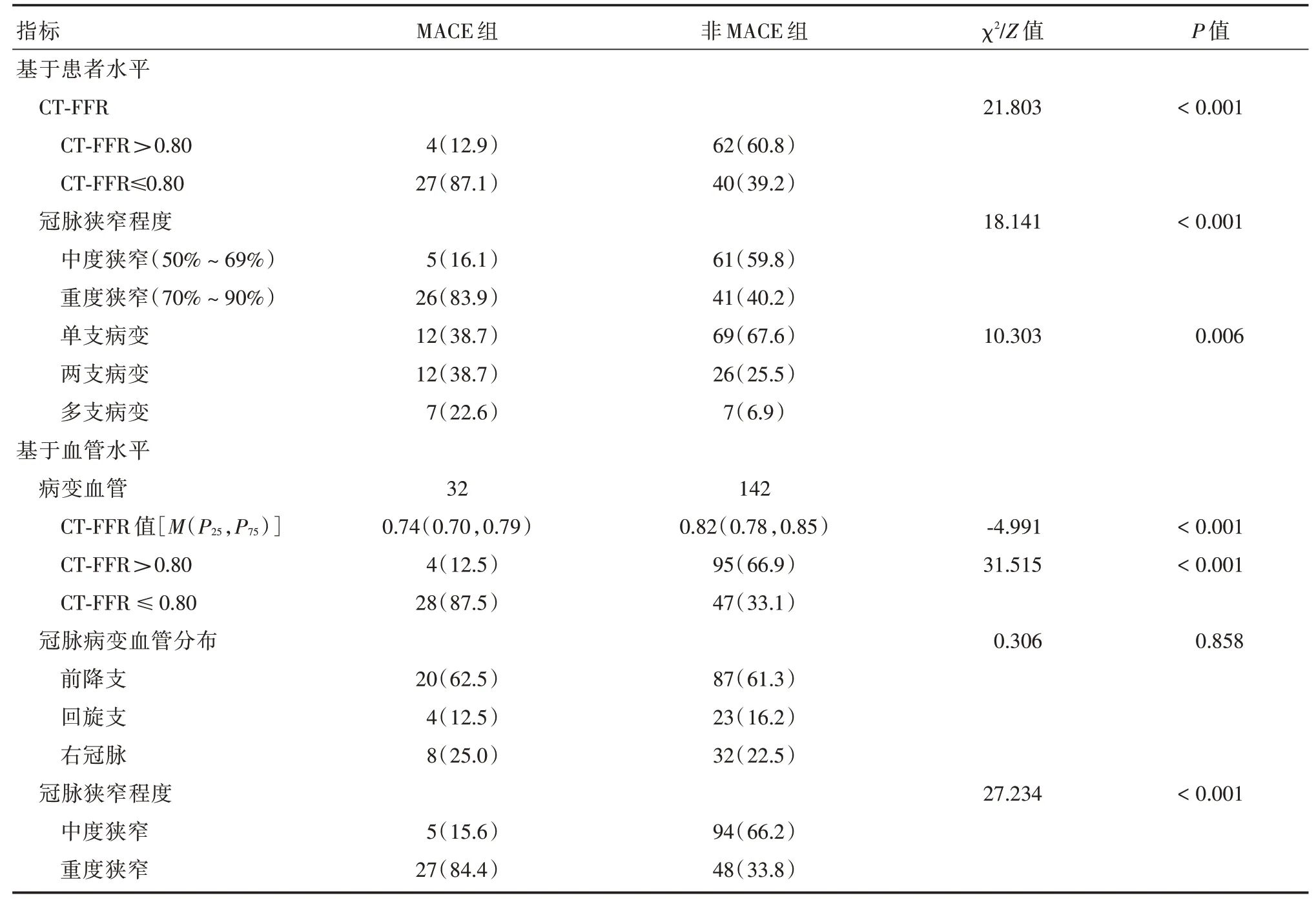
表2 两组间冠脉基线资料的比较Tab.2 Comparison of basic coronary data between the two groups 例(%)
2.3 患者发生MACE 的影响因素分析多因素Cox 回归分析显示,CT-FFR 值≤0.80(HR= 4.41,95%CI:1.46~13.32)、糖尿病(HR= 2.54,95%CI:1.22~5.30)、冠脉狭窄程度≥70%(HR=3.65,95%CI:1.34~9.95)是阻塞性CAD 患者发生MACE 的独立危险因素,LVEF 增大(HR= 0.92,95%CI:0.85~0.99)是阻塞性CAD 患者发生MACE 的保护因素,见表3。不同CT-FFR 和冠脉狭窄程度患者的生存曲线见图2。
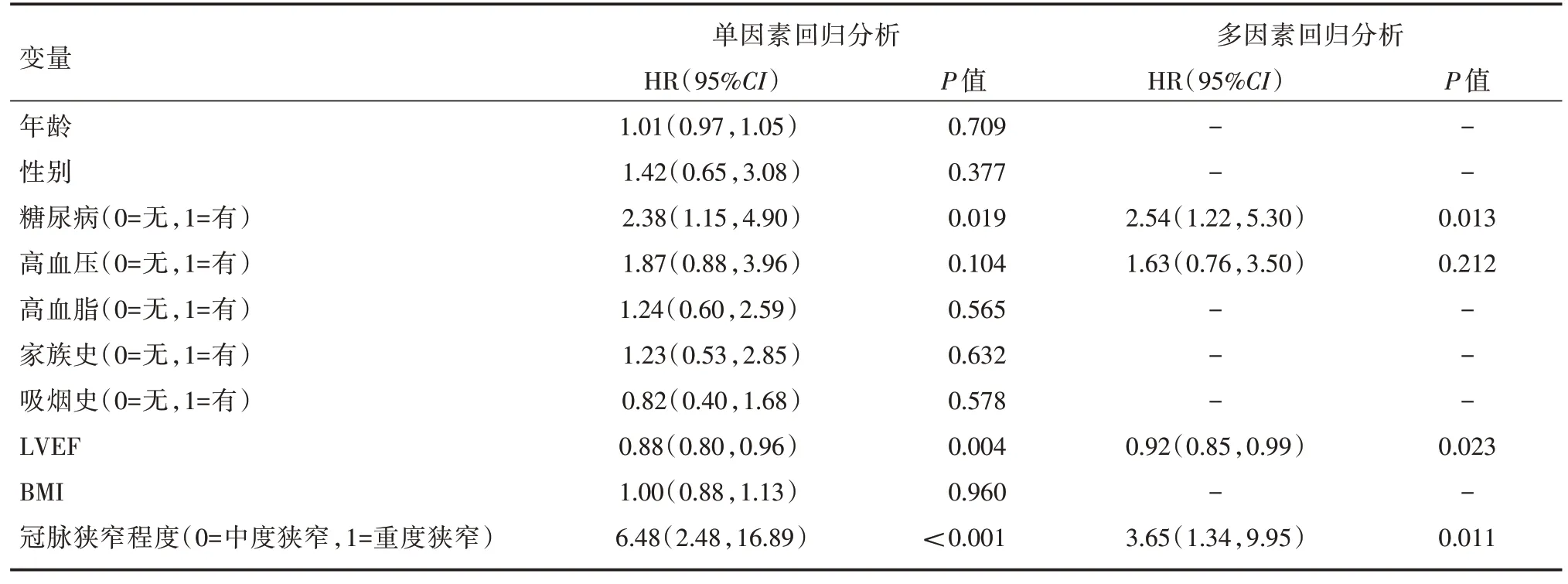
表3 临床心血管危险因素、冠脉狭窄程度、CT-FFR 的Cox 回归分析Tab.3 Cox regression analysis of clinical cardiovascular risk factors、coronary artery stenosis and CT-FFR
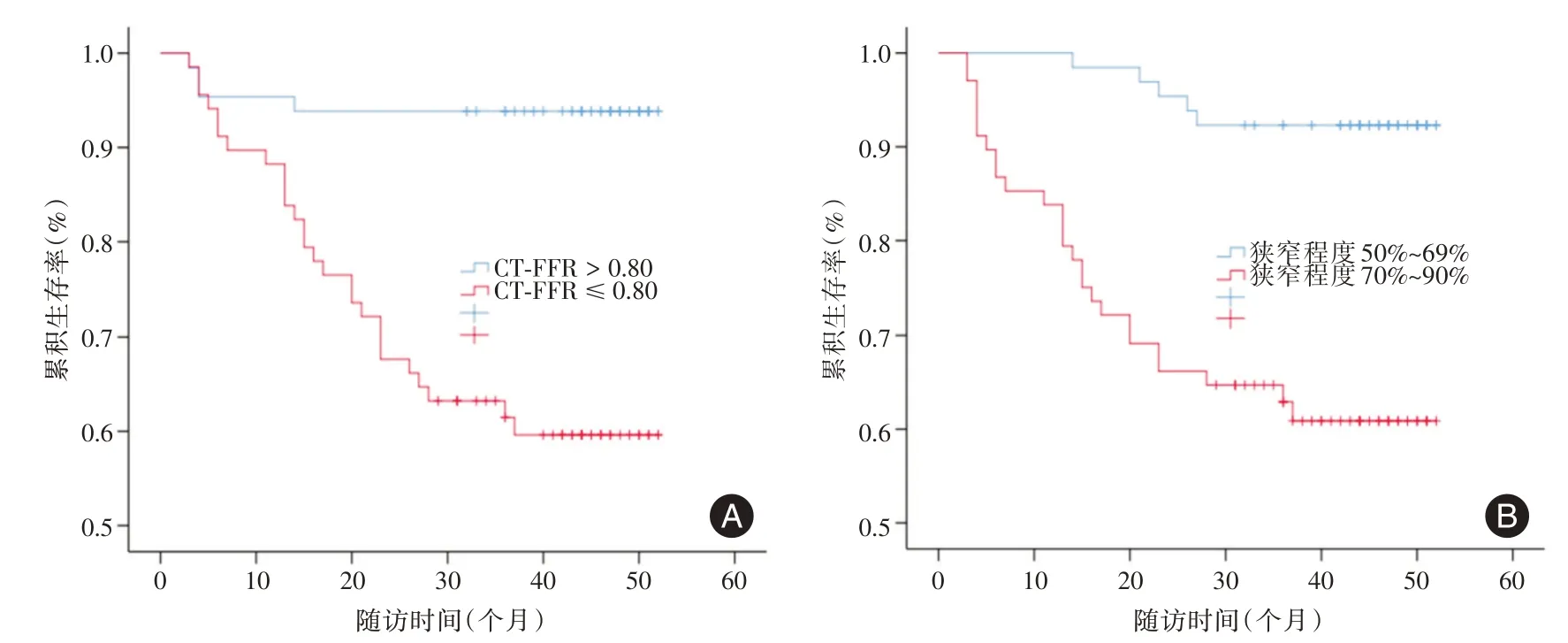
图2 不同CT-FFR 和冠脉狭窄程度患者的生存曲线分析Fig.2 Survival curve analysis of patients with different CT-FFR and coronary artery stenosis
2.4 3种模型预测MACE 能力的比较3 种模型的ROC 曲线分析见图3,其中模型3 的AUC 最大(AUC = 0.86,95%CI:0.79 ~0.91),大于模型1(AUC = 0.74,95%CI:0.66 ~0.81)和模型2(AUC =0.79,95%CI:0.71 ~0.86)。3 个模型的AUC 两两比较差异均有统计学意义(P<0.05)。

图3 3 种模型预测MACE 的ROC 曲线Fig.3 Three models predict the ROC curve of MACE
3 讨论
既往研究已证实CT-FFR 作为一种解剖学和功能学相结合的评估方法,可以准确评估冠脉狭窄引起的特异性缺血性病变,通常认为CT-FFR≤0.80 为阳性(即提示该病变为缺血性病变)。近年来CT-FFR 逐渐用于评估CAD 患者预后及指导血运重建,被认为是斑块进展[5]和MACE[6]的独立预测指标。ADVANCE 试验发现CT-FFR 可以预测疑似或确诊CAD 患者90 d 发生MACE 的风险,降低CAD 患者的ICA 检查率[7],1年后的随访数据亦证实,CT-FFR ≤0.80 的患者发生MACE 的风险明显高于CT-FFR阴性患者。本研究显示,出现MACE事件的患者中74%接受了靶血管血运重建(23/31),其中87%接受靶血管血运重建的患者CT-FFR 呈阳性(20/23),与PROMISE 试验[3]的子研究结果相吻合,这说明CT-FFR ≤0.80 对指导血运重建具有重要的参考价值。在本研究中,多因素Cox回归分析显示,CT-FFR ≤0.80 的阻塞性CAD 患者发生MACE 的风险比为4.41(95%CI:2.82~23.10),提示CT-FFR ≤0.80 是预测MACE 发生的独立危险因素,与既往研究结果[6]一致,其原因可能与CTFFR ≤0.80时,病变远端心肌血流灌注压降低,引起功能性心肌缺血,从而引发MACE的发生有关。
国内外已有研究表明冠脉狭窄程度是不良心血管事件的重要预测指标[6,8],可作为CAD 患者远期预后的评估方法。MCNABNEY 等[6]研究发现,冠脉狭窄≥50%是CAD 患者MACE 发生的独立危险因素。而本研究结果表明,冠脉重度狭窄是CAD患者发生MACE 的独立危险因素,其原因可能与本研究纳入的人群为阻塞性CAD 患者其冠脉狭窄程度普遍较重有关。本研究分析显示,CT-FFR 值≤0.80 预测阻塞性CAD 患者MACE 发生的风险比(HR=8.07,P<0.001)高于冠脉重度狭窄(HR=6.48,P<0.001),提示CT-FFR ≤0.80 在预测血运重建或MACE 方面优于冠脉重度狭窄,与PROMISE 试验的子研究[3]结果一致,其原因可能与冠脉狭窄程度与血流动力学受损的程度存在差异[9]且CT-FFR在评估血流动力学异常方面优于传统CCTA[10]有关。
在CAD 患者中,合并糖尿病会加重糖脂代谢紊乱,从而导致冠脉病变程度加重,以致易诱发不良心血管事件的发生。国内学者研究证实[11]合并2 型糖尿病的CAD 患者更易诱发急性冠脉综合征的发生,本研究中糖尿病是阻塞性CAD 患者发生MACE的独立危险因素(HR=2.54,P=0.013),提示合并糖尿病的CAD 患者MACE 的发生风险增加。因此在临床工作中应以纠正糖脂代谢作为目标,加强CAD 和糖尿病的共病管理,以期达到改善患者预后、降低MACE 发病风险的目的。此外,本研究发现LVEF 增大是患者发生MACE 的保护因素,与既往研究结果一致[12]。
本研究发现CT-FFR 联合冠脉狭窄程度和临床心血管危险因素的预测模型优于CT-FFR 模型,AUC 下面积由0.74 提高到了0.86,联合预测模型可提高对阻塞性CAD 患者MACE 发病风险的预测能力,从而用于指导CAD 患者的诊疗策略和血运重建的实施,改善患者的风险分层及临床预后。本研究存在的局限性:(1)本研究样本量较少和随访时间较短,可能存在选择偏倚。(2)本研究没有金标准即有创的FFR 进行对比,但关于CT-FFR 在CAD 患者的研究中已有初步的证实[13-14]。
综上所述,CT-FFR、冠脉狭窄程度和临床心血管危险因素对MACE 有较好的预测价值,并且CT-FFR 在预测MACE 方面优于冠脉狭窄程度和临床心血管危险因素,三者联合应用有效提高了对阻塞性CAD 患者MACE 的预测效能,从而为临床提供一种无创、有效的MACE 风险预测方法。

