Box-Behnken响应面法优化关黄柏药材中生物碱提取工艺*
冯 媛,郑玉光,刘 岩,张清清,2△
(1.河北中医学院药学院,河北 石家庄 050200; 2.河北省中药炮制技术创新中心,河北 石家庄 050200;3.河北化工医药职业技术学院,河北 石家庄 050200;4.天津天士力中药资源科技发展有限公司,天津 300000)
关黄柏为芸香科植物黄檗Phellodendron amurenseRupr.的干燥树皮,有清热燥湿、泻火除蒸、解毒疗疮功效,主要用于治疗黄疸泻痢、肠痔、口疮、热淋涩痛、遗精、目热赤痛等病症[1]。其活性成分主要包括生物碱、内酯、酚酸、苯丙素等[2-3],具有抗炎、抗菌、抗癌、抗氧化、降血糖、降血压、免疫调节等药理活性[4-6]。关黄柏中以生物碱类成分最具代表性,结构类型多样,且具有较好的药理活性,一直以来备受关注[7]。相较于正交试验法,响应面法试验周期更短,求得的回归方程准确度更高,并可研究几种因素间的交互作用[8-12]。本研究中以小檗碱、巴马汀等5个代表性生物碱成分的总含量为指标,基于响应面法优化关黄柏药材中生物碱的提取工艺,为关黄柏药材的质量控制及开发利用提供参考。现报道如下。
1 仪器与试药
1.1 仪器
Agilent 1260型高效液相色谱仪(美国Agilent公司);QUINTIX125D-1CN型电子分析天平(赛多利斯科学仪器有限公司,精度为十万分之一);Eppendorf Centrifuge 5418型离心机(德国Eppendorf AG公司);Milli-Q型超纯水仪(美国Milipore公司);KQ-300DE型数控超声波清洗仪(昆山市舒美超声仪器有限公司)。
1.2 试药
关黄柏饮片(河北省安国市祁澳中药饮片有限公司、批号为1908917171,河北省安国市深豪药业有限公司、批号为190602151,河北省安国市金康迪中药材饮片有限公司、批号为1804001C),经河北中医学院郑玉光教授鉴定为正品;木兰花碱对照品(批号为19082004,含量为99.84%),盐酸药根碱对照品(批号为19072609,含量为98.62%),小檗红碱对照品(批号为19050701,含量为98.71%),小檗碱对照品(批号为17110105,含量为98.95%),巴马汀对照品(批号为18022604,含量为99.01%),均购自成都曼思特生物科技有限公司;乙腈为色谱纯,甲醇为色谱纯和分析纯,水为超纯水。
2 方法与结果
2.1 生物碱成分含量测定
2.1.1 色谱条件
色谱柱:Diamonsil C18柱(250 mm×4.6 mm,5μm);流动相:乙腈(A)-0.1%甲酸溶液(B),梯度洗脱(0~20 min时10%A→12%A,20~27 min时12%A→22%A,27~36 min时22%A→26%A,36~65 min时26%A→40%A,65~68 min时40%A→75%A,68~70 min时75%A→10%A);检测波长:265 nm;流速:1 mL/min;柱温:30℃;进样量:10μL。
2.1.2 溶液制备
取木兰花碱、盐酸药根碱、小檗红碱、小檗碱、巴马汀对照品各适量,精密称定,分别置10 mL容量瓶中,加入70%甲醇定容,制成单标母液,分别稀释,配制成分别含木兰花碱0.0049 mg/mL、盐酸药根碱0.0006 mg/mL、小檗红碱0.0002 mg/mL、巴马汀0.0062 mg/mL、小檗碱0.0187 mg/mL的混合对照品溶液。取关黄柏药材粉末0.5 g,精密称定,浸泡30 min后置100 mL具塞三角瓶中,加入30 mL甲醇,25℃下超声(功率250 W,频率40 kHz)提取40 min,再称定质量,用甲醇补足减失的质量,混匀,取续滤液,13000 r/min离心5 min,取上清液,置5 mL EP管中,稀释10倍,经0.22μm微孔滤膜滤过,取续滤液,即得供试品溶液。
2.1.3 方法学考察
系统适用性试验:取上述混合对照品溶液、供试品溶液各适量,按2.1.1项下色谱条件进样测定,记录色谱图,详见图1。结果,理论板数按木兰花碱峰计算应不低于3000;分离度均大于1.5,基线分离良好。

图1 高效液相色谱图1.magnoflorine 2.jatrorrhizine hydrochloride 3.berberrubine 4.palmatine 5.berberine A.Mixed reference solution B.Test solutionFig.1 HPLC chromatograms
线性关系考察:精密吸取2.1.2项下混合对照品溶液1,3,5,10,15,20μL,按2.1.1项下色谱条件进样测定,以各对照品质量浓度(mg/mL,X)为横坐标、峰面积(Y)为纵坐标进行线性回归,得回归方程和线性范围,详见表1。

表1 线性关系考察结果(n=6)Tab.1 Results of the linear relation test(n=6)
精密度试验:1)日内精密度,精密量取混合对照品溶液适量,连续进样测定6次,记录峰面积。结果木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱的RSD分别为0.15%,0.51%,0.46%,0.13%,0.17%(n=6),表明仪器的日内精密度良好。2)日间精密度,精密量取混合对照品溶液适量,连续进样测定3 d,每日1次,记录峰面积。结果木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱的RSD分别为0.13%,1.51%,0.11%,1.42%,1.87%(n=3),表明仪器的日间精密度良好。
重复性试验:取同一批关黄柏药材粉末,精密称定,按2.1.2项下方法平行制备6份供试品溶液,按2.1.1项下色谱条件进样测定,记录峰面积及计算含量。结果木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱含量的RSD分别为0.78%,1.54%,1.15%,1.87%,1.83%(n=6),表明该方法重复性较好。
稳定性试验:精密吸取同一关黄柏供试品溶液,分别在室温下放置0,3,5,8,13,20,24 h时按2.1.1项下色谱条件进样测定,记录峰面积。结果木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱的RSD分别为1.77%,1.94%,1.78%,1.72%,1.12%(n=7),表明供试品溶液室温下24 h内稳定。
加样回收试验:取已知含量的关黄柏药材粉末共6份,各0.25 g,精密称定,分别加入相应对照品溶液按2.1.2项下方法制备供试品溶液,按2.1.1项下色谱条件进样测定并计算加样回收率。结果,木兰花碱、盐酸药根碱、小檗红碱、巴马汀、小檗碱的加样回收率分别为102.33%,104.53%,102.76%,100.34%,102.62%(n=6),RSD分别为1.10%,0.27%,1.10%,0.78%,0.99%(n=6)。
2.2 单因素试验
2.2.1 甲醇体积分数
取关黄柏药材样品粉末0.5 g,精密称定,平行6份,液料比为60 mL/g,分别加入体积分数为10%,30%,50%,70%,90%、100%的甲醇,25℃超声提取40 min,13000 r/min离心5 min,取上清液,置5 mL EP管中,稀释10倍,经0.22μm微孔滤膜滤过,取续滤液,进行液相分析,得5个生物碱总含量,其含量与甲醇体积分数的变化关系见图2。可见,生物碱总含量随甲醇体积分数的升高而增加,当甲醇体积分数为70%时,生物碱总含量最大。故选取甲醇体积分数50%,70%,90%3个水平进行后续试验。
2.2.2 液料比
取关黄柏药材样品粉末0.5 g,精密称定,平行处理6份,甲醇体积分数为70%,在不同液料比(20,40,60,80,100,120 mL/g)下,25℃超声提取40 min,称定质量,用甲醇补足减失的质量,13000 r/min离心5 min,取上清液,置5 mL EP管中,稀释10倍,经0.22μm微孔滤膜滤过,取续滤液进行液相分析,得5个生物碱的总含量,其含量与液料比的变化关系见图2。可见,随着液料比的增加,生物碱总含量先增加后减少,液料比在30 mL/g时,生物碱的总含量达到最大。故选取液料比40,60,80 mL/g 3个水平进行后续试验。
2.2.3 提取时间的影响
取关药材样品粉末0.5 g,精密称定,平行处理5份,液料比为60 mL/g,加入70%甲醇,分别超声处理15 min、30 min、40 min、50 min、1 h(25℃)。生物碱总含量与料液比的变化关系见图2。可见,随着提取时间的延长,生物碱总含量先增加后减少,当提取时间为40 min时,生物碱总含量最大。故选取提取时间30,40,50 min 3个水平进行后续试验。
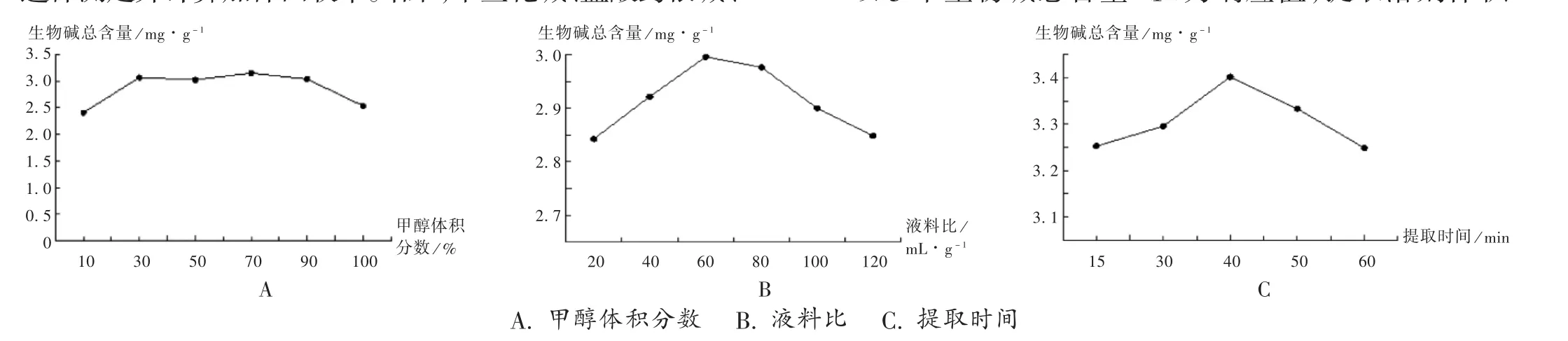
图2 单因素试验结果A.Methanol volume fraction B.Liquid-material ratio C.Extration timeFig.2 Results of the single factor test
2.3 响应面试验
2.3.1 响应面设计
以5个生物碱总含量(Y)为响应值,提取溶剂体积分数(A)、超声时间(B)、液料比(C)3个因素为自变量,且每个自变量选取低、中、高3个水平,对关黄柏生物碱超声提取工艺进行三因素三水平研究,使用Design-Expert 8.0.6软件,采用Box-Behnken原理进行中心组合设计,因素水平见表2,Box-Behnken试验设计与结果见表3。

表2 因素水平表Tab.2 The factor levels
2.3.2 方差分析与显著性检验
运用Design-Expert 8.0.6软件对表2中的试验结果进行拟合分析,得二次多项回归方程Y=3.03-0.041A+0.024 B+0.015 C-2.5×10-3AB+1×10-2AC+0.05 BC-0.22 A2-0.10 B2-0.13 C2(R2=0.8789),说明该模型拟合度较好,试验误差较小[13]。进一步对方程进行方差分析,结果见表4。
由表4可知,模型P=0.0163<0.05,说明本回归模型自变量与因变量的回归关系显著,失拟项P=0.46>0.05,说明二次多项回归方程拟合程度良好,本试验具有统计学意义[14]。各因素对关黄柏生物碱提取率的影响大小为A>B>C,二次项A2,B2,C2对响应值的影响显著,说明各因素与响应值之间不是简单的线性关系。交互项对生物碱总含量影响的强弱为BC>AC>AB,说明超声时间和液料比对响应值的影响较明显。
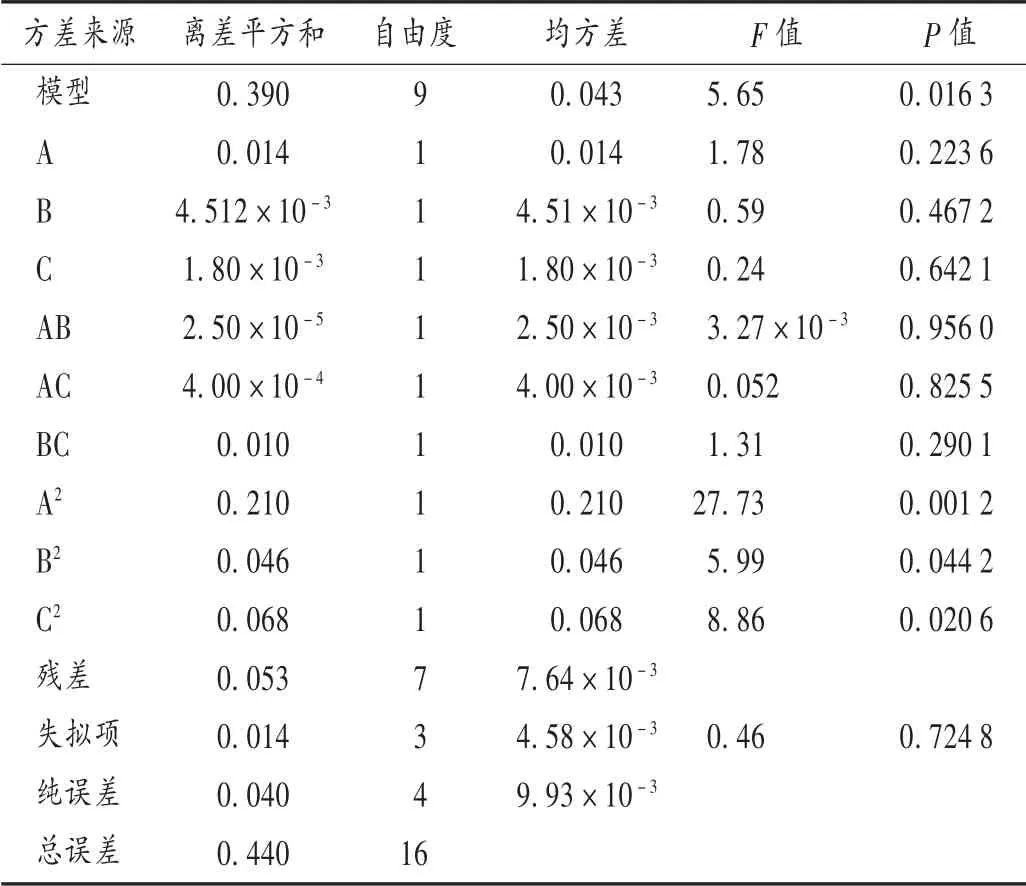
表4 方差分析结果Tab.4 Results of ANOVA
2.3.3 响应面分析
根据响应面图(见图3)评价试验因素之间的交互强度,优选出最佳提取工艺。由图3可知,因素A的曲面较陡峭,说明甲醇体积分数相对于其他2个因素对生物碱成分提取效率的影响较大。BC交互作用较强,说明提取时间与液料比的交互作用对生物碱总含量的影响显著,AB和AC交互作用较弱,说明甲醇体积分数与提取时间、液料比与提取时间的交互作用对生物碱总含量的影响较小。

图3 各因素与生物碱总提取量的响应面图A.Ultrasonic time and methanol volume fraction B.Liquid-material ratio and methanol volume fraction C.Liquid-material ratio and ultrasonic timeFig.3 Response surface diagram of each factor and total extraction amount of alkaloids
2.4 最优工艺与验证试验
优选出的最佳提取工艺为:提取时间为41.35 min,甲醇体积分数为68.17%,液料比为61.64 mL/g。结合实际,同时为方便操作,最终确定最优提取工艺为取0.5 g的关黄柏药材样品粉末,加入68%甲醇,超声提取41 min,液料比为62 mL/g。分别选取3批关黄柏药材饮片,在上述最优工艺条件下进行验证试验。结果生物碱成分总含量分别为3.030,2.979,3.007 mg/g,平均3.005 mg/g(RSD=0.85%),与模型预测值的相对误差为0.59%,表明建立的模拟回归方程拟合度较好,优化的提取工艺稳定、可靠。
3 讨论
关黄柏药材中生物碱提取方法主要包括传统的水煎煮法、酸水法、石灰水法、乙醇回流法等[15-16],提取时间较长、能耗大,一些热敏性的有效成分易被破坏,且提取效率较低。相对于传统的提取方法,超声提取法、酶辅助提取法可弥补上述缺点[17],但提取成本较高。综合考虑,本研究中采取超声法提取关黄柏药材中的生物碱成分。
前期通过预试验对不同超声次数(1,2,3次)、不同浸泡时间(15 min、30 min、1 h、2 h、4h、12 h)及不同种类提取溶剂[包括甲醇、盐酸-甲醇(1∶100,V/V)、乙酸-甲醇(1∶100,V/V)、盐酸-乙醇(1∶100,V/V)、乙醇]进行考察,结果表明,生物碱总含量在超声1次、提取溶剂为甲醇时最高。浸泡时间为4 h时生物碱总含量最高,其次为浸泡30 min,为提高提取效率,综合考虑,最终选择甲醇为提取溶剂,浸泡30 min,超声1次。此外,巴马汀和小檗碱均属原小檗碱型生物碱,化学结构相似,高效液相色谱图中保留时间十分接近,且巴马汀在关黄柏和川黄柏药材中的含量差异十分显著。
2020年版《中国药典》以盐酸小檗碱和盐酸巴马汀的含量作为关黄柏药材的质量评价指标[1],在目前已有的关黄柏最佳提取工艺研究中,多数仅以小檗碱成分作为考察指标[17]。为更全面、准确地评判关黄柏药材的质量,本试验中选取了含量较高、药理作用研究较充分的木兰花碱、盐酸药根碱、小檗红碱、巴马汀和小檗碱的总含量,作为评价指标。该方法相较于目前已有的仅以小檗碱作为对照品考察关黄柏提取工艺的研究更严谨、科学。目前有关关黄柏药材最佳提取工艺的研究中,大多都采用正交试验设计法。而响应面法可连续对试验各个水平进行分析,在单因素试验基础上,找出与原预设水平相比最优的组合条件[18-19],与正交试验相比,试验结果的精度和真实度更高、直观性更强[20-21]。但也有其局限性,如响应面试验前的单因素最佳水平选取错误,会使响应面试验无法得到预期结果[22]。本试验中通过单因素试验结合Box-Behnken响应面法,优化得到关黄柏药材中生物碱的最佳提取工艺,操作简便、效率高、稳定可靠。

