人工智能对早期肺癌结节良恶性鉴别能力探究
卢辉 李峰 胡庆 庞中好 陈圣杰 蒋志华 顾添一 基红云
近几年,肺癌在国内外的发病率及致死率逐年上升,现已跻身第一位[1],早期肺癌肺结节(pulmonary nodule)的性质及病因复杂,但随着CT(Computed Tomography)的广泛普及和应用,越来越多的肺结节被检测出来[2]。肺结节分为实性结节(Solid Nodule,SN)和亚实性结节(Subsolid Nodule,SSN)[3],亚实性结节又称磨玻璃结节(Ground Glass Nodule,GGN)。CT对肺癌早期结节病灶的筛查有重要的临床价值,使得肺癌的死亡率明显下降[4]。将人工智能数据计算应用到 CT 阅片,是有效、快速、准确筛查肺部结节的一条捷径。本研究参考病理和影像学数据结果,探讨AI技术对肺癌早期结节良恶性鉴别的临床应用价值。
资料与方法
一、研究对象
2015年1月—2020年10月江苏大学附属医院诊治的因肺结节入院且病理确诊为肺癌的患者中选取382例,其中包含胸部CT影像为SN的患者191例、胸部CT影像为GGN的患者191例,收集所有病理确诊为恶性结节患者的胸部CT,另外,搜集术后病理诊断为良性的肺结节患者的胸部CT 156例,其中包含CT影像为SN和GGN的患者各78例,共计538例影像作为检测集。纳入标准:1)、符合《肺结节诊治中国专家共识(2018年版)》相关诊断标准[5]。2)、手术切除的T1期肺癌病灶,其诊断标准为:肺部CT影像提示结节直径≤3 cm,被肺或脏层胸膜包绕,未累及叶支气管近端以上位置,术后病理报告确诊为肺恶性肿瘤[6]。排除标准:1)、结节无手术切除病理学检查结果;2)、患者入院前曾接受过放化疗。剔除标准:术后病理提示为转移性肿瘤[7]。
二、研究方法
1 图像采集:设备名称SOMATOM Definition AS CT(西门子128层螺旋CT)。患者仰卧,头先入,以胸骨柄为定位中心,患者深吸气并屏气;行胸部CT扫描,扫描参数调节:电流110~130 mA,电压120 kV,间距5 mm,层厚5 mm,矩阵512×512,螺距为1.2,范围为从肺尖以上扫描至横膈以下;发现病灶后给予CT重建,重建参数:矩阵不变,电压仍120 kV,层厚1 mm,层隔5 mm,螺距不变。
2 阅片方法:分别采用AI阅片及医师阅片判读382例确诊肺癌肺结节患者及156例良性肺结节患者胸部CT。(1)AI阅片法,由1位具有10年以上胸部读片经验的影像科主治以上医师采用本研究设计的AI肺结节筛查系统进行辅助诊断。即将所有患者的CT影响资料导入三维深度卷积神经网络(CUMedVis)算法系统(本研究提供的优化算法的肺癌智能筛查系统)中,软件能将疑似肺结节的部位进行准确标记,并可显示结节的直径,CT值,性质(磨玻璃结节、实性结节等),征象(分页征、毛刺征、血管集束征等)及恶性概率(恶性概率>70%为高危结节,恶性概率50%~70%为中危结节,恶性概率<50%为低危结节,其中恶性概率>70%的高危结节提示为恶性肺结节,其他提示为良性肺结节[8])等。(2) 本研究设计的AI肺结节筛查的优化算法:在早期肺结节的筛查上,AI的敏感度虽然与传统的机器视觉算法相似,但AI剔除假阳性结节的能力明显高于传统机器算法,最具代表性的AI算法就是 CUMedVis:三维深度卷积神经网络,可以更有效的将多样的空间信息整合起来,并升华出更典型、更具有代表性的潜在特征。卷积神经网(convolutional neural network, CNN)就是一种深度神经网络,并进一步模仿大脑的视觉皮层构造和视觉活动原理而开发[9-10],由于医疗大数据的不断积累,CNN在医疗应用中的优势越发明显。本研究采用三维CNN的三种不同框架结构,使用这三种不同的CNN处理同一空间区域的CT 影像,并通过计算得出此空间区域包含肺结节的概率,计算所得结果定为 P1、P2、P3,采用线性组合公式 P=30%×P1+40%×P2+30%×P3,计算出最终概率P。设定一个阈值,当概率P小于设定阈值时,即判断为假阳性。本研究的AI算法,很好的降低了相似体多及复杂多样的肺结节在CT影像上带来的困难。(3)医师阅片法由3位具有10年以上肺部读片经验的影像科主治以上医师,对563例肺结节患者胸部CT进行分析判断(未使用肺结节筛查系统),按照《肺结节诊治中国专家共识(2018年版)》相关诊断标准进行分类,并根据肺结节大小、密度、与血管和支气管关系进行良恶性评估。以上4位医师均不了解患者的任何病情。
三、统计学方法
本研究采用统计学软件SPSS22.0和MedCalc软件对数据进行分析。将统计的AI和医师阅片诊断肺结节的结果进行配对卡方检验进行对比分析。AI检测肺结节良恶性的效果采用敏感度、特异度、准确率来评估。AI检测结果的可靠性采用Kappa分析评价。应用受试者工作特征(ROC)曲线分析肺结节的直径大小对结节良恶性诊断的价值以及AI阅片与医师阅片对结节的诊断价值。以P<0.05为差异有统计学意义。
结 果
一、AI筛查系统对SN和GGN检出数目的比较
AI检测出191个SN中有184个为恶性结节,检出率96.3%;191个GGN中有182个为恶性结节,检出率95.3%。比较AI阅片对SN和GGN两种不同结节的良恶性的判断差异,P=0.799,差异无统计学意义。
二、AI与医师阅片诊断SN良恶性的比较
AI和医师阅片诊断出的SN数量对比,P=0.022,差异有统计学意义(见表1)。同理,AI和医师阅片诊断出的GGN数量对比,P=0.012,差异有统计学意义(见表2)。以病理结果为金标准,AI与医师阅片对两种肺结节检测结果的分析(见表3、4)。
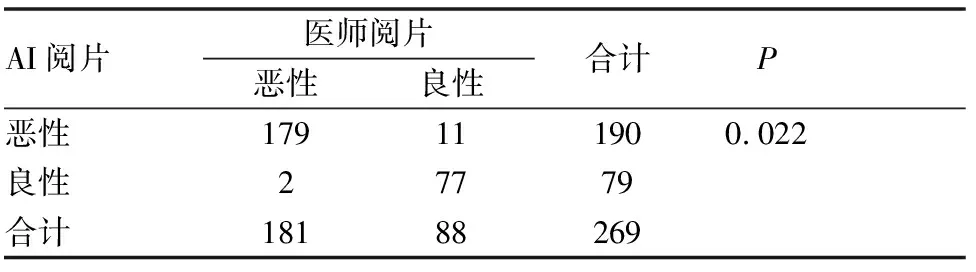
表1 AI与医师阅片诊断SN良恶性的比较
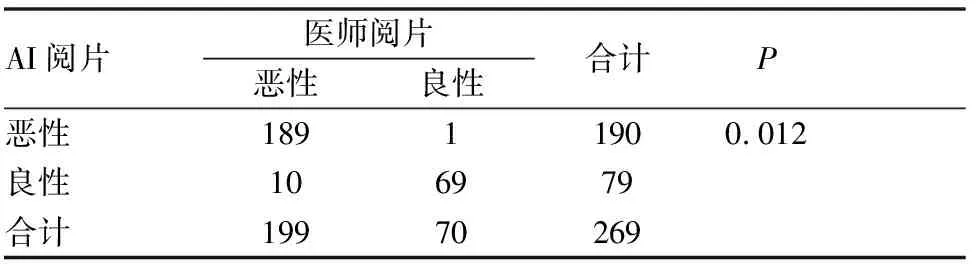
表2 AI与医师阅片诊断GGN良恶性的比较

表3 AI与医师阅片分别与病理诊断SN良恶性的比较[n(%)]
由(表3)可计算出AI和医师阅片检测SN的敏感度、特异度、阳性预测值和准确率,同理,根据(表4)可计算出AI和医师阅片检测SN的敏感度、特异度、阳性预测值和准确率。现将计算结果统计在(表5)。
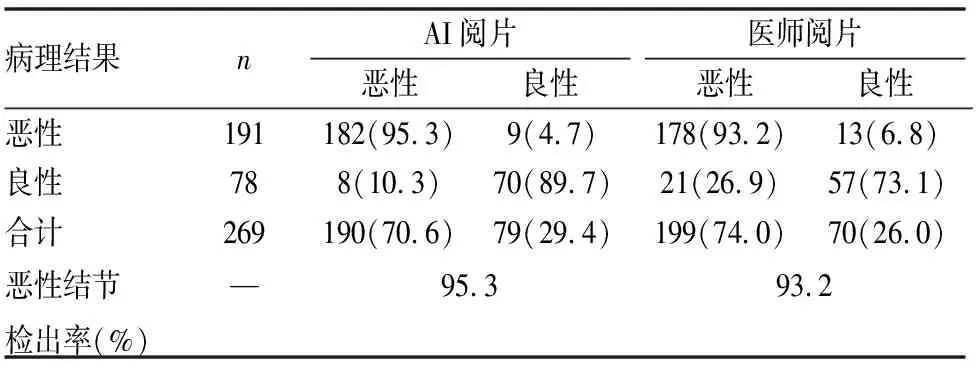
表4 AI与医师阅片分别与病理诊断GGN良恶性的比较[n(%)]
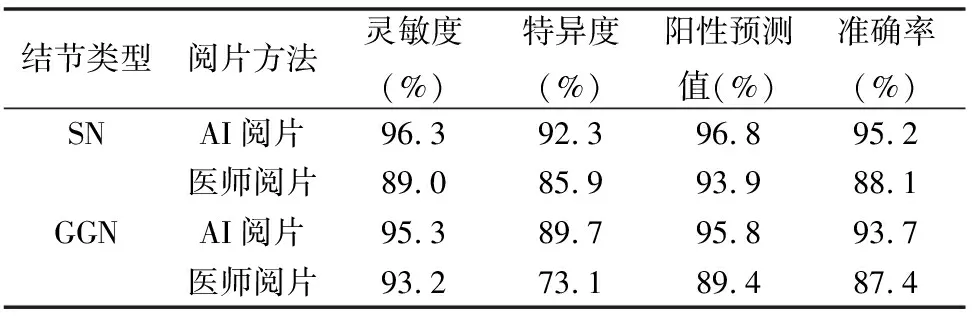
表5 两种阅片方法诊断恶性肺结节的临床价值比较
三、AI检测方法的可靠性评价
利用AI对<3 cm的肺结节CT片重复读取两次,记录统计数值,计算出重复两次读取SN的Kappa值为0.928,接近1.0,提示几乎完全一致。同理,AI重复两次读取GGN的Kappa值为0.925,接近1.0,提示几乎完全一致(见表6、7)。
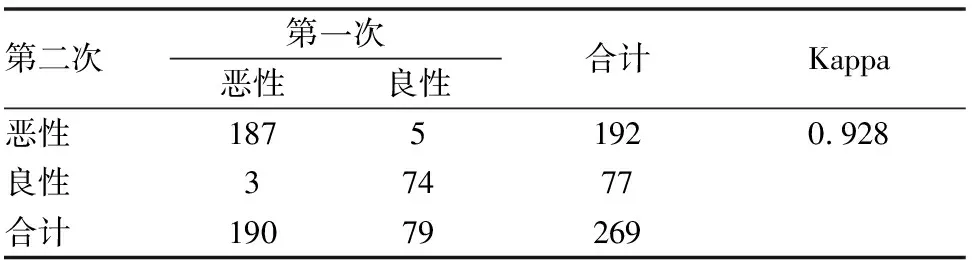
表6 AI两次筛查SN的Kappa分析

表7 AI两次筛查GGN的Kappa分析
四、将538位患者的病理诊断与每一位患者CT图像中肺结节的直径通过MedCalc软件进行对比得到以下ROC曲线:如图1。得到AUC=0.548,95%CI(0.505~0.590),P=0.076。
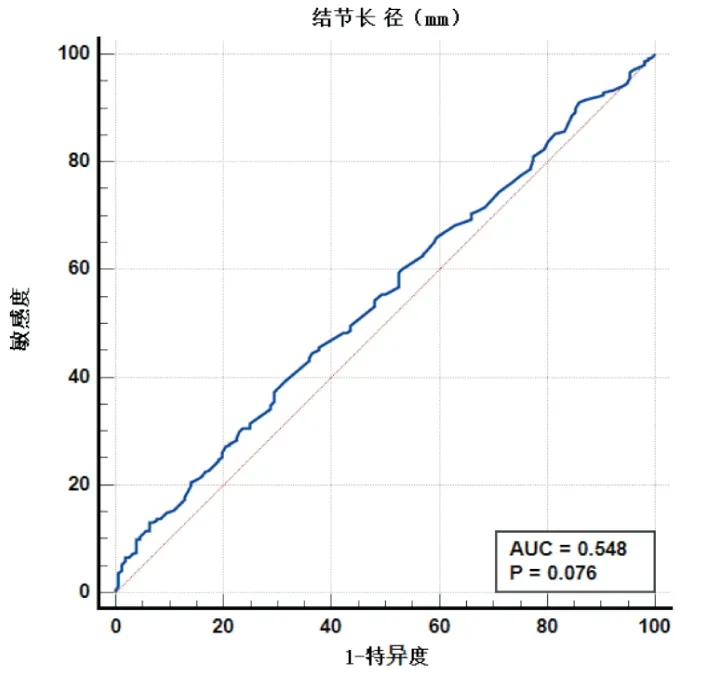
图1 结节直径大小诊断恶性肺结节的ROC曲线
将AI阅片和医师阅片的结果同病理诊断结果进行对比分析得到:图2。AI阅片:AUC=0.934,95%CI(0.910~0.954);医师阅片:AUC=0.888,95%CI(0.858~0.914);Z统计值为3.082,差异有统计学意义(P<0.05)。
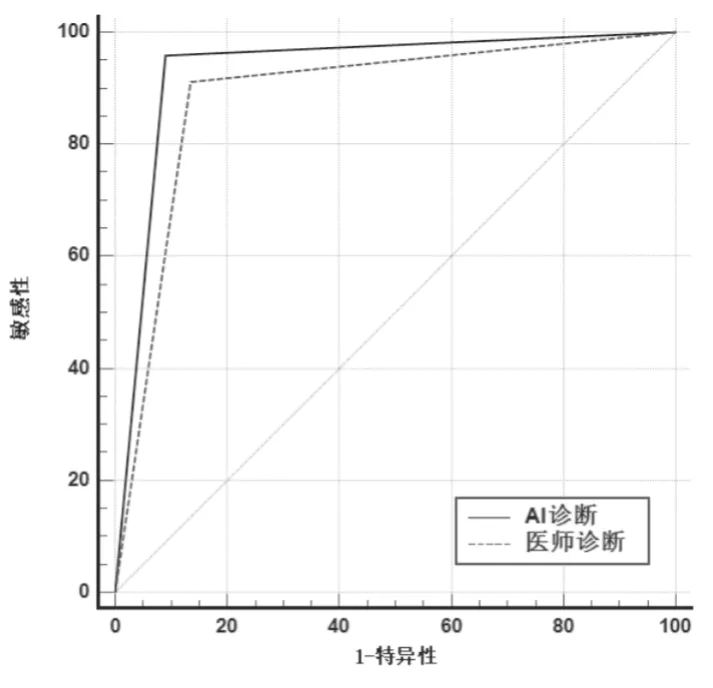
图2 AI阅片与医师阅片诊断恶性肺结节的ROC曲线
五、抽取两名患有不同类型肺结节患者作为示例,(图3)为一名54岁男性患者的CT影像,提示为右上肺磨玻璃结节,术后病理提示为(右上肺)腺癌(见图5)。(图4)为一名49岁女性患者的CT影像,提示为左下肺孤立实性结节,术后病理提示为(左肺)原位腺癌(见图6)。这两个病例的AI诊断和病理诊断结果一致。
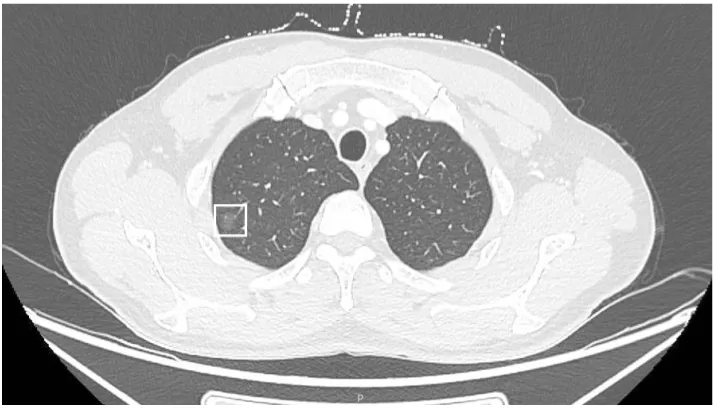
图3 患者男,54岁,右上肺磨玻璃结节

图4 患者女,49岁,左下肺孤立实性结节
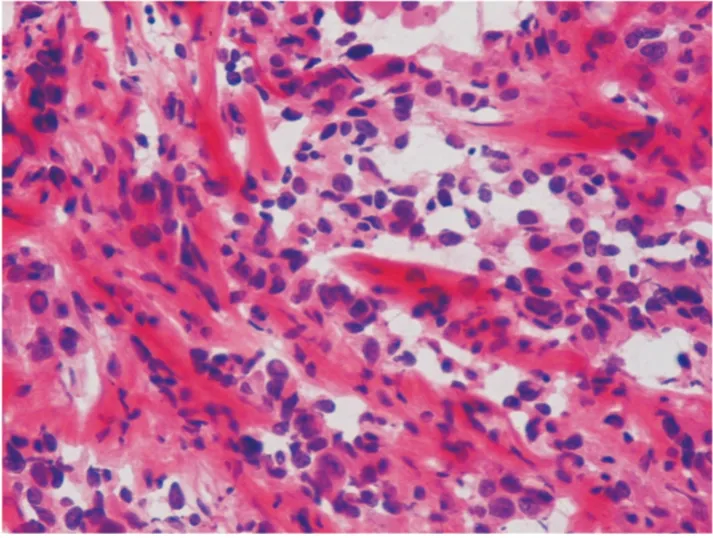
图5 病理:(右上肺)腺癌(HE×200倍)

图6 病理:(左肺)原位腺癌(HE×200倍)
讨 论
肺癌严重的损害了人类的生命健康,就发病率、病死率而言,已经远远超过其他恶性肿瘤[11]。大多数患者因为出现症状就诊时已经丧失了手术治疗的黄金时期[12],所以恶性肺结节的早发现和及时治疗对提高肺癌患者生存率[13]及改善晚期愈后至关重要。SN指肺部影像上圆形、类圆形的高密度影,其中血管及支气管影,可以被掩盖[14]。GGN指CT影像上圆形、类圆形的高密度影,肺间质结构可见肺内血管、支气管、小叶间隔影等[15]。而后者又可细分为纯磨玻璃结节(Pure Ground Glass Nodule,pGGN)和混合性磨玻璃结节(Mixed Ground Glass Nodule,mGGN)。SN恶性率最低,其次是pGGN,mGGN的恶性率最高[16]。肺结节的性质变化多样,提前发现早期肺癌结节并采取预防和治疗,就可以显著增加肺癌患者的5年生存率[17]。AI简单来讲,就是通过模拟人类的思考方式来解决人类所面临的各种实际问题[18],运用设计好的算法,在检出肺部结节的同时,对结节的形态学特征进行分析计算,最终得出结节的恶性概率,对早期肺结节的诊治有指导意义[19]。例如上图,设计的AI诊断技术可以在病理确诊之前预先判断结节的良恶性,指导临床治疗。
基于此,本研究结合病理诊断以及CT图像资料结果,采用回顾性研究,收集术后病理确诊的肺癌患者的胸部CT资料,比较AI阅片与医师阅片诊断肺结节良恶性的敏感度、特异性、阳性预测值、准确率的高低,并评估了AI阅片对SN和GGN两种不同结节的判断有无差异及AI重复阅片的可靠性。在本文结果中,AI筛查系统对SN和GGN检出数目的比较反映了AI阅片对SN和GGN两种不同结节的良恶性判断差异无统计学意义(P>0.05),同时计算结果也可以看出,AI对SN和GGN的检出率(96.3%、95.3%)略高于医师阅片的检出率(89.0%、93.2%);本研究设计的优化算法应用到AI,可以很好地降低CT图像中肺结节自身的差异以及类似体复杂多样对结果的影响,对两种不同结节的诊断没有明显统计学差异,石河子大学医学院第一附属医院的一项研究[20],也证明了AI系统对孤立实性结节和磨玻璃结节的检出效果是相同的。AI阅片和医师阅片对两种结节良恶性的诊断具有差异,P均<0.05,具有统计学意义(表1、2),从而才能从(表3~5)中得出,AI阅片组对肺结节良恶性诊断的敏感性、特异性、阳性预测值、准确率均略高于医师阅片组,另外通过MedCalc软件对两种阅片方法诊断结果进行分析(如图2),也可以得出AI阅片的诊断能力要高于医师诊断,这都说明AI在辅助放射科医师诊断肺癌早期结节诊断方面是有意义的。Kappa计算结果为-1~1,但通常在0~1之间,一致性极低的Kappa值在0.0~0.20之间,一致性一般Kappa值在0.21~0.40之间,一致性中等的Kappa值在0.41~0.60之间,高度一致性的Kappa值在0.61~0.80之间,几乎完全一致的Kappa值在0.81~1间。通过AI重复阅片(表6、7)计算出SN的Kappa值为0.928,接近1.0,GGN的Kappa值为0.921,接近1.0,提示AI对这两种结节的二次阅片结果几乎完全一致,说明AI检测两种肺结节重复检测的可靠性极好,这就为AI阅片的广泛应用提供了可靠性。这些都说明,可以通过优化AI的算法,提高AI在肺癌早期肺结节诊断中的敏感度和特异度,提高诊断准确率。另外,通过对肺结节的直径大小与良恶性的关系进行分析(图1),用ROC曲线下面积(AUC)判断诊断的准确性,AUC=0.5~0.7表示有较低的准确性,>0.7~0.9具有一定的准确性,>0.9有较高的准确性。图1中AUC=0.548接近0.5,这个结果表明肺结节的良恶性与结节的直径大小没有明显的相关性,故本实验不对肺结节的大小进行过多研究。
本研究同时也有相应的局限,首先样本量不够多,会对结果造成一定的偏差,其次,在实际的临床工作中,医生的水平良莠不齐,加上疲劳、人为测量差异等因素,都会对结果有一定的影响。
综上所述,AI系统判断肺结节良恶性虽然特异度欠佳,但总体上较影像医师的诊断能力略有优势,在检测不同类别结节上没有明显差异。而且AI诊断肺结节较快速,基于大数据集学习所得到的算法模型可以避免主观的偏差,虽然包含了一些假阳性结节,但明显降低了假阴性的发生,显著提高了临床医师的阅片效率。
但基于深度学习的肺结节检测模型还处在医疗应用初级阶段,AI检测模型的特异性 、准确性均需要进一步的提高[21]。AI的发展需要大数据的支撑以及算法的不断优化,合理的应用AI辅助诊断系统和放射科医师阅片结合,能够更加有效地提高阅片效率,使得更多的肺癌病人能够得到早期及时的诊治,更好的改善愈后及提高生存率。

