基于ZIFs的新型电化学传感器及对尿酸和L-色氨酸的测定*
李改花,刘 爽,张 宁,李港园
(唐山师范学院,唐山市绿色专用化学品重点实验室,河北 唐山 063000)
沸石咪唑框架(Zeolitic Imidazolate Frameworks,ZIFs) 是由金属离子与咪唑类配体通过配位作用形成的四配位多孔晶体材料,具有与方钠石(SOD)类似的拓扑结构[1]。由于其具有优异的化学稳定性、热稳定性和可调节性受到了科研工作者的广泛关注,在催化[2]、气体的吸附和储存、电、光传感器[3-4]等各个领域得到拓展和应用。尤其是ZIFs材料的多孔结构且具有较大的表面积和裸露的骨架结构,可以为电化学传感的检测提供了优良的的基底材料。
L-色氨酸又名α-氨基吲哚基丙酸,是人体必需的 8 种必需氨基酸之一,只能通过食物来摄取,人体日常饮食中缺乏L-色氨酸 会出现与蛋白质缺乏症类似的症状。此外,L-色氨酸能促进大脑神经细胞分泌神经递质五羟色胺,可缓解人体紧张情绪,改善人体睡眠。目前测定色氨酸的方法有很多,如流动注射、高效液相色谱法[5-6]、分光光度法[7]、电化学法[8]。考虑到设备昂贵、和分析成本操作步骤繁琐等因素,建立一种简单、速度快、准确度比较高的检测色氨酸含量的方法,显得尤为重要。电化学分析方法特别是修饰电极法已成为各国电化学分析工作者研究的重点[9]。 尿酸是嘌呤代谢的最终产物,它是一种含有碳、氮、氧、氢的杂环化合物,由人体的肝脏、骨髓、肌肉等产生。尿酸微溶于水,易形成晶体。正常人体尿液中产物主要为尿素,含少量尿酸。人体尿酸过高或过低会导致痛风、肿瘤的发生,所以说尿酸是人体必不可少的物质。尿酸在人体内起到了强有力的的抗氧化作用,人类体内的尿酸浓度相当于其他哺乳动物的10倍之多,这就是人类的寿命比较长的原因[10]。近些年来,尿酸作为有机物越来越多的被应用到电化学分析上。
本实验用室温搅拌法合成了稳定性高的ZIF-9,首次作为电化学传感器基底材料应用于电化学传感器的制备,采用循环伏安法分别对L-色氨酸和尿酸两种生物小分子进行了检测并取得了良好的实验结果。
1 实 验
1.1 材料与试剂
苯并咪唑、L-色氨酸、尿酸 上海化学工业园林(麦克林);乙酸钴、明胶 天津市大茂化学试剂厂;无水乙醇、硫酸 天津市富宇精细化工有限公司;氨水(25%) 天津市致远化学试剂有限公司;硝酸 天津化学试剂五厂;六氰合铁酸钾 国药集团化学试剂有限公司;其余所用试剂均为分析纯;实验用水均为超水。
1.2 仪器与设备
TGA-4000热失重分析仪,上海铂金埃尔默仪器有限公司;LK2005电化学分析仪,天津市兰力科化学电子高技术有限公司; D/Max-2500 X 射线衍射仪。
1.2.1 ZIF-9的合成
称取7.6 g无水乙醇、0.12 g苯并咪唑加入到100 mL圆底烧瓶中,用胶头滴管吸取2 d 25%的氨水加入,常温磁力搅拌 15 min;之后放入0.12 g的乙酸钴晶体继续搅拌4 h,得到紫色浑浊溶液,放入离心机中离心三次,每次3 min,转速为 3000 r/min,得到紫色沉淀;对沉淀进行减压抽滤并用无水乙醇清洗三次,得到紫色样品,静置24 h,自然晾干,得到紫色粉末。
1.2.2 明胶储备液的制备及与ZIF-9的融合
将2.5 g明胶(gelatin)溶解在100 g去离子水中,加热到 50 ℃,磁力搅拌2 h后立刻用漏斗趁热过滤,除去不溶性杂质,室温冷却;称取0.025 g的ZIF-9粉末溶解于10 mL明胶放入锥形瓶中,超声分散2 h,然后室温静置12 h,制得修饰膜溶液。
1.2.3 检测生物小分子
设置扫描参数:电流极性为氧化,扫描速度为0.1 V/s,扫描范围设为-1.0~1.0 V,按照L-色氨酸溶液的浓度从低到高的顺序依次进行循环伏安测试;去离子水冲洗三种电极,按照测试L-色氨酸溶液的步骤测试不同浓度的尿酸小分子溶液。
2 结果与讨论
2.1 ZIF-9的表征分析
ZIF-9是由金属Co2+与苯并咪唑配体通过配位作用形成的四配位的晶体材料。对ZIF-9进行了用FT-IR表征,447.23 cm-1处的特征吸收峰为Co-N伸缩振动峰,说明苯并咪唑中的N原子已经与乙酸钴中的Co原子已成键;511.37 cm-1处的吸收峰为 C=N 的伸缩振动峰;1334.32 cm-1附近的特征吸收峰为C-N的伸缩振动峰;1447.56 cm-1处的吸收峰为苯环上C=C伸缩振动峰;在3343.52 cm-1附近出现强而宽的峰,是O-H的伸缩振动的特征吸收峰,出峰位置与报道文献一致[11]。合成产品衍射峰与ZIF-9单晶数据模拟的XRD相比,其特征衍射峰的位置一致,说明该配合物具有较高的相纯度。从热重曲线可以看出,合成的ZIF-9材料在320 ℃时发生分解,表明ZIF-9的耐热性强,框架结构稳定至320 ℃左右,热稳定性较好,远远大于原材料苯并咪唑和乙酸钴的稳定性。
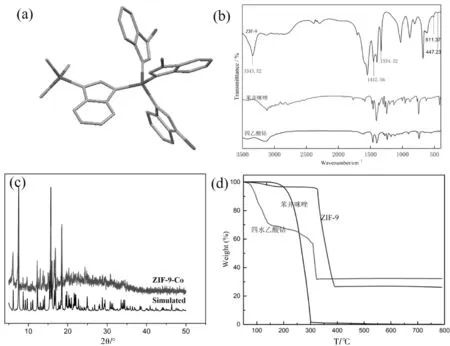
图1 ZIF-9的配位环境(A)、红外光谱图谱(B)、XRD(C)、热重图谱(D)Fig.1 (A)Coordinated environment; (B)FT-IR; (C) XRD; (D) TG of ZIF-9
2.2 缓冲溶液不同扫速的循环伏安图
三电极电解池在0.2 mol/L的NaH2PO4-Na2HPO4的缓冲溶液(pH=6.86)中按照上述参数进行不同扫速条件下的循环伏安扫描。由图2(a)发现:随着扫速的增大,氧化峰的电位向正向移动,还原峰的电位向负向移动,且电流峰的数值也随扫速的增大而增大。根据氧化还原峰电流(ip)与扫速的平方根(ν1/2)的关系图可以看出,峰电流和扫速的平方根存在线性关系,这说明ZIF-9与玻碳电极之间的电子传导受扩散过程的影响[12]。

图2 ZIF-9/gelatin/GCE在缓冲溶液中不同扫速的CV图(a)、峰电流(ip)与扫速的平方根(ν1/2)的关系图(b)Fig.2 CV diagram of ZIF-9/gelatin/GCE in buffer solution with different scanning speed(a); Diagram of ip and ν1/2 (b)
2.3 ZIF-9/gelatin/GCE对尿酸的检测
通过循环伏安法依次对不同浓度尿酸进行了检测。在Epa= 0.47 V处出现了明显的氧化峰,并且氧化峰的电流(ipa)随着尿酸溶液浓度的增加而呈现递增的趋势;在-0.66 V处可以看到ZIF-9/gelatin/GCE明显的还原峰电位随着溶液浓度的变化不显著,且峰电流随着尿酸浓度的增大基本保持不变,进一步表明了ZIF-9作为电极修饰材料的稳定性。以峰电流(ip)与尿酸溶液浓度(cUA)作图,线性方程为ip=45.121CUA(mmol·L-1)+2.135,R2=0.996,信噪比等于3时,尿酸的检出限为6.0×10-5mmol·L-1,如图3(b)所示。

图3 ZIF-9/gelatin/GCE在缓冲溶液中加入不同浓度的尿酸的CV图(a)、峰电流(ip)与尿Fig.3 CV diagram of ZIF-9/gelatin/GCE in buffer solution with different concentration of uric acid(a); Diagram of ip and concentration of uric acid(b)
2.4 ZIF-9/gelatin/GCE对L-色氨酸的检测
通过循环伏安法依次对不同浓度的L-色氨酸进行了检测。随着L-色氨酸溶液浓度的加大,在Epa=0.84 V处,峰电流随浓度呈现递增的趋势,从CV谱图上可知,与检测尿酸分子相比,L-色氨酸的出峰位置偏向更正的电位,所以,L-色氨酸的检测需要更大的电位。以峰电流(ip)与L-色氨酸浓度(cL-Trp)作图(图6B),线性方程为ip=47.408 CL-Trp(mmol·L-1)+0.910,R2=0.995,信噪比等于3时,检出限为2.0×10-5mol/L。

图4 ZIF-9/gelatin/GCE在缓冲溶液中加入不同浓度的L-色氨酸的CV图(a)、峰电流(ip)与L-色氨酸浓度的关系图(b)Fig.4 CV diagram of ZIF-19/gelatin/GCE in buffer solution with different concentration of L-tryptophan(a); Diagram of ip and concentration of L-tryptophan(b)
2.5 ZIF-9/gelatin/GCE对尿酸和L-色氨酸的同时测定
分别移取不同浓度的尿酸和L-色氨酸溶液,混合均匀,在pH=6.86的条件下,利用CV法测定混合溶液的氧化峰电流。结果表明,随着浓度的增大,相应的氧化峰电流也逐渐增大。尿酸和L-色氨酸在修饰电极上氧化峰电位相差443 mV,实现了尿酸和L-色氨酸的选择性测定。
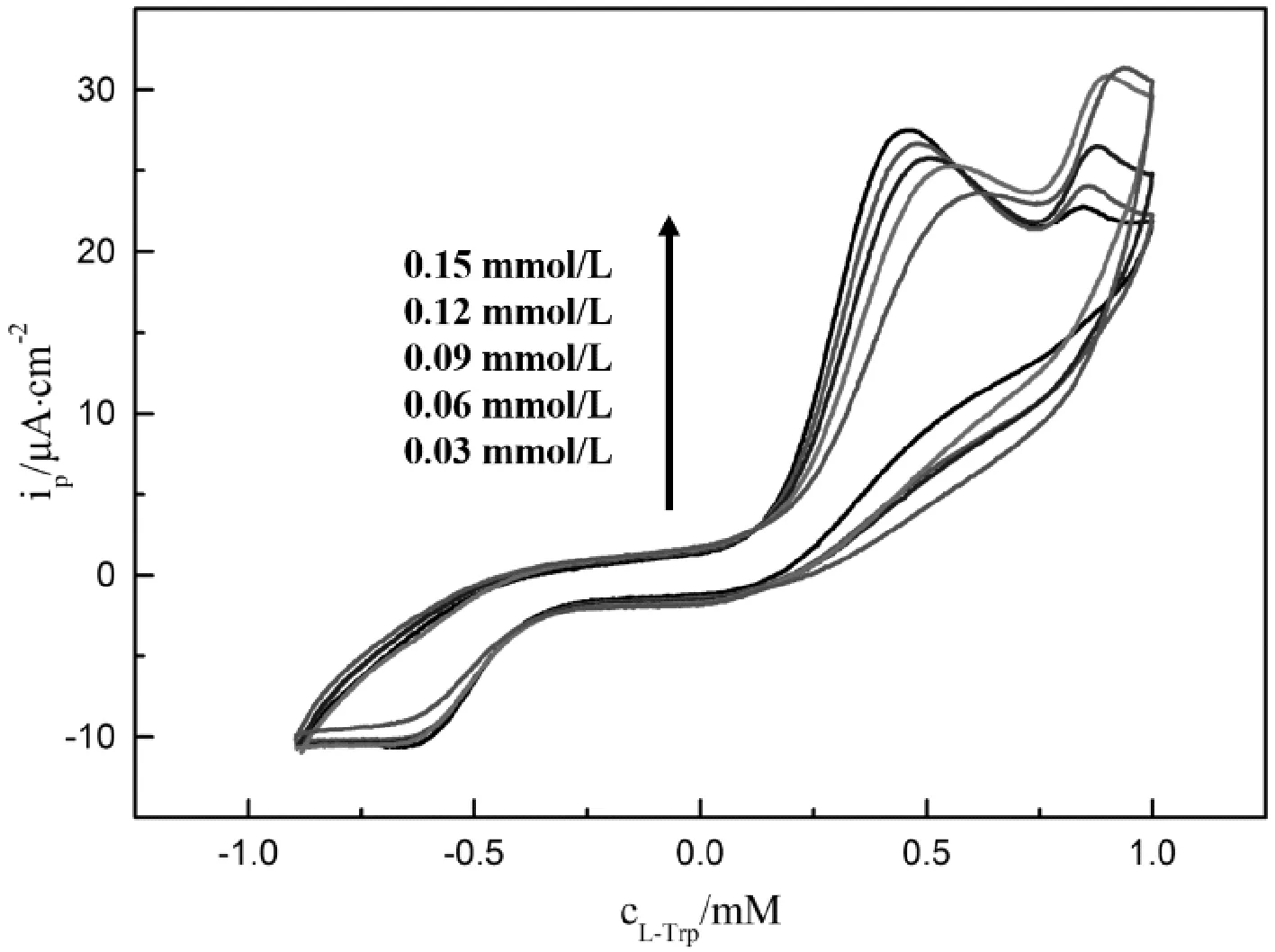
图5 ZIF-9/gelatin/GCE在含有不同浓度尿酸和 L-色氨酸溶液中的CV图(浓度:0.03,0.06,0.09, 0.12,0.15 mM)Fig.5 CV diagram of ZIF-19/gelatin/GCE in buffer solution with different concentration of uric acid and L-tryptophan
3 结 论
采用室温磁力搅拌法合成了ZIF-9,方法简单、快速。首次考察了作为电极修饰材料的可行性。经过预处理后用其来修饰玻碳电极,在最优的实验条件下对不同浓度的生物小分子溶液进行循环伏安特性曲线分析。结果表明,ZIF-9作为电极修饰材料对尿酸和L-色氨酸有良好的电化学响应。尿酸浓度在0.25~1.5 mmol/L范围内呈现良好的线性关系,检出限为6.0×10-5mol/L;L-色氨酸浓度在0.1~0.5 mmol/L范围内呈现良好的线性关系,检出限为2.0×10-5mol/L。同时对两种分子进行了同步检测,尿酸和L-色氨酸在ZIF-9修饰电极上氧化峰电位相差443 mV,实现了尿酸和L-色氨酸的选择性测定。

