改良内镜辅助经横结肠腔道取标本的腹腔镜右半结肠癌根治NOSES术(改良CRC-NOSES-Ⅷ式C法)
宁英泽 刘军广 蔡云龙 饶小龙 戎龙 汤坚强
腹腔镜手术在结直肠肿瘤的手术治疗中已经得到了广泛的应用和发展。随着患者对术后生活质量需求的提高,经自然腔道取标本手术(natural orifice specimen extraction surgery,NOSES)越来越多地被应用到腹腔镜结直肠癌手术中[1]。不同于直肠癌手术标本可经肛门直接拖出,右半结肠由于距肛门较远,且通常标本体积较大,行NOSES手术具有一定困难。目前已有经阴道或直肠取出右半结肠切除标本的报道,但上述方法需在阴道或直肠壁额外切口。为进一步减少手术创伤,本中心探索完成一例内镜辅助下经横结肠腔道取标本的右半结肠癌根治NOSES术(改良CRC-NOSES-Ⅷ式C法),现报道如下。
一、临床资料
患者78岁,男性,身体质量指数(BMI)21.0 kg/m2。主因“横结肠癌ESD切除术后半年”入院。ESD标本病理提示“横结肠管状腺瘤,Ⅱ~Ⅲ级,局灶腺体重度异型增生,并浸润间质至黏膜下层,呈高分化腺癌,浸润最深处深度约2.5 mm,距基底切缘最近处0.15 mm”。术前CT、血液检查均未见明显异常。
二、手术过程
1.术前准备
患者术前口服3袋复方聚乙二醇电解质散剂进行充分肠道准备。采用改良Lloyd-Davis体位,头低足高15度,右侧倾斜15度,常规5孔法置戳卡,观察孔取脐下。
2.手术操作
探查腹腔未见明显积液及腹膜种植结节。术中肠镜检查,见内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)术后瘢痕位于横结肠近肝曲,结合术前病史及检查结果,决定行腹腔镜下右半结肠癌根治术。先取头低足高、左侧倾斜位,行尾侧入路沿右侧Toldt's筋膜间隙完成右侧结肠系膜的游离。助手牵拉回结肠血管棘,于肠系膜上静脉右侧缘离断回结肠动静脉,并离断右结肠动静脉及结肠中血管的右侧支;保留大网膜,游离结肠肝曲并与尾侧入路会师,完整游离右半结肠。距回盲部近端10 cm回肠、肿瘤远端5 cm横结肠处内镜下使用直线切割缝合器分别离断肠管。
3.标本取出
术中肠镜进镜至横结肠断端,肠镜下稀碘伏水冲洗横结肠肠腔并吸净肠液及气体,紧邻闭合钉处切开横结肠残端。经戳卡置入一长约50 cm捆绑带,一端缝扎于右半结肠标本结肠断端,另一端用肠镜异物钳夹住,缓慢退镜,先将捆绑带经左半结肠拉至肛门口,助手配合牵拉捆绑带和右半结肠标本,经横结肠缓慢经肛门拉出标本,见图1A~1D。肠镜取标本时间约20分钟。
4.消化道重建
直线切割缝合器再次封闭横结肠断端(图1E),行回肠横结肠Overlap吻合(图1F),0/3 V-loc线关闭共同开口,并行浆肌层缝合加固吻合口与盲端。经戳卡孔置入引流管于吻合口附近。
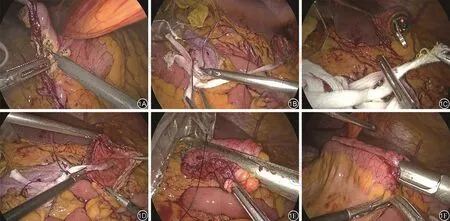
图1 经横结肠腔取右半结肠标本及消化道重建。1A:打开横结肠断端;1B:缝扎标本结肠断端与捆绑带;1C:肠镜异物钳钳夹捆绑带;1D:开始牵出标本;1E:闭合横结肠开口;1F:横结肠回肠Overlap吻合
5.术后恢复情况
手术时长210 min,术中出血20 mL。术后第一天下床活动,第二天排气,第三天饮水进要素饮食,逐渐过渡至半流食,术后第八天出院,切口和吻合口愈合良好,见图2。术后病理:ESD创面未见肿瘤残留,淋巴结均未见肿瘤。
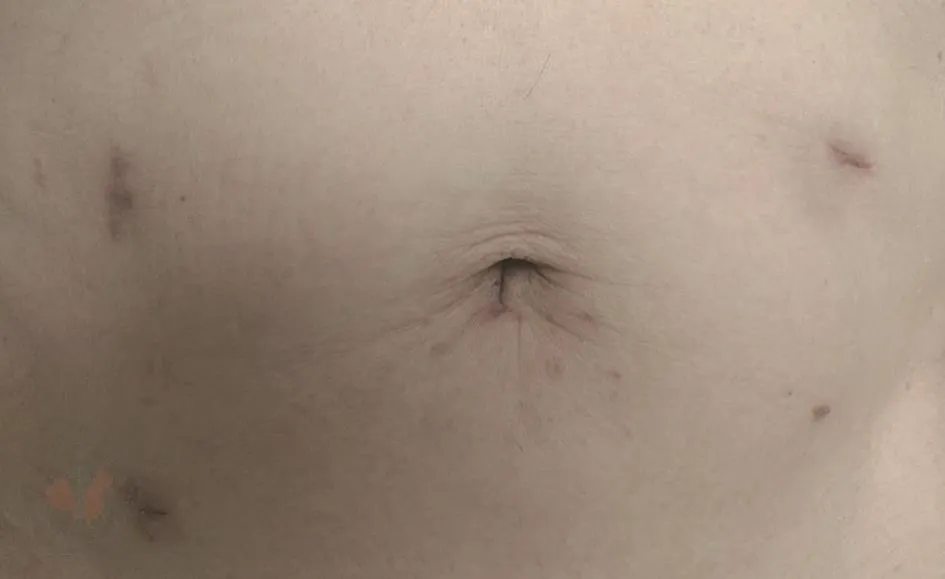
图2 患者术后腹壁图像
三、讨论
近30余年,随着腹腔镜手术技术的不断发展,创伤更小、术后恢复更快的腹腔镜结直肠癌根治术已逐渐成为常规术式。结直肠NOSES手术通过包括肛门和阴道在内的自然腔道取出切除标本,有效避免了腹壁的额外切口。这在腹腔镜微创手术的基础上进一步“微创”,减少了术后切口疼痛、感染等常见并发症,有助于患者早日下床活动,更快速地恢复胃肠道功能,从而缩短住院时间[2]。
近年来,已有不少中心进行了右半结肠癌NOSES手术的尝试。在女性患者中,阴道可作为标本取出的通道,但需在阴道后壁做一约5 cm切口[3],这可能造成盆腔感染及术后阴道瘘等并发症[4],以及可能有对性功能造成影响的担忧[5]。而对于男性患者,经直肠取出标本成为NOSES手术的常见途径,这需要面临直肠切口出血、吻合口不愈合等风险[6]。
肠镜辅助下经横结肠取标本在良性右半结肠切除术中已有相关报道,国内部分学者将其用于结肠癌根治术[7]。但肠镜取标本极为困难,对肿瘤的大小和BMI要求较高。本例将取标本方式进行改良,采用较长的捆绑带与结肠断端缝合固定,用肠镜异物钳将捆绑带拉出肛门外,经肛门牵拉捆绑带,从而将右半结肠标本取出。该方法比常规用肠镜异物钳直接取标本的可操作性更强,取标本时间也明显缩短。
本例NOSES手术同样面临无菌、无瘤原则的考验[8-9],针对肠镜辅助右半结肠癌NOSES术,我们建议采取相应的措施来进行无菌无瘤操作,避免术后出现腹腔感染和种植转移,包括:(1)充分的术前肠道准备;(2)内镜辅助牵出捆绑带时注意内镜不进入腹腔,污染视野;(3)严格控制手术指征:低BMI,系膜及肠管不肥厚,肿瘤直径小于3 cm,建议T2N0分期以下;(4)全腔镜下消化道重建防止消化液外溢,污染创面。本例选择的是ESD术后早癌标本,拖出时未使用保护套,此为该术式需要进一步改进的地方。若为进展期肿瘤,应使用保护套包裹标本,以减少肿瘤播散风险。对于标本肿瘤较大或肠管较粗者,可事先碘伏润滑乙状结肠肠道,以减少拖出阻力。拖出时若捆绑带不慎脱落,可选择肠镜下用异物钳继续将标本取出。
综上,改良内镜辅助下经横结肠腔道取标本的腹腔镜右半结肠癌根治术安全可行,但应严格把握适应证,其对术后的近期和远期疗效的影响还有待进一步扩大样本量进行对照研究。

